癫痫撤药致可逆性胼胝体压部病变患者的影像学表现和临床特征
陈立新,陈新焰,刘琦,郭金竹,郭毅,卢强,周祥琴,有慧,窦万臣
随着影像学技术的普及,可逆性胼胝体压部病变(reversible splenial lesions of the corpus callosum, RSLCC)的报告逐渐增多,但是临床医生对该疾病的认识仍有待提高。因此,对药物所致RSLCC的病例的报道进行分析有助于提高我国医务工作者对这种疾病的认识,合理使用或减停药物,避免误诊甚至施行侵入性手术。本研究报道北京协和医院近年来诊治的2例因抗痫性发作药物(anti-seizure medication,ASM)快速撤药所致RSLCC的患者,并对相关病例进行文献复习。
1 病例资料
病例1,女,24岁,因“发作性愣神、咂嘴6年”于2019年3月20日收入本院行癫痫术前评估检查。入院前规律口服左乙拉西坦1 g、2次/d,奥卡西平0.45 g、2次/d,托吡酯100 mg、2次/d。入院查体:身高170 cm,体质量65 kg。生命体征正常,神经系统查体未见明显异常。入院辅助检查:全血细胞分析、尿常规+流式尿沉渣分析、肝功+肾功、凝血2项、输血8项(-)。头部PET示发作间期左侧颞叶代谢减低。头皮动态脑电图结果提示左侧颞部导联可见尖波及尖慢波发放。入院诊断为药物难治性部分性癫痫。入院后首先做长程视频脑电图监测,嘱患者逐渐减药。因患者急于捕捉发作症状而未遵医嘱,于数天内自行快速减停奥卡西平及左乙拉西坦,导致发作频率较平时明显升高,但发作形式类似。患者于2019年3月28日行头颅MRI扫描提示胼胝体压部可见T2WI片状长信号,DWI呈高信号,ADC信号较低。结合临床考虑胼胝体压部细胞毒性病变,可能与快速减停ASM有关。脑电图检查结束后恢复之前用药。14 d后复查头部MRI提示胼胝体压部异常信号恢复正常。病程中患者始终无明显异常临床表现。
病例2,女,22岁,因“发作性愣神4年余”于2020年10月9日收入本院。曾因“低级别胶质瘤”行左侧颞叶外侧病变切除术,余无特殊。规律口服卡马西平400 mg、2次/d,左乙拉西坦500 mg、2次/d。入院查体:身高163 cm,体质量53 kg。生命体征稳定,神清语利,神经系统查体未见明显异常。入院辅助检查:血常规检查中白细胞计数为3.26×109/L[参考范围为(3.50~9.50)×109/L],中性粒细胞计数为1.46×109/L[参考范围为(2.00~7.50)×109/L],余均正常,肝肾功能及凝血等其他常规化验检查均未见异常。尿酸+叶酸(血清)+VB12+同型半胱氨酸(HCY):SFA为2.5 μg/L(参考范围为>4.0 μg/L),HCY为20.7 μmol/L(参考范围为<15.0 μmol/L);抗神经抗原抗体检测(NMDA+GAD+VGKC)正常。头颅MRI提示左侧颞叶外侧病变切除术后,左侧海马体积略小于对侧。视频脑电图监测结果显示左中颞慢波及低波幅尖波发放。入院诊断为症状性癫痫、左颞叶病变切除术后。行长程视频脑电图监测过程中患者自主快速减停卡马西平和左乙拉西坦。于2020年10月20日行头颅MRI提示胼胝体压部可见小片状异常信号,T1WI呈略低信号,T2WI及FLAIR呈稍高信号,DWI呈高信号,ADC信号明显减低。结合临床考虑RSLCC,与快速减停ASM有关。因患者无不适主诉及神经系统阳性体征,给予临床观察。后于2020年10月27日及2020年11月11日行颅内电极植入术及左侧标准前颞叶切除术,术后复查头颅MRI见胼胝体压部异常信号消失。
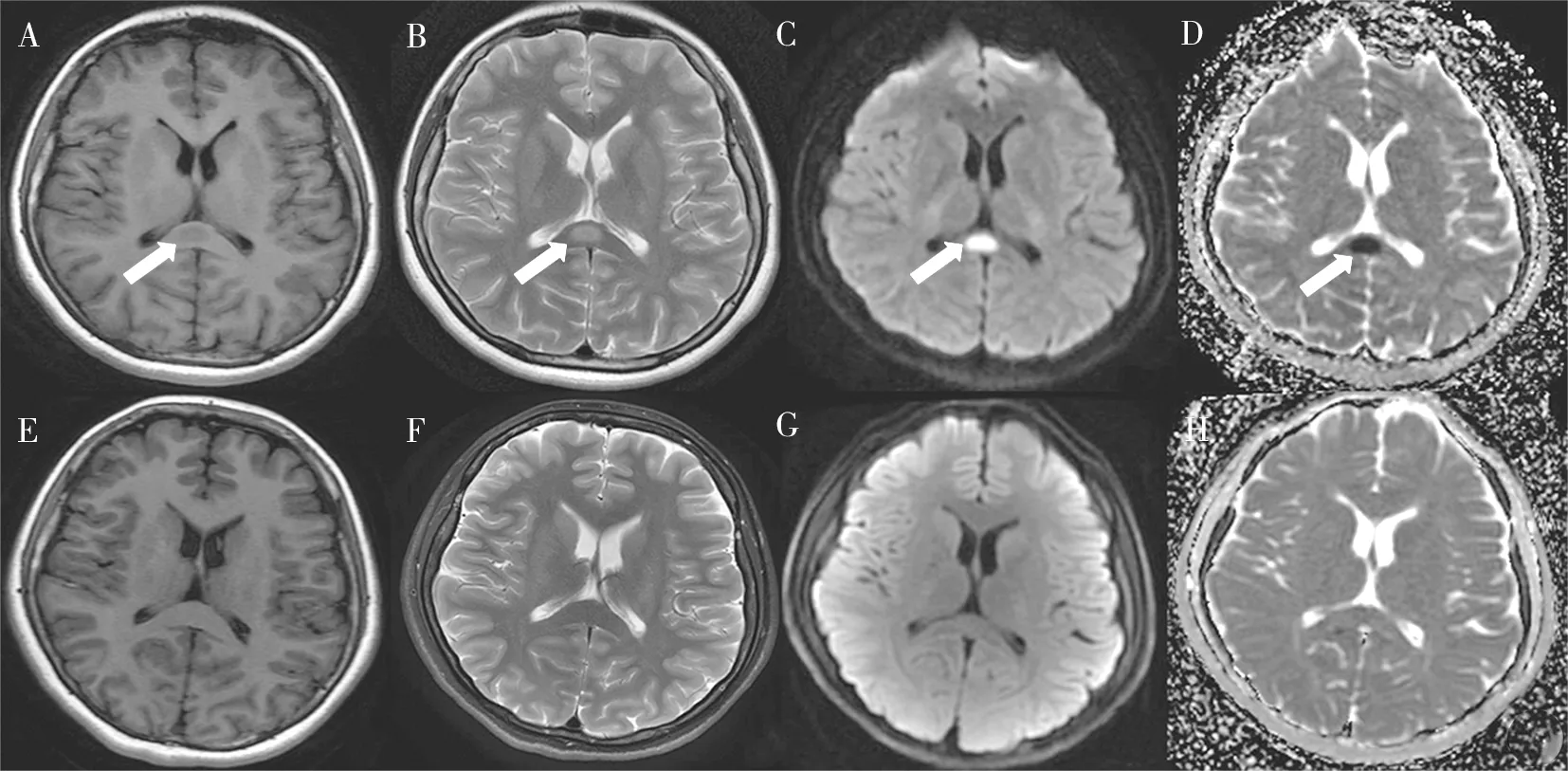
注:A~D为撤药后的头颅MRI图像,胼胝体压部可见异常信号(箭头所示);E~H为间隔14 d后复查头颅MRI相应序列的影像,提示之前的病变已经完全消失。A为T1WI显示略低信号;B为T2WI显示高信号;C为DWI显示高信号;D为ADC显示低信号。
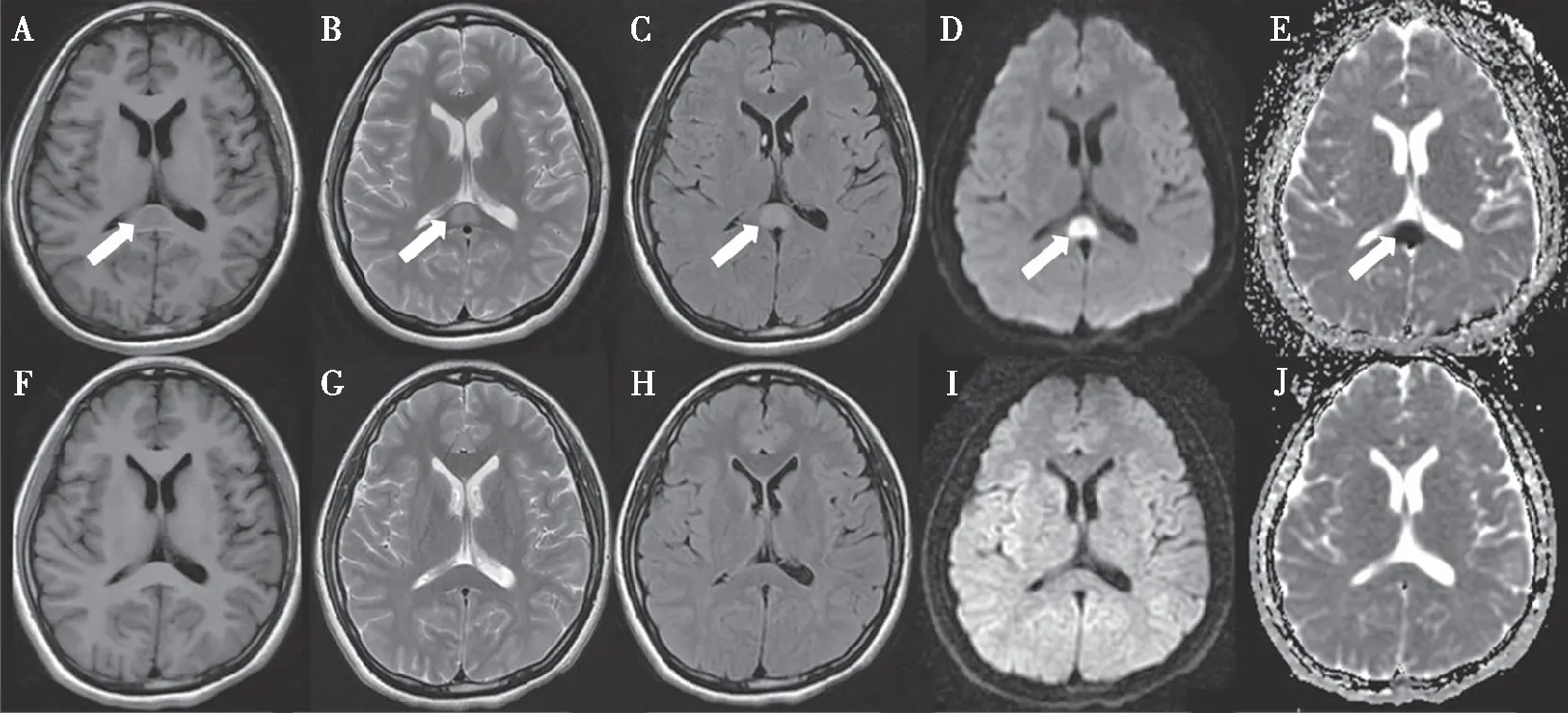
注:A~E为撤药后的MRI图像,胼胝体压部可见异常信号(箭头所示);F~J为间隔28 d后复查MRI相应序列的影像,提示之前的病变已经完全消失。A为T1WI显示略低信号;B为T2WI显示高信号;C为FLAIR显示略高信号;D为DWI显示高信号;E为ADC显示低信号。
2 文献复习
2.1 文献检索
于2022年9月以“corpus callosum”“ transient splenial lesion”“antiepileptics”“withdrawal”等为关键词, 查找PubMed、Embase及Cochrane数据库中从2000年9月至2022年9月的相关英文文献报道。对其中有详细病史的患者的病因、年龄、性别、症状及病程等进行总结, 分析疾病的相关特点。
2.2 纳入标准和排除标准
纳入标准:(1)既往有癫痫病史,起病与用药剂量改变相关;(2)胼胝体压部病变呈可逆性;(3)进行连续的头颅MRI检查,有完整的影像学资料。排除标准:(1)头颅MRI显示有胼胝体压部以外病变, 如脑皮层病变、皮质下白质病变、脊髓病变、海马病变及视神经病等;(2)随访不及时或失访致病史不完整,无法正确统计;(3)患者年龄<6岁;(4)同时合并多发性硬化、急性播散性脑脊髓炎、外伤、胼胝体肿瘤及梗死等其他可能导致的疾病。
2.3 检索结果
共搜集到13篇病例研究总计16例RSLCC患者,其临床资料见表1[1-13]。病因均为癫痫患者病程中突然改变用药剂量。其中男8例、女8例,年龄12~48岁、平均31岁,临床无症状者接近50%, 其余患者的临床症状为癫痫大发作、视幻觉、疲劳、共济失调步态及头痛晕厥等。头颅MRI显示RSLCC的持续时间为10~240 d,平均66 d,影像学特征是T1WI稍低或等信号, T2WI、DWI高信号, ADC低信号, FLAIR上无或稍高异常信号, 行增强MRI者未发现病灶强化。

表1 16例癫痫撤药致RSLCC患者的相关病例资料
3 讨论
胼胝体位于大脑半球纵裂的底部,相比于脑部其他结构,其压部的神经元有较多受体分布,例如细胞因子受体、谷氨酸受体、毒素受体及药物受体等[14-15]。因此在免疫反应、炎症刺激及药物作用下,通过细胞内外离子的沟通,常出现胼胝体细胞毒性病变[16]。随着大量临床病例的报道,有研究进行了分析总结,提出了伴有可逆性胼胝体压部损伤的轻度脑病的概念,其临床特点为有前驱感染病史,而后出现急性脑炎或脑病,主要表现为发热、头痛、呕吐、意识障碍及谵妄等,头颅MRI可见胼胝体压部受累,病程较短,1个月左右病灶完全消失[17]。Garcia-Monco等[18]研究认为可逆性的压部病变可伴随多种临床症状,但其影像学表现有一致性,以影像学特征命名更合适,并建议以可逆性胼胝体压部综合征命名。而Kim等[19]的研究最先于1999年在癫痫患者群体中报道了RSLCC,发现在服用苯妥英钠以及托吡酯的患者中,其头颅MRI提示胼胝体压部出现局灶性及一过性的病变,并认为这一症状可能与ASM的毒性有关。但是关于细胞毒性病变的证据也并不充足,相互矛盾的现象和观点经常出现,因此关于RSLCC的发病机制目前没有定论[6, 12, 20-25]。
RSLCC患者的头颅MRI有特征性的表现,其病灶一般位于胼胝体压部中心,呈边界清楚的孤立圆形(或卵圆形),平扫中一般信号均匀,无坏死或囊性改变、无明显周围性水肿及占位效应等。病变在T1WI呈低信号至等信号,T2WI及FLAIR呈略高信号,DWI呈高信号,ADC值较低。注射造影剂后,病灶无强化。除了常规的断层影像学,行MRS检查也是协助诊断的方法。Cirnigliaro等[26]的研究对RSLCC患者进行波谱分析,发现其脑代谢物及MI升高,NAA正常,Lip和Glx无明显峰值,表明神经细胞的完整性未破坏,没有不可逆的轴突损伤。这也与之前的病理生理机制研究结果相一致[27]。
ASM与体液平衡关系密切。有研究报道,卡马西平等药物可作用于胞膜上的阳离子通道,并且能增强抗利尿激素的效用,从而引起渗透压的变化,而撤药容易导致药物诱导性的脑水肿[28-29]。因此,突然停用卡马西平后可使患者抗利尿激素功能不足,从而导致脑组织特别是胼胝体压部的有效渗透压下降,进而引起局部的细胞毒性水肿。但是并非所有患者在快速改变药物剂量后都会出现可逆性的病变。Gröppel等[30]对24例患者研究发现,无论是停药周期还是体内药物浓度水平,均与RSLCC的发生无显著相关,这表明不同人种、不同人群间的药物反应和耐受性差异较大。因此RSLCC可能与特定癫痫患者的药物代谢的遗传特征有关[31]。特别是患者服用多种精神类药物时,由于细胞色素P450(CYP)相关基因的多样性使得不同个体的药物代谢速率不同,再加上药物之间的相互作用,导致个体用药剂量有较大差别,这也给临床诊治带来一定的困难和挑战[26]。
对于临床医生而言,累及胼胝体的病变并不少见,因此需要与其他疾病进行鉴别诊断。主要有(1)多发性硬化症:此病通常累及中年女性,表现为脑室及脊髓的白质区域多灶性病变,并有显著的“环状”强化;(2)Marchiafava-Bignami病:即胼胝体脱髓鞘病变,通常累及中老年男性,有长期酗酒史,在体、膝部表现为异常信号,在MRI上有占位效应和对比增强。近年来随着DTI广泛应用于其机制的探究,可从分子和细胞水平层面评价组织细胞的病理变化过程[32];(3)急性播散性脑脊髓炎:常发生于感染后或疫苗接种后,表现为双侧大脑半球白质以及胼胝体的体、膝部的不对称性病变,MRI上有显著的对比强化;(4)胼胝体肿瘤:通常出现瘤周水肿、占位效应及可变对比度增强等表现;(5)可逆性后脑病综合征:患者通常有高血压病病史或子痫病史,多为枕叶、颞叶、小脑及基底核区受累,可同时累及胼胝体;(6)胼胝体梗死:表现为缺血性病变,多在后循环缺血的老年患者中出现。
目前对RSLCC尚无特效治疗方法,主流治疗思路都是尽快去除诱因,因此病例研究报道主要是使用激素冲击、抗病毒药物及免疫球蛋白治疗[33]。有研究表明,胼胝体压部病变患者的转归与潜在的病因密切相关,癫痫患者快速撤药导致的RSLCC预后良好,通常无遗留后遗症[34]。本例患者在去除诱因及恢复癫痫用药后,胼胝体压部病灶最终消失,预后良好。
综上所述,癫痫撤药所致的RSLCC是一种具有潜在病因和特殊影像学表现的疾病,并无特殊治疗措施,预后良好。随着近些年对于该疾病的认识不断加深,其诊断率也逐年上升,有研究相继报道若干相关病例,进一步明确了这一疾病的诊治思路及要点[35-36]。一方面,神经外科医生需要加强对该病的认识,掌握其临床特点,避免手术切除病变;另一方面,临床治疗癫痫患者的过程中切忌快速撤药,尽可能做到阶梯减药,以避免该疾病的发生及发展。

