骨骼肌质量指数预测维持性血液透析病人衰弱的应用价值
张 园,张瑞丽,刘 兰,张东雪,王 洋,胡春燕
1.河北医科大学第四医院,河北 050000;2.河北医科大学
维持性血液透析(maintenance hemodialysis,MHD)是终末期肾脏病(end stage renal disease,ESRD)病人重要的肾脏替代疗法之一[1]。MHD 病人由于长期透析治疗使体内蛋白质和结合氨基酸大量丢失,又加之其久坐、久躺导致肌肉合成受损和体能下降,易引发衰弱[2]。据国外报道,MHD 病人的衰弱患病率为13.8%~73.0%[3]。衰弱是一种重要的医学综合征,是由多种原因引起,以力量以及耐力下降、生理机能下降为表现,对死亡更加敏感[4]。衰弱可导致MHD 病人发生意外伤害,如跌倒、骨折等,影响生活质量,增加了病人住院率及死亡率[5⁃6]。因此,研究衰弱的发生发展及影响因素对预防MHD 病人发生衰弱至关重要。骨骼肌质量指数(skeletal muscle mass index,SMI)是四肢骨骼肌质量与身高平方的比值,用来评价肌肉的质量,是反映病人营养状态的重要指标[7⁃10],而营养不良又是导致MHD 病人发生衰弱的直接或间接影响因素[5,11⁃12]。本研究通过测量SMI,探究其与MHD 病人衰弱之间的关系,为日后的临床治疗提供依据,现报道如下。
1 对象与方法
1.1 对象 选取2021 年12 月在河北省某三级甲等医院行MHD 病人384 例,年龄(57.34±15.18)岁;男239例,女145 例。纳入标准:①行MHD≥3 个月,年龄≥18 岁;②每周透析2 次或3 次,每次透析4 h;③签署知情同意书。排除标准:①合并严重并发症;②痴呆及各种精神病;③言语交流沟通障碍;④体内放置有金属支架或起搏器和截肢的病人。本研究已经过我院伦理委员会批准。
1.2 调查工具及内容
1.2.1 FRAIL 量表 该量表包括疲乏感、阻力感、步行能力、多病共存>5 种疾病、体重下降5 个条目,共5分,评分≥3 分为衰弱,<3 分为非衰弱[13]。
1.2.2 营养不良⁃炎症评分量表(MIS) 该量表由病史、体格检查、体质指数(BMI)和实验室检查4 个部分内容组成,共10 项,每项采用4 级评分,0 分为正常,3分为严重,得分越高表示营养不良和炎症程度越严重[14]。
1.2.3 人体学及体成分测量 由专业营养师测量身高、体重、中臂肌围(MAC)、肱三头肌皮褶厚度(TSF),应用EH101 电子握力计测量握力,测量3 次取平均值。采用人体成分分析仪InbodyS10(生物电阻抗法)测定体成分指标:蛋白质、体脂肪、骨骼肌(SMM)等。亚洲肌肉减少症工作组(AWGS)根据人体成分测量标准定义SMI 减少为男性<8.87 kg/m2、女性<6.46 kg/m2[15]。
1.2.4 生化指标 收集病人人体成分测量前后的生化指标,包括白蛋白(ALB)、前白蛋白(PAB)、血清铁蛋白、C 反应蛋白及钙、磷、钾、钠、二氧化碳等。
1.3 调查及资料收集方法 为保证护理人员对量表条目的理解和测评方法达到一致,项目开始前由研究者对科室护士进行培训,介绍两种量表使用目的、测评方法、计分方法等,所有量表的评估均于透析日在病人床旁进行。人体学测量由经过统一培训的专业营养师测量,体成分测量采用生物电阻抗法,通过人体成分分析仪于病人下机后休息10~15 min 进行测量,所有步骤严格按照操作说明进行。使用医院电子病历管理系统(学透通系统)收集符合纳入标准的MHD 病人的临床资料及相关化验检查结果。最终所有数据由双人录入后并交叉核对,保证录入数据准确性。
1.4 统计学方法 采用SPSS 22.0 软件对数据进行统计分析。调查对象的一般资料用描述性统计方法,符合正态分布定量资料采用均数±标准差(±s)进行统计描述,采用独立样本t检验进行组间比较;偏态分布资料用中位数(四分位数)[M(P25,P75)]描述,采用Mann⁃WhitneyU秩和检验。定性资料采用例数、百分比(%)表示,组间比较采用χ2检验。采用二元Logistic回归分析建立风险预测模型,并采用受试者工作特征曲线(ROC)检验预测模型的拟合效果,以灵敏度、特异度和正确率验证模型的应用效能。以P<0.05 为差异有统计学意义。
2 结果
2.1 MHD 病人临床资料 384 例MHD 病人中发生衰弱80 例,发生率为20.8%,衰弱组与非衰弱组临床资料比较见表1。

表1 衰弱组与非衰弱组病人临床资料比较
2.2 两组病人SMI 发生情况分析 衰弱组低SMI 病人27 例,发生率为33.7%,非衰弱组病人低SMI 病人41 例,发生率为13.5%,两组比较差异有统计学意义(χ2=17.845,P<0.001)。
2.3 MHD 病人衰弱的相关因素分析 Spearman 相关分析结果显示,MIS 评分、C⁃反应蛋白、铁蛋白与衰弱评分呈正相关(r值为0.170,0.243,0.157,P<0.05)。Pearson 相关分析显示,年龄与衰弱评分呈正相关(r=0.686,P<0.05),前白蛋白、白蛋白、蛋白质含量、骨骼肌含量、基础代谢率、SMI 与衰弱评分呈负相关(r值为-0.448,-0.398,-0.210,-0.199,-0.155,-0.182,P<0.001)。
2.4 MHD 病人衰弱风险预测模型 384 例MHD 病人中,以衰弱为因变量(衰弱=1,非衰弱=0),将年龄、C⁃反应蛋白、前白蛋白、白蛋白、铁蛋白、MIS 评分、蛋白质含量、骨骼肌含量、基础代谢率、SMI(均为实测值)为自变量,进行Logistic 回归分析,结果显示:年龄、MIS 评分是MHD 病人衰弱的独立危险因素,白蛋白、SMI 是MHD 病人衰弱的保护因素,见表2。
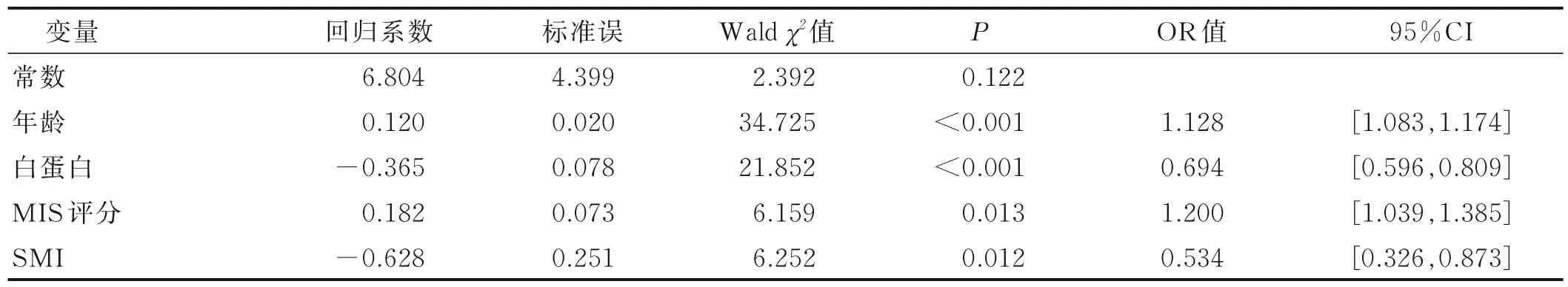
表2 MHD 病人衰弱影响因素的Logistic 回归分析结果
2.5 SMI 对MHD 病人衰弱预测模型的效果 采用ROC 曲线分析SMI、MIS 评分、白蛋白、年龄单独和联合检测诊断MHD 病人衰弱的临床预测效果,ROC 曲线下面积(AUC)依次为0.717,0.672,0.813,0.857 及0.927,见表3、图1。
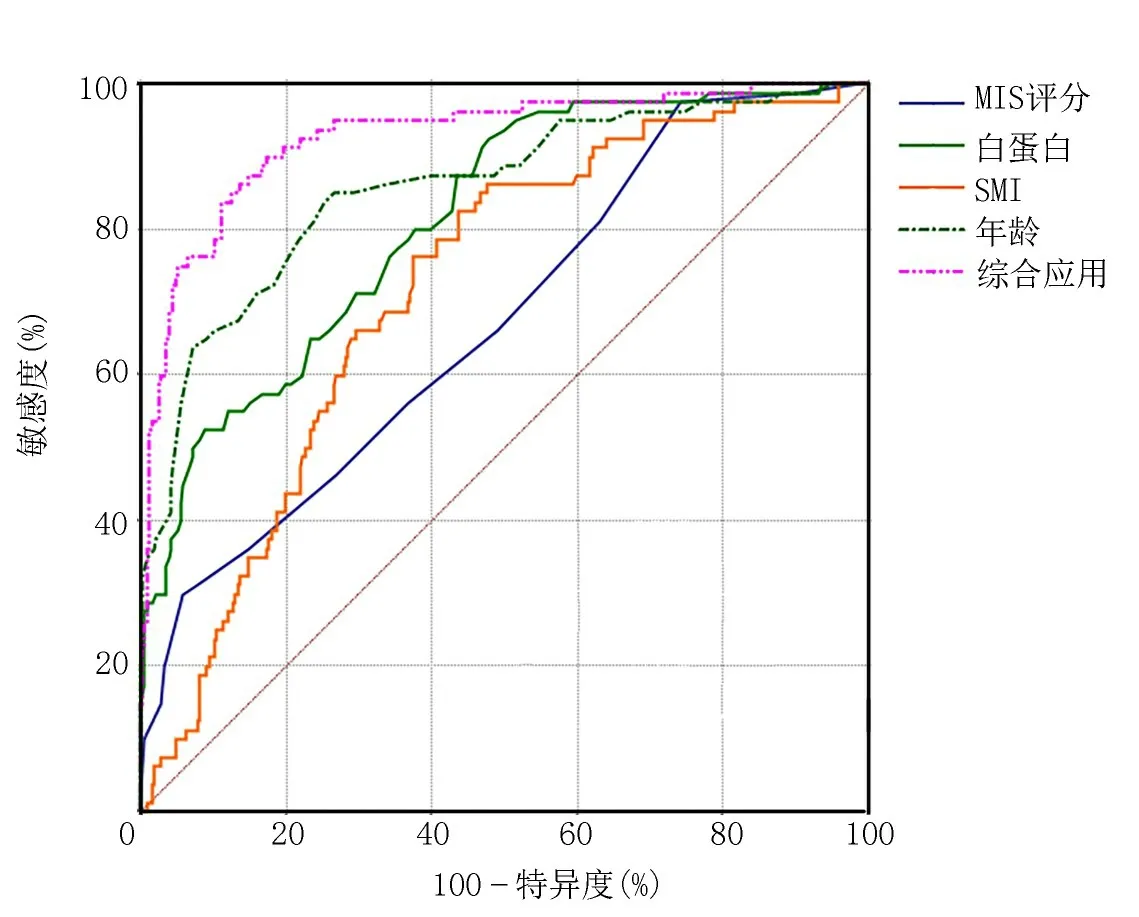
图1 SMI、MIS 评分、白蛋白、年龄单独和联合检测诊断MHD 衰弱的ROC 曲线图
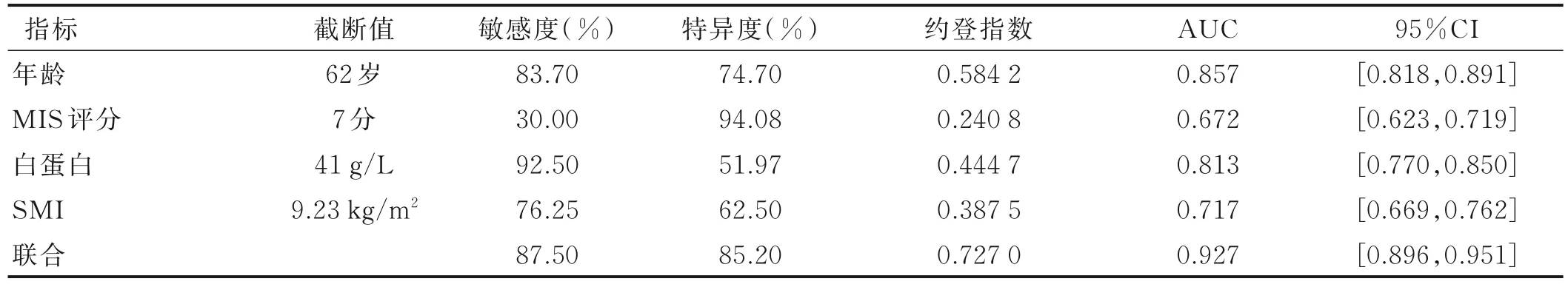
表3 SMI、MIS 评分、白蛋白、年龄对MHD 病人衰弱的预测价值
3 讨论
MHD 病人因合并多种并发症,使其衰弱患病率增高,发病风险为普通人群的6 倍左右[16⁃17],且衰弱增加了MHD 病人跌倒及骨折的风险[18⁃19],增加了病人住院率及死亡率,严重影响MHD 病人生活质量及预后。但衰弱状态具有可逆性,及早识别并进行干预可延缓、逆转病情,改善预后[20]。因此,研究衰弱的发生发展及影响因素对提前预防MHD 病人发生衰弱至关重要。
本研究结果显示,透析龄长、高龄是MHD 病人衰弱的危险因素,年龄>62 岁病人衰弱的发生风险较高,白蛋白是衰弱的保护因素。随着年龄增长和透析时间延长,病人的器官机能、新陈代谢能力等均显著下降,衰弱程度逐渐增高[21]。MHD 病人由于透析过程中的营养物质丢失及低磷饮食限制了蛋白质的摄入,导致病人体内蛋白质和能量的过度消耗,因此出现营养不良,进而导致衰弱。本研究结果还显示,衰弱组的炎症指标升高,MIS 是MHD 病人发生衰弱的危险因素,MIS 评分>7 分,衰弱的发生风险更高。有研究显示,C 反应蛋白是反映炎症状态敏感且特异的炎性指标,衰弱与慢性炎症密切相关[22]。有研究证实,MIS 对MHD 病人营养风险有预测作用[23⁃24],进而对衰弱有一定预测价值。
MHD 病人中的低SMI 病理生理学机制复杂,可能与尿毒症毒素、氧化应激、胰岛素抵抗有关、营养不良和身体不活动等有关[25⁃26]。低SMI 在MHD 病人中患病率为20%~55%,并导致MHD 病人死亡风险增加[27⁃28]。本研究探讨SMI 和MHD 病人衰弱之间的关系发现,衰弱组病人SMI 偏低,且衰弱与SMI 呈负相关。研究显示,MHD 病人由于长期透析、食欲下降、营养物质摄入不足,每次透析都将丢失部分氨基酸和蛋白质,且合成蛋白质等营养物质的能力降低,导致病人营养不良的发生率升高[29]。营养不良会降低骨骼肌质量,增加骨质疏松症、骨折、跌倒等风险[30],而这些均能促进衰弱的发展。由于代谢性酸中毒、未解决的尿毒症和促炎细胞因子水平升高导致的蛋白质分解代谢加速,透析本身可能会降低MHD 病人的骨骼肌质量[31]。本研究结果显示,SMI 是MHD 病人衰弱的保护因素,为验证SMI 对MHD 病人衰弱发生的预测价值,ROC 曲线显示,SMI 对MHD 病人衰弱有诊断预测价值,且联合MIS、白蛋白、年龄对MHD 病人衰弱的预测价值最高,为MHD 病人预测衰弱的发生提供依据。但本研究为单中心研究,样本量较少,且为回顾性研究,后期将使用前瞻性研究方法进一步探索SMI 在衰弱诊断中的价值。

