多发性大动脉炎的临床特点及眼部表现
肖迎,王梦雅,王琪
(1.山东第一医科大学附属省立医院,济南 250021;2.山东省第二人民医院,济南 250299)
多发性大动脉炎又称Takayasu病(Takayasu’s arteritis,TA)、高安氏病、无脉症,是一种临床相对比较少见的累及主动脉弓及其分支的慢性血管炎性阻塞性病变,可引起严重的器官缺血症状。多发性大动脉炎多见于年轻女性,发病隐匿,容易被漏诊或误诊,死亡率也较高。值得注意的是,多发性大动脉炎可累及眼部,而且有可能因眼部异常而首诊于眼科。本研究通过回顾性分析山东第一医科大学附属省立医院诊治的14例多发性大动脉炎患者的系统及眼部表现,探讨此类患者的眼部病变特点,旨在增强眼科医师对大动脉炎的正确识别能力,提高对该疾病的正确诊断和治疗能力。
1 对象与方法
1.1 研究对象
回顾性病例系列研究。收集2018年3月至2022年5月山东第一医科大学附属省立医院风湿免疫科确诊、经眼科会诊的14例多发性大动脉炎患者的临床资料,其中男性1例、女性13例,年龄21~50岁,年龄(35.57±9.77)岁,病程8 d~37年,随访时间6个月~ 4年。患者均已签署由本院伦理委员会批准的知情同意书。
1.2 诊断依据及临床分型分期标准
根据1990年美国风湿病学会颁布的多发性大动脉炎标准作为诊断依据: 1)发病年龄≤40岁;2)肢体间歇性乏力或跛行;3)一侧或双侧肱动脉搏动减弱;4)双上肢收缩压差≥10 mmHg(1 mmHg=0.133 kPa);5)锁骨下动脉或主动脉杂音;6)动脉造影显示主动脉及一级分支或上下肢近端的大动脉狭窄或闭塞,病变常为局灶或节段性,并排除动脉粥样硬化、纤维肌性发育不良或其他原因引起。上述6项诊断依据中,符合3项即可诊断多发性大动脉炎。所有患者根据大动脉炎累及的部位进行临床分型,分为:1)Ⅰ型头臂动脉型(主动脉综合征):累及主动脉弓及其分支、头臂干的患者;2)Ⅱ型胸腹主动脉型:累及降主动脉、腹腔动脉分支;3)Ⅲ型肺动脉型:累及肺动脉;4)Ⅳ型广泛型:同时具有以上2种类型及以上临床特征的患者。
多发性大动脉炎患者的眼部病变主要表现为低灌注性视网膜病变(又称Takayasu视网膜病变)、高血压视网膜病变两种类型。根据Uyama分期[1],将Takayasu视网膜病变分为以下四期:1期,小血管扩张期:视网膜动脉压降低,视网膜静脉及毛细血管扩张、管径不均,色泽暗沉;2期,微血管瘤形成期:在扩张的视网膜小血管附近可见串珠状或葡萄状分布的微血管瘤,视网膜静脉流速缓慢,可能出现视网膜出血及棉绒斑,视网膜动脉压进一步下降,眼压开始降低;3期,视网膜动静脉异常吻合期:视网膜动脉静脉之间在视盘周围形成异常交通,或出现新生血管,呈现典型的视盘周围花冠状结构,球结膜血管代偿性扩张,眼球可能出现内陷;4期,并发症期:严重的视网膜缺血可出现多种眼部并发症,如玻璃体积血、增殖性视网膜病变、继发性视网膜脱离等,患者可同时伴有瞳孔散大、虹膜萎缩、虹膜红变、继发性青光眼、严重的并发性白内障。高血压视网膜病变分为四期:1期,视网膜动脉管径变细,动静脉比例1:2或1:3,动脉痉挛或狭窄,管径粗细不均;2期,视网膜动脉反光增强呈铜丝状、银丝状,并出现动静脉交叉压迫征;3期,视网膜血管内屏障破坏,出现视网膜水肿、出血、硬性渗出、棉绒斑;4期,又称恶性高血压,除了视网膜出血、渗出外,出现视盘水肿,严重时可出现渗出性视网膜脱离。
1.3 检查方法
所有患者均经风湿免疫科确诊,并定期进行血沉、C反应蛋白、血管超声等检查。所有患者均进行常规眼科检查,包括视力、最佳矫正视力(Best corrected visual acuity,BCVA)、眼压、裂隙灯照相、散瞳眼底检查、眼底照相、光学相干断层成像(optical coherence tomography,OCT)、血流OCT(OCTA)、眼底荧光素钠血管造影(fundus fluorescein angiography,FFA)等检查。
2 结果
2.1 多发性大动脉炎临床分型及全身表现
14例患者中,Ⅰ型7例(50%),Ⅱ型2例(14.3%),Ⅲ型0例,Ⅳ型5例(35.7%),均为头臂动脉联合胸腹主动脉型。受累动脉中,头臂干受累共1 2例(85.7%),腹主动脉干5例(35.8%),肾动脉4例(28.6%),肠系膜动脉2例(14.3%),髂动脉1例(7.1%)。就诊于眼科时,患者红细胞沉降率(血沉)6~121 mm/h,其中血沉正常者4例。
患者全身表现多样(表1),全身症状的病程为6个月~37年。除发热、皮疹等非特异表现外,比例最高的系统表现是上肢低血压、脉搏细弱或无脉,占全部患者人数的64.3%,均见于Ⅰ型及Ⅳ型患者,Ⅱ型患者则可能出现上肢高血压。伴随肢体血压的变化,35.6%的患者主诉手脚冰冷、四肢麻木,1例Ⅱ型患者出现跛行现象。在本组病例中,各型患者均有出现严重心脑血管并发症的病例,占患者总人数的28.6%。
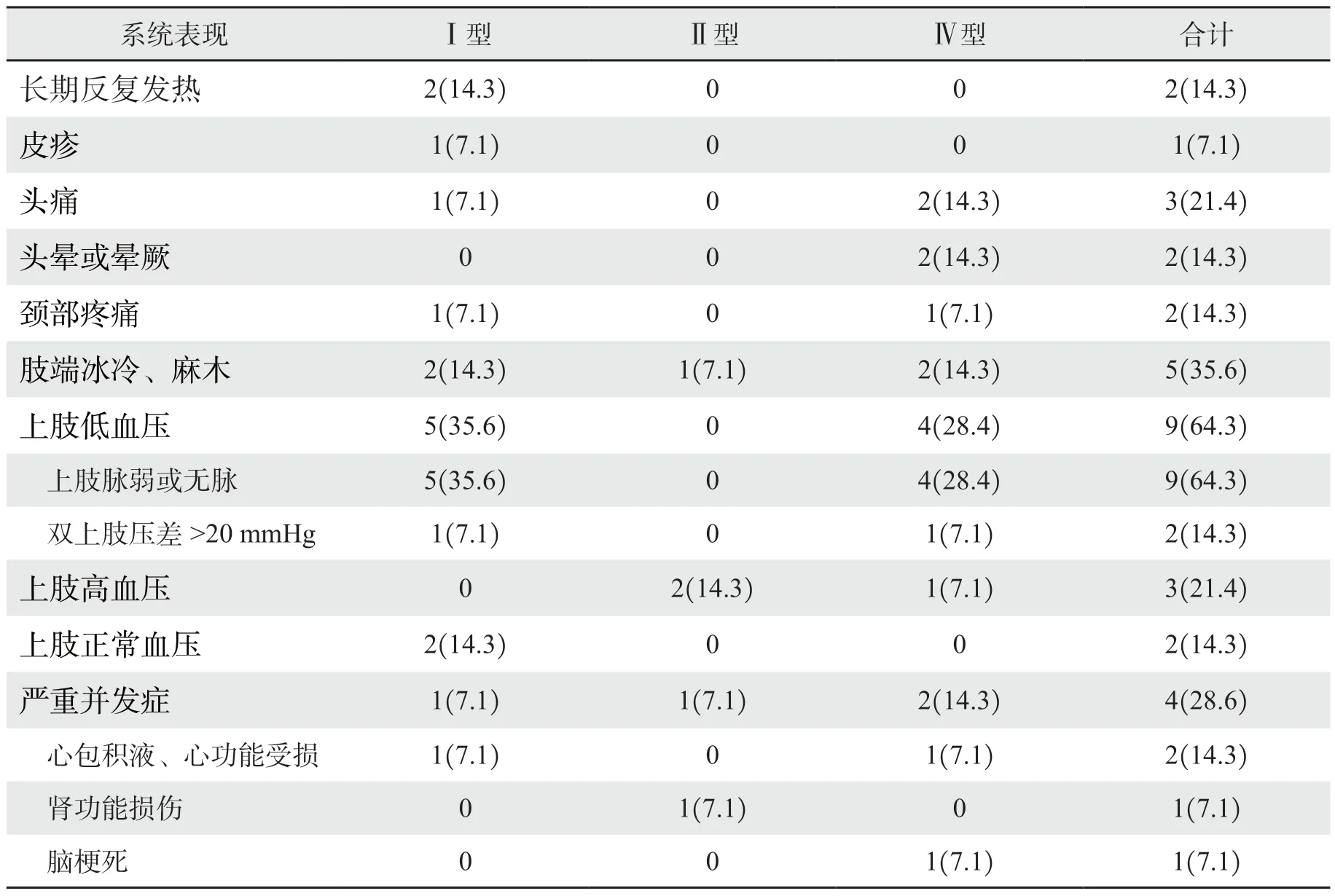
表1 不同临床分型多发性大动脉炎患者的全身表现[n(%)]Table 1 Systemic symptoms of Takayasu arteritis [n(%)]
2.2 多发性大动脉炎的眼部表现
本组有5例(35.7%)患者以眼部症状为首发表现并首诊于眼科。其中,3例(21.4%)为单眼无痛性视力下降,视力手动/20 cm~0.2。其中,1例外院首诊为“右眼白内障,视网膜病变”,先后行白内障手术及视网膜光凝治疗,视力不提高;2例外院首诊为单眼“白内障”,白内障手术后视力不提高且出现反复发作的前房炎症反应,需长期应用糖皮质激素及非甾体抗炎滴眼液,后经眼底及全身检查后确诊为TA;1例首发症状为双眼阵发性黑蒙,每日多次发作,持续数十秒至数分钟,活动后加重;1例首诊时即光感丧失,曾诊断为“右眼角膜变性、白内障、陈旧性视网膜脱离”。
TA患者有很高的眼部受累比例,在本组患者中,仅2例患者尚未出现眼部病变,其中Ⅰ型、Ⅳ型患者各1例,占全部患者的14.3%。其余12例患者共24眼(85.7%)有多种多样的眼部异常体征,各型患者的眼部表现详见表2。在28眼中,21眼(75%)BCVA≥1.0,4眼视力严重受损,BCVA低于0.1(14.3%),且均为Ⅰ型及Ⅳ型患者。
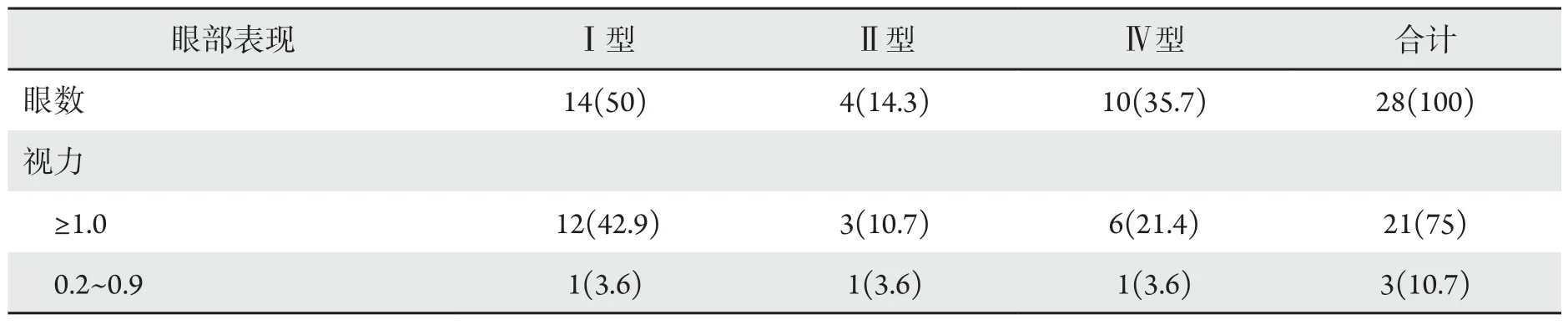
表2 不同临床分型多发性大动脉炎患者的眼部表现[眼数(%)]Table 2 Ocular manifestations of Takayasu arteritis [eyes(%)]
如表2所示,本组病例Ⅱ型患者眼部受累程度较轻,仅表现为轻度白内障和早期高血压视网膜病变。Ⅰ型和Ⅳ型患者多出现典型的TA相关眼部表现,其中最常见的眼前节表现(图1)为晶体异常(28.6%)和结膜巩膜血管扩张(17.9%)。另外,眼前节严重缺血导致的瞳孔散大和虹膜萎缩也是较常见的前节异常。Ⅰ型、Ⅳ型患者中,除各有1例患者无明显眼部受累、1例Ⅳ型患者表现为1期高血压视网膜病变外,其他患者均伴有不同程度的Takayasu视网膜病变,是本研究中最常见的眼底表现(71.4%)。其中9眼为严重的3期至4期病变(32.1%),表现为周边视网膜血管闭塞及动静脉异常吻合、后极花冠状血管环、视盘新生血管、玻璃体视网膜增殖等(图2)。
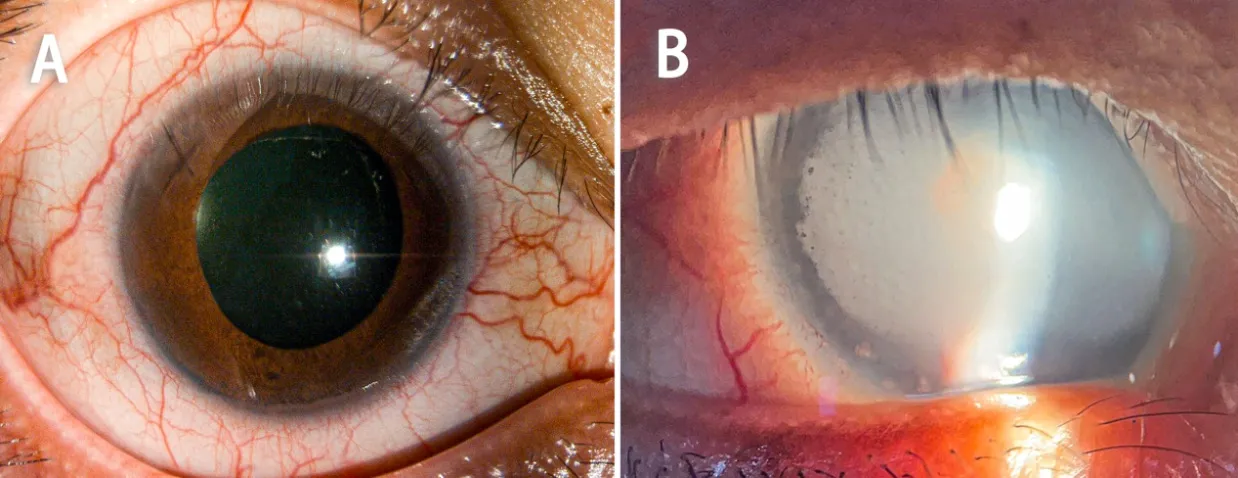
图1 多发性大动脉炎患者的眼前节表现Figure 1 Ocular anterior segment manifestations of Takayasu arteritis
在14例患者中,21眼完成眼底血管造影检查,17眼(81%)出现FFA异常,其中1例Ⅱ患者为双眼高血压视网膜病变,其余15眼(71.4%)为程度不等的Takayasu视网膜病变(图3、4):9眼(42.9%)视网膜血管充盈迟缓,充盈时间32~195 s;10眼视网膜后极及周边可见微血管瘤、无灌注区、异常动静脉吻合和交通支形成(47.6%),微血管瘤周边部较密集,周边血管中断及异常交通支附近最明显;3眼出现视盘周围典型的花冠状血管(14.4%);3眼视盘新生血管(14.4%),2眼视网膜新生血管(9.6%);12眼造影晚期视网膜血管壁染色、荧光素渗漏(57.1%)。其中,在BCVA为1.0的16眼中,9眼(56%)已出现程度不同的眼底造影改变。
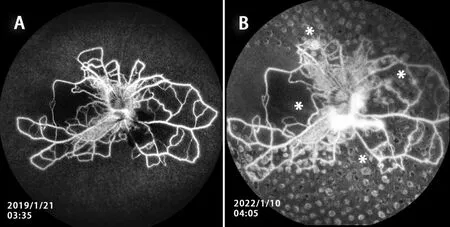
图3 多发性大动脉炎患者典型的花冠状血管吻合FFA表现及其发展变化Figure 3 Representative FFA images of wreath-like anastomosis in a TA patient and the progression of the disease
2.3 多发性大动脉炎患者的治疗
所有患者经风湿免疫科确诊后,均长期应用中、小剂量糖皮质激素,联合免疫抑制剂及阿司匹林等抗血小板聚集药物,其中2例患者应用甲氨蝶呤、3例应用环孢素、8例应用吗替麦考酚酯,2例联合应用生物制剂阿达木单抗。3例患者在长期治疗过程中,反复多次病变活动及复发。经眼部检查后,1例患者因“孔源性视网膜脱离”行左眼玻璃体切割视网膜复位术;2例2眼患者视网膜周边格子样变性区及干性裂孔周围行视网膜光凝;1例患者因视盘、视网膜新生血管行抗VEGF药物玻璃体腔注射1次及全视网膜光凝术,术后视盘新生血管渗漏明显减轻,视网膜新生血管消退;2例患者行周边无灌注区视网膜光凝;上述患者随访至今病变稳定。另2例患者共3眼因视网膜大范围无灌注区、花冠状血管环伴视盘或视网膜新生血管形成,行全视网膜光凝术,术后新生血管消退,但随访过程中,可见视网膜循环时间延长(图4),并观察到视网膜残余血管分支进行性闭塞的现象(图3)。1例患者拒绝激光治疗,其余患者予以临床观察随访。
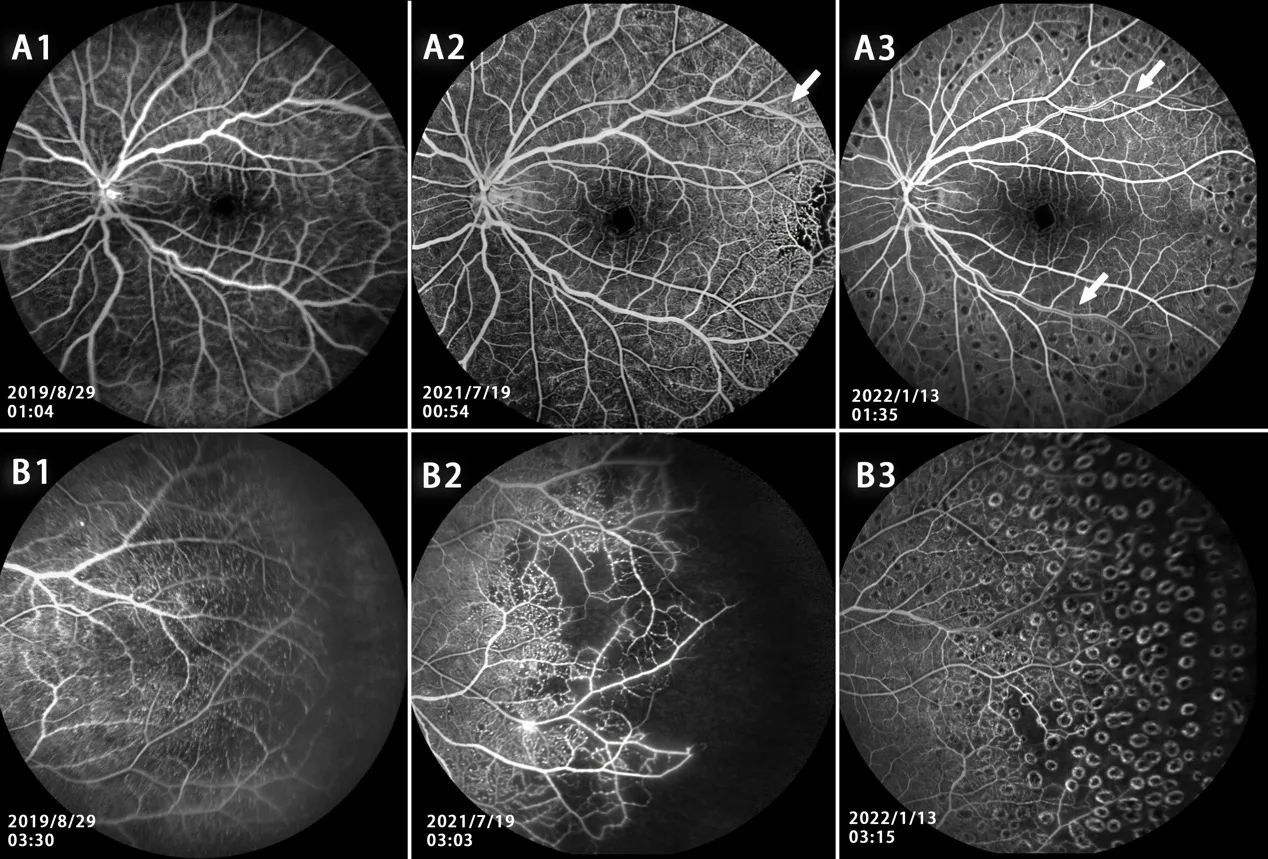
图4 多发性大动脉炎患者Takayasu视网膜病变及其发展变化的FFA表现Figure 4 Representative FFA images for Takayasu retinopathy and the progression of the disease
3 讨论
TA是一种罕见的、以主动脉弓及其分支等大中血管为靶点的慢性血管炎性疾病,发病率约0.004%[2]。动脉壁全层炎症导致管腔狭窄至闭塞,晚期出现管壁纤维化、假性动脉瘤或夹层,严重者管壁破裂危及生命[3]。TA多见于东亚及中东地区20~30岁的年轻女性[4,5],男女患病比例约 1∶4至1∶12[6-8]。本组14例患者中,女性13例,雌激素促进多种炎症因子及自身抗体的产生,上调免疫递呈细胞活性,刺激血管炎加重,可以部分解释大动脉炎的典型性别差异[9-10]。
本组患者系统表现轻重不一,与受累血管的部位和程度密切相关。早期患者可仅表现为发热、乏力等非特异症状,随着不同部位大血管阻塞加重,患者逐渐出现相应症状。TA发病率低,以往的回顾性研究中,各临床分型所占比例有很大不同[11-15]。本组患者85.7%累及头臂动脉,患者主要表现为头部及上肢缺血,最典型的体征是桡动脉搏动减弱或无脉、上肢低血压,可伴头颈部疼痛、头晕甚至晕厥。当双上肢血管炎症程度不等时,可出现双侧血压差>20 mmHg。由于患者多为既往无重大疾病的年轻女性,此时仍易漏诊。Ⅱ型患者腹腔动脉受累,主要表现为下肢缺血如足背动脉减弱或间歇性跛行,而且发病更为隐匿、影响患者就诊和确诊时间,这可能是本组Ⅱ型比例较低的原因之一。既往研究发现,TA中男性患者仅占很低的比例,但是腹腔动脉更容易受累,肾性高血压及心脑意外的发生率更高[8]。本研究中仅1例21岁男性患者,头臂动脉及肾动脉均受累,已出现高血压、心包积液、心功能受损、胸腔积液和脑梗,与文献报道一致。无论何种分型,血管重度阻塞最终将导致严重的心脑血管并发症,患者15年生存率显著降低[13]。本组患者严重并发症发生率28.6%,早期诊断和规范治疗对患者的长期存活极其重要。
TA患者早期诊断率较低,长期血管病变导致眼部受累率高达33%~67%[12,16-17],是其临床特点之一。本组病例头臂干受累率高,长期颈内动脉狭窄或闭塞致眼部灌注压降低。严重的眼前段缺血可导致一系列表现,如结膜及浅层巩膜血管代偿性扩张、慢性充血;重度虹膜缺血导致瞳孔括约肌麻痹、瞳孔散大伴虹膜萎缩;睫状体缺血导致房水分泌减少和低眼压;长期眼前段缺血导致晶体代谢障碍,患者出现不明原因的白内障,与本组患者最常见的眼前节表现一致。在眼底,视网膜中央动脉灌注压降低后首先发生毛细血管代偿性扩张,为1期Takayasu视网膜病变;随后周边小动脉逐步闭塞,出现大量微血管瘤及无灌注区,是2期病变的特征;无灌注区自周边向后极进展,缺血边缘出现代偿性动静脉吻合,最终形成本病最为典型的以视盘为中心、环形或花冠状分布的吻合支,是3期病变的特点,也是TA最典型的眼底表现;缺血持续进展,则出现新生血管性青光眼、增殖性玻璃体视网膜病变等4期病变,视功能严重受损。本研究结果显示,眼底病变类型与疾病分型密切相关:Ⅰ型患者上肢低血压,较Ⅱ型患者更易发生Takayasu视网膜病变;Ⅱ型患者因上肢高血压发生高血压视网膜病变;Ⅳ型患者同时累及多处血管,可能出现上述两种病变。以上结果说明TA患者眼底病变与疾病分型关系密切,临床表现取决于受累血管的位置和病变程度。
本研究中85%患者已存在眼部异常,说明大部分患者实际病程已经较长,TA早期诊断率并不理想。视网膜花冠状血管虽然极具特征性,但由于早期周边视网膜缺血对视力影响小,眼底病变容易被遗漏。相比而言,眼前段缺血引发的白内障、充血及瞳孔散大则相对较容易被发现。本组病例中,5例(35.7%)患者首诊于眼科,但均未被眼科医生正确识别原发疾病。3例曾误诊为单眼“白内障”并行手术治疗,术后视力不改善,且出现持久的前房反应,才确诊TA,这种情况文献中也有多次报道[13,18-20],需要引起眼科医生的高度重视。研究证实,40.5%TA患者因白内障发生视力下降,是TA影响视力的首要原因[14,21],若眼科医生对疾病特点认识不足,极易漏诊误诊。因此,临床上遇到年轻女性出现不明原因的白内障、伴或不伴瞳孔散大及眼部充血、或白内障术后视力改善不良、或出现视网膜低灌注病变时,应考虑到有TA可能,尽早进行血沉、C反应蛋白、血管超声及DSA等检查以明确诊断。
由于病变部位和程度、诊断和治疗时机有很大的区别,TA患者眼部表现具有多样性,同一患者双侧血管阻塞程度不等时,双眼也存在较大的临床表现差异。同时,视力与眼部病情严重程度也不完全成正比,特别是视网膜病变尚未累及后极时。本组患者中,75%患者BCVA≥1.0,但眼部未受累的患者仅占14.3%;在视力正常的病例中,56%已出现视网膜病变,急需治疗。因此,所有疑似或诊断为TA的患者,均应仔细观察眼底,并行FFA检查或广角OCTA检查,便于正确诊断和评估病情。
TA的治疗方法包括皮质类固醇、免疫抑制剂、抗凝药、生物制剂及手术治疗。传统药物治疗效果并不理想,难以防止复发[22],靶向生物制剂及血管介入手术主要用于临床重症患者。眼部治疗中,最重要的是针对无灌注区进行视网膜光凝,减少缺血、缺氧带来的严重后果。目前抗VEGF药物也开始用于TA相关视网膜病变的治疗[18,23],可快速消退视盘及视网膜新生血管,同时并未发现血流灌注情况的恶化。对于重症患者,研究发现,介入手术后80%以上患者视力稳定或提高,因此主张对急慢性视力丧失,或矫正视力>0.1、同时伴重度大血管闭塞的患者可适时考虑介入手术[18]。在本研究中,所有病例均长期应用糖皮质激素、免疫抑制剂等药物,但仍有患者动脉炎反复发作;针对眼部病变进行PRP等治疗后,大多数患者病情好转或稳定,但仍有3眼出现视网膜循环时间延长,残余血管进行性闭塞的现象(图3、图4),可见治疗的长期性和艰巨性,未来需要考虑尽早联合生物制剂甚至介入手术;也说明TA患者需终生随访,及时发现病情变化,最大程度延缓患者视功能损伤。另外,有患者出现视网膜干性裂孔及孔源性视网膜脱离,一方面可能与近视相关,另一方面,缺血加剧视网膜萎缩,更易发生周边裂孔和视网膜脱离。因此,除了典型的低灌注视网膜病变外,其他并发的眼部异常也需要引起关注并进行同步处理。
总之,TA比较罕见,发病隐匿,临床表现多样,往往在长期缺血导致严重功能障碍时才被发现。其眼部表现虽极具特点,但漏诊误诊率较高。广大眼科医生仍需提高对该疾病的警惕性,对年轻女性患者不明原因的视力下降及低灌注性眼部损伤,应及时进行大动脉炎的排查,以利于患者早期诊断和治疗。
利益冲突所有作者均声明不存在利益冲突
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。详情请访问:https://creativecommons.org/licenses/by-ncnd/4.0/。

