UPLC-Q-Exactive-MS/MS测定伤痛宁胶囊中马兜铃酸Ⅰ的含量
朱立华,黄生武,沈冰冰,谢谊

〔摘要〕 目的 建立UPLC-Q-Exactive-MS/MS测定伤痛宁胶囊中马兜铃酸Ⅰ的含量。方法 采用Hypersil GOLD C18色谱柱(2.1 mm× 50 mm,1.9 μm),流动相为乙腈和0.1%甲酸水溶液(含5 mmol/L甲酸铵),梯度洗脱,流速0.5 mL/min,柱温30 ℃。采用电喷雾离子源正离子模式,进行平行反应监测模式,选择质荷比(m/z)359.0→298.0和359.0→296.0离子对进行监测。结果 马兜铃酸Ⅰ在0.06~0.2 ng范围内线性关系良好(R2=0.999 5),精密度和稳定性的RSD值均小于3%,加样回收率均值为104.1%(RSD=4.29%)。不同批次伤痛宁胶囊样品中马兜铃酸Ⅰ的含量均值为0.000 004 90%,从药材到成品的转移率均值为103.7%,RSD值为19.5%。结论 该方法专属性好,灵敏度高,准确可靠、耐用,可以用于伤痛宁胶囊中马兜铃酸Ⅰ的含量测定。
〔关键词〕 伤痛宁胶囊;马兜铃酸Ⅰ;UPLC Q-Exactive MS/MS;定量分析
〔中图分类号〕R284 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2023.08.011
Determination of aristolochic acid Ⅰ in Shangtongning
Capsule by UPLC-Q-Exactive-MS/MS
ZHU Lihua1, HUANG Shengwu1, SHEN Bingbing2, XIE Yi2*
1. Hunan Guohua Pharmaceutical Co., Ltd., Changsha, Hunan 410013, China;
2. Hunan Academy of Chinese Medicine, Changsha, Hunan 410013, China
〔Abstract〕 Objective To develop a method of UPLC-Q-Exactive-MS/MS for the determination of aristolochic acid Ⅰ in Shangtongning Capsule. Methods The chromatography was performed on Hypersil GOLD C18 column (2.1 mm×50 mm, 1.9 μm) with mobile phases consisting of acetonitrile and 0.1% formic acid aqueous solution (containing 5 mmol/L ammonium formate) at a gradient elution rate of 0.5 mL/min, and the column temperature was 30 ℃. Electrospray ionization in positive ionization mode was used for parallel reaction monitoring, and ion pairs with mass-to-charge ratios (m/z) of 359.0→298.0 and 359.0→296.0 were selected for monitoring. Results Aristolochic acid Ⅰ had a good linear relationship in the range of 0.06-0.2 ng (R2=0.999 5), RSDs of precision and stability were less than 3%, and the average recovery was 104.1% (RSD=4.29%). The average content of aristolochic acid Ⅰ in different batches of Shangtongning Capsule was 0.000 004 90%, the mean transfer rate from medicinal materials to finished products was 103.7% and RSD was 19.5%. Conclusion With high specificity, sensitivity, and accuracy, the method is reliable and reproducible, and can be used for the determination of aristolochic acid Ⅰ in Shangtongning Capsule.
〔Keywords〕 Shangtongning Capsule; aristolochic acid Ⅰ; UPLC-Q-Exactive-MS/MS; quantitative analysis
傷痛宁胶囊是由制乳香、制没药、甘松、醋延胡索、细辛、醋香附、山柰和白芷8味药组成,是《中华人民共和国药典》(2020年版)收录品种“伤痛宁片”的剂改品种[1],具有散瘀止痛功效,主要用于跌打损伤、闪腰挫气等[2]。现代药理动物实验和人体临床病例都已经证明,细辛中马兜铃酸类物质具有肾毒性、致癌和致突变作用[3-6],2020年版《中华人民共和国药典》也规定了马兜铃酸Ⅰ的限量标准(不得超过0.001%)。因此,为了保证用药安全,对含马兜铃酸类物质的中药复方进行含量检测是非常必要的。
目前,有关马兜铃酸类成分的检测方法主要有高效液相色谱法、液质联用色谱法等[7-11]。近些年来,液相质谱联用技术发展迅速,已成为中药及复方研究的强大分析工具[12-13]。超高液相色谱分析时间短,对复杂样品的高分离能力与质谱的高选择性、高灵敏度,以及提供相对分子质量与结构信息的优点结合起来,在医药分析、食品安全和环境分析等领域获得了广泛的应用[14-16]。因此,本研究在原注册标准基础上进行提升,通过建立UPLC-Q-Exactive-MS/MS测定伤痛宁胶囊中马兜铃酸Ⅰ含量的方法,为伤痛宁胶囊的安全性提供科学依据。
1 仪器与试剂
Thermo Q-Exactive型液质联用色谱仪(美国赛默飞公司);Mettler Toledo AL-204型电子天平、Mettler Toledo XPE-105型电子天平[梅特勒托利多科技(中国)有限公司];KM-500DB型中文液晶台式超声波清洗器(昆山美美超声仪器有限公司);乙腈色谱纯(德国Merck公司);甲酸色谱纯[阿拉丁试剂(上海)有限公司];纯净水[华润怡宝饮料(中国)有限公司];其余试剂均为分析纯。马兜铃酸Ⅰ(中國食品药品检定研究院,批号:110746-201912,纯度为99.1%);甲酸铵(美国ACS恩科化学试剂公司,批号:AF-6266-0025)。细辛药材(批号:B24-1811-007、ZY-026P-2204-002、ZY-026-2204-004和ZY-026-2212-001~ZY-026-2212-005)和伤痛宁胶囊(批号:S-20200801~S-20200803、220501~220503、220901、20230201~20230205)由湖南国华制药有限公司提供。
2 方法与结果
2.1 色谱条件
Hypersil GOLD C18色谱柱(2.1 mm×50 mm,1.9 μm),流动相A为乙腈,B为0.1%甲酸水溶液(含5 mmol/L甲酸铵),梯度洗脱(0~10 min,62%~55% B);流速0.5 mL/min,柱温30 ℃,进样量5 μL。
2.2 质谱条件
四极杆/静电场轨道肼质谱检测器;电喷雾离子源;检测方式:正离子模式;范围:100~1 500 m/z;喷雾电压:3.5 kV,鞘气体积流量为35 arb,辅助体积流量为10 arb,辅助气温度375 ℃。毛细管温度320 ℃,二级碰撞能量:10 eV。扫描方式采用全扫描一级质谱、特征离子扫描一级质谱,平行反应监测。
2.3 溶液的制备
2.3.1 马兜铃酸Ⅰ标准品的配制 取标准品适量,精密称定,加70%甲醇制成每1 mL含20 ng的溶液,作为对照品溶液。
2.3.2 伤痛宁供试品溶液 取伤痛宁胶囊样品适量,研细,混匀,精密称取1.0 g,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定重量,超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
2.3.3 细辛样品溶液 取细辛粉末(过三号筛),精密称取0.5 g,置具塞锥形瓶中,精密加入70%甲醇50 mL,密塞,称定重量,超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
2.3.4 缺细辛阴性样品溶液 取除细辛外的其余处方量药材,按生产工艺制成阴性样品,取适量研细,混匀,精密称取1.0 g,置具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定重量,超声处理(功率250 W,频率40 kHz)30 min,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
2.4 方法学考察
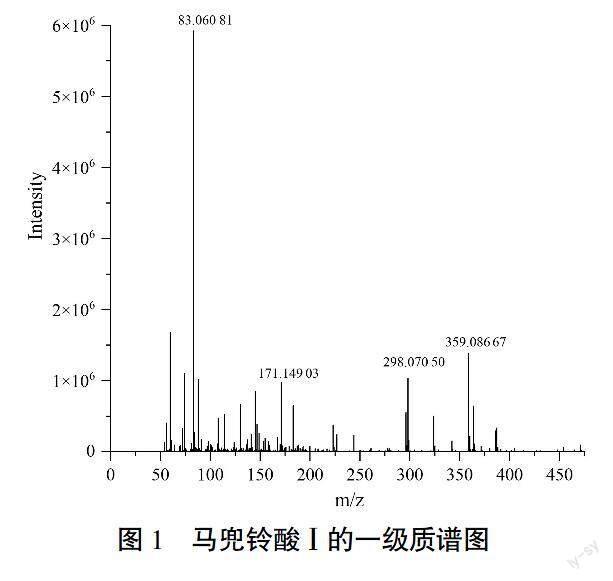
2.4.1 马兜铃酸Ⅰ检测离子对的选择 通过优化流动相,确定马兜铃酸Ⅰ标准品在0.1%甲酸水溶液(含5 mmol/L甲酸铵)条件下的质谱响应较高,尤其是正模式下分子离子峰359.086 67[M+NH4]+(图1)。在二级质谱图中,主要产生298.070 62[M+H-CO2]+、296.067 26[M+H-NO2]+、281.068 12[M+H-CO2-H2O]+、265.037 05[M+H-NO2-OCH3]+等碎片离子,其中298.070 62的响应最高,作为定量离子,296.067 26可作为定性离子(图2)。
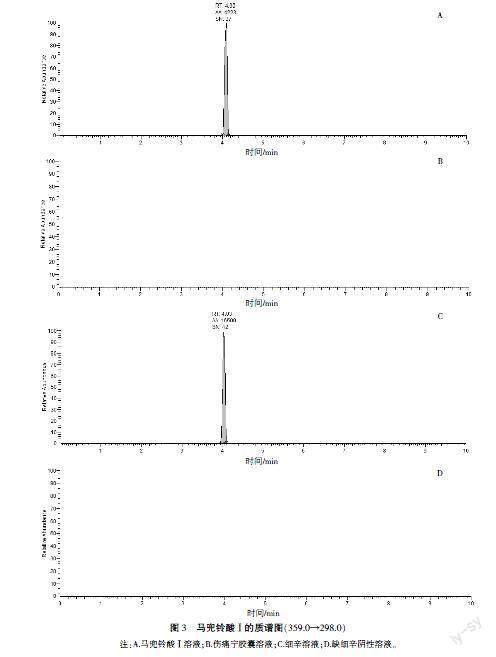
2.4.2 专属性 按照“2.1”项下色谱条件和“2.2”项下质谱条件,将马兜铃酸Ⅰ对照品溶液、伤痛宁胶囊溶液、细辛溶液和缺细辛阴性对照溶液分别进样,记录质谱色谱图并积分,结果显示在缺细辛阴性对照溶液的图谱中,与马兜铃酸Ⅰ对照品溶液保留时间相同的位置上未显示色谱峰。详见图3。
2.4.3 检出限 取马兜铃酸Ⅰ标准品溶液逐步稀释,以S/N=3∶1计算,得到马兜铃酸Ⅰ的检出限为1 pg。
2.4.4 线性关系 取同一马兜铃酸Ⅰ标准品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件,分别进样3、4、5、6、8、10 μL,记录质谱色谱图并积分,以马兜铃酸Ⅰ的峰面积为Y,马兜铃酸Ⅰ的量(ng)为X进行线性回归,得到回归方程Y=115 901X-5 480.8(R2=0.999 5)。结果表明,马兜铃酸Ⅰ在0.06~0.2 ng范围内线性关系良好。
2.4.5 精密度 取同一马兜铃酸Ⅰ标准品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件连续进样6次,记录质谱色谱图并积分,结果显示马兜铃酸Ⅰ峰面积的RSD为2.78%,试验表明本方法精密度良好。
2.4.6 稳定性 取同一马兜铃酸Ⅰ标准品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件分别在0、2、4、6、8 h进样,记录质谱色谱图并积分,结果马兜铃酸Ⅰ峰面积的RSD为1.92%,试验表明本方法在8 h内稳定性良好。
2.4.7 加样回收率 精密称取同一伤痛宁胶囊制备供试品溶液,分别加入马兜铃酸标准品溶液(100 ng/mL)6.5、5、3.5 mL,按方法“2.3.2”项下处理供试品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件依次进样,记录质谱色谱图并积分,结果如表1所示,加样回收率为104.1%(RSD=4.29%),试验表明本方法加标回收率较好。
2.4.8 样品检测 (1)细辛药材马兜铃酸Ⅰ含量的检测:按“2.3.3”项下方法处理供试品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件依次进样,记录质谱色谱图并积分。计算8批细辛药材马兜铃酸Ⅰ的含量均值为0.000 107%,小于《中华人民共和国药典》规定的0.001%[1]。详见表2。
(2)伤痛宁胶囊马兜铃酸Ⅰ含量的检测:按“2.3.2”项下方法处理供试品溶液,按照“2.1”项下色谱条件和“2.2”项下质谱条件依次进样,记录质谱色谱图并积分,计算伤痛宁胶囊中马兜铃酸的含量和转移率。详见表2。
3 讨论
根据国内外学者对马兜铃酸类成分的详细研究,已证实马兜铃酸具有肾毒性和致癌性,大量服用可能会引起急性马兜铃酸肾病,出现急性肾小管坏死、急性肾衰竭等病理变化[17-19]。我国自2003年起,就已经对含马兜铃酸的药材及中成药采取了包括禁止使用马兜铃酸含量高的关木通、广防己和青木香;调整药材使用部位,将细辛的药用部位由全草改为根和根茎等一系列风险控制措施[18]。因此,必须对含有马兜铃酸药材作为原料生产的产品进行检查,进一步加强检测检验。目前,马兜铃酸Ⅰ的经典检测方法主要是紫外分光光度法、色谱法和色谱-质谱联用法,其中色谱-质谱联用法是将液相色谱的高效分離技术和质谱的快速定性、定量技术相结合的一种重要的分析方法,具有操作简单、高效灵敏、准确可靠等优点,因此,常被用于中药(复方)中化合物的快速定性定量分析[20]。另外,还有一些新型的快速检测方法被报道,例如荧光探针法[21]、酶联免疫吸附法[22]、近红外光谱法[23]等。本研究对象伤痛宁胶囊中存在含有马兜铃酸类成分的药材细辛,并且复方化学类型多样,成分复杂,常见的紫外检测器等灵敏度难以满足要求,因此,准确性、选择性和灵敏度更高的液质联用法是首选。马兜铃酸Ⅰ化合物是弱极性的小分子化合物,在电喷雾离子源质谱中的离子化效率不高。前期通过参考文献[24-25]和单因素考察实验,发现马兜铃酸Ⅰ在流动相中加入5 mmol/L甲酸铵的情况下出现分子离子峰359.0[M+NH4]+,且响应最高。因此,采用电喷雾离子源正离子模式,进行平行反应监测模式,选择质荷比(m/z)359.0→298.0和359.0→296.0离子对进行监测。
因此,建立了UPLC-Q-Exactive-MS/MS测定伤痛宁胶囊中马兜铃酸Ⅰ含量的方法。该方法在0.06~0.2 ng范围内线性关系良好(R2=0.999 5),精密度、稳定性的RSD均小于3%,加样回收率在99.75%~110.96%范围内,RSD为4.29%,适合马兜铃酸Ⅰ的检测。细辛样品检测马兜铃酸Ⅰ的含量均远小于《中华人民共和国药典》2020年版[1]规定的限量要求(不得超过0.001%)。伤痛宁胶囊中16 g细辛药材制成1 000粒(每粒0.33 g),经药味分析每克胶囊样品含细辛药材0.048 g,根据《中华人民共和国药典》2020年版[1]规定细辛药材中马兜铃酸Ⅰ的限量,按照100%的转移率可知,伤痛宁胶囊中马兜铃酸Ⅰ的限量应不得超过0.000 048%。伤痛宁胶囊成品中6批未检测出马兜铃酸Ⅰ,其余6批马兜铃酸Ⅰ的含量均值为0.000 004 90%,从药材到成品的转移率均值为103.7%,RSD值为19.5%,含量均远小于0.000 048%的限量,是合格的、安全的。综上所述,该方法专属性好,灵敏度高,准确可靠、耐用,可以用于伤痛宁胶囊中马兜铃酸Ⅰ的含量测定。本研究不仅为伤痛宁中马兜铃酸Ⅰ的限量检查提供了数据支撑,也为伤痛宁胶囊中细辛的合理、安全使用提供了科学依据。
参考文献
[1] 国家药典委员会. 中华人民共和国药典: 2020年版一部[M]. 北京: 中国医药科技出版社, 2020.
[2] 肖德华. 伤痛宁胶囊质量标准研究[J]. 湖南中医杂志, 2005, 21(4): 72-74.
[3] HAN J Y, XIAN Z, ZHANG Y S, et al. Systematic overview of aristolochic acids: Nephrotoxicity, carcinogenicity, and underlying mechanisms[J]. Frontiers in Pharmacology, 2019, 10: 648.
[4] ZHANG H M, ZHAO X H, SUN Z H, et al. Recognition of the toxicity of aristolochic acid[J]. Journal of Clinical Pharmacy and Therapeutics, 2019, 44(2): 157-162.
[5] LU Z N, LUO Q, ZHAO L N, et al. The mutational features of aristolochic acid-induced mouse and human liver cancers[J]. Hepatology, 2020, 71(3): 929-942.
[6] 郭 宁, 赵 雍, 孙 奕, 等. 马兜铃酸类物质的生物标记物与减毒策略研究进展[J]. 药学学报, 2021, 56(4): 972-982.
[7] 顾从文, 卜 超, 王学芹, 等. 复方辛夷滴鼻液的指纹图谱及7种成分含量测定研究[J]. 湖南中医药大学学报, 2022, 42(6): 934-940.
[8] 梁诗瑶, 刘倩倩, 黄 胜, 等. 六味地黄丸药渣中4种活性成分含量测定及抗氧化活性研究[J]. 湖南中医药大学学报, 2021, 41(5): 707-713.
[9] 刘 静, 刘 阳, 武营雪, 等. 液质联用法测定齿痛消炎灵颗粒中马兜铃酸Ⅰ和马兜铃内酰胺Ⅰ[J]. 药物分析杂志, 2022, 42(2): 237-242.
[10] 米士丽, 施海蔚, 谭 力, 等. 9种含马兜铃酸类毒性物质中药材中马兜铃酸类成分的定性与定量分析[J]. 药学学报, 2021, 56(7): 1980-1987.
[11] 袁金斌. 马兜铃酸类物质的液相色谱联用技术及应用[D]. 长沙: 湖南大学, 2008.
[12] 陈明曦, 李艳梅, 孙 婷, 等. 液相色谱-质谱联用技术在中药质量研究中的应用[J]. 中国药剂学杂志, 2021, 19(1): 12-17.
[13] 王 迪, 俞 佳, 詹 固, 等. 液质联用技术在中药研究中的应用进展[J]. 中华中医药学刊, 2022, 40(2): 68-71.
[14] 王郡瑶, 程显隆, 李明华, 等. 液质联用数据库技术的研究进展及其在中药分析领域的应用[J]. 药物分析杂志, 2021, 41(7): 1107-1113.
[15] 張朝辉, 周娜姣, 刘 星, 等. 药品、环境和食品中马兜铃酸分析检测方法的研究进展[J]. 分析化学, 2021, 49(11): 1792-1803.
[16] MARTINS DE BARROS R, LISSALDE S, GUIBAL R, et al. Development of a multi-hormone analysis method by LC-MS/MS for environmental water application using diffusive gradient in thin films[J]. Talanta, 2022, 243: 123390.
[17] 邵 鑫, 张 月, 郑雁雪, 等. 中药中马兜铃酸快速检测及分离技术研究进展[J]. 中草药, 2022, 53(19): 6200-6212.
[18] 田婧卓, 梁爱华, 刘 靖, 等. 从马兜铃酸含量影响因素探讨含马兜铃酸中药的风险控制[J]. 中国中药杂志, 2017, 42(24): 4679-4686.
[19] LU Z N, LUO Q, ZHAO L N, et al. The mutational features of aristolochic acid-induced mouse and human liver cancers[J]. Hepatology, 2020, 71(3): 929-942.
[20] 邵 鑫, 张 月, 郑雁雪, 等. 中药中马兜铃酸快速检测及分离技术研究进展[J]. 中草药, 2022, 53(19): 6200-6212.
[21] 欧爱芬. 马兜铃酸Ⅰ抗体识别特性及快速免疫分析方法研究[D]. 广州: 广东工业大学, 2022.
[22] LI S Z, WU X L, SONG S S, et al. Development of ic-ELISA and an immunochromatographic strip assay for the detection of aristolochic acid Ⅰ[J]. Food and Agricultural Immunology, 2019, 30(1): 140-149.
[23] CHEN X Y, CHAI Q Q, LIN N, et al. 1D convolutional neural network for the discrimination of aristolochic acids and their analogues based on near-infrared spectroscopy[J]. Analytical Methods, 2019, 11(40): 5118-5125.
[24] 陈奕君, 王 伟, 肖红斌. 基于液相色谱-质谱联用的清肺排毒汤中痕量马兜铃酸Ⅰ的监测及定量分析[J]. 药学学报, 2020, 55(8): 1903-1907.
[25] 刘 静, 刘 阳, 武营雪, 等. 液质联用法测定齿痛消炎灵颗粒中马兜铃酸Ⅰ和马兜铃内酰胺Ⅰ[J]. 药物分析杂志, 2022, 42(2): 237-242.
(本文编辑 周 旦)
——凹脉马兜铃

