A型主动脉夹层术后急性肾损伤危险因素与预测价值分析*
肖文彬,涂洪文,周 坤,蒋迎九
重庆医科大学附属第一医院胸心外科,重庆 400016
A型主动脉夹层是极为凶险的大血管急症,若未能及时手术,常常会因为大血管破裂或重要脏器缺血而导致患者死亡[1-2]。根据夹层破口的位置及病变累及部位的差异,可能需要采取不同的体外循环灌注方法和不同的手术方式治疗[3]。而术中诸多因素及术后并发症的发生同样可能会影响患者预后[4],甚至还会导致患者死亡。急性肾损伤(AKI)是A型主动脉夹层术后常见的并发症之一,有文献报道其发生率为6.7%~20.2%[5-6]。A型主动脉夹层术后发生AKI常常可以自行恢复,但有可能导致患者住院时间延长、增加医疗费用、死亡风险加大,并且还有2%~8%的患者需要进行肾脏替代治疗[7]。早期识别术后AKI高风险的患者并及时实施针对性保护策略十分重要,可明显减少中度或者重度AKI发生,缩短重症监护病房(ICU)滞留时间及总住院时间,从而改善患者预后[8-9]。为此,本研究探讨A型主动脉夹层术后发生AKI的危险因素及其对术后发生AKI的预测价值,现报道如下。
1 资料与方法
1.1一般资料 选取2015年1月至2021年12月入住本院行A型主动脉夹层手术的111例患者作为研究对象,按照术后是否发生AKI分为AKI组(69例)和无AKI组(42例)。所有研究对象均知情同意并签署知情同意书。本研究经本院医学伦理委员会审核通过。纳入标准:经CT血管照影(CTA)及超声心动图检查确诊为Stanford A型主动脉夹层,并在本院胸心外科接受手术治疗的患者。排除标准:既往有慢性肾衰竭(CRF)或存在自身免疫性肾病的患者;术中或术后48 h内死亡或自动出院的患者。AKI诊断标准:根据KDIGO指南[10],术后AKI定义为血清肌酐(SCr)由基础值增加1.5倍以上;或由基础值增加≥26.5 μmol/L;或连续6~12 h尿液<0.5 mL/(kg·h)。本研究采用患者入院第1天的SCr水平作为基础值,与术后48 h内复查的SCr比较,从而判断患者是否在术后发生了AKI。
1.2方法 收集所有患者资料,如:年龄、性别、体质量指数(BMI)、合并症(如高血压、糖尿病、心血管疾病等),以及术前白细胞计数、降钙素原(PCT)、清蛋白、肾功能指标水平;术中情况包括尿量、体外循环时间、主动脉阻断时间、深低温停循环时间、出血等;术后24 h内输血量、住院时间及随访30 d内病死率等。麻醉与手术方法:所有患者术前常规禁食、禁饮4 h,接送至手术室前给予吗啡镇静、镇痛。入室后建立静脉通路,连接监护仪,常规监测血压、心率、经皮脉搏血氧饱和度。麻醉诱导后行气管插管,采用容量控制呼吸,调节呼吸机参数。麻醉后行桡动脉(股动脉)穿刺监测血压及动脉血气指标。采用静脉+吸入复合麻醉,维持脑电双频指数。开始体外循环后,通过调节灌注量维持理想血压;术中深低温停循环期间保持单侧或双侧脑灌注。手术方式根据术前评估及术中探查夹层累及的范围,采用孙氏手术、Bentall手术、Wheat手术及David手术等。非体外循环期间在术中则通过补液、输注浓缩红细胞,以及给予去氧肾上腺素或麻黄碱控制或调整血压。术毕所有患者均保持气管导管,处于麻醉状态下返回ICU。
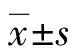
2 结 果
2.1AKI组和无AKI组临床资料比较 AKI组和无AKI组年龄、性别、BMI、基础病史,以及术前心功能分级、左室射血分数及合并症等比较,差异均无统计学意义(P>0.05);AKI组术前白细胞计数、PCT、SCr水平均明显高于无AKI组,差异均有统计学意义(P<0.05)。AKI组术中急诊手术占比高于无AKI组,体外循环总时间、主动脉阻断时间、深低温停循环时间均长于无AKI组,差异均有统计学意义(P<0.05);AKI组和无AKI组术中手术方式及出血量比较,差异均无统计学意义(P>0.05)。AKI组术后30 d内死亡人数虽稍多于无AKI组,但差异无统计学意义(P>0.05);AKI组和无AKI组术后24 h内输红细胞悬液量、尿量及总住院时间比较,差异均无统计学意义(P>0.05);而AKI组术后ICU滞留时间明显长于无AKI组,差异有统计学意义(P<0.05)。见表1。

表1 AKI组和无AKI组临床资料比较[n(%)或或M(P25,P75)]
2.2多因素Logistic回归分析 以术后是否发生AKI作为因变量,将表1中差异有统计学意义的指标(术前白细胞计数、PCT水平、SCr水平、术中急诊手术占比、体外循环总时间、主动脉阻断时间及深低温停循环时间均原值输入)作为自变量纳入多因素Logistic回归分析。结果显示,只有术前白细胞计数升高、术前PCT水平升高、术中深低温停循环时间增加是A型主动脉夹层术后发生AKI的独立危险因素(P<0.05)。见表2。
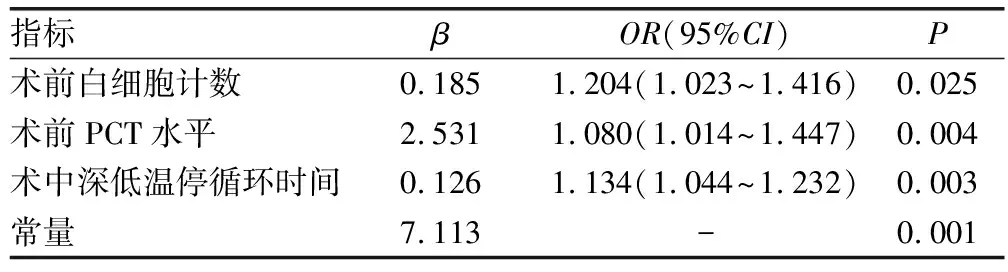
表2 多因素Logistic回归分析
2.3危险因素对术后发生AKI的预测价值 以发生AKI为阳性标本,未发生AKI为阴性标本,绘制ROC曲线分析术前白细胞计数、术前PCT水平、术中深低温停循环时间对术后发生AKI的预测价值。ROC曲线分析结果显示,术前白细胞计数、术前PCT水平、术中深低温停循环时间对A型主动脉夹层术后发生AKI的AUC分别为0.667、0.661、0.504,3项指标联合检测预测术后发生AKI的AUC为0.758。见表3。

表3 各独立危险因素及3项指标联合检测对术后发生AKI的预测价值
3 讨 论
A型主动脉夹层是心外科最凶险的疾病之一,其发展快,病死率高,常需要手术治疗挽救生命。然而,即使手术成功,术后各种并发症仍然会影响患者预后,其中最为常见的就是AKI。本研究结果显示,A型主动脉夹层术后AKI发生率为62.16%,与文献[6]报道的40.6%~71.4%相近。近年来,随着CTA、核磁共振在基层医院不断普及,以及各级医院对主动脉夹层的诊断率提高,A型主动脉夹层入院的数量及在心脏外科手术中的占比持续增长。因此,加强对患者术后发生AKI的危险因素进行筛查并采取相应策略,对降低术后发生AKI及改善患者预后具有重要意义。
A型主动脉夹层可以累及腹段主动脉进而影响肾动脉,造成直接性肾缺血,也可因为发生血流动力学改变影响肾脏血供而引起肾损伤;大范围血管内膜撕裂,组织细胞及血细胞破碎产物通过血液循环到达肾脏,亦可以造成AKI[11];机体各种代谢异常、血流动力学改变、炎症介质激活、氧化应激反应、神经内分泌激素等改变,也会进一步加快AKI发生[12]。主动脉夹层围术期合并肾功能受损时更易发生心功能不全、感染、呼吸衰竭等,再加上体外循环术后又常伴有电解质紊乱、酸碱平衡失调、容量高负荷等,从而增加病死率及医疗费用等[13]。本研究结果显示,AKI组术后ICU滞留时间长于无AKI组,说明术后发生AKI是影响主动脉夹层术后患者预后的相关危险因素,需要高度重视。
本研究结果显示,术前白细胞计数、PCT水平升高是A型主动脉夹层术后发生AKI的独立危险因素。主动脉夹层的形成必然带来不同程度和范围的血管内膜撕裂,产生大量组织细胞及血细胞破碎产物,通过血液循环到达肾脏,可能会对肾小管毛细血管造成直接损伤,从而引发AKI[14],亦可作为炎症反应始发因子激活炎症介质及氧化应激反应,从而导致术前白细胞计数、PCT水平升高[15];如果合并感染,则又增加了病原微生物的炎症介质激活改变,也会通过白细胞计数、PCT水平升高加以反映。有研究显示,炎症反应通过对动脉血管壁重构施加影响,亦是参与主动脉夹层发生、发展的重要机制[16]。由此可见,术前白细胞计数、PCT水平升高之所以会成为A型主动脉夹层术后发生AKI的独立危险因素,可能是综合反映或代表了主动脉夹层患者术前全身炎症反应的状况。
本研究结果显示,术中深低温停循环时间增加是A型主动脉夹层术后发生AKI的独立危险因素。主动脉夹层手术过程中,术中深低温停循环期间,肾动脉处于完全停血供状态,后面恢复循环,意味着肾脏会经历典型的缺血再灌注损伤,时间越长,越容易诱发急性肾小管坏死、炎症反应和细胞凋亡、肾小管上皮细胞死亡,最终造成肾功能障碍[14];同时,此过程中必然会产生大量的氧化应激损伤产物,加重缺血损伤和肾功能不全。有研究表明,肾缺血时间每增加5 min,AKI发生的风险就上升16%[17];常温下超过25 min,一定会发生肾损伤。所以,术中深低温停循环时间增加作为A型主动脉夹层术后发生AKI的独立危险因素,具有必然性,而且应当高度关注,要尽量缩短。此外,体外循环作为一种仿生理的非搏动性血流灌注方式,存在低灌注、血细胞破坏等病理生理性改变,导致肾脏滤过屏障破坏,还会激活肾素-血管紧张素-醛固酮系统,进一步降低滤过率,引发AKI[18]。主动脉阻断时间的长短与体外循环时间存在高度关联性,而且与心脏缺血再灌注损伤的严重程度直接关联[19],所以,时间越长,必然代表心肌的损伤、血细胞的破坏越重,肾脏承受低压灌注的时间也越长,越易诱发AKI。本研究中多因素Logistic回归分析并未显示主动脉夹层手术患者主动脉阻断时间是术后发生AKI的影响因素,但其他心脏手术的研究中有显示术中主动脉阻断时间是术后发生AKI的影响因素。
本研究发现,术前白细胞计数、术前PCT水平及术中深低温停循环时间3项指标联合检测预测术后发生AKI的AUC为0.758,有一定的价值。因此,对于行A型主动脉夹层手术的患者,当发现术前白细胞计数≥10.02×109/L,术前PCT水平≥0.22 ng/mL,术中深低温停循环时间≥38 min时,应该高度警惕术后发生AKI,及早进行预警防范,改善患者预后。
有研究表明,高血压、糖尿病、肥胖均有明确导致慢性肾损害的机制[4],尤其是慢性高血压,因为血压长期升高,可引起肾小动脉发生病变,导致肾脏出现缺血性损害,出现肾小动脉管壁增厚、管腔狭窄、肾小球滤过率降低,以及肾小球缺血性损伤等[20]。有研究显示,高血压、糖尿病、BMI升高均是心脏手术术后发生AKI的独立危险因素。本研究多因素Logistic回归分析未显示高血压、糖尿病、BMI升高为A型主动脉夹层术后发生AKI的独立危险因素,但这些因素控制不佳也可引发肾损伤,而且高血压控制不佳还是国内主动脉夹层患者发病的重要诱因。所以,加强高血压、糖尿病等在健康人群中的有效防治宣教工作,显然对减少主动脉夹层的发病及施行手术后AKI的发生具有重要意义,应密切关注。
A型主动脉夹层术后发生AKI与多种因素相关,术前白细胞计数、术前PCT水平升高及术中深低温停循环时间增加是术后发生AKI的独立危险因素,3项指标联合检测对预测术后AKI发生有一定的价值,密切监测这3项指标有利于早期发现并进行干预,降低术后AKI的发生。但本研究样本量较小,且为单中心研究,结果可能存在一定的偏倚,未来仍需扩大样本量及多中心研究加以验证。

