体外阻断在腹腔镜肝切除手术中的应用
陈秋凯 陈雄琴 陈秋华 袁阳春
广东省揭阳市人民医院普通外科 522000
近年来,随着腹腔镜技术的不断发展,腔镜下肝脏切除术发展也较快,越来越多的肝脏良恶性病变患者选择腹腔镜手术治疗[1]。但由于肝脏具有丰富的血流,分别为来自肝动脉及门静脉的血液灌注系统,因此增加了在进行解剖和肝实质离断时的出血风险,导致手术出血量较多[2]。目前,虽然国内外已经出现了腹腔镜下在全肝或半肝切除时应用体外血流阻断设备入肝进行血流阻断的报道,但由于取材不便、价格高等问题,因此国内临床上很少使用[3]。由于腹腔镜下肝门阻断技术能够提高腹腔镜肝切除术的安全性,通过控制入肝血流,从而减少肝切除过程中的出血量[4]。目前,国内常采用体内阻断进行入肝血流阻断,需在腔镜直视下进行操作,以对阻断带进行收紧或松开,操作起来十分不便。由于临床上关于腹腔镜肝切手术中应用体外入肝血流阻断器的报道较少,鉴于此,本研究旨在探讨自制第一肝门体外阻断设备在腹腔镜肝切除手术中的应用。
1 资料与方法
1.1 一般资料 选取2021年6月—2022年12月就诊于我院的45例行腹腔镜肝切除术患者,以术中阻断入肝血流的方法作为分组依据,分为体内阻断带Pringle法组(体内组,n=22)和自制体外阻断带Pringle 法组(体外组,n=23)。纳入标准:年龄≥36周岁;知情同意者;经临床症状及腹部B超或CT检查确诊为肝脏有病变需行肝切除者;术前 Child-Pugh分级为A或B级者。排除标准:中转开腹者;临床病理资料不完整者;病变位于肝脏尾状叶及肝门部者。体内组中男10例,女12例;年龄39~79(54.11±4.43)岁;BMI(23.85±3.17)kg/m2;Child-Pugh分级:A级20例,B级2例;其中肝恶性肿瘤7例,肝内结石13例,肝血管瘤1例,肝胆管囊性扩张症1例;其中行腹腔镜左半肝切除16例,左外叶切除5例,右半肝切除1例。体外组中男9例,女14例;年龄39~80(53.63±4.41)岁;BMI(24.15±3.35)kg/m2;Child-Pugh分级:A级22例,B级1例;其中肝恶性肿瘤7例,肝内结石14例,肝血管瘤2例;其中行腹腔镜左半肝切除17例,左外叶切除4例,右半肝切除2例。两组一般资料对比无差异(P>0.05)。
1.2 方法
1.2.1 体内阻断带Pringle法。将橡胶阻断带置入,环绕肝十二指肠韧带约一周。于腹腔镜下打结阻断入肝血流,夹毕固定,每次行间断阻断时的阻断时间为10~15min,复流时间为5min。
1.2.2 自制体外阻断带 Pringle 法。选择杆身长度36cm、304不锈钢材质的超声刀杆,由观察孔左侧旁2cm处切1个约0.5cm的刀口,将5mm Trocar置入腹腔后再拔除Trocar,将超声刀杆身的一端穿入至腹腔,让其套入至3cm的红色导尿管,于体外端套上5cm橡皮管(见图1)。使用硬质的胆道镜活检钳将棉线一端钳夹后,自体外穿入超声刀头杆身管腔,由后绕过肝十二指肠韧带(见图2)后,用硬质的胆道镜活检钳自超声刀头杆身管腔处将棉线引出体外(见图3),于阻断杆体外端的橡胶管处夹上直钳,防止出现漏气,在阻断时收此棉线,夹紧棉线阻断第一肝门入肝血流。阻断入肝血流时,在体外对两根棉线进行牵拉,以收紧阻断带。每次进行间断阻断的时间为10~15min,复流时间5min。

图1 自制体外阻断设备

图2 胆道镜下图像

图3 术中照片
1.3 观察指标 (1)手术相关指标:包括手术时间、术中失血量、肝门阻断次数、术中血流阻断时间、收缩阻断带时间。(2)肝功能指标。(3)住院天数、治疗费用。(4)并发症发生率。

2 结果
2.1 两组手术相关指标比较 体外组手术时间及血流阻断时间短于体内组,术中失血量及肝门阻断次数少于体内组,但组间比较差异无统计学意义(P>0.05)。体外组的收缩阻断带使用时间短于体内组,差异有统计学意义(P<0.05)。见表1。

表1 两组手术相关指标比较
2.2 两组肝功能指标比较 治疗后两组的肝功能指标均高于治疗前,比较有统计学差异(P<0.05);但治疗后,两组间肝功能指标比较,差异无统计学意义(P>0.05)。见表2。

表2 两组肝功能指标比较
2.3 两组住院天数、治疗费用比较 与体内组比较,体外组的住院天数更短,治疗费用更低,差异有统计学意义(P<0.05)。见表3。

表3 两组住院天数、治疗费用比较
2.4 两组并发症发生率比较 与体内组比较,体外组的并发症发生率更低,差异有统计学意义(χ2=4.500,P=0.034<0.05)。见表4。
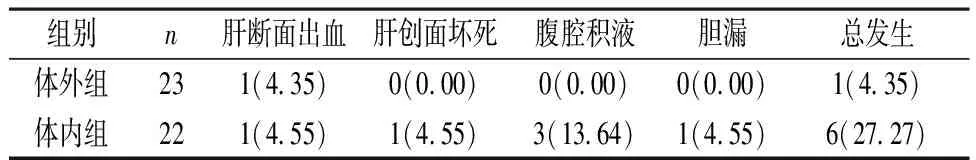
表4 两组并发症发生率比较[n(%)]
3 讨论
与开腹肝脏切除术相比,腹腔镜肝脏切除术具有切口小、术后恢复快及并发症少等优势[5]。由于腹腔镜的视野存在一定的局限,腹腔镜下对肝断面出血控制的难度增加,术中大量出血导致术中转开腹[6-7]。因此,亟须找到能够在腹腔镜下肝门血流阻断设备[8]。体内阻断法是采用橡胶管对肝十二指肠韧带捆绑后进行肝门阻断,由于肝十二指肠的韧带较厚,在腔镜下使用橡胶管进行打结或者压迫套管的方法,会导致入肝血流阻断不彻底,依然会有部分血流由肝门流入到肝脏[9-10]。而体外阻断带利用腹壁将血流直接引出体外,当进行阻断入肝血流时,可在体外使用手对阻断带进行直接收紧,以达到快速、有效阻断入肝血流的作用[11]。
丁炎宝[12]的研究数据显示,体内阻断带Pringle组与自制体外阻断带Pringle组在手术相关指标、肝功能指标、住院时间、并发症等方面均无统计学差异(P>0.05)。但本研究结果显示,体外组的住院天数短于体内组,治疗费用、并发症发生率低于体内组(P<0.05)。本研究部分数据验证了丁炎宝[12]研究数据的可靠性,但在其基础上缩短了住院天数,降低了治疗费用和并发症发生率。结果说明,在腹腔镜下肝切除术中应用自制体外阻断带阻断入肝血流的效果优于体内阻断法,且安全性更高。分析原因可能为:(1)自制体外阻断带在制作和放置时需要增加5~7min,几乎不会占用更多的时间。而体内阻断带在放置完成后,腔镜下打结、夹毕固定、阻断带松解等操作都会延长手术时间[13]。因此体外阻断在手术时间上略短于体内阻断。(2)采用体外Pringle法时收紧阻断带的操作几乎不耽误时间,不会增加因收紧阻断带导致肝断面的持续出血[14-15]。(3)在腹腔镜肝切除术中应用自制第一肝门体外阻断设备不会对肝功能产生影响,阻断效果良好,几乎阻断了入肝血流,从而提供更佳的手术解剖层面,更精准的手术解剖,避免过多残余无效的肝组织,减少了胆漏,肝创面坏死,胸腹腔积液等的发生率,减少了住院时间和治疗费用。
综上所述,在腹腔镜肝切除术中应用自制第一肝门体外阻断设备更加安全、有效。此文的研究结果为自制第一肝门体外阻断设备在腹腔镜肝切除术中应用的后期标准制定提供了借鉴内容。

