锌-二氧化锰锌离子电池:一个研究型综合性化学实验的设计与实践
吴兴隆,吕红艳,杜苗,王嗣泽,王晓彤,张凯洋,李炜晨
1 东北师范大学化学学院,长春 130024
2 东北师范大学紫外光发射材料与技术教育部重点实验室,长春 130024
化学是一门以实验为基础的学科。化学实验是化学理论的延伸与补充,其中,综合化学实验是在学生掌握基础化学实验的基本原理与技能的基础上,与学科前沿紧密结合,旨在提高学生的综合实验知识与技能,培养学生的科研素养和创新能力的实验课[1]。为了响应教育部印发的《关于加快建设高水平本科教育全面提高人才培养能力的意见》,促进最新科研成果及时转化为教育教学内容,以高水平科学研究支撑高质量本科人才培养,越来越多的高校将科研成果引入综合实验中,促进了教学与科研的深度融合。与此同时,2022年全国高考甲卷化学的第10题,对水系锌离子电池(aqueous zinc-ion batteries,AZIBs)的反应原理及离子迁移方向进行了考查,也体现了科研成果的重要性。
近年来,高效的电化学储能技术(如广泛商用的锂离子电池(lithium-ion batteries,LIBs))是由化石能源向清洁能源转变的关键技术之一,同时也是实现“双碳战略”的重要组成部分。但在LIBs大规模应用于智能电网、电动汽车和便携式设备的同时,锂资源有限、LIBs安全性低且成本高等短板逐渐暴露,因此人们开始寻求LIBs的补充品[2,3]。相比于传统的有机系电池,Zn-MnO2AZIBs凭借以下优势[4]成为了储能领域的一个研究开发热点:
① 安全性高;
② 成本低廉;
③ 理论容量高;
④ 操作简单。
由于课程设置的原因,本科生缺乏对材料结构/形貌的表征及循环伏安法等电化学测试的实践应用[5,6]。考虑到电池在我们日常生活中的普遍及重要性,学生对电化学实验充满兴趣,本实验将前沿性科研成果转化为综合化学实验,通过水热法以KMnO4和MnSO4为主要原料制备了绿色且低成本的α-MnO2(图1),选用α-MnO2为正极,Zn片为负极制备了Zn-MnO2AZIBs并进行了电化学性能测试,以物理化学综合实验的形式,引入大学化学实验中,以科研促进实验教学,以教学辅助科研创新,推动科研与教学的密切联系。我们对实验进行了合理的设计,原料易得,实验操作简单(材料的制备过程简单;相比于锂离子电池等电池体系,AZIBs的组装无需苛刻的无水无氧条件),反应条件绿色温和,实验现象明显,学生可通过现象来直观地判断进展,更易激发学生的热情。该实验锻炼了学生的离心分离、加热、搅拌和烘干等基本实验技能,将材料的制备、表征、测试及分析融为一体,使本科生建立“合成-表征-应用”的科研思维模式;使实验具有更强的操作性、综合性和前沿性;此外,该实验梳理了电化学相关知识点,实验所涵盖的材料、物理、无机和分析化学等基础化学课程的交叉相融有利于学生将理论与实践相结合,培养绿色理念及可持续发展思想。
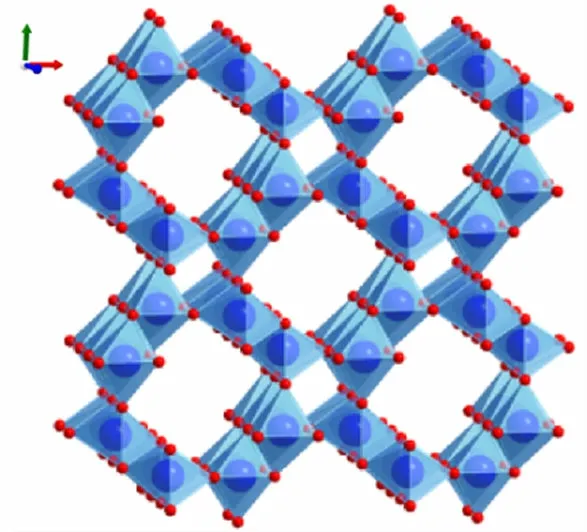
图1 α-MnO2的晶体结构
1 实验教学安排
本综合化学实验适合开设于大三上至大四上学期,需要28学时完成,可多人讨论,分组进行,可2-3人/组;也可作为大二学生的研究性实验,6人/组,每组再分为2人一组的小组。在实验前,学生应查阅相关文献,提前了解电池工作的基本原理,以及X射线衍射(XRD)、扫描电子显微镜(SEM)等测试的内容,回顾离心、搅拌等基本实验操作的内容,实验结束后每组进行实验汇总与讨论,总结结果并分析与处理数据。
本实验可分模块进行实验教学,根据不同课时需求选择不同的模块进行教学,灵活机动。这种模块化教学方式既注重对理论知识的讲解,又重视理论和实践的结合,学生可以创造性地提出自己的想法,以研究任务驱动学习,以模拟科学研究的方式开展实验教学,提升了综合实验的高阶性和创新性,为建设一流课程提供了最核心的要素。
2 实验部分
2.1 实验原理
通过水热法,以KMnO4和MnSO4为主要原料制备α-MnO2的反应方程式如下:
Zn-MnO2二次电池的充放电反应通常可简单表示为(正反应为放电过程,逆反应为充电过程):
MnO2电极材料理论容量(Cs)的计算公式:
其中,Cs为材料的理论容量(mAh·g-1),96485为法拉第常数(C·mol-1),n为转移电子数,M为MnO2的分子量(g·mol-1)。根据该式,可计算出MnO2的理论容量为308 mAh·g-1。
研究表明纳米MnO2的大隧道结构利于储存Zn2+,Zn2+在大隧道的锰基材料中具有快速且可逆的脱嵌行为[7],图2为Zn-MnO2二次AZIBs充放电过程的原理示意图。Zn-MnO2AZIBs的工作机理为:放电时,Zn2+嵌入MnO2的晶体结构中形成ZnMn2O4,锌负极失去电子生成Zn2+;充电时,正极中的Zn2+从ZnMn2O4脱出并在锌负极沉积生成锌单质,同时电子经过外电路被输送到负极上[8,9]。
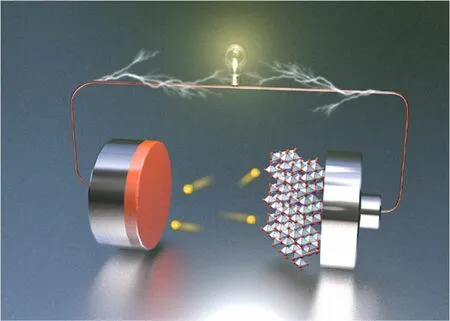
图2 Zn-MnO2 AZIBs的原理示意图
2.2 实验试剂
高锰酸钾(Aladdin),一水合硫酸锰(Aladdin),七水合硫酸锌(Aladdin),N-甲基吡咯烷酮(Macklin),聚偏氟乙烯(Sigma),乙炔黑(广州新稀冶金化工),无水乙醇(北京化工厂),以上试剂除乙炔黑为工业级外,均为分析纯。
2.3 实验仪器
实验所需仪器:电子天平,100 mL烧杯,集热式恒温油浴锅,磁力搅拌器,台式高速离心机,电热鼓风干燥箱,真空干燥箱,管式炉,NEWARE电池测试系统(CT-4000,深圳市新威尔电子有限公司),电化学工作站(CHI600e,上海辰华仪器有限公司)。
表征所需大型测试仪器:通过粉末XRD (D8,德国Bruker公司)技术研究正极材料的晶体结构,所用X射线为CuKα(λ= 0.15406 nm),扫描范围为2θ= 10°-80°;通过SEM (SU8000,日本Hitachi)对制备的α-MnO2粉末的形貌和粒径尺寸进行表征。
2.4 实验步骤
2.4.1 正极材料的制备
准确称取1.359 g MnSO4和0.948 g KMnO4于100 mL的烧杯中,加入40 mL的去离子水,室温下搅拌使其溶解。将上述溶液完全转移至100 mL的聚四氟乙烯内衬,再将其装入配套的不锈钢水热反应釜中,在140 °C下恒温水热处理24 h。待反应结束自然降至室温后,将聚四氟乙烯内衬中溶液倒入离心管中,在8000 r·min-1的条件下用蒸馏水和乙醇进行离心、洗涤。离心结束后弃掉上层清液,将离心后的固体粉末在60 °C的真空干燥箱中干燥24 h,经充分研磨后在空气气氛下300 °C退火1 h,得到棕黑色的α-MnO2正极材料。
2.4.2 电极片的制备
首先按7 : 2 : 1的质量比依次称取所需质量的α-MnO2材料、导电剂碳黑和粘结剂聚偏氟乙烯,随后将称取的粉末材料全部转移至研钵中,充分研磨至固体粉末均匀混合。将研磨均匀的粉末样品完全转移至样品瓶中并加入适量的N-甲基吡咯烷酮溶剂,过夜搅拌至得到均匀且具有一定粘度的浆料。取3-4片表面完整、干净且干燥的碳纸,用移液枪移取定量的浆料均匀涂覆再已知质量的碳纸上,并置于100 °C的真空干燥箱中干燥24 h,即得到α-MnO2电极片。最后将制备完成的正极片称重,扣除碳纸的重量后,按比例计算得到正极活性材料的负载量。
2.4.3 电池的组装
图3为组装2032型纽扣电池的步骤。按照负极壳、锌负极片、隔膜、电解液(2 mol·L-1ZnSO4+ 0.5 mol·L-1MnSO4)、α-MnO2正极片、垫片、弹片、正极壳的顺序从下到上依次组装好,然后在小型液压电池封装机上封口成型,即可得到Zn-MnO2AZIBs。
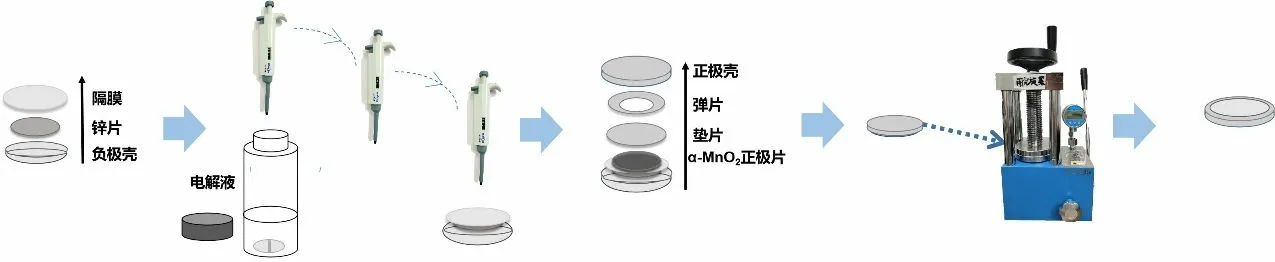
图3 Zn-MnO2 AZIBs的组装步骤
2.4.4 电化学性能测试
将装配好的电池连接到电池测试系统上,在1.0-1.8 V的电压区间内测试其电化学性能。依次进行多扫速循环伏安测试(扫速:0.1、0.2、0.3及0.5 mV·s-1,),倍率性能测试(电流密度:0.1、0.2、0.3、0.5 A·g-1)和循环性能测试(电流密度:0.5 A·g-1),最后对所装配的Zn-MnO2AZIBs电池进行实际应用测试。记录测试原始数据,并使用Origin软件进行绘图。
3 结果与讨论
3.1 α-MnO2的结构和形貌表征
3.1.1 结构表征——XRD
利用XRD测试对制备的α-MnO2粉末进行结构表征,所得测试谱图如图4所示。从图中可以看出,所有的主要衍射峰都与α-MnO2的标准卡片(PDF#44-0141)相一致,在12.78°、18.10°、28.84°、37.52°、49.66°、60.27°、69.7°出现的衍射峰分别对应于α-MnO2的(110)、(200)、(310)、(211)、(411)、(521)、(541)晶面,且不存在明显的杂峰,证明制备的α-MnO2材料具有较高的纯度。
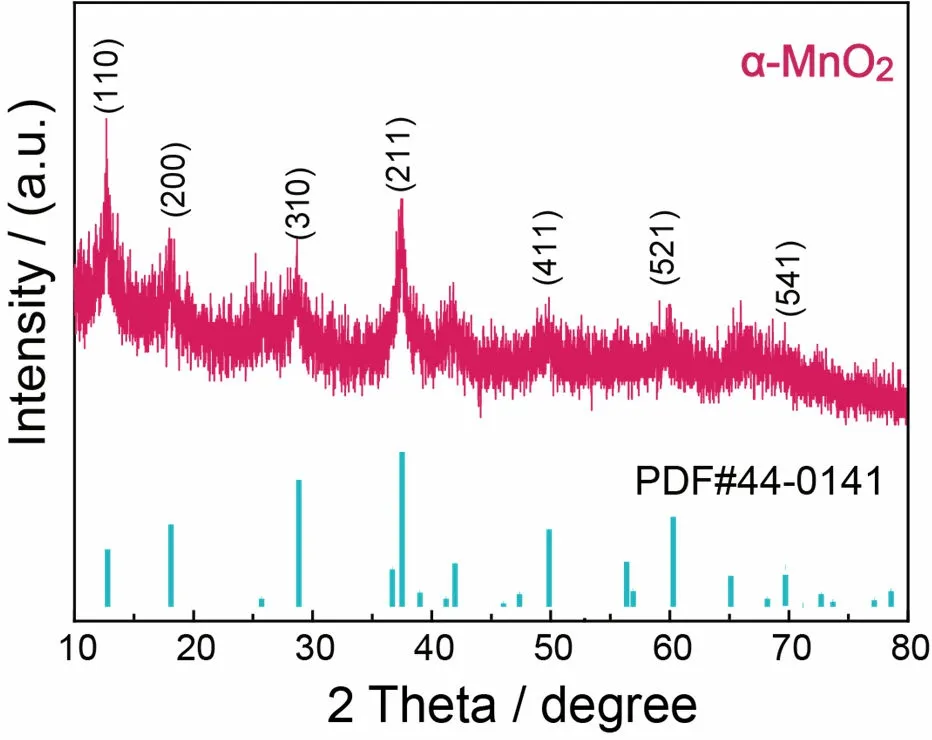
图4 α-MnO2的XRD谱图
3.1.2 形貌表征——SEM
利用SEM对制备的α-MnO2材料进行形貌表征,所得图像如图5所示。SEM结果表明,通过水热法制备的α-MnO2为纳米级,产物为直径在100 nm左右的纳米棒状结构,且α-MnO2纳米棒的粗细均匀,分散良好。

图5 α-MnO2的SEM谱图
3.2 电化学性能测试
3.2.1 循环伏安测试(CV)
图6为以锌片为负极、α-MnO2为正极且2 mol·L-1ZnSO4+ 0.5 mol·L-1MnSO4为电解液而组装成的AZIBs循环伏安曲线。在电解液中加入MnSO4,可以减少α-MnO2在循环过程中的溶解。根据CV曲线可确定电极反应的机制为Zn2+在正极的嵌入/脱出和在负极的溶解/沉积。如图所示,CV曲线存在两对位于1.58/1.23 V和1.62/1.35 V (vs.Zn2+/Zn)的明显的氧化还原峰,对应于一个两步反应。此外,不同扫速下的CV曲线基本一致,没有发生明显的改变,表明Zn2+在α-MnO2正极中的脱嵌行为具有高度的可逆性。
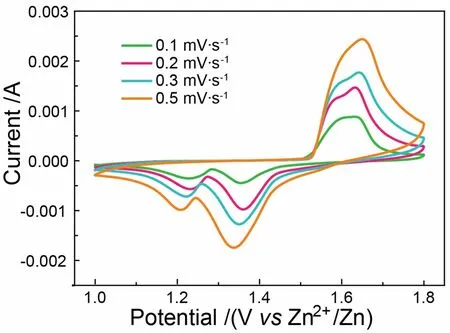
图6 α-MnO2 AZIBs的循环伏安曲线
3.2.2 倍率性能测试
Zn-MnO2AZIBs的倍率测试结果如图7a所示。分别在0.1、0.2、0.3、0.5、0.1 A·g-1的电流密度下对电池进行了恒流充放电性能测试(GCD),在上述电流密度的平均放电容量分别保持在260.1、239.5、210.9、153.7和259.5 mAh·g-1。当电流密度恢复到0.1 A·g-1时,电池的放电容量基本恢复到初始比容量(~260 mAh·g-1),并保持稳定。除此之外,电池的库伦效率较高,基本可以维持在100%。图7b展示了不同电流密度(0.1、0.2、0.3、0.5 A·g-1)下的恒流充放电曲线,各组充放电曲线的形状基本一致,进一步说明材料具有较好的倍率性能和较高的稳定性。
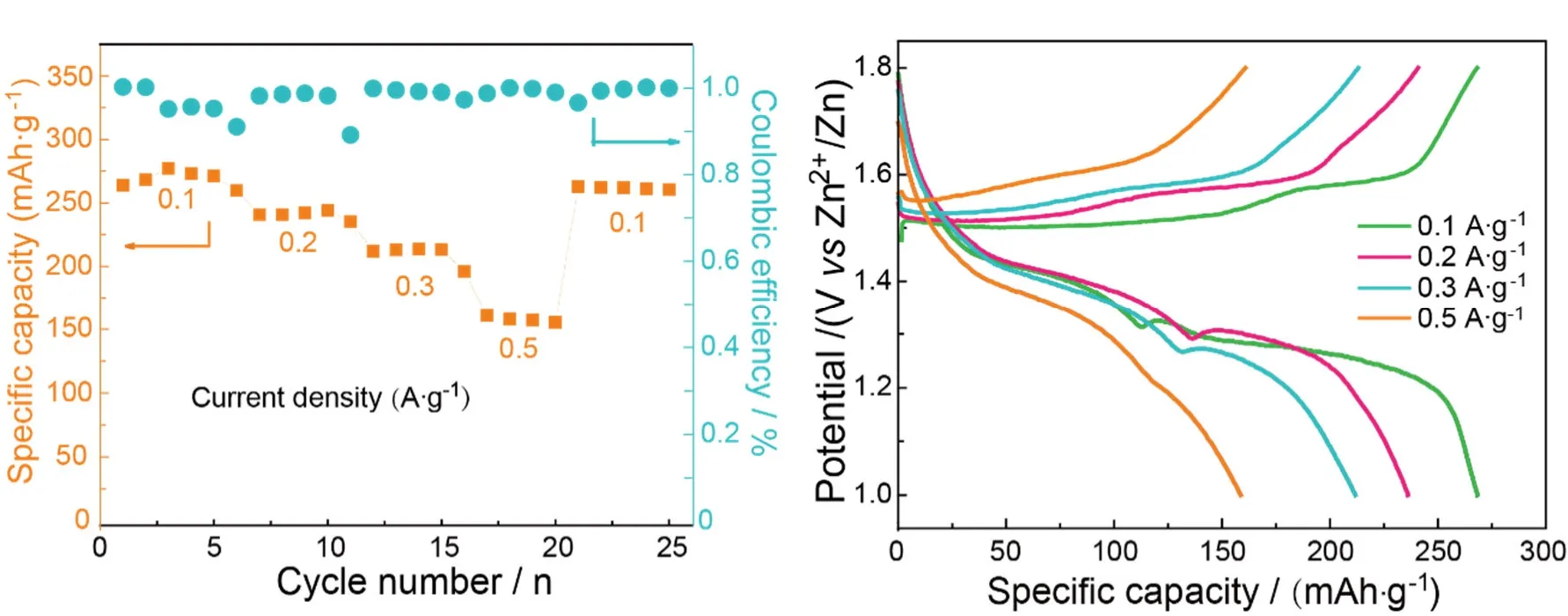
图7 Zn-MnO2 AZIBs在不同电流密度下的倍率测试结果及相应的GCD曲线
3.2.3 循环性能测试
由循环测试结果(图8)可知,当电流密度为0.5 A·g-1时,Zn-MnO2AZIBs在循环100圈后的容量保持率为75%,证明制备的α-MnO2材料具有良好的循环稳定性。
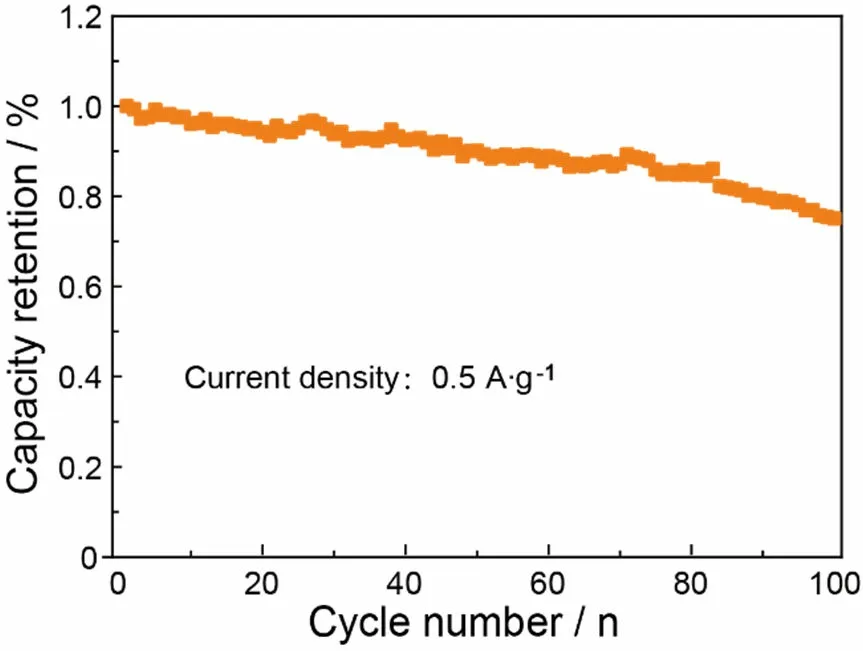
图8 Zn-MnO2 AZIBs在0.5 A·g-1电流密度下的循环性能
3.2.4 Zn-MnO2 AZIBs的实际应用测试
图9展示了Zn-MnO2AZIBs的实际应用测试。如图所示,制备的Zn-MnO2AZIBs可以成功点亮红色LED灯,证明其具有巨大应用潜力,有望应用于新一代储能系统中。

图9 Zn-MnO2电池的实际应用测试
4 结语
本实验以性能优异、原料易得、组装简单的Zn-MnO2AZIBs的设计与组装为主题,通过α-MnO2正极材料的制备、电极材料的表征、电池的组装、电池的电化学性能测试四部分深入探究和讨论了Zn-MnO2AZIBs的电化学工作原理和性能。由于电池在日常生活中发挥着重要的作用,学生普遍对实验内容比较感兴趣,且该综合实验所涵盖的基础实验操作具有较强的可操作性,能很好地锻炼学生的实验技能和处理分析实验数据的能力。从科研成果转化的实验课题有利于培养学生的科研意识,更有助于学生了解学科知识与前沿科学研究的密切相融性。此外,实验涉及多个实验现象及可探究的实验变量,如原材料的选择、水热反应的温度、时长及MnO2的不同结构类型,学生可以通过探究不同的温度、时间及原材料,并表征及测试其相应的结构与电化学性能,得到合成MnO2的最佳条件,该过程有利于培养学生设计实验的能力,进一步激发学生的求知欲及自主创新能力。

