盐炙小茴香醋酸乙酯部位化学成分及抗酪氨酸酶活性研究
董维茂,朱奎霖,杨 兴,尹 蕊,邓徐丽,陈章贤,张洪川,王一谋,何红平,董发武
云南中医药大学中药学院 云南省南药可持续利用研究重点实验室,云南 昆明 650500
小茴香为伞形科植物茴香FoeniculumvulgareMill.的干燥成熟果实[1],其原名蘹香。其药用历史悠久,始载于《唐本草》,有1 千多年药用历史[2]。除药用外,小茴香还是常用的食品香料,故为药食两用之佳品。小茴香分布广泛,主要分布于地中海地区[3],我国主要分布于西北地区的山西、甘肃、内蒙古,以及东北地区的辽宁等地区[4],其资源丰富,以栽培为主,栽培面积广泛,其中以山西产量最大、内蒙古河套附近产品质优。
小茴香味辛、性温,具有散寒止痛、理气和胃之功效[5-6]。小茴香化学成分主要为苯丙素,以及糖苷、脂肪油、黄酮、酚酸等多种类型的化合物[7]以及部分含量较少的无机元素。现代研究表明,小茴香具有改善肠道微生物平衡、促进胃肠运动、抗菌、抗肿瘤、镇痛抗炎等的作用[8-15]。其中主要成分苯丙素类化合物还具有抑制酪氨酸酶活性的作用[16]。包括雀斑在内的皮肤病都与黑色素的合成有关,其中酪氨酸酶作为黑色素形成的关键性调节酶[17-20]。因此,从天然产物中寻找抑制酪氨酸酶活性的化合物成为该领域中研究的热点。目前,对小茴香生品的研究主要注重于挥发油成分,然而关于小茴香盐炙品化学成分及药理活性研究报道不多,因此本实验对小茴香盐炙品进行成分分离纯化,从其醋酸乙酯部位分离得到 20 个化合物,分别鉴定为bombasinol A(1)、齐墩果酸(oleanolic acid,2)、山柰素(kaempferide,3)、槲皮素(quercetin,4)、(1R,2R)-1-(4-methoxypheny)propane-1,2-diol(5)、(1S,2R)-1-(4-methoxyphenyl)propane-1,2-diol(6)、(3S,5R,6S,7E)-3,5,6-trihydroxy-7-megastigmen-9-one(7)、齐墩果酮酸(oleanonic acid,8)、刺五加酮(acanthone,9)、phenylpropanoid(10)、(Z)-4-[30-(β-D-glucopyranosyloxy)butylidene]-3,5,5-trimethyl-2-cyclohexen-l-one ( 11 )、 3-oxo-α-ionol-β-Dglucopyranoside(12)、(+)-松脂素-β-D-吡喃葡萄糖苷 [(+)-pinoresinol-β-D-glucopyranoside,13]、trans-4-(1-propenyl)-phenol-β-D-glucopyranoside(14)、1-O-β-D-glucopyranosyl-4-allybenzene ( 15 )、 3-hydroxyestragole β-D-glucopyranoside(16)、黄花夹竹桃黄酮(thevetiaflavone,17)、3,5-dihydroxyestragole 3-O-β-D-glucopyranoside(18)、水杨酸(salicylic acid,19)和benzyl β-D-glucopyranoside(20)。并对分离的单体成分进行了体外抗酪氨酸酶的活性研究。此外,通过分子对接推测其可能的相互作用机制。
1 材料与仪器
1.1 材料
酪氨酸酶(Sigma-Aldrich 公司);L-酪氨酸(上海麦克林生化科技有限公司)、β-熊果苷(上海源叶生物科技有限公司,质量分数98%);色谱硅胶(200~300、300~400 目,青岛海洋化工厂);GF254薄层色谱硅胶(青岛海洋化工厂);LH-20 羟丙基葡聚糖凝胶(Sephadex LH-20,美国Pharmacia 公司);MCI 树脂(日本三菱化学公司);反相C18柱色谱材料(ODS,德国Merck 公司);D101 大孔吸附树脂(天津市大钧科技有限公司);薄层色谱显色剂(10%硫酸乙醇溶液);甲醇、乙醇、丙酮、正丁醇、醋酸乙酯、二氯甲烷、石油醚等试剂为重蒸的工业或化学纯溶剂;色谱乙腈(上海星可高纯溶剂有限公司)。
小茴香药材于2022年9月购自新螺蛳湾药材市场,由云南中医药大学李宏哲副教授鉴定为伞形科植物茴香F.vulgareMill.的干燥成熟果实,标本(D2022-001)保存于云南省高校民族药质量标准研究重点实验室。
1.2 仪器
Synergy2 多功能酶标仪(美国BIOTEK 公司);Bruker Avance III 400 MHz 及Bruker DRX 500 MHz超导核磁共振仪,TMS 为内标(德国Bruker 公司);Agilent 1200 型高效液相色谱仪(美国Agilent 公司);离子井飞行时间质谱仪Esquire HCT 型(德国Bruker 公司);万分之一分析天平FA2004(上海舜宇恒平科学仪器有限公司);循环水式多用真空泵SHB-Ⅲ(巩义市予华仪器有限公司);海道夫旋转蒸发仪Hei-VAP Core HL/G(德国heidolph 公司)。
2 提取与分离
2.1 小茴香的盐炙
取小茴香20 kg,加入2000 mL 配制好的0.2 g/mL 盐水,密封,焖透30 min,而后置炒制容器内,以文火加热,不间断翻炒,并炒至微黄且至规定程度时,取出,放凉备用。
2.2 提取
盐炙小茴香样品20 kg 粉碎过筛(10 目),在10 L 的75%乙醇中(10 L×2 h×5)回流提取。合并得提取液,通过减压浓缩得到2.387 kg 粗提物,粗提物加水混悬并使用石油醚、醋酸乙酯、正丁醇依次分别萃取5 次,合并萃取液,减压浓缩得到石油醚相(203.6 g)、醋酸乙酯相(73.9 g)、正丁醇相(316.7 g)和水相(759.3 g)。
2.3 分离及纯化
醋酸乙酯部位经正向硅胶色谱(200~300 目),以二氯甲烷-甲醇(100∶1~1∶1)梯度洗脱,得到7 个组分(Fr. 1~7)。Fr. 2(13.9 g)经MCI 柱色谱以甲醇-水(30∶70~100∶0)梯度洗脱,得到6 个流分(Fr. 2.1~2.6),Fr. 2.3 经Sephadex LH-20 色谱(甲醇)进行分离,再通过二次凝胶得到Fr. 2-3-1-1,Fr.2-3-1-1 经半制备液相(乙腈-水24∶76;体积流量3 mL/min;检测波长365 nm)纯化得化合物1(3.0 mg)。Fr. 2.4 经反相ODS 柱色谱,以甲醇-水(30∶70~100∶0)洗脱,经Sephadex LH-20 色谱(甲醇)纯化得化合物2(52.4 mg)。Fr. 2.5 经Sephadex LH-20 色谱(甲醇)分离再经半制备液相(乙腈-水20∶80;体积流量3 mL/min;检测波长365 nm)纯化得化合物19(13.4 mg)。Fr.2.6 经Sephadex LH-20 色谱(甲醇)分离纯化得化合物3(2.4 mg)。Fr. 2.6.5 经MCI 柱色谱以甲醇-水(30∶70~100∶0)梯度洗脱,再经Sephadex LH-20色谱(甲醇)分离纯化得化合物4(8.8 mg)。Fr.4(9.1 g)经正向硅胶色谱(200~300 目),以石油醚-醋酸乙酯(6∶1~1∶1)梯度洗脱,再经Sephadex LH-20 色谱(甲醇)分离得化合物7(1.9 mg)和8(4.0 mg),再通过半制备液相(乙腈-水15∶85;体积流量3 mL/min;检测波长:365 nm)纯化得化合物5(17.6 mg)和6(12.9 mg)。Fr.5(8.2 g)经正向硅胶色谱(200~300 目),以石油醚-醋酸乙酯(2∶1~1∶1)梯度洗脱,反相ODS 柱色谱,以甲醇-水(20∶80~100∶0)洗脱,再通过半制备液相(乙腈-水21∶79;体积流量3 mL/min;检测波长254 nm)纯化得化合物9(3.0 mg)。Fr. 26(11.0 g)经正向硅胶色谱(100~200 目),以二氯甲烷-甲醇(50∶1-1∶1)梯度洗脱,再经Sephadex LH-20 色谱(甲醇)分离半制备液相(乙腈-水26∶74;体积流量3 mL/min;检测波长254 nm)纯化得化合物10(3.0 mg)。Fr. 7(12.1 g)经正向硅胶色谱(100-200目),以二氯甲烷-甲醇(50∶1~1∶1)梯度洗脱得到9 个流分(Fr. 7.1~7.9),Fr. 7.5 以反相ODS 柱色谱,以甲醇-水(20∶80~100∶0)梯度洗脱得到6 个流分,Fr. 7.5.3 以Sephadex LH-20 色谱(甲醇)分离得到化合物13(5.0 mg),再以半制备液相色谱(乙腈-水33∶67;体积流量3 mL/min;检测波长365 nm)纯化得化合物11(6.0 mg)和12(6.0 mg),Fr.7.5.6 经Sephadex LH-20 色谱(甲醇)分离得再以半制备液相(乙腈-水 46∶54;体积流量 3 mL/min;检测波长365 nm)纯化得化合物20(18.8 mg),Fr. 7.6 以反相ODS 柱色谱,以甲醇-水(20∶80~100∶0)梯度洗脱得到6 个流分,Fr.7.6.4经正向硅胶二氯甲烷-甲醇(50∶1)等度洗脱再以半制备液相(乙腈-水12∶88;体积流量3 mL/min;检测波长365 nm)纯化得化合物16(17.0 mg),Fr.7.6.2 经Sephadex LH-20 色谱(甲醇)分离得再以半制备液相(乙腈-水15∶85;体积流量3 mL/min;检测波长365 nm)纯化得化合物14(9.9 mg)和15(24.3 mg),Fr. 7.9 以正向硅胶色谱(100~200目),以二氯甲烷-甲醇(30∶1~1∶1)梯度洗脱得Fr. 7.9.2,Fr. 7.9.2 经 MCI 柱色谱以甲醇-水(20∶80~100∶0)梯度洗脱,再经Sephadex LH-20色谱(甲醇)分离最后以半制备液相(乙腈-水23∶77;体积流量3 mL/min;检测波长254 nm)纯化得化合物17(4.2 mg)和18(32.6 mg)。
3 酪氨酸酶抑制活性测试
3.1 溶液的配制
3.1.1 磷酸盐缓冲液的配制 精密量取20 mL 10×PBS 缓冲液,用超纯水稀释至200 mL,最后使用0.2 mol/L 氢氧化钠调节pH 6.5~7.5(规定范围)即得PBS 缓冲液。
3.1.2 酪氨酸酶试液的配制 精密移取提前分装好的1000 units/mL 的酪氨酸酶9 mL,加入PBS 缓冲液稀释至30 mL 即得300 units/mL 的酪氨酸酶试液,将试液放入−20 ℃冰箱待用。
3.1.3L-酪氨酸溶液的配制 精密称取5 mgL-酪氨酸粉末于100 mL EP 管中加入50 mL PBS 缓冲液,摇匀,即得0.1 mg/mLL-酪氨酸溶液,放置,待用。
3.1.4 样品溶液的配制
(1)阳性药溶液的配制:精密称取β-熊果苷4 mg,加入30 μL DMSO 使其完全溶解,再使用移液枪精密加入970 μL PBS 即得4 mg/mL 阳性药试液,再将阳性药依次梯度稀释浓度为2、1、0.5、0.25 mg/mL,待用。
(2)待测样品溶液的配制:精密称取样品适量,加入30 μL DMSO 使其完全溶解,再精密加入PBS使其质量浓度依次为1、0.5、0.25、0.125、0.062 5 mg/mL;其中化合物15 稀释质量浓度依次为0.25、0.125、0.062 5、0.031 25、0.015 625 mg/mL,待用。
3.2 酪氨酸酶活性抑制率的测定
用移液枪按表的体积向96 孔板依次加入PBS缓冲液、不同浓度梯度的化合物受试液、不同浓度梯度的熊果苷对照液和酪氨酸酶液,37 ℃下孵育10 min 后,加入L-酪氨酸试液,同等条件下孵育30 min,孵育完成后立即放入多功能酶标仪在492 nm测定其吸光度(A),并记录数据,每个浓度实验做3 个平行组,使用3 组数据的平均值,按照公式计算测定化合物对酪氨酸酶的抑制率。
T 为加样品且加酪氨酸的反应液组别;B 为加样品且未加酪氨酸的反应液组别;C 为未加样品且加酪氨酸的反应液组别;N 为未加样品且未加酪氨酸的反应液组别;AT为T 组反应液在492 nm 处测得的A值;AB为B 组反应液在492 nm 处测得的A值;AC为C 组反应液在492 nm 处测得的A值;AN为N 组反应液在492 nm 处测得的A值
3.3 数据处理与分析
运用IBM SPSS Statistics 26 进行计算IC50,并采用GraphPad Prism 9 软件进行做图。
4 分子对接
4.1 化合物结构的获取与处理
在Chemdraw 2D 中画出所需化合物的2D 平面结构,再通过Chemdraw 3D 将其转化为PDB 格式的3D 结构文件。
4.2 靶蛋白的获取与处理
从PDB 数据库(https://www.rcsb.org/)获得酪氨酸酶蛋白的PDB 格式的三维晶体结构文件,运用OpenBabel 2.4.1、AutoDockTools 1.5.7 软件进行前期处理,得到相对应的PDB 文件,备用。
4.3 化合物与靶蛋白的对接
将上述处理好的化合物与靶蛋白文件导入Autodock vina,并通过Autodock vina 进行分子对接,最后将Autodock vina 对接并对对接结果打分,将得到的PDB 格式文件,使用PyMol 软件对分子对接结果进行可视化。
5 结果与分析
5.1 结构鉴定
化合物1:黄色油状物,分子式为C21H24O6,HR-ESI-MSm/z: 395.146 0 [M+Na]+(计算值395.146 5)。1H-NMR (400 MHz, CD3OD)δ: 6.95(1H, d,J= 1.9 Hz, H-2′), 6.82 (1H, dd,J= 8.1, 1.9 Hz, H-6′), 6.77 (1H, d,J= 8.1 Hz, H-5′), 6.66 (2H, d,J= 1.5 Hz, H-2, 6), 4.72 (2H, d,J= 4.2 Hz, H-7, 7′),4.25 (2H, dd,J= 9.1, 6.7 Hz, H-9α, 9′α), 3.88 (3H, s,3′-OMe), 3.86 (6H, s, 3, 5-OMe), 3.85 (2H, dd,J=8.5, 3.5 Hz, H-9β, 9′β), 3.15 (2H, m, H-8, 8′);13C-NMR (100 MHz, CD3OD)δ: 149.4 (C-3, 5), 149.2(C-3′), 147.4 (C-4′), 134.3 (C-1), 133.8 (C-1′), 120.1(C-6′), 116.1 (C-5′), 111.0 (C-2′), 106.2 (C-4), 104.5(C-2, 6), 87.7 (C-7), 87.5 (C-7′), 72.7 (C-9′), 72.6(C-9), 56.8 (3, 5-OMe), 56.4 (3′-OMe), 55.6 (C-8),55.3 (C-8′)。以上数据与文献报道一致[21],故鉴定化合物1 为bombasinol A。
化合物2:白色固体,分子式为C30H48O3,HR-ESI-MSm/z: 479.348 8 [M+Na]+(计算值479.349 6)。1H-NMR (400 MHz, Pyridine-d5)δ: 5.52(1H, s, H-12), 3.47 (1H, m, H-3α), 3.33 (1H, dd,J=14.1, 4.6 Hz, H-18), 1.31 (3H, s, H-27), 1.27 (3H, s,H-23), 1.05 (9H, s, H-24, 25, 30), 0.97 (3H, s, H-29),0.92 (3H, s, H-26);13C-NMR (100 MHz, Pyridine-d5)δ: 180.7 (C-28), 145.3 (C-13), 123.0 (C-12), 78.6(C-3), 56.3 (C-5), 48.6 (C-4), 47.2 (C-9), 46.9 (C-17),42.7 (C-19), 42.5 (C-14), 40.2 (C-18), 39.9 (C-1), 39.4(C-8), 37.9 (C-10), 37.7 (C-2), 33.8 (C-21), 33.8(C-29), 33.7 (C-22), 31.4 (C-7), 29.3 (C-20), 28.8(C-15), 28.6 (C-23), 26.6 (C-27), 24.3 (C-30), 24.2(C-1), 24.2 (C-16), 19.3 (C-24), 17.9 (C-6), 17.0(C-26), 16.0 (C-25)。以上数据与文献报道一致[22],故鉴定化合物2 为齐墩果酸。
化合物3:黄色粉末,分子式为C16H12O6,HR-ESI-MSm/z: 323.052 4 [M+Na]+(计算值323.052 6)。1H-NMR (600 MHz, CD3OD)δ: 8.08(2H, d,J= 8.5 Hz, H-2′, 6′), 6.90 (2H, d,J= 8.5 Hz,H-3′, 5′), 3.34 (3H, s, 4′-OMe);13C-NMR (150 MHz,CD3OD)δ: 177.4 (C-4), 165.6 (C-7), 162.5 (C-9),160.6 (C-4′), 158.3 (C-5), 148.1 (C-2), 137.2 (C-3),130.7 (C-2′, 6′), 123.8 (C-1′), 116.3 (C-3′, 5′), 104.5(C-10), 99.3 (C-6), 94.4 (C-8), 56.5 (4′-OMe)。以上数据与文献报道一致[23],故鉴定化合物3 为山奈素。
化合物4:黄色粉末,分子式为C15H10O7,HRESI-MSm/z: 303.049 2 [M+H]+(计算值303.049 9)。1H-NMR (400 MHz, CD3OD)δ: 7.75 (1H, d,J= 2.2 Hz, H-2′), 7.65 (1H, dd,J= 8.4, 2.2 Hz, H-6′), 6.90(1H, d,J= 8.4 Hz, H-5′), 6.40 (1H, d,J= 2.0 Hz,H-8), 6.19 (1H, d,J= 2.0 Hz, H-6);13C-NMR (100 MHz, CD3OD)δ: 177.4 (C-4), 165.6 (C-7), 162.5(C-5), 158.2 (C-9), 148.8 (C-2), 148.0 (C-4′), 146.2(C-3′), 137.3 (C-3), 124.2 (C-1′), 121.7 (C-6′), 116.2(C-5′), 115.9 (C-2′), 104.5 (C-10), 99.2 (C-6), 94.4(C-8)。以上数据与文献报道一致[24],故鉴定化合物4 为槲皮素。
化合物5:无色针状结晶(甲醇),分子式为C10H14O3,HR-ESI-MSm/z: 205.082 6 [M+Na]+(计算值205.083 5)。1H-NMR (400 MHz, CD3OD)δ:7.26 (2H, d,J= 8.7 Hz, H-2, 6), 6.86 (2H, d,J= 8.7 Hz, H-3, 5), 5.08 (1H, d,J= 5.0 Hz, H-1′), 4.40 (1H,dq,J= 5.0, 6.0 Hz, H-2′), 3.75 (3H, s, 4-OMe), 1.09(1H, d,J= 6.0 Hz, H-3′);13C-NMR (100 MHz,CD3OD)δ: 160.5 (C-4), 135.4 (C-1), 129.2 (C-2, 6),114.4 (C-3, 5), 78.7 (C-1′), 72.4 (C-2′), 55.6 (4-OMe),18.4 (C-3′)。以上数据与文献报道一致[25],故鉴定化合物 5 为 (1R,2R)-1-(4-methoxyphenyl)propane-1,2-diol。
化合物6:无色针状结晶(甲醇),分子式为C10H14O3,HR-ESI-MSm/z: 205.082 5 [M+Na]+(计算值205.083 5)。1H-NMR (400 MHz, CD3OD)δ:7.23 (2H, d,J= 8.7 Hz, H-2, 6), 6.86 (2H, d,J= 8.7 Hz, H-3, 5), 4.26 (1H, d,J= 7.0 Hz, H-1′), 3.82 (1H,dq,J= 6.0, 7.0 Hz, H-2′), 3.75 (3H, s, 4-OMe), 0.91(1H, d,J= 6.0 Hz, H-3′);13C-NMR (100 MHz,CD3OD)δ: 160.7 (C-4), 135.3 (C-1), 129.3 (C-2, 6),114.6 (C-3, 5), 79.9 (C-1′), 72.9 (C-2′), 55.6 (4-OMe),19.2 (C-3′)。以上数据与文献报道一致[25],故鉴定化合物6 为 (1S,2R)-1-(4-methoxyphenyl) propane-1,2-diol。
化合物7:白色针状结晶(甲醇),分子式为C13H22O4,HR-ESI-MSm/z: 265.142 5 [M+Na]+(计算值265.141 0)。1H-NMR (600 MHz, CD3OD)δ:7.15 (1H, d,J= 15.7 Hz, H-7), 6.16 (1H, d,J= 15.7 Hz, H-8), 3.74 (1H, m, H-3), 2.29 (1H, ddd,J= 14.3,5.0, 1.7 Hz, H-4a), 2.28 (3H, s, H-10), 1.64 (1H, dd,J= 14.3, 9.2 Hz, H-4b), 1.56 (1H, ddd,J= 12.9, 3.4,1.7 Hz, H-2a), 1.25 (1H, m, H-2b), 1.18 (3H, s, H-12),1.16 (3H, s, H-13), 0.94 (3H,s, H-11);13C-NMR (150 MHz, CD3OD)δ: 200.3 (C-9), 145.4 (C-7), 133.8(C-8), 70.8 (C-6), 68.8 (C-5), 64.4 (C-3), 47.7 (C-2),41.3 (C-4), 36.1 (C-1), 29.8 (C-12), 27.4 (C-10), 25.1(C-11), 20.0 (C-13)。以上数据与文献报道一致[26],故鉴定化合物 7 为 (3S,5R,6S,7E)-3,5,6-trihydroxy-7-megastigmen-9-one。
化合物 8:白色无定形粉末,分子式为C30H46O3,HR-ESI-MSm/z: 455.351 4 [M+H]+(计算值455.352 0)。1H-NMR (400 MHz, CDCl3)δ: 5.30(1H, s, H-12), 2.84 (1H, m, H-18), 2.54 (1H, m, H-2),2.36 (1H, m, H-2), 1.14 (3H, s, H-27), 1.08 (3H, s,H-23), 1.05 (3H, s, H-25), 1.03 (3H, s, H-24), 0.93(3H, s, H-30), 0.91 (3H, s, H-29), 0.81 (3H, s, H-26);13C-NMR (100 MHz, CDCl3)δ: 217.9 (C-3), 183.7(C-28), 143.8 (C-13), 122.6 (C-12), 55.5 (C-5), 47.6(C-4), 47.0 (C-9), 46.7 (C-17), 45.9 (C-19), 41.9(C-14), 41.2 (C-18), 39.4 (C-1), 39.3 (C-8), 36.9(C-10), 34.3 (C-2), 33.9 (C-21), 33.2 (C-29), 32.6(C-22), 32.3 (C-7), 30.8 (C-20), 27.8 (C-15), 26.6(C-23), 25.9 (C-27), 23.7 (C-30), 23.6 (C-1), 23.1(C-16), 21.6 (C-24), 19.7 (C-6), 17.2 (C-26), 15.2(C-25)。以上数据与文献报道一致[27],故鉴定化合物8 为齐墩果酮酸。
化合物9:无色针状结晶(甲醇),分子式为C22H26O9,HR- ESI-MSm/z: 435.165 3 [M+H]+(计算值435.165 0)。1H-NMR (400 MHz, CD3OD)δ:7.35 (2H, s, H-2, 6), 6.69 (2H, s, H-2′, 6′), 4.61 (1H, s,H-7′), 4.26 (1H, m, H-8), 4.19 (2H, m, H-9a, 9b), 3.88(6H, s, 3, 5-OMe), 3.82 (6H, s, 3′, 5′-OMe), 3.64 (2H,m, H-9′a, 9′b), 2.61 (1H, m, H-8′);13C-NMR (100 MHz, CD3OD)δ: 200.3 (C-7), 149.2 (C-3′, 5′), 148.1(C-3, 5), 136.2 (C-4), 132.9 (C-1′), 128.0 (C-1), 107.7(C-2, 6), 105.1 (C-2′, 6′), 85.4 (C-7′), 71.6 (C-9), 61.3(C-9′), 56.9 (3, 5-OMe), 56.8 (3′, 5′-OMe), 55.2(C-8′), 49.9 (C-8)。以上数据与文献报道一致[28],故鉴定化合物9 为刺五加酮。
化合物10:无色油状物,分子式为C10H14O4,HR-ESI-MSm/z: 221.077 5 [M+Na]+(计算值221.078 4)。1H-NMR (400 MHz, CD3OD)δ: 7.30(2H, d,J= 8.6 Hz, H-2′, 6′), 6.89 (2H, d,J= 8.6 Hz,H-3′, 5′), 4.55 (1H, d,J= 6.2 Hz, H-1), 3.78 (3H, s,4′-OMe), 3.66 (1H, m, H-2), 3.47 (1H, m, H-3b), 3.34(1H, m, H-3a);13C-NMR (100 MHz, CD3OD)δ: 160.7(C-4′), 135.3 (C-1′), 129.1 (C-2′, 6′), 114.6 (C-3′, 5′),77.6 (C-2), 75.2 (C-1), 64.2 (C-3), 55.7 (4′-OMe)。以上数据与文献报道一致[29],故鉴定化合物10 为phenylpropanoid。
化合物11:无色针状结晶(甲醇),分子式为C19H30O7,HR-ESI-MSm/z: 393.188 0 [M+Na]+(计算值393.188 4)。1H-NMR (400 MHz, CD3OD)δ:5.97 (1H, t,J= 7.8 Hz, H-1′), 5.91 (1H, s, H-2), 4.43(1H, d,J= 7.8 Hz, H-1′′), 4.04 (1H, m, H-3′), 2.62 (2H,m, H-2′), 2.37 (2H, d,J= 6.0 Hz, H-6), 2.30 (3H, s, H-9),1.34 (3H, d,J= 5.3 Hz, H-4′), 1.22 (6H, s, H-7, 8);13C-NMR (100 MHz, CD3OD)δ: 202.1 (C-1), 159.1(C-3), 143.7 (C-4), 134.4 (C-1′), 125.6 (C-2), 103.9(C-1′′), 78.2 (C-3′′), 77.9 (C-3′), 77.2 (C-5′′), 75.3(C-2′′), 71.7 (C-4′′), 62.8(C-6′′), 54.7 (C-6), 39.3(C-5), 37.7 (C-2′), 29.3 (C-8), 29.2 (C-7), 22.7 (C-9),22.2 (C-4′)。以上数据与文献报道一致[30],故鉴定化合物 11 为 (Z)-4-[30-(β-D-glucopyranosyloxy)butylidene]-3,5,5-trimethyl-2-cyclohexen-l-one。
化合物12:无色固体,分子式为C19H30O7,HR-ESI-MSm/z: 393.188 2 [M+Na]+(计算值393.188 4)。1H-NMR (400 MHz, CD3OD)δ: 5.88(1H, s, H-4), 5.74 (1H, dd,J= 15.4, 9.3 Hz, H-7), 5.58(1H, dd,J= 15.4, 7.8 Hz, H-8), 4.49 (1H, m, H-9),4.34 (1H, d,J= 7.8 Hz, H-1′), 3.87 (1H, dd,J= 11.9,2.1 Hz, H-6′a), 3.64 (1H, dd,J= 11.9, 5.9 Hz, H-6′b),3.23 (4H, m, H-2′), 2.71 (1H, d,J= 9.3 Hz, H-6), 2.44(1H, d,J= 16.7 Hz, H-2b), 2.07 (1H, d,J= 16.7 Hz,H-2a), 1.94 (3H, d,J= 1.4 Hz, H-13), 1.28 (3H, d,J=5.9 Hz, H-10), 1.05 (3H, s, H-11), 1.03 (3H, s, H-12);13C-NMR (100 MHz, CD3OD)δ: 201.9 (C-3), 165.5(C-5), 137.1 (C-8), 131.4 (C-7), 126.2 (C-4), 101.0(C-1′), 78.3 (C-3′), 78.2 (C-5′), 75.0 (C-2′), 74.8 (C-9),71.8 (C-4′), 62.9 (C-6′), 56.9 (C-6), 48.4 (C-2), 37.1(C-1), 28.1 (C-12), 27.7 (C-11), 23.7 (C-13), 22.2(C-10)。以上数据与文献报道一致[31],故鉴定化合物12 为3-oxo-α-ionol-β-D-glucopyranoside。
化合物13:无色针状结晶(甲醇),分子式为C26H32O11,HR-ESI-MSm/z: 519.187 3 [M-H]−(计算值519.187 2)。1H-NMR (400 MHz, CD3OD)δ:6.86 (6H, m, H-2, 5, 6, 2′, 5′, 6′), 4.85 (1H, d,J= 7.0 Hz, H-1′′), 4.74 (1H, d,J= 4.0 Hz, H-7), 4.69 (1H, d,J= 4.0 Hz, H-7′), 4.22 (2H, m, H-9, 9′), 3.85 (6H, s, 3,3′-OMe), 3.11 (2H, m, H-8, 8′);13C-NMR (100 MHz,CD3OD)δ: 150.9 (C-3′), 149.1 (C-3), 147.5 (C-4),147.3 (C-4′), 137.5 (C-1′), 133.7 (C-1), 120.1 (C-6),119.8 (C-6′), 117.9 (C-5), 116.1 (C-5′), 111.6 (C-2),110.9 (C-2′), 102.8 (C-1′′), 87.5 (C-7′), 87.1 (C-7),78.2 (C-5′′), 77.8 (C-3′′), 74.9 (C-2′′), 72.7 (C-9′), 72.7(C-9), 71.3 (C-4′′), 62.5 (C-6′′), 56.7 (3-OMe), 56.4(3′-OMe), 55.5 (C-8′), 55.4 (C-8)。以上数据与文献报道一致[32],故鉴定化合物13 为 (+)-pinoresinol-β-Dglucopyranoside。
化合物14:白色粉末状结晶(甲醇),分子式为C15H20O6,HR-ESI-MSm/z: 319.115 2 [M+Na]+(计算值319.115 2)。1H-NMR (400 MHz, CD3OD)δ:6.36 (1H, d,J= 15.8 Hz, H-7), 6.15 (1H, dq,J= 15.8,6.5 Hz, H-8), 3.80 (5H, m, H-2′~6′), 1.85 (3H, d,J=6.5 Hz, H-9);13C-NMR (100 MHz, CD3OD)δ: 158.1(C-4), 133.8 (C-1), 131.6 (C-7), 127.8 (C-2, 6), 124.8(C-8), 117.8 (C-3, 5), 102.4 (C-1′), 78.1 (C-3′), 77.9(C-5′), 74.9 (C-2′), 71.4 (C-4′), 62.5 (C-6′), 18.5 (C-9)。以上数据与文献报道一致[33],故鉴定化合物14 为trans-4-(1-propenyl)-phenol-β-D-glucopyranoside。
化合物15:白色粉末状结晶(甲醇),分子式为C15H20O6,HR-ESI-MSm/z: 319.114 9 [M+Na]+(计算值319.115 2)。1H-NMR (400 MHz, CD3OD)δ:7.11 (2H, d,J= 8.6 Hz, H-2, 6), 7.03 (2H, d,J= 8.6 Hz, H-3, 5), 5.95 (1H, m, H-8), 5.06 (1H, d,J= 15.4 Hz, H-9b), 5.02 (1H, d,J= 8.9 Hz, H-9a), 3.90 (1H,dd,J= 12.0, 1.9 Hz, H-6b), 3.71 (1H, dd,J= 12.0, 4.8 Hz, H-6a), 3.45 (4H, m, H-2′~5′), 3.33 (2H, d,J= 7.1 Hz, H-7);13C-NMR (100 MHz, CD3OD)δ: 157.5(C-4), 139.2 (C-8), 135.2 (C-1), 130.5 (C-3, 5), 117.8(C-2, 6), 115.7 (C-9), 102.5 (C-1′), 78.0 (C-3′), 77.9(C-5′), 74.9 (C-2′), 71.4 (C-4′), 62.5 (C-6′), 40.3(C-7)。以上数据与文献报道一致[34],故鉴定化合物15 为1-O-β-D-glucopyranosyl-4-allybenzene。
化合物16:无定形粉末,分子式为C16H22O7,HR-ESI-MSm/z: 350.1292 [M +Na]+(计算值350.129 2)。1H-NMR (400 MHz, CD3OD)δ: 7.03(1H, d,J= 2.0 Hz, H-2), 6.93 (1H, d,J= 8.3 Hz, H-5),6.83 (1H, dd,J= 8.3, 2.0 Hz, H-6), 5.96 (1H, ddt,J=17.0, 10.0, 6.8 Hz, H-2′), 5.69 (1H, d,J= 7.0 Hz,H-1′′), 5.09 (1H, dd,J= 10.0, 2.0 Hz, H-3′), 5.02 (1H,dd,J= 17.0, 2.0 Hz, H-3′), 3.84 (3H, s, 4-OMe), 3.32(2H, d,J= 6.8 Hz, H-1′)。13C-NMR (100 MHz,CD3OD)δ: 149.1 (C-3), 147.9 (C-4), 139.0 (C-2′),134.6 (C-1), 123.8 (C-6), 118.5 (C-2), 115.8 (C-3′),113.8 (C-5), 102.9 (C-1′′), 78.2 (C-3′′), 77.8 (C-5′′),74.9 (C-2′′), 71.3 (C-4′′), 62.5 (C-6′′), 56.9 (4-OMe),40.5 (C-1′)。以上数据与文献报道一致[35],故鉴定化合物16 为3-hydroxyestragole β-D-glucopyranoside。
化合物17:淡黄色粉末,分子式为C16H12O5,HR-ESI-MSm/z: 307.057 0 [M+Na]+(计算值307.057 7)。1H-NMR (400 MHz, CD3OD)δ: 7.45(2H, d,J= 8.5 Hz, H-2′, 6′), 7.02 (2H, d,J= 8.5 Hz,H-3′, 5′), 6.22 (1H, d,J= 2.1 Hz, H-8), 6.19 (1H, d,J= 2.1 Hz, H-6), 3.78 (3H, s, 5-OMe);13C-NMR (100 MHz, CD3OD)δ: 175.9 (C-4), 162.1 (C-7), 160.5(C-4′), 160.1 (C-2), 159.8 (C-5), 159.6 (C-9), 127.5(C-2′, 6′), 121.6 (C-1′), 115.9 (C-3′, 5′), 106.9 (C-3),106.7 (C-10), 96.7 (C-6), 96.0 (C-8), 57.6 (4-OMe)。以上数据与文献报道一致[36],故鉴定化合物17 为黄花夹竹桃黄酮。
化合物18:无色针状结晶(甲醇),分子式为C16H22O8,HR-ESI-MSm/z: 365.120 6 [M+Na]+(计算值365.120 7)。1H-NMR (400 MHz, CD3OD)δ:6.55 (1H, d,J= 2.0 Hz, H-2), 6.41 (1H, d,J= 2.0 Hz,H-6), 5.93 (1H, ddt,J= 16.9, 10.0, 6.7 Hz, H-2′), 5.73(1H, d,J= 7.0 Hz, H-1′′), 5.07 (1H, dd,J= 16.9, 2.2 Hz, H-3′b), 5.02 (1H, dd,J= 2.2, 1.0 Hz, H-3′a), 3.83(3H, s, 4-OMe), 3.25 (2H, d,J= 6.7 Hz, H-1′);13C-NMR (100 MHz, CD3OD)δ: 152.1 (C-5), 151.6(C-3), 138.7 (C-2′), 137.6 (C-4), 136.7 (C-1), 115.9(C-3′), 111.6 (C-6), 109.2 (C-2), 102.6 (C-1′′), 78.1(C-3′′), 78.0 (C-5′′), 74.9 (C-2′′), 71.3 (C-4′′), 62.5(C-6′′), 61.6 (4-OMe), 40.0 (C-1′)。以上数据与文献报 道 一 致[37], 故 鉴 定 化 合 物 18 为 3,5-dihydroxyestragole 3-O-β-D-glucopyranoside。
化合物19:白色结晶性粉末,分子式为C7H6O3,HR-ESI-MSm/z: 139.038 2 [M +H]+(计算值139.039 0)。1H-NMR (400 MHz, CD3OD)δ: 8.02(1H, dd,J= 7.8, 1.8 Hz, H-6), 7.77 (1H, dd,J= 8.3,1.8 Hz, H-4), 7.34 (1H, t,J= 7.8 Hz, H-5), 6.81 (1H,d,J= 8.3 Hz, H-3);13C-NMR (100 MHz, CD3OD)δ:174.3 (C=O), 163.1 (C-2), 136.1 (C-4), 131.6 (C-6),119.9 (C-5), 117.9 (C-3), 110.9 (C-1)。以上数据与文献报道一致[38],故鉴定化合物19 为水杨酸。
化合物 20:白色无定形粉末,分子式为C13H18O6,HR-ESI-MSm/z: 293.099 3 [M+Na]+(计算值293.099 6)。1H-NMR (400 MHz, CD3OD)δ:7.31 (5H, m, H-2~6), 4.91 (1H, d,J= 11.8 Hz,H-7b), 4.63 (1H, d,J= 11.8 Hz, H-7a), 4.32 (1H, d,J= 7.7 Hz, H-1′α), 3.86 (1H, dd,J= 11.9, 2.1 Hz,H-6′b), 3.66 (1H, dd,J= 11.9, 5.7 Hz, H-6′a);13C-NMR (100 MHz, CD3OD)δ: 139.0 (C-1), 129.3(C-3, 5), 129.2 (C-2, 6), 128.7 (C-4), 103.2 (C-1′),78.1 (C-3′), 78.0 (C-5′), 75.1 (C-2′), 71.7 (C-7), 71.7(C-4′), 62.8 (C-6′)。以上数据与文献报道一致[39],故鉴定化合物20 为benzyl β-D-glucopyranoside。
5.2 化合物对酪氨酸酶抑制活性的影响
采用酪氨酸酶催化L-酪氨酸的方法,对小茴香醋酸乙酯部位分离出的20 个化合物进行体外酪氨酸酶抑制活性筛选,共筛选出5 个活性较好的具有酪氨酸酶抑制作用的化合物(4、13~15、17),其中以化合物15 和17 对酪氨酸酶的抑制作用最为明显,在实验浓度范围内,化合物17 对酪氨酸酶的抑制率已达到88.27%。各化合物IC50结果见表1。5 个化合物IC50均小于阳性药β-熊果苷,其中化合物15 和17 的IC50值最小,表明这2 个化合物对酪氨酸酶抑制作用最强,抑制效果最好,化合物13和14 对酪氨酸酶的抑制率相当,化合物4 在其中抑制效果较弱。
表1 各化合物的酪氨酸酶抑制活性 (, n = 3)Table 1 Tyrosinase inhibitory activity of compounds (,n = 3)

表1 各化合物的酪氨酸酶抑制活性 (, n = 3)Table 1 Tyrosinase inhibitory activity of compounds (,n = 3)
与β-熊果苷相比:*P<0.05*P < 0.05 vs β-arbutin
化合物 IC50/(mg·mL−1)4 0.783±0.024 13 0.532±0.091 14 0.575±0.022*15 0.113±0.032*17 0.092±0.011*β-熊果苷 1.784±0.240
5.3 分子对接结果
通过对酪氨酸酶抑制活性最好的2 个化合物(15、17)进行分子对接并对其打分。
化合物15 对接结果如图1 所示,化合物15 分别通过与酪氨酸酶蛋白中的半胱氨酸(Cys)、甘氨酸(Gly)残基形成氢键,其键长分别为1.9、2.0、2.3、2.8、3.2,分子对接结合能为−3.5 kJ/mol,表明其具有良好的自由能结合能力。
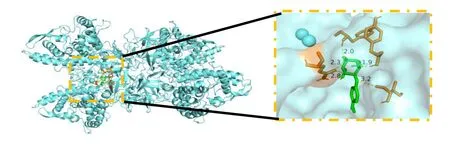
图1 化合物15 分子对接结果Fig. 1 Molecular docking results of compound 15
化合物17 对接结果如图2 所示,化合物17 分别通过与酪氨酸酶蛋白中的Cys 残基形成氢键,其键长分别为2.0、2.0、2.4、2.8,分子对接结合能为−5.74 kJ/mol,表明其具有良好的自由能结合能力。
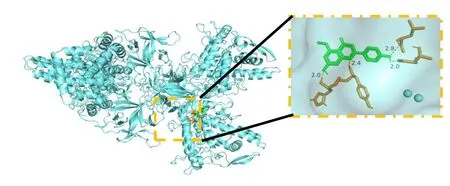
图2 化合物17 分子对接结果Fig. 2 Molecular docking results of compound 17
6 讨论
酪氨酸酶是一种氧化还原酶,广泛存在于植物和动物体中,是生物体合成黑色素的关键酶。黑色素的生物合成是由酪氨酸酶催化体内L-酪氨酸(L-Tyr)生成多巴,多巴经过进一步氧化生成多巴醌,多巴醌再经过一系列的化学反应,最后生成黑色素的过程,研究表明[40],酪氨酸酶的活性与黑色素合成量相关,控制其活力即可控制黑色素生成量。
本研究报道了20 个从小茴香醋酸乙酯部位分离出来的化合物,并对其进行抑制酪氨酸酶活性实验,实验结果显示化合物4、13~15、17 具有良好的酪氨酸酶抑制活性,抑制效果均高于阳性药β-熊果苷,其中化合物15 和17 效果最好,其IC50分别为0.113、0.092 mg/mL,基于此对化合物15 和17进行分子对接,分子对接结果显示化合物15 具有更好的与酪氨酸酶蛋白结合的能力,该结果与活性实验结果一致。化合物15 抑制效果优于化合物14,可能由于化合物15 的末端双键具有更好的代替多巴被氧化成黑色素这一过程,因此化合物15 的效果优于化合物14。本研究结果将为小茴香化学成分美白效果的进一步开发和利用提供科学依据和参考价值。
利益冲突所有作者均声明不存在利益冲突

