节制索上右束支起源的特发性室性心律失常的心电图特征及射频消融疗效
胡志鹏 梁卓 刘旭 张涛 王云龙
节制索(moderator band,MB)是位于右心室内的心肌结构,最常见的起源点为室间隔中部,从右心室前间隔流入道的下部连接至位于右心室游离壁的前乳头肌基底部,是隔缘小梁的一部分,为三尖瓣前乳头肌提供物理支撑[1]。右心浦肯野系统由右束支(right bundle branch,RBB)及浦肯野纤维构成。RBB通过MB分布于前乳头肌与右心室游离壁,形成心内膜下心室丛[2](图1)。目前,部分研究阐述了乳头肌起源的室性心律失常特点,仅有少量研究报道了MB上起源的室性心律失常(ventricular arrhy thm ias,VAs)[3-6]。但关于M B上RBB起源的VAs的研究甚少。本研究纳入一组右心室MB上RBB(MB-RBB)来源的VAs,主要研究其心电图及心电生理特点,探讨其射频消融治疗的疗效。
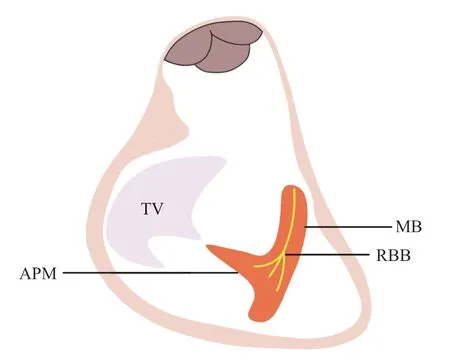
图1 MB、RBB 与APM 解剖关系Figure 1 The anatom ical relationship of MB,RBB and APM
1 对象与方法
1.1 研究对象
2019年4月至2022年7月连续就诊于首都医科大学附属北京安贞医院心律失常中心的290例接受射频消融的特发性VAs患者中,经心内电生理检查明确诊断为M B-RBB起源VAs 10例。所有患者接受射频消融治疗前均使用过至少1种抗心律失常药物,且药物治疗难以控制。消融术前所有患者停用抗心律失常药物5个半衰期以上,签署知情同意书后接受电生理检查及射频消融治疗。本研究遵循《赫尔辛基宣言》,通过了首都医科大学附属北京安贞医院伦理委员会批准。
1.2 体表心电图
患者术前均记录窦性心律及VAs时的12导联心电图,走屏速度100 mm/s,测量并分析QRS形态;电轴;QRS宽度; V1、V2导联R波时限;V1、V2导联RS间期(从QRS波起始到S波最低点的持续时间);胸前导联移行位置;V1、V2导联S波下降支是否存在切迹。
1.3 电生理检查、标测及消融
所有患者均经股静脉8.5 F长鞘(SL1,Abbott M ed ical,Nathan Lane North Plym ou th,M N)或者可调弯鞘(Agilis NxT,Abbott M edical)经三尖瓣环置入右心室,以3.5 mm盐水灌注导管(NaviStar SmartTouch,Biosense Webster) 行三维电解剖标测(CARTO,BiosenseWebster,Dia-mondBar,CA,USA)及消融。将10 F心腔内超声(intracardiac echocardiography,ICE)导管(SoundStar; Biosense Webster)经股静脉置入右心房及右心室,通过短轴和长轴成像对右心室及M B进行三维解剖重建。以ICE导管的实时腔内图像确定消融导管位置。1例患者沿M B放置十极导管(DECA,Biosense Webster)进行标测。在窦性心律和VAs时采集激动图,确定H is-RBB的激动顺序及最早激动位点(earliest activation site,EAS)。局部激动时间定义为从局部电位开始到QRS波开始的时间间隔。双极信号30~500 Hz。起搏标测时的起搏周长为500 ms,刺激电流为起搏阈值+1 m A。良好的起搏标测定义为相对于自发VAs QRS波群,起搏的QRS波群在12个导联中的11个导联匹配。无自发性VAs的患者予以静脉滴注异丙肾上腺素(2~5 mg/m in)。在EAS上以功率控制模式(35 W,17 m l/m in,43℃)射频消融60 s。若消融5 s后室性期前收缩(premature ventricular contraction,PVC)未消失或室性心动过速不能终止,则重新标测靶点。消融后等待30 m in重复静脉应用异丙肾上腺素未见自发或可诱导的VAs,证明消融成功。
1.4 随访
射频消融术后常规心电监护至少24 h,所有患者术后停用抗心律失常药物,并随访至少6个月,术后3个月每月复查24 h动态心电图。
1.5 统计学分析
使用SPSS 26.0统计软件进行统计分析。计量资料以均值±标准差()表示,采用Studentt检验进行比较;计数变量以例数(构成比)表示,采用卡方检验或Fisher精确概率法检验进行比较。以P<0.05为差异有统计学意义。
2 结果
2.1 临床特征及心电图特征
本研究共入选10例患者,男性4例,平均年龄(39.7±15.4)岁。平均症状持续时间为(12.5±9.7)个月。9例表现为频发性PVC,1例(病例8)表现为阵发性室性心动过速。所有PVC患者平均期前收缩负荷为24 h动态心电图(19 300±5 717)次,左心室射血分数(63.0±4.7)%。所有患者均无明显心脏结构异常。
窦性心律下体表心电图均无明显异常。发病时体表心电图呈典型的左束支传导阻滞(left bundle branch block,LBBB)图形,发作VAs时QRS波时限为(120.10±7.35)ms,电轴均向左上;RS时限V1导联平均为(50.00±6.26)ms,V2导联平均为(49.50±6.71)ms;R波时限V1导联平均为(23.10±3.30)ms,V2导联平均为(22.60±4.22)ms(表1)。V1、V2导联均为rS波,且S波无顿挫,VAs时R波移行于V4~V6导联,均晚于窦性心律,V6导联均有正向R波(图2)。

表1 起源于MB-RBB VAs 体表心电图分析Table1 Electrocardiographic characteristics of MB-RBB VAs

图2 MB-RBB VAs 体表12 导联心电图,扫描速度为100 mm/sFigure 2 Twelve-lead electrocardiogram of MB-RBB VAs.The sweep speed was 100 mm/s
2.2 MB标测及消融
所有患者均标测到窦性心律下RBB传导顺序,结果显示RBB沿MB由近端到远端传导。在VAs时EAS处均有领先的RBB电位,领先PVC体表心电图(17.80±2.82)m s,同时靶点位置窦性心律下也有RBB电位。在VAs下行激动标测,可见RBB双向传导(图3)。平均HV间期为(-21.10±4.01)ms。10例患者中,5例(病例1、5、7、8、10)EAS位于MB游离壁侧,4例(病例2、3、4、6)位于MB体部,1例(病例9)位于MB间隔部,起搏标测图形3例(病例3、5、8)患者与自发VAs图形相似。消融领先RBB电位均有效地消除了VAs。消融后10例患者中6例(2、4、7、8、9、10)出现右束支传导阻滞(right bund le branch block,RBBB),随访过程中2例(病例4、8)术后RBBB恢复。所有患者术中及术后均未出现并发症。
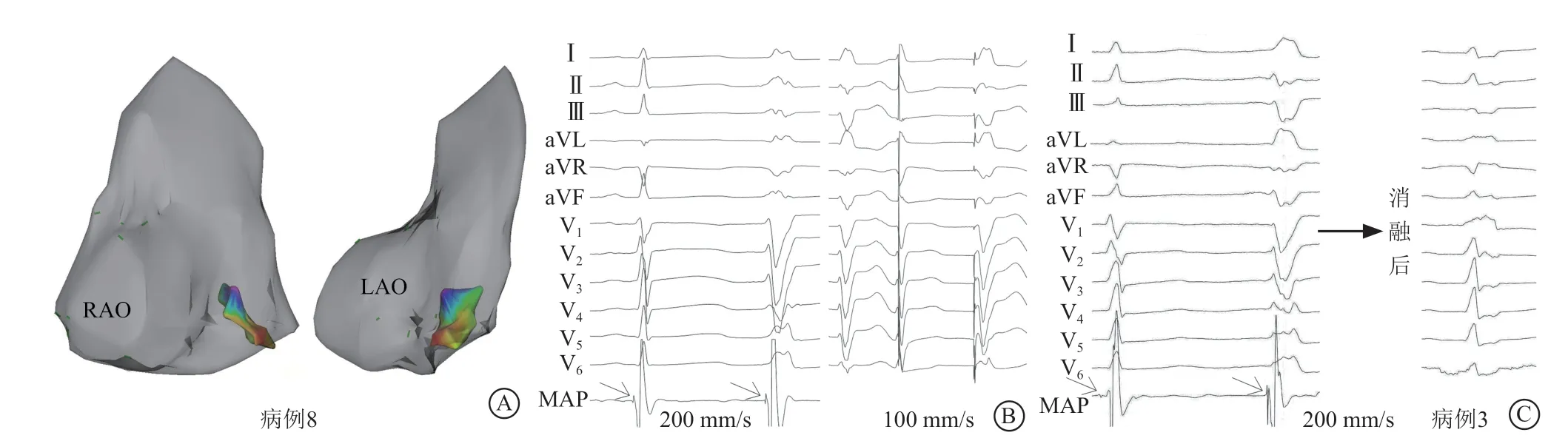
图3 三维标测及心腔内电生理图 A.病例8 发作VAs 时消融导管标测MB 示游离壁侧激动最早,激动沿MB 向双侧传导;B.病例8 于窦性心律及VAs 时均可在EAS 处标测到领先于QRS 波的RBB 电位(箭头所示),消融导管起搏图形不佳;C.病例3 于窦性心律及VAs 时均可在EAS 处标测到领先于QRS 波的RBB 电位(箭头所示),消融后出现右束支阻滞。Figure 3 Three-dimensional mapping and intracardiac electrophysiological mapping.
2.3 疗效及随访
所有患者均消融成功,术后均无脑卒中、脑出血、心脏压塞、冠状动脉损伤及瓣膜损伤等。术后随访过程中,所有患者均停用抗心律失常药,且无VAs复发。
3 讨论
本研究通过ICE导管构建MB、右心室等结构,以消融导管标测VAs,明确起源于MB-RBB VAs心电图及心电生理特点:(1)心电图表现为典型LBBB、电轴左偏、呈现较窄的QRS波群、胸前导联R波移行晚于窦性心律;(2)VAs下激动标测可见RBB双向传导,且消融领先RBB电位均有效消除了VAs;(3)消融后患者中部分出现了RBBB。这与既往研究结果相一致[3-4,7-10]。
在研究中发现M B-RBB VAs的QRS波较窄,呈典型LBBB图形,这些特征符合His-Purkin je系统来源的VAs[11]。在本研究中,通过ICE定位及起搏标测发现游离壁侧、MB体部及间隔侧的PVC形态无明显区别,这与既往研究结果相一致[4]。M BRBB VAs于EAS前可标记到领先的RBB电位,消融领先的RBB电位成功消除了VAs,且消融后部分患者出现了RBBB,支持VAs起源于RBB的理论。本研究中患者术后随访过程中均未出现VAs复发,故不能明确出现RBBB及阻滞的恢复是否对患者的预后有所影响。既往研究M B起源VAs中部分患者并未在EAS处标测到RBB电位[3-4,12]。这可能与VAs具体起源的组织成分不同有关,即这些VAs起源于MB的心肌组织,而并非起源于MB-RBB。既往研究总结了起源于前乳头肌的VAs特点,其心电图V1和V2导联的平均RS间期更长,S波下降支斜率更低,V1或V2导联S波下降支切迹更常见,V2导联的平均R波持续时间更长,用消融导管进行标测时,RBB电位少见[5,9,13]。
由于RBB在MB上位置表浅,标测过程中导管的机械接触可引起RBBB,而且MB形态及解剖位置多变,消融导管在MB上的压力难以保持稳定,过度的机械刺激可能导致VAs无法诱发,因此谨慎且细致的导管操作极其重要[7,9,14]。三维标测技术对射频消融有着良好指导作用,在治疗过程中应用ICE对MB的定位有益[3,8,15]。既往研究提示冷冻消融相对于射频消融具有更好的接触稳定性,这可能有益于MB的消融[16]。
相比既往研究,本研究更关注于MB-RBB VAs的心电图及电生理特征,遇到符合上述特征的VAs心电图时,重点标测MB及RBB电位可能提高手术成功率及消融效率。临床工作中发现近似心电图特征时建议应用ICE导管进一步构建MB及临近解剖部位结构,这有助于指导消融过程。
本研究存在一定局限性。本研究为观察性研究,纳入的样本量较小,结论仍需要大规模临床数据支持。
利益冲突 所有作者均声明不存在利益冲突

