替雷利珠单抗药物利用评价标准的建立与应用
周 炜,蒋俊杰,夏一淼,王利媛,王法财
0 引言
免疫检查点抑制剂(Immunological checkpoint inhibitors,ICIs)的发现和应用改变了肿瘤的治疗方式[1]。最受关注的ICIs主要有抗程序性死亡受体1(Programmed death-1,PD-1)药物和抗程序性死亡受体配体1(Programmed death-ligand 1,PD-L1)药物等[2-4]。2019年12月,替雷利珠单抗(Tislelizumab)首次通过国家药品监督管理局(NMPA)批准,用于治疗典型霍奇金淋巴瘤患者,之后又获批多个适应证[5-6]。本文主要基于药物利用评价(Drug use evaluation,DUE)标准,结合药品说明书、指导原则、临床指南和专家共识等参考资料,制定我院替雷利珠单抗的合理应用评价标准,为临床合理用药提供参考。
1 资料与方法
1.1 资料 自2019年12月替雷利珠单抗上市以来,已获批多个适应证。经医院药事管理和药物治疗学委员会通过,替雷利珠单抗(商品名:百泽安,规格:10 ml∶100 mg,贮藏方式:避光,2~8 ℃保存,国药准字:S20190045,生产企业:广州百济神州生物制药有限公司)于2020年10月进入我院药品目录。采用医院信息系统(HIS系统)及合理用药系统(PASS系统)抽取2021年1月1日至2022年12月31日六安市人民医院使用替雷利珠单抗的出院患者。纳入标准:在医院医嘱信息中共使用至少2个疗程的替雷利珠单抗。
1.2 替雷利珠单抗DUE标准的建立 主要基于替雷利珠单抗药品说明书,并参考《新型抗肿瘤药物临床应用指导原则(2022版)》《2023CSCO免疫检查点抑制剂临床应用指南》《中国非小细胞肺癌免疫检查点抑制剂治疗专家共识(2020年版)》《免疫检查点抑制剂相关不良反应的管理专家共识》、相关肿瘤诊疗规范和国内外相关文献。根据DUE标准的基本要求,初步拟定替雷利珠单抗DUE标准,并通过抗肿瘤药物治疗管理组相关专家讨论和修订,最终确定替雷利珠单抗的DUE标准。确定替雷利珠单抗DUE标准为用药指征、用药过程、用药结果和用药监护共4个一级指标和16个二级指标。见表1。

表1 替雷利珠单抗DUE标准
1.3 建立替雷利珠单抗医嘱点评标准 设计点评表格,主要包括患者姓名、性别、年龄、住院号、住院科室、入院时间、住院时间、出院诊断以及替雷利珠单抗DUE标准所包含的所有内容。
1.4 替雷利珠单抗DUE标准的应用 采用医院信息系统抽取使用替雷利珠单抗的用药医嘱,同时获取患者姓名、性别、年龄和住院号等信息。再次采用HIS系统查阅患者实验室检查和影像学检查、用药医嘱和病案信息等。根据患者以上的所有信息,采用替雷利珠单抗DUE标准进行用药合理性评价。
2 结果
2.1 基本情况 抽取2021年1月1日至2022年12月31日使用替雷利珠单抗的病例704例,排除147例仅使用1个疗程的病例,至少使用2个疗程的病例共557例(有3例患者用药8个疗程,年龄23~94岁),557例均有检查信息和完整的病案记录,全部纳入本次研究。男性455例(占81.69%),女性102例(占18.31%)。使用2个疗程的例数最多,占23.70%,其次为3个疗程(占22.08%)。呼吸科患者最多(占44.88%)。因肺癌使用替雷利珠单抗的次数最多(占70.74%),其次为肝癌患者(占22.98%)。见表2。
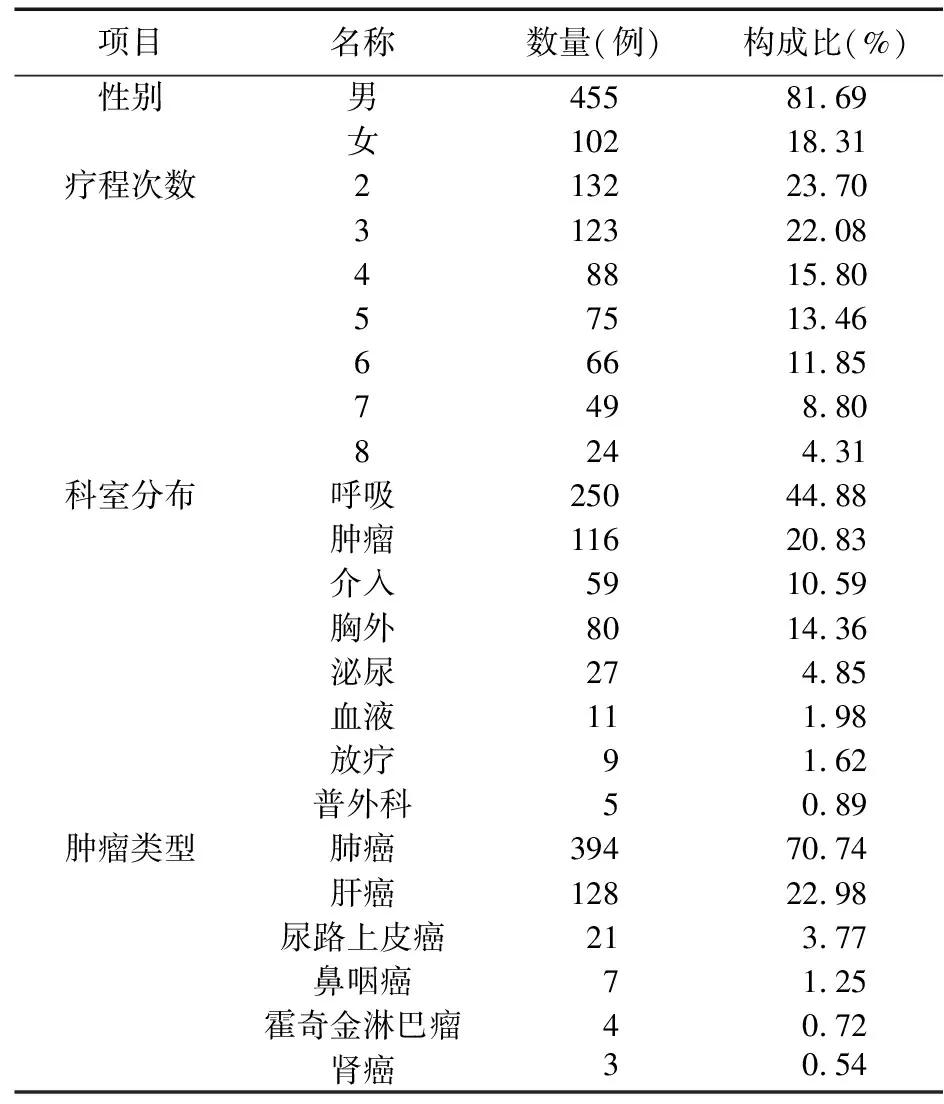
表2 患者基本分布情况
2.2 使用替雷利珠单抗合理性评价结果 临床合理用药直接关系到用药的有效性、安全性和经济性。本研究基于替雷利珠单抗DUE标准,由抗肿瘤药物治疗管理组相关专家和临床药学专家审核替雷利珠单抗使用的合理性,并对结果进行统计分析。合理率为100%的项目有禁忌证、基线要求、给药方式、溶媒配制、配伍、适用年龄、患者肝肾损伤情况和器官移植情况。用药指征不适宜15例,不合理率为2.69%。预防性使用激素68例,不合理率为12.21%。不良反应累及系统和器官及主要临床表现见表3。临床不合理用药分布情况见表4。

表3 不良反应发生情况
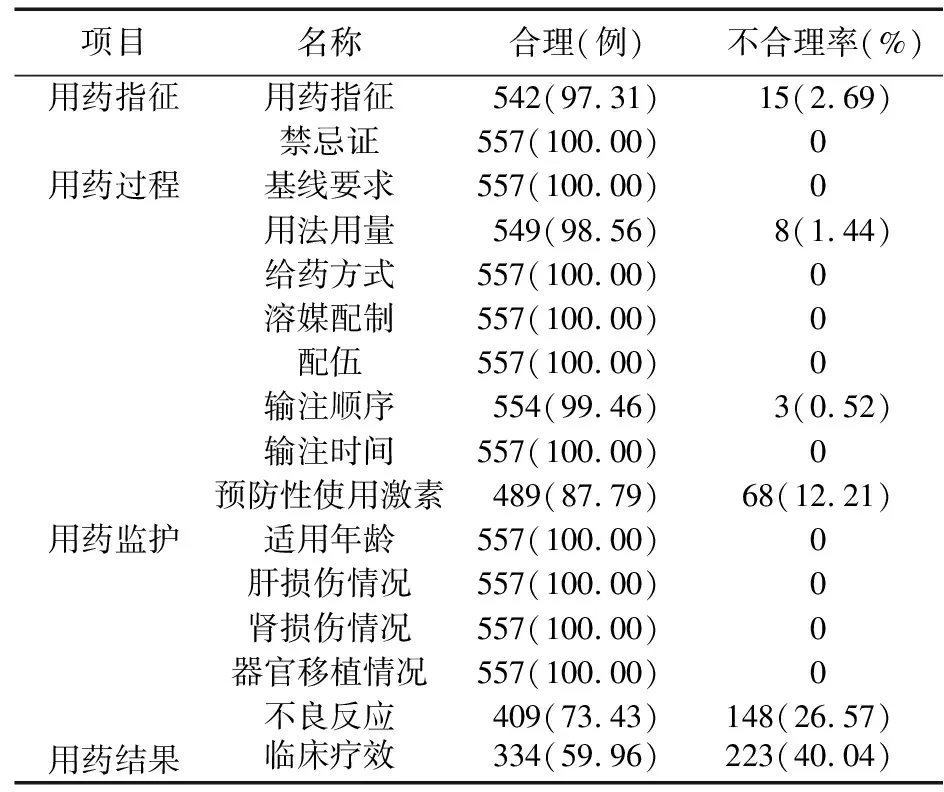
表4 临床不合理用药分布情况[例(%)]
3 讨论
由于ICIs的药理机制基本一致,不具有靶向性,因此有多个适应证。在临床应用中,可能出现超适应证用药情况,导致疗效降低、增加用药风险和经济负担。ICIs引起的药品不良反应发生时间中位数约为8周[7-9],因此,对于仅使用1次替雷利珠单抗者,无法准确判断不良反应发生情况,甚至无法观察用药的结果。本研究纳入至少有2次使用替雷利珠单抗医嘱的病例。
3.1 用药指征合理性分析 本研究中,用药指征不适宜15例。其中,有12例肝恶性肿瘤患者使用替雷利珠单抗不适宜。根据替雷利珠单抗药品说明书和《2023CSCO免疫检查点抑制剂临床应用指南》,使用替雷利珠单抗时,患者应至少接受过1种全身肝细胞癌(HCC)治疗。本研究中,有12例使用替雷利珠单抗之前,并未进行全身性肝细胞癌治疗。有3例使用替雷利珠单抗治疗肾癌,在药品说明书及指南中并未提及其可以用于肾癌。
《原发性肝癌诊疗指南(2022年版)》[10]指出,替雷利珠单抗作为二线抗肝细胞癌证据等级3级,B类推荐。《肝细胞癌免疫治疗中国专家共识(2021版)》中,替雷利珠单抗作为二线免疫治疗方案证据等级Ⅱb,A类推荐[11]。一项全球、多中心的Ⅱ期研究(RATIONALE208)结果显示,替雷利珠单抗用于接受过一线全身治疗患者的客观缓解率(ORR)为13.8%[12]。替雷利珠单抗并不作为肝细胞癌的一线用药。研究表明,替雷利珠单抗用于治疗肾癌具有较好的疗效和安全性,但是由于病例数较少,并不具有较高的指导价值[13-14]。替雷利珠单抗说明书中并未提及其可用于治疗肾癌,本文中,有3例使用替雷利珠单抗治疗肾癌,属于超说明书用药。近年来,随着新型ICIs研发投入增加,新的ICIs上市速度加快,一些具有高级别循证医学证据的ICIs用法未能及时在药品说明书中得到修订,限制了临床治疗的发展。广东省药学会发布的《超药品说明书用药目录(2022年版)》和《山东省超药品说明书用药专家共识(2021年版)》[15]均未表明替雷利珠单抗可以用于肾癌的免疫治疗。本次合理用药评价发现,3次替雷利珠单抗用于肾癌的治疗属于超说明书用药,且属于不合理用药。
3.2 用药过程合理性分析 本研究中,有8例使用替雷利珠单抗100 mg,每3周1次。替雷利珠单抗药品说明书推荐剂量为200 mg/次,每3周1次,轻中度肝肾功能不全时无需调整剂量。此8例病例未出现严重的肝肾功能不全。ICIs的药代动力学/药效学特性与传统的细胞毒性和小分子抗肿瘤药物不同。因此,不能完全使用传统的药动学模型来确定ICIs的最佳剂量。ICIs最初根据体重给药,随着人群药代动力学数据的积累,研究显示,固定剂量的给药方案可以改善ICIs治疗效果[16-17]。只有患者疗效得到保证的情况下,才能更改用药方案。替雷利珠单抗说明书和《2023CSCO免疫检查点抑制剂临床应用指南》均未提到根据体重调整剂量,而是使用固定剂量。因此,此8例使用替雷利珠单抗100 mg (每3周1次)的医嘱判定为不合理。
另外,有3例为替雷利珠单抗与铂类药物同日输注,并未在铂类药物输注前用药。在使用ICIs前使用铂类药物,可能会抑制ICIs药物的药效。一项关于PD-1/L1和MAPK靶向治疗用药先后顺序的研究表明,PD-1/L1抑制剂先于MAPK抑制剂用药,可能会克服先天和后天的抗性[18]。通过促进巨噬细胞的促炎症极化和巨噬细胞的克隆性扩展,使反应的持久性得到提高,进而提高用药的有效性。唐浩淳等[19]研究ICIs与化疗用药顺序对免疫相关不良反应的影响,结果表明,先使用ICIs后行化疗治疗的患者,其免疫治疗相关不良反应(Immune-related adverse events,irAEs)发生率(44.0%)远低于先行化疗后使用ICIs的患者(64.0%)。丘九望等[20]关于ICIs与化疗使用先后顺序的研究表明,先使用ICIs激发人体的免疫系统以达到更好的效果,同样可减少药品不良反应。因此,这3例在使用铂类药物之后应用替雷利珠单抗,属于不合理用药。
在用药过程中发现预防性使用激素不合理的例数最多,共68例,不合理率为12.21%。ICIs影响机体的免疫系统,在使用过程中可影响所有的器官和系统[21]。常见的不良反应有疲劳、瘙痒、皮疹和腹泻等,也可能会出现肺炎、肝炎和神经毒性等严重的irAEs[22]。研究表明,ICIs的发生率在20%左右[23-24]。有临床医生在临床治疗过程中因担心出现irAEs而预防性使用糖皮质激素。糖皮质激素通过多种作用影响免疫细胞的凋亡、分化、细胞因子的释放和克隆扩增,从而影响T细胞的活化和降低免疫调节作用[25]。研究表明,预防性使用糖皮质激素可降低ICIs治疗非小细胞肺癌(Non-small cell lung cancer,NSCLC)的疗效[26-27]。替雷利珠单抗药品说明书中明确表示不能预防性使用糖皮质激素,可以在使用替雷利珠单抗后使用糖皮质激素治疗irAEs。因此,68例预防性使用糖皮质激素属于不合理用药。
3.3 用药监护情况分析 在用药监护过程中,患者年龄、肝损伤、肾损伤和器官移植情况全部符合用药条件。然而,药品不良反应发生率较高(26.57%),主要表现为皮肤及其附件系统损害、内分泌系统损害和消化系统损害等。Shen等[28]一项随机Ⅲ期研究(RATIONALE-302)显示,替雷利珠单抗引起的irAEs发生率约为73.3%。Lu等[29]一项随机Ⅲ期研究(RATIONALE-304)显示,替雷利珠单抗引起的3级及以上irAEs发生率高于20%。另外,有研究表明,ICIs的irAEs总体发生率约为50%,甚至更高[8-9]。本研究中的irAEs发生率低,可能与药物本身性质、数据量较少以及实际发生irAEs但病程中并未详细记录有关。本研究中,患者irAEs经停药与积极对症治疗后均好转。需要警惕ICIs可引起严重的irAEs,其中结肠炎、肺炎、肝炎和神经毒性可能导致死亡,有研究表明,ICIs致死亡的发生率约为0.6%[30]。因此,在使用ICIs期间,需要密切监测患者可能发生的irAEs。
3.4 用药效果情况分析 使用替雷利珠单抗的临床疗效主要是根据患者的临床症状是否好转及影像学显示肿瘤体积是否缩小和保持不变进行判断。张敬宝等[31]考察替雷利珠单抗联合吉西他滨+顺铂 (GP)化疗方案治疗晚期NSCLC的疗效及其对免疫功能的影响,其ORR为54.67%。另外,一项关于替雷利珠单抗联合化疗一线治疗局部晚期或转移性非鳞状非小细胞肺癌的肿瘤缓解特征研究显示,其ORR为57.4%[32]。上述研究结果与本研究结果基本一致,表明替雷利珠单抗具有较好的抗肿瘤作用。
综上所述,建立药物利用评价标准,可帮助临床医生准确、快速掌握如何正确合理地使用ICIs。基于药品说明书、《新型抗肿瘤药物临床应用指导原则(2022版)》、《2023CSCO免疫检查点抑制剂临床应用指南》等权威性资料,结合我院临床数据制定的替雷利珠单抗药物利用评价标准,可促进临床合理用药,提高替雷利珠单抗的使用效果,减少药品不良反应和经济负担。

