腹腔镜辅助与常规开腹Soave’s 术治疗患儿先天性长段型巨结肠的疗效对比
李 芊,张宏伟,刘丰丽,张建军
先天性巨结肠症是一种先天性缺陷,由肠神经细胞向远端肠道的异常迁移导致部分肠道神经缺失而造成[1],据统计约每5000 名新生儿中就有1 名患先天性巨结肠,男性和女性患病比例约为4.32 ∶1[2]。 先天性巨结肠最突出的症状是便秘, 其他症状包括呕吐、腹痛、腹泻和生长缓慢等,通常在婴儿出生的头2个月最明显,其并发症包括小肠结肠炎、肠梗阻和肠穿孔等,严重影响患儿预后[3]。目前手术仍然是先天性巨结肠治疗的首选方法,Soave’s 术是最常用的术式之一,即“经直肠肌鞘结肠拖出术”。 是以意大利儿外科医生Franco Soave 的名字命名,包括去除直肠的黏膜和黏膜下层,并将肠管置于无神经节肌的“袖带”内[4]。 传统开腹手术对于患儿创伤大,安全性低,手术风险高; 随着医疗水平的进步和发展, 腹腔镜辅助Soave’s 术治疗越来越广泛。 笔者研究拟对比腹腔镜辅助Soave’s 术与常规开腹Soave’s 术治疗先天性长段型巨结肠对患儿肛门功能及远期并发症的影响,旨在为临床选择治疗方式提供理论依据。
1 资料与方法
1.1 临床资料
回顾性选择徐州市儿童医院诊疗中心2012 年1月至2021 年4 月先天性长段型巨结肠患儿102 例,其中男性83 例,女性19 例;年龄11 天~10 个月,平均年龄3.08 个月(标准差0.48 个月);体质量5.34 ~7.98 kg,平均体质量6.63 kg(标准差0.87 kg);出生体质量2.89 ~3.76 kg,平均出生体质量3.15 kg(标准差0.36 kg);5 例患儿有家族史。参考先天性巨结肠的诊断及治疗专家共识[5]:临床表现如便秘、腹胀、胎粪排出延迟、肛门直肠抑制反射消失等,下消化道造影、直肠肛管测压及直肠黏膜活检诊断为先天性巨结肠(术中冷冻活检进一步证实诊断, 术后对切除标本进行常规组织病理学诊断再次证实)。 根据患儿的手术记录信息,按照手术方式不同分为两组,其中56 例行腹腔镜辅助Soave’s 术患儿作为观察组,46 例行常规开腹Soave’s 术患儿作为对照组。 观察组男性46 例,女性10 例;年龄11 天~10 个月,平均年龄3.12 个月(标准差0.59 个月);体质量5.56 ~7.63 kg,平均体质量6.52 kg(标准差0.91 kg);出生体质量3.01 ~3.76 kg,平均出生体质量3.19 kg (标准差0.37 kg);3例患儿有家族史。对照组男性37 例,女性9 例;年龄15 天~10 个月,平均年龄3.01 个月(标准差0.47 个月);体质量5.34 ~7.98 kg,平均体质量6.75 kg(标准差0.89 kg);出生体质量2.98 ~3.65 kg,平均出生体质量3.13 kg(标准差0.38 kg);2例患儿有家族史。
选择标准:①临床分型为长段型;②年龄为11 天~10 个月的小婴儿; ③患儿家长对笔者研究的内容及过程知晓并且签署知情同意书。
排除标准:①全结肠神经节细胞缺失或唐氏综合征;②早产儿和低体质量儿;③合并先天性心脏病者;④自身免疫病患儿;⑤凝血功能障碍患儿;⑥临床资料不全者。
两组患者的临床资料比较, 差异无统计学意义(P >0.05)。
1.2 方法
1.2.1 手术方法
入院后首先对患儿直肠冲洗7 ~10 d, 术前3 d给予口服抗生素进行肠道准备。 患儿仰卧位,全身麻醉,腹部、阴部和下肢进行消毒处理。
对照组患儿进行常规开腹Soave’s 术:患儿采取膀胱截石位, 扩肛后在肛门处缝4 根线进行牵引,在齿状线上方放置2 根牵引线, 提起上方直肠黏膜,在0.5 cm 处切开直肠黏膜, 进行上下分离直肠黏膜到6 ~7 cm;同时用电刀进行止血,进一步切开直肠肌肉层,彻底暴露直肠上段及乙状结肠后拖出肛门;同时在结扎结肠系膜后拖出乙状结肠,取少量肠壁组织送病理室活检;切开直肠肌鞘后去除多余的肌鞘,呈现前高后低肌鞘, 前距离齿状线3 cm, 后距离齿状线0.5 cm,缝合近端肠管和直肠肌鞘,以及将肠管全层和齿状线上方的直肠黏膜间断缝合。将长约5 cm 管子插入肛门引流,术后留置3 ~7 d。 术后2 周开始扩肛,持续3 ~6 个月。
观察组患儿接受腹腔镜Soave’s 术:腹腔镜在脐部从脐部下缘穿刺建立气腹,于右上腹肝下缘处置5 mm Trocar 放Olympus 45°腹腔镜。 首先进行腹部探查,明确患儿的病变范围,其次取多处的直肠样本作为术中冷冻活检以确认诊断。彻底分离直肠系膜和直肠侧韧带, 反折于腹膜下1 cm 位置后结扎肠系膜血管,检查患儿腹腔脏器有无损伤与肠管有无活动性出血,确定无异常后关闭气腹。开展会阴手术,患儿采取双下肢悬吊截石位,围绕肛门缝合牵引线,牵拉同时暴露肛管直肠黏膜,在齿状线上5 mm 左右进行直肠黏膜环切处理, 近端直肠黏膜缝合处理且向下牵拉,分离黏膜到直肠腹膜反折部位, 拖出游离结直肠,在腹腔镜下检查肠管病变范围,切除病变肠管,缝合完成之后固定肠管,同时通过二氧化碳气腹检查肠管有无出血、扭转,确定无异常后关闭气腹。
1.2.2 观察指标
(1)记录两组患儿围手术期相关指标,包括两组患儿手术时间、术中出血量、术后留置导尿管时间、术后胃肠功能恢复时间、总住院时间等。
(2)术后肛门功能恢复:肛门功能Kelly 评估量表,大便控制(正常没有污粪2 分,偶发漏便1 分,没有控制、经常污粪0 分),污粪(总是清洁2 分,偶发污粪1 分,总是污粪0 分),括约肌(强而有力的收缩2分,弱和部分收缩1 分,没有收缩0 分)。 得分5 ~6分为优,3 ~4 分为良,0 ~2 分为差[6]。
(3)肛门静息压和肛管高压区长度的测量:采用消化道动力仪(Solar GT。Mui Scientific 公司,加拿大)进行肛管高压区长度、肛门静息压的检测。 在测量前应充分清洁肠道,嘱咐患儿尽量排尽尿液,并且采取左侧卧位,右髋关节曲屈,将带气囊的测压导管用石蜡油润滑后,轻轻分开臀缝,将导管缓慢插入肛管,使肛管测压孔进入达10 ~12 cm,给予气囊注气时慢慢向外牵拉导管,记录压力值。 肛门静息压指患儿完全放松30 s 时所测到的压力值; 肛管高压区长度可以反映内外括约肌功能,是在患儿左侧卧位、右髋关节曲屈的过程中,仪器定速缓慢拉出测定时,从高压开始出现到最后消失的长度。
1.2.3 术后并发症
术后随访1 年,记录患儿术后肛周皮炎、肠梗阻、小肠结肠炎、吻合口出血、污粪、大便失禁、便秘复发等情况。
1.3 统计学方法
应用SPSS 23.0 统计软件进行分析。 正态分布的计量资料以均数± 标准差表示,两组之间比较采用t检验,比较同组治疗前后采用配对t 检验;计数资料以绝对数表示, 组间比较采用χ2检验或Fisher 确切概率法检验。 P <0.05 为差异有统计学意义。
2 结果
2.1 两组患儿围手术期指标比较
与对照组相比,观察组手术时间明显缩短,术中出血量减少,总住院时间缩短,差异均有统计学意义(P<0.05)。 但两组胃肠功能恢复时间、术后留置导尿时间比较,差异无统计学意义(P >0.05)。 见表1。
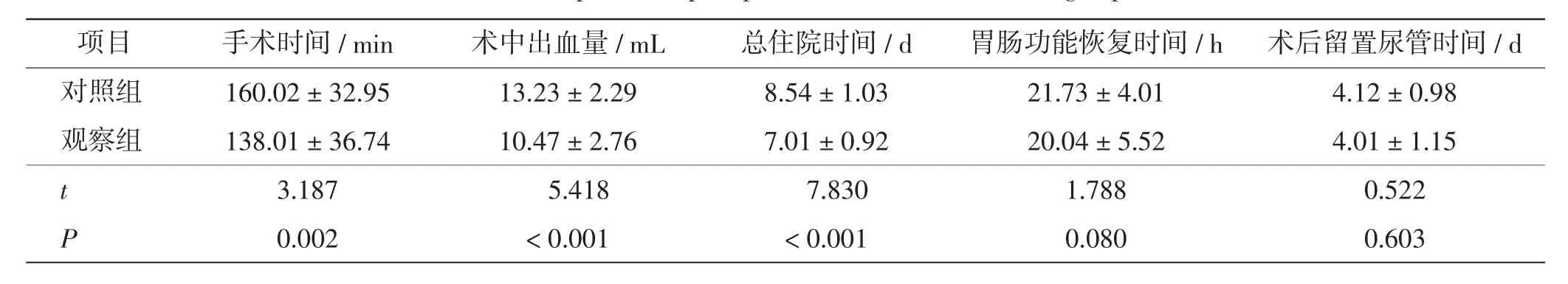
表1 两组患儿围手术期指标比较Tab.1 Comparison of perioperative indicators between 2 groups
2.2 两组患儿肛门恢复功能比较
无论是对照组还是观察组,术后3 个月Kelly 评分都有所升高,且肛管高压区长度和肛门静息压相比术前均有所提高,差异有统计学意义(P <0.05)。 同时,术后3 个月观察组Kelly 评分为(5.83±0.42)分,明显高于对照组;肛管高压区长度、肛门静息压分别为(2.26 ± 0.29) cm、(53.63 ± 7.53) mmHg,与对照组相比,差异有统计学意义(P <0.05)。 见表2。
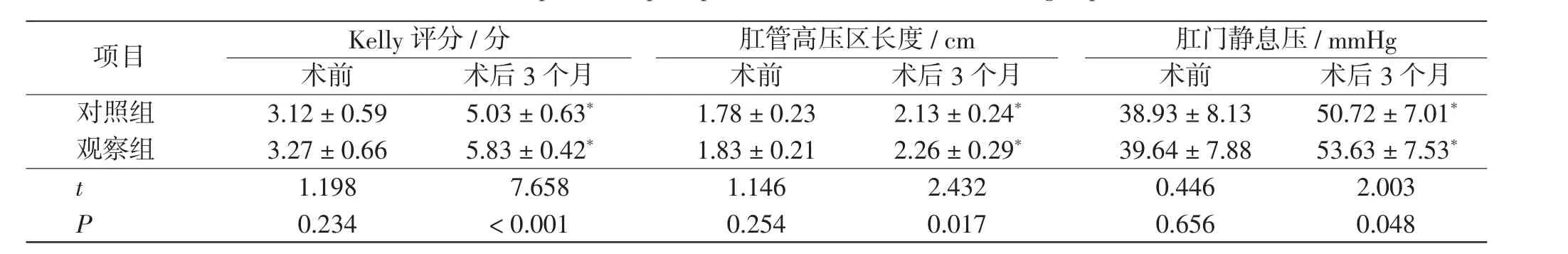
表2 两组患儿术后肛门功能比较Tab.2 Comparison of postoperative anal function between 2 groups
2.3 两组患儿并发症比较
对照组术后1 年并发症,肛周皮炎4 例,肠梗阻1 例,小肠结肠炎6 例,吻合口出血3 例,肛门狭窄10例,污粪3 例,大便失禁1 例,便秘复发4 例,并发症发生率69.57%。观察组术后1 年并发症,肛周皮炎1例,肠梗阻0 例,小肠结肠炎1 例,吻合口出血2 例,肛门狭窄5 例,污粪1 例,大便失禁1 例,便秘复发2例,并发症发生率23.21%。 观察组并发症发生率小于对照组, 差异有显著统计学意义 (χ2=22.010,P=0.001 <0.01)。观察组小肠结肠炎发生率低于对照组,差异有统计学意义(P <0.05)。 见表3。

表3 两组患儿术后1 年并发症情况比较Tab.3 Comparison of complications after operation 1-year between 2 groups
3 讨论
先天性巨结肠的特征是肠内不同程度肠神经系统神经节细胞的缺乏,它是最常见的先天性肠动力障碍,受影响的新生儿通常在出生后的头几天出现远端肠梗阻[7]。 先天性巨结肠可能与唐氏综合征或Waardenburg 综合征等其他遗传疾病相关, 约一半的病例与特定的基因突变有关,其中一些以常染色体显性方式发生。 据报道,如果父母中有一个孩子患有先天性巨结肠,下一个孩子患病风险可达4%[8]。先天性巨结肠分为5 种类型,短段型、常见型、长段型、全结肠型、全肠型。 疾病程度具体取决于肠道受影响的程度。 在极少数情况下,小肠也可能受到影响。 目前的治疗包括切除无神经节细胞的肠管和“拉直”手术以将正常受神经支配的肠管拉至肛缘[9]。 在先天性长段型巨结肠中,患儿极容易患小肠结肠炎,高达75%患儿有失禁或便秘问题,相当一部分患儿继续经历持续的术后肠功能障碍[10],不同程度的大便失禁、便秘和小肠结肠炎会影响患儿及家庭的生存质量,因此探索有效安全的手术方式对于缓解和减少此类患儿的并发症及提高术后生存质量尤为重要。
传统的开腹Soave’s 术对患儿造成创伤大,由于创伤严重,腹部瘢痕明显,腹部脏器暴露时间长,易造成术中出血较多, 术后粘连性肠梗阻可延误进食时间、延长住院时间,术后恢复时间长,患儿易并发多种并发症[11]。 随着腹腔镜器械和手术技术的进步,采用微创治疗成为治疗先天性巨结肠的发展趋势。腹腔镜辅助手术具有创伤小、操作简单、安全有效、并发症少等优点。 近年来,腹腔镜辅助Soave’s 术在多个国家得到广泛成功应用。 自1995 年开展了腹腔镜辅助Soave’s 术, 此后陆续报道了各种腹腔镜下先天性巨结肠根治术,由于长段结肠或全结肠难以通过肛门拔出,长段和全结肠先天性巨结肠是腹腔镜辅助手术的最佳适应证[12,13]。
笔者研究结果发现,腹腔镜术后围手术期指标有所改善,患儿胃肠功能,术后恢复均较快,左铭君等[14]也发现腹腔镜辅助经肛门Soave’s 术后患儿手术时间、住院时间、胃肠功能恢复时间降低与笔者研究结果类似。 同时相比传统手术组,患儿肛门功能也有明显改善。 Fang Y 等[15]总结了32 例采用腹腔镜辅助Soave’s 术的先天性巨结肠患儿,发现所有患儿术后即刻无并发症发生。便秘均未再复发,仅6 例(19.3%)术后3 个月内并发相关性小肠结肠炎,5 例患儿(16.1%)在第一年出现了污粪。长段先天性巨结肠是术后并发小肠结肠炎的独立危险因素,术后3 个月内发生小肠结肠炎最高,由于小肠结肠炎后果严重,可表现为发热、腹泻、腹胀甚至感染性休克[16],因此早期诊断、及时治疗可有效改善小肠结肠炎的预后。 笔者研究发现,腹腔镜辅助Soave’s 术后小肠结肠炎患儿明显减少,说明其效果良好,同时抗感染和输液药物也是重要的术后护理治疗方法。 与传统开腹手术相比,腹腔镜辅助Soave’s 术具有以下优点:首先,该手术通过将直肠与腹膜分离, 再将肠管无神经节部分拉出,减少了对患儿盆腔深部组织的损伤;其次,腹腔镜易于从多方位、多角度观察腹腔和盆腔的结构,并同时处理腹腔内的任何隐匿疾病[17],可更清楚判断神经节段范围,观察有无扭转,监测肠道血液供应及有无腹腔出血等情况,提高操作的准确性。 还可以降低肛门外括约肌损伤的风险,提高新生肠道的粪便储存和排便控制功能,减少便秘的发生率,促进术后恢复[18]。 同时切口小、微创,减少对腹腔的污染,避免肠道暴露。 因此腹腔镜手术后肠道蠕动功能恢复快,减少了肠粘连和肠梗阻的发生。
同时,笔者也总结了腹腔镜辅助Soave’s 术中需要关注的要点。由于患儿腹壁薄,支撑力不足,因此置入套管针后缝合于腹壁, 不仅可以将套管针固定到位,还可以根据术者的需要帮助回缩腹壁,扩大手术视野;其次神经节段根治性切除及肛门神经节段吻合对减少便秘和先天性巨结肠相关性小肠结肠炎的复发具有根治性作用。 术前应仔细复查结肠造影,初步判断狭窄段、移行段和扩张段的区域;术中腹腔镜检查肠道,包括扩张至接近正常厚度,肠壁由粗糙增厚变为薄软,光泽和弹性发生变化。 如果病理报告显示有神经节细胞,则可以确定切除水平。 通过电凝或超声手术刀在结肠系膜中创建一个孔,沿孔切开结肠系膜紧贴肠壁向下延伸至腹膜反折以下1 ~2 cm,避免损伤输尿管, 同时结肠系膜切口应沿血管弓继续向上,直至达到预期的切除水平,在腹腔镜直视下,可帮助肠管向外牵拉时确保拔出的肠管不发生扭曲。术后保证肠道气体和粪便的排出, 减少与吻合口的接触,避免吻合口感染和小肠结肠炎,促进吻合口早日愈合和避免肛周糜烂。
综上所述,笔者研究发现先天性长段型巨结肠患儿应用腹腔镜辅助Soave’s 术比常规开腹手术更有优势,手术出血少,恢复快,总住院时间短,可加快患儿术后肛门功能恢复同时减少并发症的发生; 当然,笔者研究的局限性在于其为回顾性研究且样本量较少,故仍需要更大规模的前瞻性随机研究和详尽的长期随访来探索两种手术方式之间的差异。

