长效胰岛素联合口服降糖药治疗2 型糖尿病的疗效
张晶晶
在内分泌科疾病中, T2DM 属于慢性疾病中一种高发和常见病, 在多种因素共同作用下, 该病的发病率呈现逐年升高趋势;成年人中, T2DM 存在较高的发生率,特别是>35 岁的人群中, 同其他年龄段的人群相比, 其存在更高的发病率[1]。T2DM 不但病程长, 同时治愈难度较高, 对患者的身心健康存在严重影响。有研究表示[2], 肥胖会降低糖耐量, 进而导致T2DM 疾病的发生, 因此肥胖、年龄等原因都是导致T2DM 出现的危险因素中的独立因素。现阶段, T2DM 已经是全球的一种流行病, 并且目前我国T2DM 的发生率也是显著升高, 且日渐趋向于年轻化, 所以, 临床需要高度重视此类患者, 利用有效的药物对血糖水平进行控制而显著改善预后。现阶段, 临床对于该病并没有特效的治疗方法, 其中药物保守治疗仍然为重要的方法。该病早期并没有明显的临床症状, 某些T2DM 患者会存在乏力、口渴、多饮、多尿等临床症状, 常常被忽略, 通常在体检时才被确诊。对于已经确诊的T2DM 患者来讲, 使用口服降糖药物可刺激机体, 确保胰岛素恢复正常的分泌量。本研究将96 例T2DM 患者作为研究对象,分析长效胰岛素与口服降糖药物联合治疗T2DM 的效果, 报告如下。
1 资料与方法
1.1 一般资料 选取2020 年10 月~2021 年10 月本院收治的96 例T2DM 患者, 随机分为观察组和对照组, 每组48 例。观察组男26 例, 女22 例, 平均年龄(65.27±4.59)岁;对照组男27 例, 女21 例, 平均年龄(64.39±3.87)岁。两组一般资料比较, 差异均无统计学意义(P>0.05), 具有可比性。
纳入标准:①精神状态良好者;②性别不限;③无感染征象、中度症状者;④年龄≥18 岁且病情稳定者;⑤没有认知沟通障碍者;⑥患者对研究内容知情。排除标准:①对本次研究所用药物过敏者;②伴有急慢性感染者;③精神异常者;④妊娠期、哺乳期妇女;⑤临床资料不全者;⑥合并其他免疫系统疾病者;⑦沟通障碍者;⑧患有癫痫、抑郁、躁狂等精神疾病者;⑨生命体征不平稳者;⑩依从性较差者。
1.2 方法 两组患者均实施饮食指导、健康教育、心理护理等常规护理措施。
对照组给予口服降糖药治疗。口服格列本脲(修正药业集团股份有限公司;国药准字H22021085)2.5 mg, 轻症者在三餐前服用1.25 mg, 治疗7 d 后增加药量至2.5 mg/次, 用药量<15 mg/d。
观察组给予长效胰岛素+口服降糖药治疗。口服降糖药应用方法同对照组一致。首次注射长效胰岛素[赛诺菲安万特(北京)制药有限公司, 国药准字J20120031]8~10 U, 后结合患者的具体病情对用药剂量进行调整。
1.3 观察指标及判定标准 比较两组患者治疗前后的血糖(HbA1c、2 h PG、FPG)水平、生活质量(总体健康、精力、社会功能、心理健康、躯体疼痛、躯体角色功能、情绪角色功能、躯体健康)评分以及不良反应发生情况(体重增加、低血糖)、治疗效果。患者生活质量评分采用简明健康状况调查量表(SF-36)评价[3], 分数越高表示生活质量越好。治疗效果判定标准:显效:血糖水平处在正常范围内;有效:血糖水平趋近于正常范围;无效:血糖水平未改善甚至升高。总有效率=(显效+有效)/总例数×100%。
1.4 统计学方法 采用SPSS19.0 统计学软件处理数据。计量资料以均数±标准差(±s)表示, 采用t检验;计数资料以率(%)表示, 采用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 两组患者治疗前后血糖水平比较 治疗前, 观察组患者HbA1c(9.85±1.31)%、2 h PG(12.12±2.09)mmol/L、FPG(9.13±1.52)mmol/L 与对照组的(9.84±1.29)%、(11.73±2.14)mmol/L、(9.06±1.40)mmol/L 比较无显著差异(P>0.05)。治疗后, 观察组患者HbA1c(6.20±0.91)%、2 h PG(8.63±1.37)mmol/L、FPG(5.83±0.72)mmol/L均低于对照组的(8.34±1.15)%、(9.56±1.60)mmol/L、(7.91±1.31)mmol/L, 差异具有统计学意义(P<0.05)。见表1。
表1 两组患者治疗前后血糖水平比较( ±s)
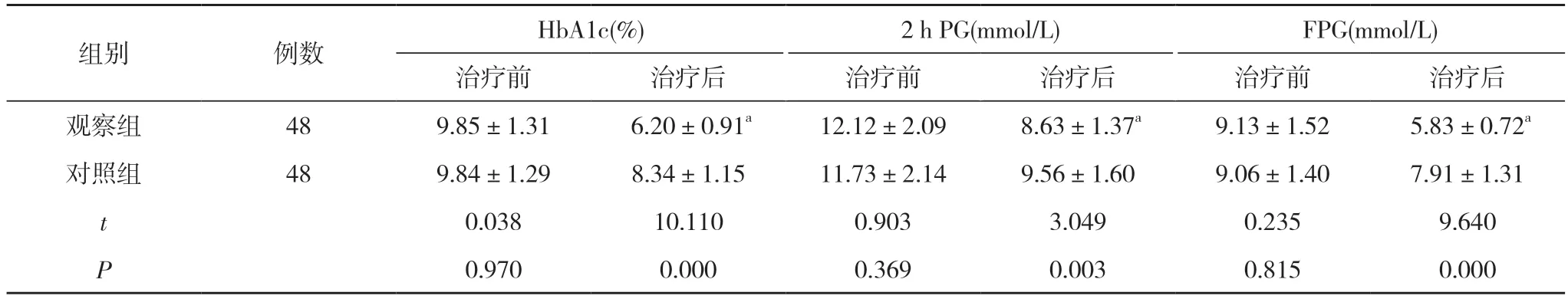
表1 两组患者治疗前后血糖水平比较( ±s)
注:与对照组治疗后比较, aP<0.05
组别 例数 HbA1c(%) 2 h PG(mmol/L) FPG(mmol/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 48 9.85±1.31 6.20±0.91a 12.12±2.09 8.63±1.37a 9.13±1.52 5.83±0.72a对照组 48 9.84±1.29 8.34±1.15 11.73±2.14 9.56±1.60 9.06±1.40 7.91±1.31 t 0.038 10.110 0.903 3.049 0.235 9.640 P 0.970 0.000 0.369 0.003 0.815 0.000
2.2 两组患者不良反应发生情况比较 观察组体重增加0 例、低血糖1 例(2.08%);对照组体重增加5 例(10.42%)、低血糖2 例(4.17%)。观察组不良反应发生率2.08%(1/48)低于对照组的14.58%(7/48), 差异具有统计学意义(χ2=4.909, P<0.05)。
2.3 两组患者治疗前后生活质量评分比较 治疗前,观察组患者总体健康评分(52.30±4.45)分、精力评分(60.48±4.57)分、社会功能评分(72.38±3.25)分、心理健康评分(61.78±3.58)分、躯体疼痛评分(62.38±3.75)分、躯体角色功能评分(59.48±4.68)分、情绪角色功能评分(66.38±3.11)分、躯体健康评分(51.48±3.51)分;对照组患者总体健康评分(52.35±3.14)分、精力评分(60.40±4.65)分、社会功能评分(71.93±3.70)分、心理健康评分(62.30±2.31)分、躯体疼痛评分(62.52±3.78)分、躯体角色功能评分(59.91±4.25)分、情绪角色功能评分(66.87±3.46) 分、躯体健康评分(52.12±2.75)分。两组患者治疗前总体健康、精力、社会功能、心理健康、躯体疼痛、躯体角色功能、情绪角色功能、躯体健康评分评分比较差异无统计学意义(P>0.05)。治疗后, 观察组患者总体健康评分(63.25±4.48) 分、精力评分(74.25±4.54) 分、社会功能评分(83.67±3.91)分、心理健康评分(81.48±4.25)分、躯体疼痛评分(74.48±6.38)分、躯体角色功能评分(73.54±4.18)分、情绪角色功能评分(84.54±3.67)分、躯体健康评分(71.37±4.28)分;对照组患者总体健康评分(54.54±3.25)分、精力评分(61.22±4.01)分、社会功能评分(76.32±2.75)分、心理健康评分(61.24±3.75)分、躯体疼痛评分(66.58±4.70)分、躯体角色功能评分(61.24±4.42)分、情绪角色功能评分(73.05±2.50)分、躯体健康评分(52.31±2.76)分。观察组患者总体健康、精力、社会功能、心理健康、躯体疼痛、躯体角色功能、情绪角色功能、躯体健康评分均高于对照组, 差异有统计学意义(P<0.05)。见表2。
表2 两组患者治疗前后生活质量评分比较( ±s, 分)
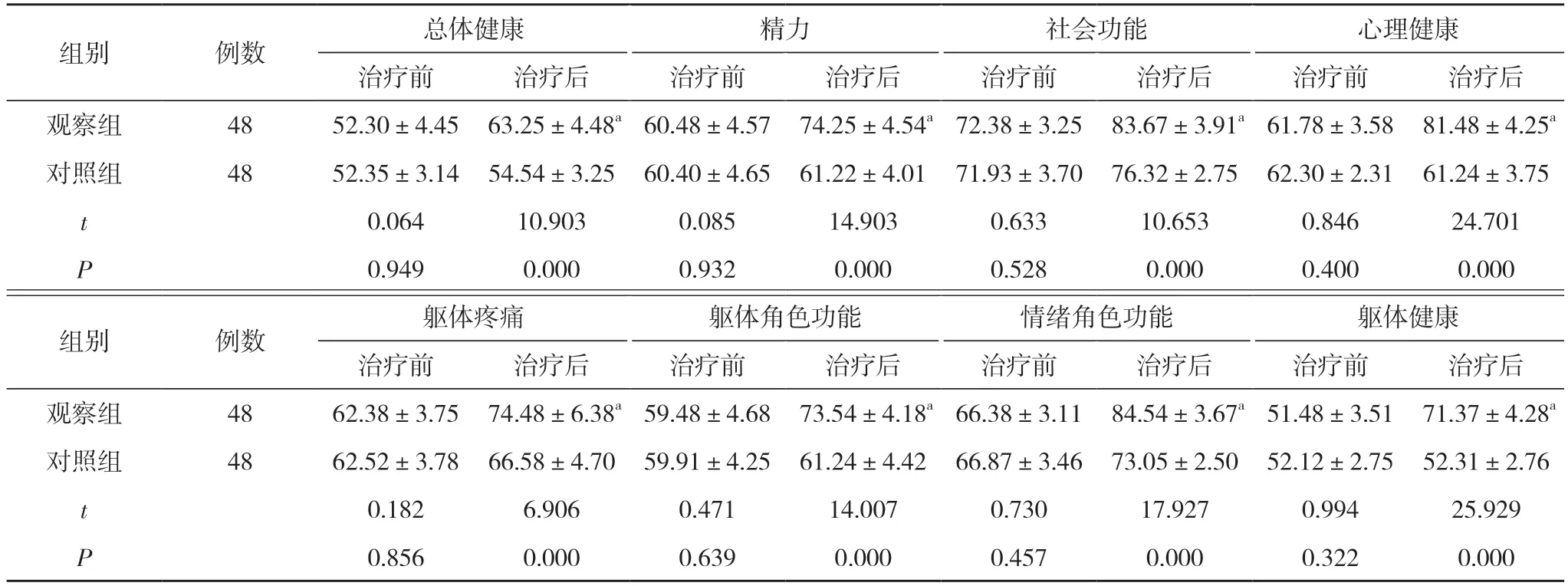
表2 两组患者治疗前后生活质量评分比较( ±s, 分)
注:与对照组治疗后比较, aP<0.05
组别 例数 总体健康 精力 社会功能 心理健康治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 48 52.30±4.45 63.25±4.48a 60.48±4.57 74.25±4.54a 72.38±3.25 83.67±3.91a 61.78±3.58 81.48±4.25a对照组 48 52.35±3.14 54.54±3.25 60.40±4.65 61.22±4.01 71.93±3.70 76.32±2.75 62.30±2.31 61.24±3.75 t 0.064 10.903 0.085 14.903 0.633 10.653 0.846 24.701 P 0.949 0.000 0.932 0.000 0.528 0.000 0.400 0.000组别 例数 躯体疼痛 躯体角色功能 情绪角色功能 躯体健康治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 48 62.38±3.75 74.48±6.38a 59.48±4.68 73.54±4.18a 66.38±3.11 84.54±3.67a 51.48±3.51 71.37±4.28a对照组 48 62.52±3.78 66.58±4.70 59.91±4.25 61.24±4.42 66.87±3.46 73.05±2.50 52.12±2.75 52.31±2.76 t 0.182 6.906 0.471 14.007 0.730 17.927 0.994 25.929 P 0.856 0.000 0.639 0.000 0.457 0.000 0.322 0.000
2.4 两组治疗效果比较 观察组治疗总有效率95.83%高于对照组的79.17%, 差异具有统计学意义(P<0.05)。见表3。

表3 两组治疗效果比较(n, %)
3 讨论
现阶段, 我国人口老龄化日益严重, 使得和老年人有关的疾病发生率也越来越高, 其中糖尿病属于慢性疾病中存在较高发病率的一种疾病, 该病的发生同遗传、环境等因素有关, 发病机制是人体内未分泌足量的胰岛素, 并且胰岛素的敏感性出现降低, 进而引起患者发生水电解质紊乱及尿糖、血糖升高[4]。T2DM 利用口服降糖药物可以对血糖浓度有效控制, 但是因为该类疾病病程长, 所以单纯利用口服降糖药物治疗很难获得理想的血糖控制效果[5]。并且患者体内存在偏高的血糖水平, 会使氧化应激反应增加而增多体内的糖基化产物、活性氧产物, 进而对患者的组织器官产生损伤, 同时导致较多的并发症[6]。在治疗T2DM 过程中, 若两种降糖药物联用也未有效控制血糖水平, 那么就需要利用胰岛素对其进行治疗[7]。
现阶段, 国内的胰岛素存在较多的种类, 同时控制效果也是参差不齐, 且使用比较频繁, 对于维持患者胰岛素水平24 h 内均处在正常水平较难, 由于个体差异也会使患者出现不良反应, 如夜间出现低血糖、增加体质量, 进而导致多数的患者对于长时间进行治疗并没有较高的依从性。过去的胰岛素最初治疗计划是口服降糖药物与中效胰岛素联合应用, 该种治疗计划可以有效控制大多数患者的血糖, 但是对于维持24 h 的长效难度较高, 同时作用高峰期显著, 易使患者发生低血糖, 进而对控制血糖稳定以及长期达标产生不利影响。甘精胰岛素属于人胰岛素类似物中的一种, 经过皮下注射而进入到人体的皮下组织, 酸性溶液被中和而变成了微小的沉积物, 2 h 内即可产生效果, 并且存在5 h 的延迟期, 持续发挥作用的时间在24 h 左右, 会稳定且连续的将甘精胰岛素释放出来, 且人体短期内并不会将类胰岛素代谢出来。
HbA1c 是对糖尿病病情控制评价的一个重要指标, 在有关研究中, 如果T2DM 患者的血糖水平控制不够理想, HbA1c 则会在体内生成[8]。分析其原因:HbA1c 是细胞内的血红蛋白与血液中的葡萄糖结合后通过非酶促反应而生成一种产物, 其含量会在血液中葡萄糖浓度升高的过程中增加, 所以, HbA1c 可以将患者的平均血糖有效的反映出来[9-12]。国内的研究指出, 口服降糖药与甘精胰岛素联合治疗可以将HbA1c的达标率显著提升, 是低血糖的发生了显著降低[13]。在本研究结果中, 经过治疗后的两组患者其HbA1c 水平均降低显著, 但是观察组患者HbA1c 水平降低程度优于对照组, 说明了口服降糖药物与长效胰岛素联合治疗T2DM 的效果明显优于单纯的口服降糖药物治疗, 并且观察组的并发症发生率低于对照组, 证实了联合治疗安全性较高。而且在于谦等[9]研究中, 采取联合用药的治疗组与实施单一用药的对照组相比, 其2 h PG、HbA1c、FPG、不良反应发生率均更低, 结果表示, T2DM 患者结合患者采取口服降糖药物与长效胰岛素联合治疗可显著改善血糖水平, 同时不良反应少, 具有较高的治疗安全性。另外, 在唐转敏等[14]研究中, 观察组采取联合治疗的总有效率为96.36%, 对照组采取单一口服降糖药物治疗的总有效率为74.55%,观察组优于对照组。本研究结果同上述研究结果相近,证实联合治疗效果确切。此外本研究结果中, 观察组生活质量评分均优于对照组, 表示联合治疗可提升患者生活质量。
总之, 对于T2DM 患者实施长效胰岛素联合口服降糖药物治疗可有效控制血糖, 且用药安全性高, 同时提升患者生活质量, 值得推广应用。

