毛细管电泳法测定食品中8种添加剂
杨桂君,高文惠*
(河北科技大学生物科学与工程学院,河北省 石家庄 050018)
毛细管电泳法测定食品中8种添加剂
杨桂君,高文惠*
(河北科技大学生物科学与工程学院,河北省 石家庄 050018)
为建立毛细管电泳法同时测定亮蓝、香兰素、山梨酸、苯甲酸、日落黄、新红、苋菜红、柠檬黄8种食品添加剂的分析方法。采用毛细管区带电泳-紫外检测法,以磷酸-硼砂缓冲体系为运行缓冲液,于240nm波长处对饮料、果冻、蜜饯样品进行检测,一次进样分析在8min内完成。结果表明:该方法的线性范围为2.5~1000μg/mL,线性相关系数在0.9986~0.9998之间,平均回收率在85.2%~100.3%之间,相对标准偏差(RSD)≤6.98%(n=5),检测限为0.25~10μg/mL。该方法操作方便,检测快速,在食品添加剂的检测上取得了令人满意的效果。
食品;添加剂;毛细管电泳;紫外检测器
随着全球农业和食品生产能力的日益发达,消费者对食品的安全性提出了越来越高的要求。毛细管电泳(CE)兼有电泳和色谱技术的双重优点,而且拥有众多的高效分离模式,可以满足基体复杂的食品分析要求,再加上其与样品前处理技术兼容性好,CE在食品安全分析方面的应用日趋广泛。由于食品添加剂长期过量摄入会给人们带来危害,在我国食品添加剂使用卫生标准中[1],对食品添加剂使用范围和最大使用限量均有规定,目前已有较多文献[2-10]报道了采用HPLC法分离分析食品添加剂。但是国内外文献[11-15]报道的采用毛细管电泳对食品添加剂的检测多是针对少数几种,因此本实验拟建立一种采用CE同时分离分析多种食品添加剂的方法,以期为CE检测食品中多种添加剂的研究提供一定的参考依据。
1 材料与方法
1.1 材料与试剂
桔子味醒目饮料、果冻、阿胶贡枣 市售。
碳酸氢钠、硼砂、磷酸二氢钾、β-环糊精、氢氧化钠、亮蓝、香兰素、山梨酸、苯甲酸、日落黄、新红、苋菜红、柠檬黄(均为分析纯)。
1.2 仪器与设备
高效毛细管电泳仪 北京彩陆科学仪器有限公司;
HW-2000数据处理系统 上海千谱软件有限公司;PHS-3C型pH计 上海精密科学仪器有限公司雷磁仪器厂;SK5200LHC型超声波清洗器 上海科导超声器有限公司;溶剂过滤器 江苏省建湖县飞达玻璃仪器厂;0.45μm的微孔滤膜 上海兴亚净化器材厂;内径75μm弹性石英毛细管 河北永年光纤厂;AL104分析天平 梅特勒-托利多仪器有限公司;DL-5低速大容量离心机 上海安亭科学仪器厂;SZ-93自动双重纯水蒸馏器 上海亚荣生化仪器厂。
1.3 方法
1.3.1 溶液的配制
标准溶液(150μg/mL):分别取1mg/mL储备液150μL,然后加入850μL水,混匀即可得150μg/mL的标准液。
混合标准液:亮蓝标准液150μL;香兰素、胭脂红、苋菜红、日落黄、柠檬黄标准液各30μL;苯甲酸标准液100μL;山梨酸标准液10μL;然后加入620μL水,摇匀待测。
缓冲溶液的配制:4mmol/L的硼砂、11mmol/L的磷酸二氢钾缓冲液,加入4mmol/L β-环糊精,用1mol/L NaOH溶液调节pH11。
1.3.2 样品的前处理
饮料:经超声脱气,除去二氧化碳,0.45μm的微孔膜过滤两次,备用。
果冻:取5g果冻样品,加水研磨,置于25mL的具塞量筒中,加水定容,剧烈振荡后,分别取均匀的样品2份放入4mL的离心管中,4000r/min离心10min。取上清液,过0.45μm的微孔滤膜,待测。
蜜饯:将蜜饯放进捣碎机捣碎,取10g样品放入研钵研磨后,加入20mL双蒸水进行溶解,搅拌均匀后提取上清液,将上清液经0.45μm的微孔滤膜过滤后,方可上机。
1.3.3CE条件
内径75μm弹性石英毛细管50cm,有效长度44cm;分离电压15kV;检测波长240nm;进样时间为5s;为了提高重现性,2次进样之间用0.1mol/L NaOH溶液冲洗2min,再用水冲洗2min,最后用缓冲液冲洗2min。
2 结果与分析
2.1 电泳条件的确定
2.1.1 检测波长的选择
不同检测波长物质的响应信号不同,通过紫外光谱扫描可知,8种食品添加剂的最大吸收波长在210~350nm之间。苯甲酸的最大吸收波长为225nm,且吸收范围很窄,超过250nm吸收较弱,综合考虑实验选择240nm为检测波长。
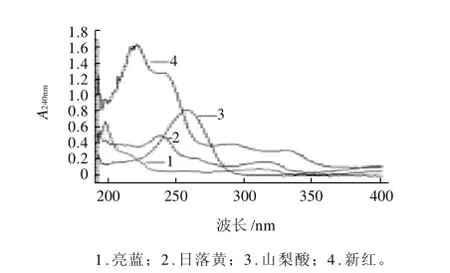
图1 亮蓝、日落黄、山梨酸、新红的紫外-可见光谱扫描图Fig.1 UV-visible scanning spectra of food blue 2, food yellow 3, sorbic acid and food red 10
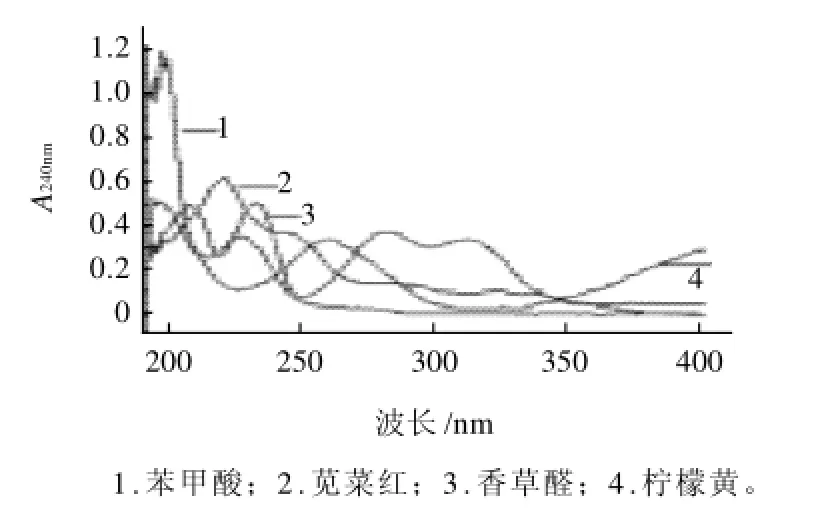
图2 苯甲酸、苋菜红、香草醛、柠檬黄的紫外-可见光谱扫描图Fig.2 UV-visible scanning spectra of benzoic acid, amaranth, vanillin and tartrazine
2.1.2 缓冲液种类的选择
不同的缓冲液及其不同的配比产生的分离效果相差很大,本实验考察硼砂体系、磷酸盐缓冲体系、硼砂与十二烷基硫酸钠(SDS)混合体系、硼砂-磷酸盐混合体系,并调节不同的pH值,进行实验。结果表明,当单独使用硼砂缓冲体系时新红与苋菜红不能分离;当单独使用磷酸缓冲体系时苯甲酸,山梨酸不能实现基线分离;然而在硼砂-磷酸盐混合体系中8种添加剂均实现了基线分离,故选择硼砂-磷酸盐混合体系作为缓冲液。
2.1.3 缓冲液比例的选择
硼砂-磷酸盐混合体系作为缓冲液中硼砂与磷酸盐5个不同的浓度比(分别为10:5、8:7、6:9、4:11、2:13)对8种添加剂进行分离,结果表明,当缓冲液的配比为4:11时,分离效果最佳,8种物质均实现分离,且峰形尖锐、对称。
2.1.4 缓冲液中添加剂的选择
在缓冲液硼砂-磷酸氢二钾浓度比为4:11条件下,向缓冲液中添加表面活性剂β-环糊精,添加量分别为2、3、4、5、6mmol/L。考察表面活性剂的添加量对8种添加剂色谱分离的影响,由于食品添加剂与β-环糊
精之间主客体相互作用不同,其添加量对分离效果影响不同,结果表明,8种添加剂随着β-环糊精添加量的增多,迁移速率加快。当添加量为4mmol/L时,8种添加剂实现了良好的分离。
2.1.5 操作电压的选择
在毛细管电泳中,分离电压对分离度有很大的影响。在实验中确定5个水平13、14、15、16、17kV来进行检测。结果表明,从13~17kV改变工作电压,8种食品添加剂的迁移时间逐渐减少,电泳电流增加,各峰峰形变得尖锐。但是,电压升高产生的焦耳热增多,导致谱带展宽,分离度下降,物质之间不能实现完全分离,因此选择电压为15kV。
2.1.6pH值的选择
毛细管的电渗流(EOF)对于pH值的改变很敏感,较高的pH值可以增大电渗流,提高分离速度但是电渗流的加快会使迁移时间缩短,各组分不能完全分离。此外,pH值改变影响化合物的解离程度,进而影响其与固定相的作用,因此影响其保留值,进而影响分离度,因此pH值对分离有较大影响。本实验考察缓冲液pH值在8~12范围内对迁移时间的影响(图3),实验结果表明在pH11时分离效果最好。
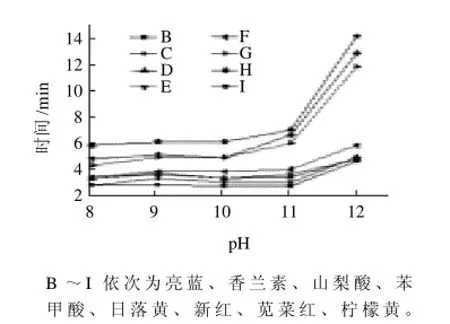
图3 不同pH值条件下8种食品添加剂的保留时间变化Fig.3 Retention time of eight food additives under different pH conditions
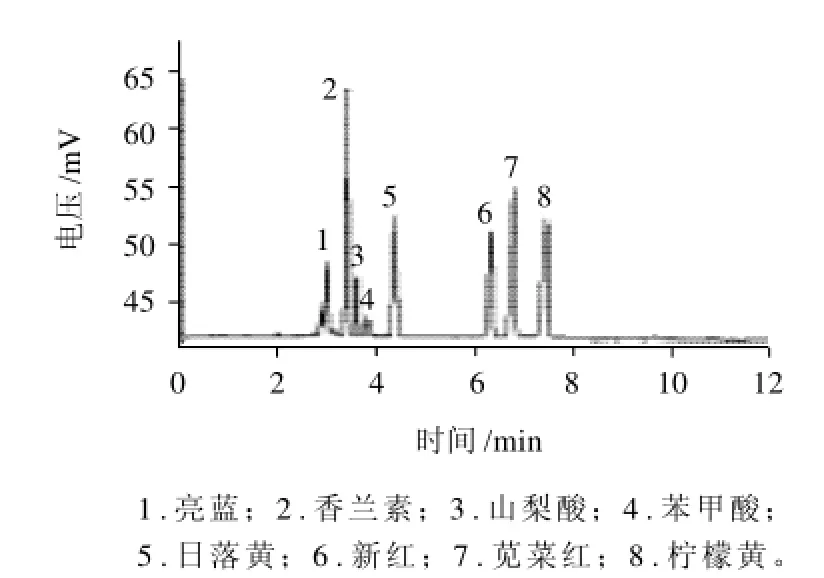
图4 8种食品添加剂在最佳条件下的CE分离图Fig.4 HPCE chromatogram of eight food additives under optimized conditions
通过对各影响因素的考察,实验确定最佳电泳条件为4mmol/L的硼砂、11mmol/L的磷酸二氢钾缓冲液,加入4mmol/L β-环糊精、pH11、λ=240nm、电压15kV,在此条件下,8种食品添加剂在8min内得到了良好的分离,分离效果如图4所示。
2.2 线性范围和最小检出限
将8种食品添加剂分别配制成一系列不同浓度的标准溶液,在最佳色谱操作条件下绘制8种食品添加剂的线性关系曲线。8种食品添加剂的线性方程、线性相关系数、线性范围和最小检出限见表1。
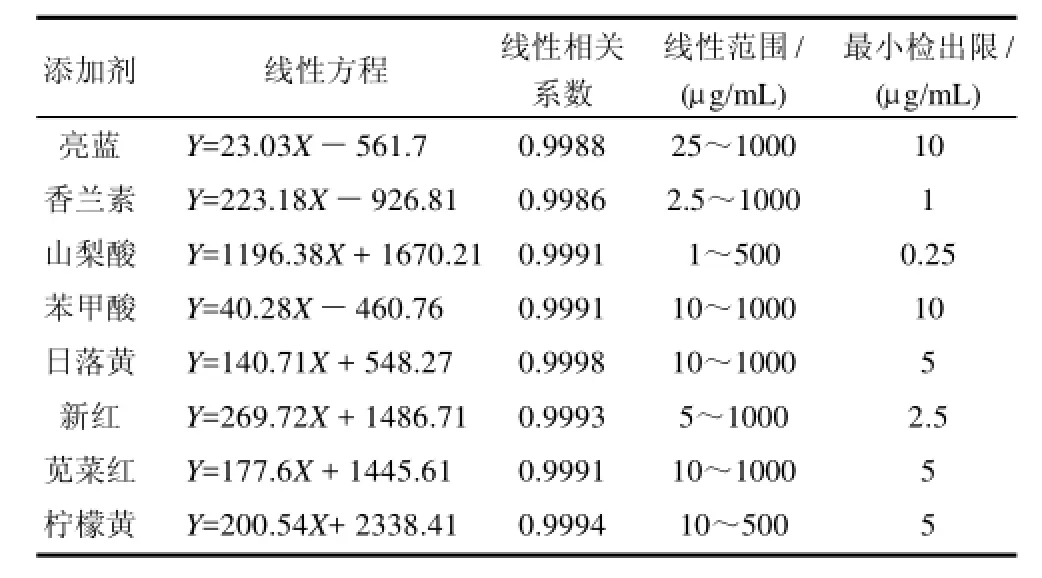
表1 8种食品添加剂的线性关系及最小检出限Table 1 Standard curves for determining eight food additives by HPCE and their limits of detection
由表1可以看出,该方法的线性范围为2.5~1000μg/mL,线性相关系数≥0.9986,最小检出限为0.25~10μg/mL。2.3样品的测定与回收率实验
2.3.1 样品的测定
按照1.3.2节方法处理样品,然后在最佳的色谱条件下分别对醒目饮料、果冻和蜜饯进行测定,采用外标法定量。由图5~7可知,在饮料样品中检测到苯甲酸、日落黄两种食品添加剂,在果冻样品中检测到香兰素,山梨酸、苯甲酸,蜜饯样品中检测到柠檬黄。除蜜饯外,在欲分离的几种食品添加剂出峰处基本无杂质干扰。

图5 醒目饮料的色谱分离图Fig.5 HPCE chromatogram of Smart orange-flavored beverage
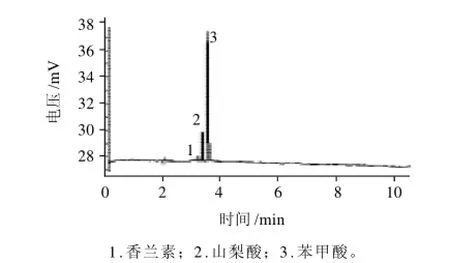
图6 果冻的色谱分离图Fig.6 HPCE chromatogram of Xizhilang fruit-flavored jelly
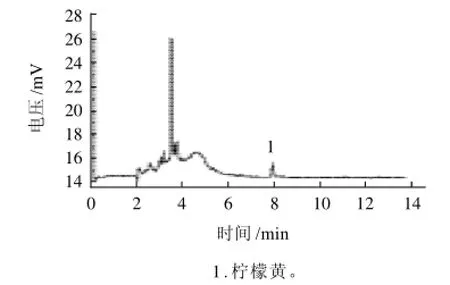
图7 蜜饯的色谱分离图Fig.7 HPCE chromatogram of preserved date
2.3.2 回收率实验
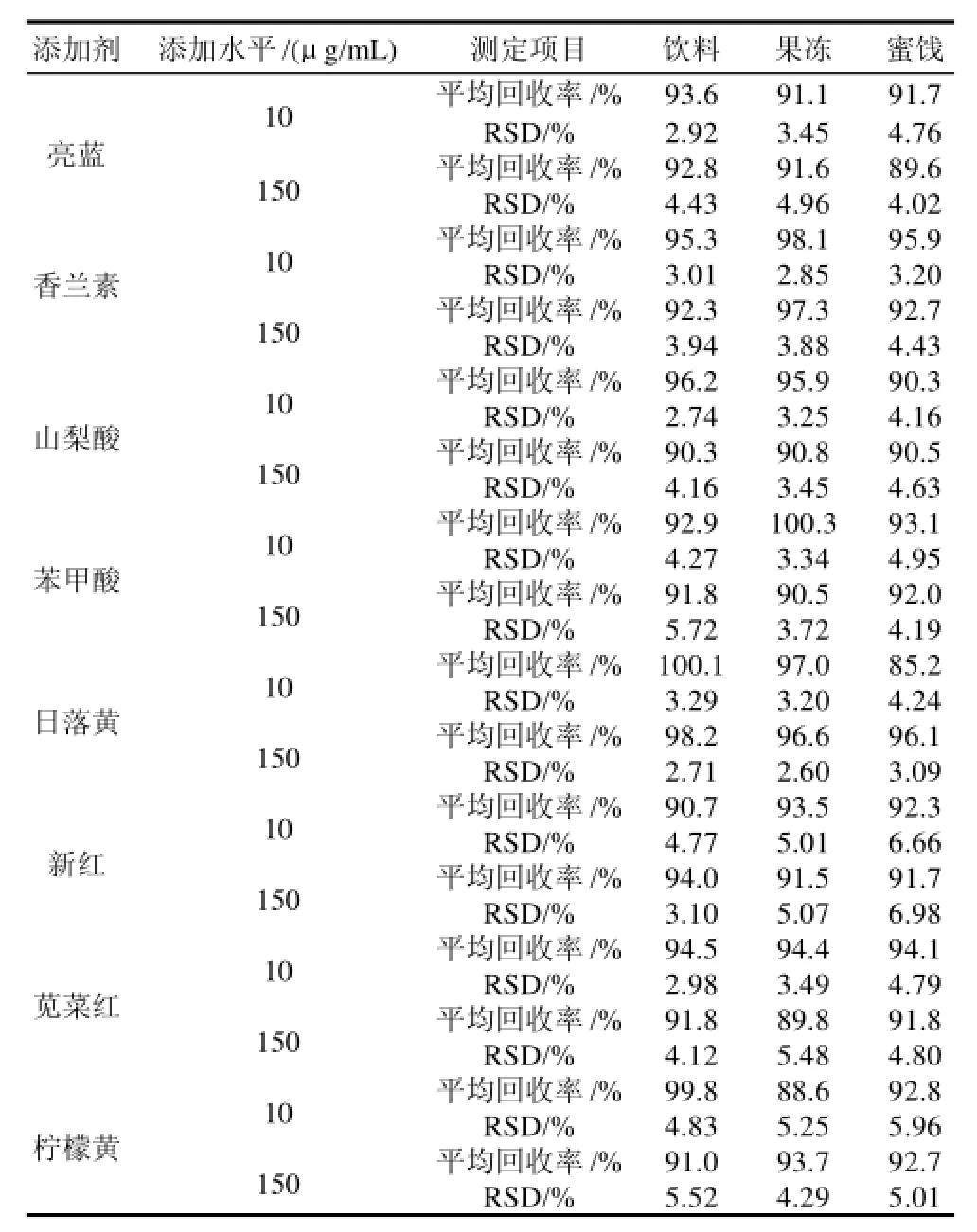
表2 不同样品的8种食品添加剂在不同添加水平回收率实验结果(n=5)Table 2 Recovery rates of 8 food additives in different samples spiked at various levels (n=5)
采用本方法对饮料、果冻、蜜饯等样品,在10μg/mL和150μg/mL两个添加水平下,进行添加回收率实验,其分析结果如表2所示。
由表2可以看出,该方法的平均回收率在85.2%~100.3%之间,相对标准偏差(RSD)≤6.98%(n=5)。说明方法有良好的可靠性和精密度。
3 结 论
本研究建立了一种简便、快速、灵敏、准确的同时测定食品中8种添加剂的检测方法。最佳操作条件为内径75μm弹性石英毛细管,有效长度44cm,工作电压15kV,检测波长240nm,进样时间5s,缓冲液为硼砂-磷酸缓冲液(浓度比4:11),并添加表面活性剂β-环糊精4mmol/L。用该方法对饮料、果冻、蜜饯样品进行检测。该方法的线性范围为2.5~1000μg/mL,线性相关系数≥0.9986,平均回收率在85.2%~100.3%之间,相对标准偏差(RSD)≤6.98%(n=5),最小检出限为0.25~10μg/mL。
[1]GB/T 2760—1996 食品添加剂使用卫生标准[S].
[2]王骏, 胡梅, 张卉, 等. 超高效液相色谱快速测定饮料中的16 种食品添加剂[J]. 食品科学, 2010, 31(2): 195-198.
[3]高文惠, 耿静静, 裴红. 高效液相色谱法同时测定食品中多种添加剂[J]. 食品科学, 2008, 29(9): 472-475.
[4]林钦, 黄红霞. 高效液相色谱法同时检测食品中十种食品添加剂[J].食品科学, 2007, 28(11): 485-487.
[5]胡美珍, 王文铮, 张燕琴. 毛细管电泳法分离测定食品中的山梨酸、苯甲酸、糖精[J]. 上海师范大学学报: 自然科学版, 2004, 33(3): 63-65.
[6]吴光斌, 吕禹泽, 陈发河. 反相高效液相色谱法同时测定九种食品添加剂[J]. 食品科学, 2006, 27(11): 457-461.
[7]陈发河, 吴光斌, 林华玲, 等. 固相萃取-反相高效液相色谱法同时测定多种食品添加剂[J]. 中国食品学报, 2006, 6(6): 126-132.
[8]何云亚, 陆昱养. 高效液相色谱法同时测定食品中5种添加剂[J]. 中国卫生检验杂志, 2007, 17(4): 655-659.
[9]SAAD B, BARI F M, SALEH I M, et al. Simultaneous determination of preservatives (benzoic acid, sorbic acidm, ethylparaben and propylparaben) in foodstuffs using high-performance liquid chromatography [J]. Journal of Chromatography A, 2005, 1073: 393-397.
[10]TECHAKRIENGKRAI I, SURAKARNKUL R. Analysis of benzoic acid and sorbic acid in Thai rice wines and distillates by solid-phase sorbent extraction and high-performance liquid chromatography[J]. Journal of Food Composition and Analysis, 2007, 20: 220-225.
[11]HUANG H Y, SHIH Y C, CHEN Y C. Determining eight colorants in milk beverages by capillary electrophoresis[J]. Journal of Chromatography A, 2002, 959(1/2): 317-325.
[12]赵欣颖, 贾丽, 周晓晶, 等. 毛细管电泳法同时测定糖果中5种人工合成色素的含量[J]. 现代仪器, 2008(4): 58-60.
[13]MASAR M, KANIANSKY D A, MADAJOVA V. Separation of synthetic food colourants by capillary zone electrophoresis in a hydrodynamically closed separation compartment[J]. Journal of Chromatography A, 1996, 724(1/2): 327-336.
[14]RYVOLOVA M, TABORSKY P, VRABEL P, et al. Sensitive determination of erythrosine and other red food colorants using capillary electrophoresis with laser-induced fluorescence detection[J]. Journal of Chromatography A, 2007, 1141: 206-211.
[15]王咏梅, 刘恺, 卢玉妹, 等. 毛细管区带电泳法测定食品中山梨酸、苯甲酸和糖精的含量[J]. 食品科技, 2007(6): 227-229.
Determination of Eight Food Additives in Different Matrices by Capillary Electrophoresis
YANG Gui-jun,GAO Wen-hui*
(College of Biological Science and Engineering, Hebei University of Science and Technology, Shijiazhuang 050018, China)
A method using high performance capillary electrophoresis (HPCE) with ultraviolet detection was developed for the simultaneous determination of eight food additives, i.e. food blue 2, vanillin, sorbic acid, benzoic acid, food yellow 3, food red 10, amaranth and tartrazine. The running buffer system used was composed of phosphoric acid and borax, and the detection wavelength was set as 240 nm. Different sample preparation methods were used for the determination of three chosen matrices, including Smart orange-flavored beverage, fruit-flavored jelly and preserved date. Once-off injection was accomplished in 8 min. The linear range of the developed method was between 2.5μg/mL and 1000 μg/mL, with a correlation coefficient ranging from 0.9986 to 0.9998. The average spike recoveries (n = 5) for these eight analytes varied from 85.2% to 100.3%, with a relative standard deviation of less than 6.98%. The limits of detection for them were between 0.25μg/mL and 10 μg/mL. Satisfactory results were obtained in determining the above matrices. This method has the benefits of convenient operation and rapidity.
food;additive;capillary electrophoresis;ultraviolet detector
TS202.3;O657.8
A
1002-6630(2010)18-0377-04
2010-06-09
河北省科技厅重大科技攻关项目(09227134D);河北省科技支撑计划项目(10276902D);河北省自然科学基金项目(B2008000669)
杨桂君(1983—),女,硕士研究生,研究方向为食品安全与分离科学。E-mail:yangguijun2@sina.com
*通信作者:高文惠(1963—),女,教授,博士,研究方向为食品安全与分离科学。E-mail:wenhuigao@126.com

