固溶体Bi2Mo1-xWxO6的水热合成及光催化性能
李红花 李坤威 汪 浩
(北京工业大学材料学院,北京 100124)
固溶体Bi2Mo1-xWxO6的水热合成及光催化性能
李红花 李坤威 汪 浩*
(北京工业大学材料学院,北京 100124)
采用水热法,在较低温度下合成了系列Bi2Mo1-xWxO6固溶体。结果表明,W的替代抑制了固溶体的晶粒生长,导致了较小的晶粒尺寸。随着x的增加,红外光谱中840 cm-1处M-O键的振动频率νM-O有规律地向低频率方向移动,表明Mo6+离子逐步被W6+替代,生成了无限互溶的固溶体。光吸收性能研究表明,随着W6+逐步替代Mo6+,带隙出现了先降后升的趋势,x=0.4时带隙最小。而固溶体的光催化性能随着x的增加,出现了先增后减的趋势,x=0.4时光催化活性最高。此外,含W样品的光催化活性高于Bi2MoO6。这与固溶体的带隙、带结构和晶粒尺寸变化有关。
Bi2Mo1-xWxO6;固溶体;水热合成;光催化
许多类质同象的晶体能生成均匀的、组分可变的类似溶液一样的固溶体。一般形成固溶体的条件可归结为离子半径和极化性能比较接近,其次是晶格的形状和大小相差不多[1]。通过形成固溶体来调控能带结构是设计可见光响应光催化剂的策略之一。前驱物在反应过程中,离子间通过相互晶格渗入形成新的晶格,其电子结构得以重组。当宽带隙半导体和窄带隙半导体形成固溶体时,可以制备带隙宽度连续变化的新型光催化剂,获得可见光响应的催化性能。例如Sr2Nb2O7-Sr2Ta2O7[2]、AgInS2-ZnS[3]、SnO2-TiO2[4]等。另外,形成固溶体也是提高光催化活性的有效途径。Lin等[4]以Sn替代金红石相TiO2中的Ti制备了固溶体Ti1-xSnxO2(0.00≤x≤0.10),研究表明固溶体的光催化活性随着Sn含量的增加而增大,当Sn含量为0.075时光催化活性最高,比纯的金红石相增加了15倍。Yu等[5]采用无模板水热法制备了锐钛矿相中空微米球Ti1-xSnxO2固溶体,Sn4+离子的掺入明显抑制了锐钛矿相的结晶,促进了锐钛矿相向金红石相的转变,减小了晶粒尺寸,增大了比表面积, 使得吸收带边蓝移。 nSn4+∶(nSn4+
+nTi4+
)=0.025和0.05时,固溶体的光催化活性高于纯TiO2和P-25。Wang等[6]用固相反应法制备了系列新型的固溶体(AgNbO3)1-x(SrTiO3)x(0≤x≤1),研究表明钙钛矿型固溶体在(0≤x<0.9)时为正交晶系,在(0.9≤x≤1)时为立方晶系。固溶体的导带由Ti3d和Nb4d杂化轨道组成,价带由O2p与Ag4d杂化轨道组成,这种杂化调制了能带结构,从而影响了光物理和光催化性能。对于可见光下光催化产氧和降解 2-丙醇,(AgNbO3)0.75(SrTiO3)0.25都显示了最高的活性。
Aurivillius结构是由一维的钙钛矿层和(Bi2O2)2+层有规则地相互交替排列而成,其化学通式为(Bi2O2)2+(An-1BnO3n+1)2-(其中A=Ca、Sr、Ba、Pb、Na、K,B= Ti、Nb、Ta、Mo、W、Fe),此处A为适合于十二配位的+1、+2、+3、+4价离子或由它们组成的复合离子,B为适合于八面体配位的离子或由它们组成的复合离子,n为一整数,对应钙钛矿层(An-1BnO3n+1)2-内的八面体层数,其值可为1~5[7]。Aurivillius结构的层间距一般在纳米量级,可以认为是一种二维的纳米材料。
Bi2MoO6是一种重要的催化剂模板材料,已广泛应用于丙烯的选择性氧化脱氢制备丙烯醛、氨氧化制备丙烯腈以及丁烯的氧化脱氢制备丁二烯[8,9]。此外,这种化合物由于其优异的物理化学性能而在离子导体[10]、太阳能电池[11]、气敏[12]等方面有着广阔的应用前景。Bi2WO6具有热电、铁电/压电、离子导电和非线形介电系数等重要的物理性能[13]。近年来,这两种化合物显示了优异的可见光光催化性能[14-18]。
Bi2MoO6和Bi2WO6是Aurivillius结构当中最简单的两种化合物(n=1)。这两种化合物具有相同的晶体结构,其中共角、畸变的MO6(M=Mo、W)八面体钙钛矿片层镶嵌在(Bi2O2)2+片层当中。Mo6+离子和W6+的半径相近,六配位时分别为0.059和0.060 nm[19]。Thompson等[20]认为Bi2MoO6和Bi2WO6的晶体结构类似,可以共生,因而这两种化合物有可能形成无限互溶的固溶体。Castro等[21]用固相反应法和机械化学活化法制备了Bi2Mo1-xWxO6固溶体,x<0.5时,样品中有高温相γ(H)Bi2MoO6出现,当0.5<x≤1时生成了属于γ(L)Bi2MoO6和Bi2WO6结构类型的单相固溶体,并研究了代表性的Bi2Mo0.25W0.75O6的铁电性质。结合X射线、中子粉末衍射和里特沃尔德精修结构分析(Rietveld分析), 这个化合物保持了Aurivillius骨架结构,其结构特征介于γ(L)Bi2MoO6和Bi2WO6之间。
本工作采用水热法,于低温下制备了系列Bi2Mo1-xWxO6固溶体,并对固溶体的晶体结构、带隙和光催化性能进行了研究。
1 实验部分
将5 mmol的Bi(NO3)3·5H2O溶于10.0 mL 2.0 mol· dm-3HNO3当中,将化学计量比的 H2MoO4和Na2WO4·2H2O溶于去离子水中。然后,在剧烈搅拌下,将H2MoO4和Na2WO4·2H2O溶液缓慢滴加到Bi(NO3)3溶液当中,用1∶1(V/V)的氨水调节至pH=1。充分搅拌后,将所得混合溶液转移至带有聚四氟乙烯衬里的高压釜中,160℃下反应20 h。自然冷却后,产物经水和无水乙醇反复清洗,离心分离,在80℃干燥后得产物,备于后期物性测试分析。
用X射线衍射仪(XRD,Bruker Advanc D-8,Cu Kα辐射,λ=0.154 06 nm,石墨单色器,工作电压为40 kV,电流为40 mA,扫描范围2θ为10°~60°)分析固溶体的相组成。用扫描电子显微镜(SEM,Hitachi-5200N)观察粉体的晶粒尺寸和形貌。采用Bruker傅立叶变换红外光谱仪测定样品的红外光谱。用Shimadzu UV-3101PC紫外可见光谱仪观察样品的光学吸收。
光催化性能的测试在自制光催化反应仪中进行。该光催化反应仪上部为500 W高压氙灯,并配有一个420 nm的滤波片以提供可见光源,下部为光催化反应器。以罗丹明B为目标降解物。实验时,将0.1 g的光催化剂加入到100 mL,1×10-5mol·dm-3的罗丹明B溶液中,开启电磁搅拌器,打开氙灯,以后每间隔一定时间取样一次,样品经4 000 r·min-1离心分离5 min,取上清液,于722型光栅分光光度计上在553 nm的最大波长处测其吸光度。从样品吸光度值的变化根据Beer-Lambert定律求得罗丹明B浓度,降解率表达为(1-C/C0),式中C0和C分别为样品的初始浓度值和降解后的浓度值。
2 结果与讨论
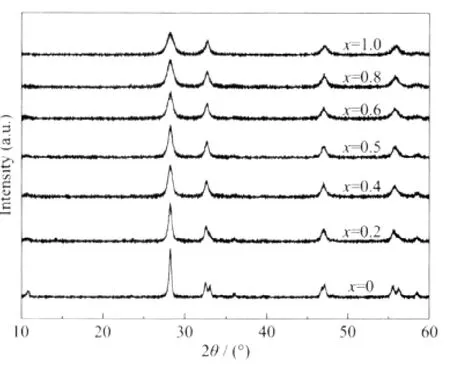
图1 固溶体Bi2Mo1-xWxO6的XRD图Fig.1 XRD patterns of solid solution Bi2Mo1-xWxO6
图1给出了在160℃反应20 h合成的系列化合物 Bi2Mo1-xWxO6(x=0、0.2、0.4、0.5、0.6、0.8、1.0)的 XRD图。图中所有的衍射峰都对应纯相的Bi2MoO6和Bi2WO6的结构,没有发现其它相的存在。x=0时,样品为正交结构的Bi2MoO6(JCPDS No.72-1524,空间群Pbca(No.61))。当x=1时,XRD衍射峰对应着单相正交结构的 Bi2WO6(PDF No.73-2020,空间群B2ab(No.41))。由于Mo6+和W6+在六配位时的离子半径相近,随着x从0增加到1.0,XRD图上没有明显的峰移发生。但随着W的掺入,XRD衍射峰相对强度逐渐降低,发生了明显的宽化。根据谢乐公式从(131)峰算出的固溶体的平均晶粒尺寸如表1所示。从表中可以看出,固溶体的平均晶粒尺寸随着x的增加单调减小,表明由于W的掺入,提供了不同的边界,抑制了固溶体的晶粒生长[22],导致了较小的晶粒尺寸。

表1 固溶体Bi2Mo1-xWxO6的平均晶粒尺寸Table 1 Average grain size of solid solution Bi2Mo1-xWxO6
室温下固溶体Bi2Mo1-xWxO6的结构参数可以通过TOPAS程序进行确定。TOPAS程序是基于非线性最小二乘法建立起来的全谱图分析模拟软件,适用于Rietveld结构精修方法。得到的具体结构参数如表2所示。结果表明,随着钼原子逐步被钨原子取代,Bi2Mo1-xWxO6的晶格参数a和c随之逐渐减小,而b逐渐增大,晶胞体积随着x的增加逐渐减小。晶胞参数有规律的变化表明合成的样品为固溶体而非Bi2MoO6和Bi2WO6的混合物。
红外光谱常用来表征化合物的结构。图2显示了固溶体Bi2Mo1-xWxO6的红外光谱。其中840、797、734 cm-1处的带为共角的MO6(M=Mo、W)八面体的ν1(A)和ν3(F2)振动(M-O伸缩振动),577 cm-1处的带为M-O-Bi振动模式[23,24]。从图2可以看出,随着x的增加,840 cm-1处M-O键的振动频率νM-O有规律地向低频率方向移动。当x从0增加到1时,νM-O从842 cm-1移到了824 cm-1,同时797 cm-1处的带逐渐消失。表3具体列出了840 cm-1处M-O键的振动频率νM-O随x的变化规律。表明Mo6+离子逐步被W6+替代,生成了无限互溶的固溶体。

表2 固溶体Bi2Mo1-xWxO6的晶格参数与样品组成的变化关系Table 2 Variation of the lattice parameters as a function of the composition of Bi2Mo1-xWxO6

表3 固溶体Bi2Mo1-xWxO6的红外振动频率Table 3 IR vibration frequency of solid solution Bi2Mo1-xWxO6
图3为3个典型的固溶体x=0、x=0.4、x=1样品的扫描电镜照片。x=0时Bi2MoO6的形貌为形状不规则的片状结构,平均厚度为100 nm,边长可达1 μm。Bi2Mo0.6W0.4O6样品为厚度20~30 nm的纳米片,而Bi2WO6为厚度更薄、边长更小的纳米片,但团聚得比较严重。
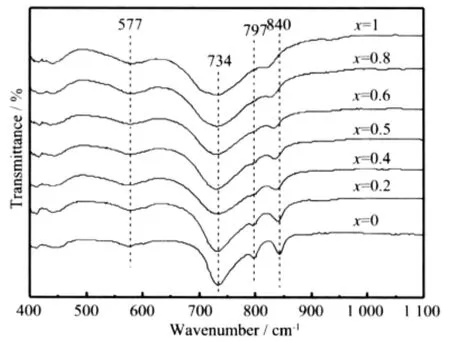
图2 固溶体Bi2Mo1-xWxO6的红外光谱图Fig.2 IR spectra of solid solution Bi2Mo1-xWxO6
固溶体的光吸收性能采用UV-Vis漫反射图谱进行检测。图4为固溶体的UV-Vis漫反射图谱。从图中可以看出,固溶体在可见光区具有较陡峭的吸收带边,表明它们的可见光吸收产生于其本身的带间跃迁,而非杂质的能级作用。从吸收带边估算出的固溶体的带隙分别为2.55 eV(x=0)、2.53 eV(x=0.2)、2.46 eV(x=0.4)、2.49 eV(x=0.5)、2.54 eV(x=0.6)、2.70 eV(x=0.8)、2.84 eV(x=1.0),即随着W6+的替代,带隙出现了先降后升的趋势。Bi2Mo0.8W0.2O6的带隙为2.53 eV,与Bi2MoO6差别不大;x=0.4时带隙最小,为2.46 eV;此后带隙逐渐增大,到Bi2WO6时带隙为2.84 eV。带隙的变化一方面与W6+的替代有关, 另一方面与晶粒尺寸有关。 据文献报道[15,25,26],Bi2MoO6的导带由Mo4d轨道组成,价带由O2p轨道组成,而Bi2WO6的导带由W的5d轨道组成,价带由Bi3+的6s轨道和O2p轨道构成的杂化轨道组成,由于Bi2WO6的Bi6s轨道的参与,提升了价带位置,使得带隙减小,因而x值较小时,随着W6+的掺入,带隙减小。此后,由于晶粒尺寸的下降,带隙又逐渐增大。

图3 固溶体Bi2Mo1-xWxO6样品的SEM图Fig.3 SEM images of solid solution Bi2Mo1-xWxO6
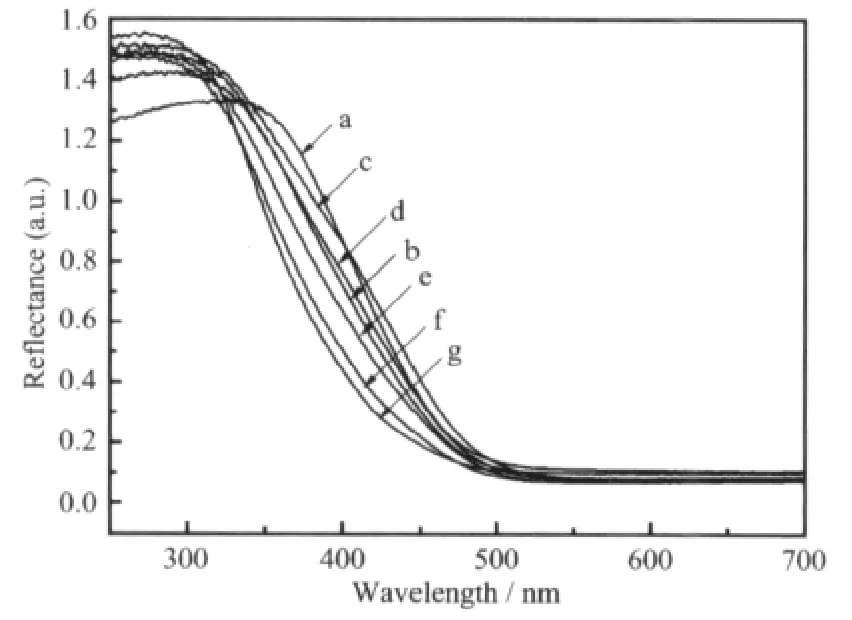
图4 固溶体Bi2Mo1-xWxO6的紫外-可见漫反射图谱Fig.4 UV-Vis diffuse reflectance spectra of solid solution Bi2Mo1-xWxO6
可见光下固溶体Bi2Mo1-xWxO6对RhB的光催化降解如图5所示。从图中可以看出,Bi2MoO6的光催化性能最差,随着x的增大,对RhB的降解增加,到x=0.4时,光催化活性最高。此后,随着x的继续增大,光催化性能又下降。相应的降解率图如图6所示。60 min后,当x从0到1时,降解率分别为82.6%、91.7%、99.6%、97.2%、93.5%、87.1%、88.1%。从图5及图6还可以看出,含W的样品的光催化活性高于Bi2MoO6。

图5 可见光下(λ>420 nm)RhB在固溶体Bi2Mo1-xWxO6样品上的光催化降解图。Fig.5 Photocatalytic degradation of RhB over solid solution Bi2Mo1-xWxO6under visible-light irradiation(λ>420 nm);

图6 Bi2Mo1-xWxO6对RhB的降解率图Fig.6 Degradation ratio of RhB over solid solution Bi2Mo1-xWxO6
从以上结果可以看出,固溶体的光催化性能随着x的增加,出现了先增后减的趋势,这与文献报道的固溶体的光催化性能对成分的依赖关系一致[4-6,22]。光催化性能与以下因素有关:晶粒尺寸和比表面积、带隙和带结构等。如表1所示,W的替代减小了固溶体的晶粒尺寸,而晶粒尺寸的减小可使电子、空穴迁移到粒子表面的时间缩短,从而导致电子和空穴的复合几率降低,量子效率相应提高。由扩散方程τ=r02/(π2D)(其中τ为扩散平均时间,r0为粒子半径,D为电子和空穴在半导体中的扩散系数)可知,扩散时间和粒子半径的平方成正比。所以催化剂颗粒的半径减小到纳米数量级时,电子和空穴的复合几率就比微米级的降低104~106倍,因而可以大大提高量子效率。此外,对于半导体纳米粒子而言,其粒径通常小于空间电荷层的厚度,在此情况下,空间电荷层的影响可以忽略,光生载流子可以通过简单的扩散从粒子的内部迁移到粒子的表面而与电子给体或受体发生氧化或者还原反应。这就意味着对半导体而言,粒径越小,电子和空穴的复合几率就越小,光催化活性就越高。另外,Bi2MoO6的导带由Mo4d轨道组成,价带由O2p轨道组成;而Bi2WO6的导带由W5d轨道组成,价带由O2p和Bi6s组成的杂化轨道组成。随着W的掺入,W在晶格中逐步替代Mo的位置,Mo4d轨道和W5d轨道的混和使得固溶体中导带轨道重叠更多,而O2p和Bi6s轨道的杂化也使得价带中轨道重叠更多,因而含W的样品的光催化活性高于Bi2MoO6[27]。由图4可知,x= 0.4,固溶体的带隙最小,带隙的减小意味着吸收可见光子数量较多[2,28],因而光催化性能最好。
3 结 论
采用低温水热法合成了系列Bi2Mo1-xWxO6固溶体。结果表明,W的替代抑制了固溶体的晶粒生长,导致了较小的晶粒尺寸。随着x的增加,固溶体的带隙出现了先降后升的趋势,x=0.4时带隙最小,而固溶体的光催化性能出现了先增后减的趋势,x=0.4时光催化活性最高,这与固溶体的带隙、带结构和晶粒尺寸变化有关。
[1]QIAN Yi-Tai(钱逸泰).Introduction to Crystallochemistry. 3th Ed.(结晶化学导论)Hefei:University of Science and Technology of China Press,2005:236-236
[2]Kato H,Kudo A.J.Photoch.Photobio.A:Chem.,2001,145 (1/2),129-133
[3]Tsuji I,Kato H,Kobayashi H,et al.J.Am.Chem.Soc., 2004,126(41):13406-13413
[4]Lin J,Yu J C,Lo D,et al.J.Catal.,1999,183(2):368-372
[5]Yu J,Liu S,Zhou M.J.Phys.Chem.C,2008,112:2050-2057
[6]Wang D,Kako T,Ye J.J.Phys.Chem.C,2009,113:3785-3792
[7]Tsunoda Y,Shirata M,Sugimoto W,et al.Inorg.Chem.,2001, 40:5768-5771
[8]Jung J,Kim H,Kim Y,et al.Appl.Catal.A,2007,317:244-249
[9]Klisinska A,Mamede A S,Gaigneaux E M.Catal.Today, 2007,128:145-152
[10]Sim L T,Lee C K,West A R.J.Mater.Chem.,2002,12(1): 17-19
[11]MAN Yi(满 毅),ZONG Rui-Long(宗瑞隆),ZHU Yong-Fa (朱永法).Acta Phys.-Chim.Sin.(Wuli Huaxue Xuebao) 2007,23(11):1671-1676
[12]Le M,Kovanda M,Myslik V,et al.Thin Solid Films,2006, 497:284-291
[13]Utkin V I,Roginskaya Yu E,Voronkova V I,et al.Phys. Status Solidi A,1980,59:75-82
[14]Zhang C,Zhu Y.Chem.Mater.,2005,17(13):3537-3545
[15]Shimodaira Y,Kato H,Kobayashi H,et al.J.Phys.Chem. B,2006,110(36):17790-17797
[16]Zhang L,Wang W,Zhou L,et al.Small,2007,3:1618-1625
[17]Wu J,Duan F,Zheng Y,et al.J.Phys.Chem.C,2007,111: 12866-12871
[18]Ma D,Huang S,Chen W,et al.J.Phys.Chem.C,2009,113 (11):4369-4374
[19]Shannon R D.Acta Cryst.,1976,A32:751-767
[20]Thompson J G,Schmid S,Withers R L,et al.J.Solid State Chem.,1992,101(2):309-321
[21]Castro A,Begue P,Jimenez B,et al.Chem.Mater.,2003, 15:3395-3401
[22]Huang Y,Zheng Z,Ai Z,et al.J.Phys.Chem.B,2006,110: 19323-19328
[23]Hardcastle F D,Wachs I E.J.Phys.Chem.B,1991,95:10763 -10772
[24]Glaeser L C,Brazdil J F,Hazle M A,et al.J.Chem.Soc., Faraday Trans.,1985,81:2903-2912
[25]Fu H,Zhang L,Yao W,et al.Appl.Catal.B,2006,66:100-110
[26]Fu H,Pan C,Yao W,et al.J.Phys.Chem.B,2005,109 (47):22432-22439
[27]Muktha B,Madras G,Guru Row T N.J.Photoch.Photobio. A,2007,187:177-185
[28]Yao W,Ye J.J.Phys.Chem.B,2006,110:11188-11195
Hydrothermal Synthesis and Photocatalytic Properties of Bi2Mo1-xWxO6Solid Solution
LI Hong-Hua LI Kun-WeiWANG Hao*
(College of Materials Science and Engineering,Beijing University of Technology,Beijing100124)
Solid solution Bi2Mo1-xWxO6(x=0~1.0)were synthesized employing hydrothermal method at lower temperatures.XRD results showed that the introduction of W inhibited the crystalline grain growth of the solid solutions and led to smaller crystal sizes.With an increase in W content,IR band around 840 cm-1monotonically shifted to lower frequency,revealing the formation of infinitely soluble solid solutions.UV-Vis diffuse reflectance spectra showed that the band gaps of solid solutions firstly decreased.The band gap of Bi2Mo0.6W0.4O6was the smallest,and then the band gaps of solid solutions increased.At the same time,with increasing W contents,photocatalytic activities of solid solutions increased firstly,reached the best at x=0.4,and then decreased again.Furthermore, photocatalytic activities of the samples containing W were better than that of Bi2MoO6.This might be resulted from the band gap,band structure and the variation of the crystal size of solid solutions.
Bi2Mo1-xWxO6;solid solution;hydrothermal synthesis;photocatalysis
O614.6;O614.53+2;O614.61+2;O614.61+3
A
1001-4861(2010)01-0138-06
2009-07-06。收修改稿日期:2009-10-10。
北京市自然科学基金(No.4082008)资助项目。
*通讯联系人。E-mail:haowang@bjut.edu.cn
李红花,女,40岁,博士;研究方向:无机功能材料。

