新藤黄酸固体脂质纳米粒的制备与质量评价
陈延杰,陈卫东
(安徽中医学院药学院,安徽 合肥 230038)
固体脂质纳米粒(solid lipid nanoparticles)给药系统是目前亚微粒给药系统的发展热点。它以生理相容的高熔点脂质为骨架材料制备,将药物包裹或内嵌于类脂核中,制成粒径约为50~1000 nm的固体胶粒给药系统,副作用小,室温及体温下呈固态粒子[1-2]。新藤黄酸(neo-gambogid acid)是从中药藤黄中分离出的一种具有较高抗肿瘤活性的化合物,抗癌谱广,对人肝癌细胞Bel-7402、人非小细胞肺癌细胞A549、人结肠癌细胞HCT-8以及人卵巢癌细胞A2780的增殖均有明显抑制作用[3]。但新藤黄酸水溶性差,而且静脉给药时有强烈的血管刺激性,限制了其临床应用。此外,新藤黄酸在体内的半衰期短,对治疗效果也有很大的影响。结合临床需求和目前制剂的发展情况,笔者将新藤黄酸药制备成固体脂质纳米粒,控制粒径大小,期望减小新藤黄酸的血管刺激性,提高体内生物利用度,更好地发挥其药理作用。
1 仪器与试药
岛津高效液相色谱仪(LC-20AB泵,SPD-M20A紫外检测器及岛津LC-solution色谱工作站);H-800型透射电子显微镜(日本日立公司);Delsa nano C型粒度分析仪(美国Beckman Coulter公司);UV-2550型紫外可见分光光度计(日本岛津公司);CP225D型电子天平(德国赛多利斯公司);85-2型恒温磁力搅拌器(江苏金坛市环宇科学仪器厂);HH-S2型数显恒温水浴锅(江苏金坛市环宇科学仪器厂)。新藤黄酸原料药(安徽中医学院药化教研室提供);卵磷脂(安徽丰原药业股份有限公司提供);泊洛沙姆188(德国BASF公司,批号为WO39846);单硬脂酸甘油酯(汕头市西陇化工厂有限公司,批号为0906012);吐温-80(国药集团化学试剂有限公司,批号为F20050721);葡聚糖凝胶G-50(美国Pharmacia公司);其他试剂均为分析纯。
2 方法与结果
2.1 新藤黄酸固体脂质纳米粒制备
取处方量的新藤黄酸、单硬脂酸甘油酯、卵磷脂溶于适量无水乙醇中,于(75±2)℃水浴下形成有机相。另取泊洛沙姆溶于蒸馏水中,加入少量吐温-80,加热至与有机相相同温度,构成水相。在搅拌过程中用针头将有机相注入水相,按照每秒1滴的速度,整个过程中反应温度要保持在脂质材料的熔点之上。搅拌1 h,待无水乙醇挥干,将所得的半透明体系快速分散于0~2℃的冰水中,并且冰浴搅拌30 min,即得纳米粒混悬液。
2.2 外观与粒径
按照优化后的处方制备样品,将样品用质量分数为2%的磷钨酸溶液负染,然后滴至铜网上,室温放置至形成薄膜后,用透射电子显微镜观察。由图1可见,新藤黄酸固体脂质纳米粒为具有黄色乳光胶体溶液,电镜下观察纳米粒为许多圆形或椭圆形球粒,平均粒径为(113±6)nm。
2.3 包封率测定
2.3.1 检测波长选择
精密称取新藤黄酸2 mg对照品,用甲醇溶解稀释,定容到10 mL容量瓶中,振摇作为新藤黄酸浓贮备液。以浓贮备液浓度配制质量浓度为0.2 g/mL的新藤黄酸标准溶液,同法配制空白溶液作参比,用紫外分光光度计于200~600 nm波长范围内扫描,结果新藤黄酸在360 nm波长处有最大吸收,故选择360 nm为检测波长。
2.3.2 色谱条件
色谱柱:Lichrospher C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇-0.1% 磷酸(9 ∶1);流速:1.0 mL/min;柱温:25 ℃;检测波长:360 nm;进样量:20 μL。
2.3.3 方法学考察
专属性试验:取新藤黄酸对照品溶液、空白固体脂质纳米粒破乳溶液和新藤黄酸固体脂质纳米粒破乳溶液各20 μL进样分析,色谱图见图2。结果显示辅料对药物含量测定无干扰。
线性关系考察:精密吸取不同体积的贮备液,流动相分别稀释成 50,25,10,1.0,0.1μg/mL 的标准溶液,分别取 20 μL 进样,在按2.2.2项下色谱条件进行测定,计算峰面积。结果表明,以峰面积(A)为纵坐标、质量浓度(C,μg/mL)为横坐标进行线性回归分析,得标准曲线方程 A=30992 C-18289,r2=0.9995。
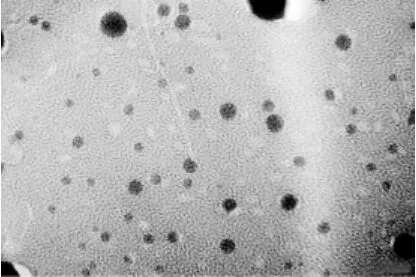
图1 透射电镜图
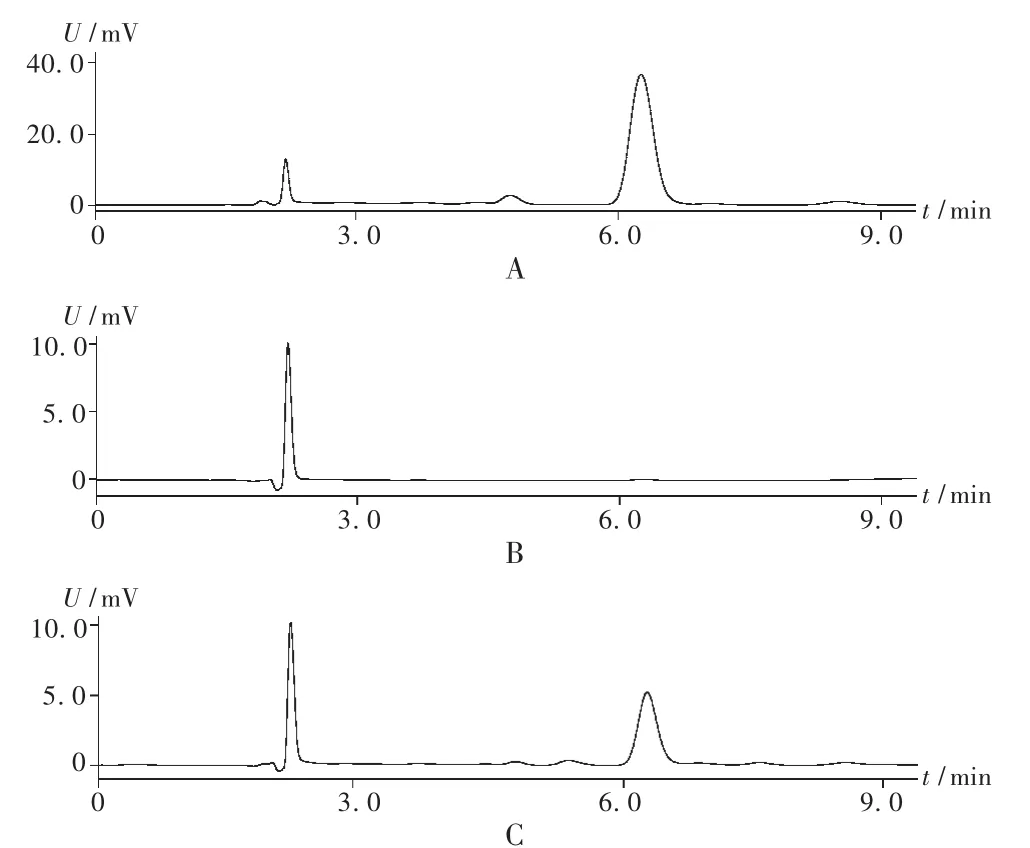
图2 高效液相色谱图
加样回收试验:按处方比例加入1 mL空白固体脂质纳米粒溶液至编号为 1,2,3的10 mL量瓶中,依次精确加入上述新藤黄酸贮备液 0.5,1,2 mL,以甲醇稀释至刻度,得质量浓度10~40μg/mL的样品溶液,分别进样20μL,测定峰面积,连续3次,代入标准曲线换算成实际测定浓度,计算回收率。结果平均加样回收率为99.3%,RSD为1.12%。
精密度试验:取同一新藤黄酸对照品溶液,连续进样5次,测定峰面积。结果峰面积的 RSD为1.02%,表明方法精密度良好。
包封率测定[4]:以Sephadex G-50葡聚糖凝胶柱色谱法分离和游离药物,测定其包封率。吸取1 mL新藤黄酸固体脂质纳米粒混悬液上柱,蒸馏水洗脱,收集带有乳光部分的洗脱液,每2 mL收集1次,加甲醇并超声破乳。另吸取1 mL新藤黄酸固体脂质纳米粒混悬液,直接加甲醇破乳并超声提取。按2.3.2项下色谱条件分别测定两样品中新藤黄酸的含量,按公式包封率=m柱/m总计算包封率。m柱为新藤黄酸固体脂质纳米粒混悬液通过Sephadex G-50后测得的新藤黄酸的含量;m总为新藤黄酸固体脂质纳米粒混悬液直接破乳后测得的新藤黄酸的含量。按处方量进行了3次重复验证试验,制备 3批固体脂质纳米粒,得平均包封率为(60.1±1.1)%。
2.4 正交试验与方差分析
在单因素考察试验结果的基础上,确定单硬脂酸甘油酯(因素A)、泊洛沙姆用量(因素B)、乳化时间(因素C)、单硬脂酸甘油酯与卵磷脂比(因素D)4个因素,每个因素设定3个水平,进行正交设计试验,以包封率为考察指标筛选最佳处方及工艺参数。因素水平设计见表1,试验结果见表2和表3。可知,本试验4个因素影响程度为A>D>C>B,方差分析结果表明,A和B因素有显著影响,初步确定最佳制备工艺为A2B1C1D3,即单硬脂酸甘油酯15 mg,泊洛沙姆浓度为0.8%,搅拌时间1 h,卵磷脂30 mg。

表1 因素水平设计表
2.5 工艺的验证与确定
根据2.4项下确定的最优处方和工艺条件平行制备3批载药固体脂质纳米粒,分别测定其包封率和载药量,确定乳化蒸发-低温固化法的工艺流程,结果见表4。验证结果表明最佳处方重复性强,包封率和载药量保持稳定。
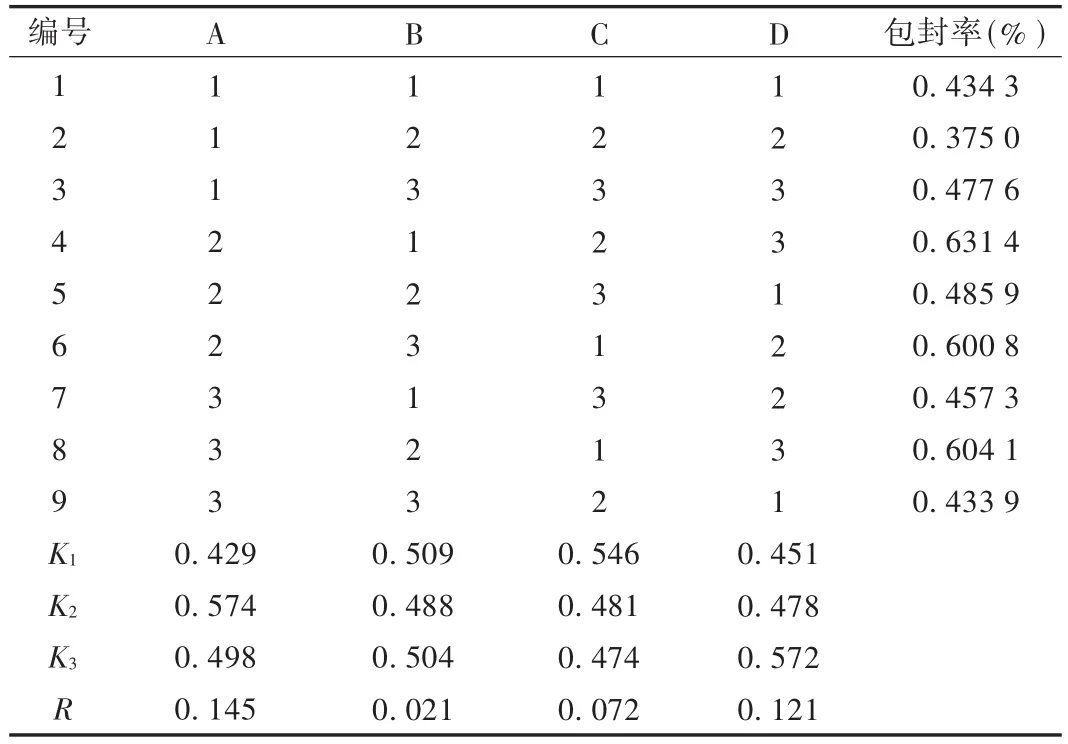
表2 正交试验结果
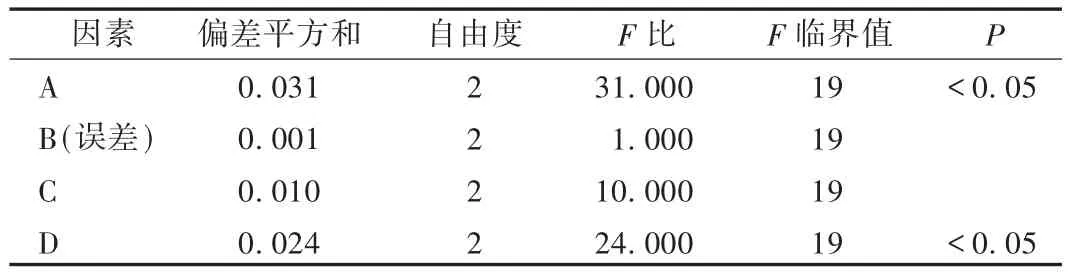
表3 方差分析结果
2.6 纳米粒粒径与电位的测定
取新藤黄酸固体脂质纳米粒混悬液适当稀释后,用纳米激光粒度仪测定粒径及分布,结果见图3、图4。结果表明制得的平均粒径为163.3 nm,粒径大小相近,Zeta电位为-16.9 mV。
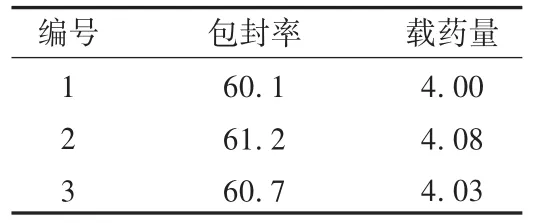
表4 重复最佳处方制备的固体脂质纳米粒的包封率和载药量(%)
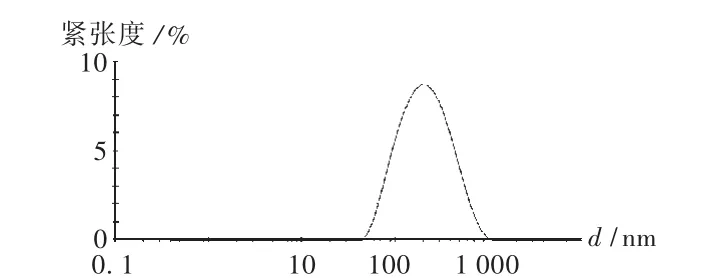
图3 新藤黄酸固体脂质纳米粒粒度分布图
3 讨论
本试验采用高温乳化-低温固化法制备新藤黄酸固体脂质纳米粒,载体材料为单硬脂酸甘油酯和卵磷脂,表面活性剂以泊洛沙姆为主,吐温-80为辅,两者混合使用可得到比较理想的固体脂质纳米粒,控制粒径在100~200 nm范围内。
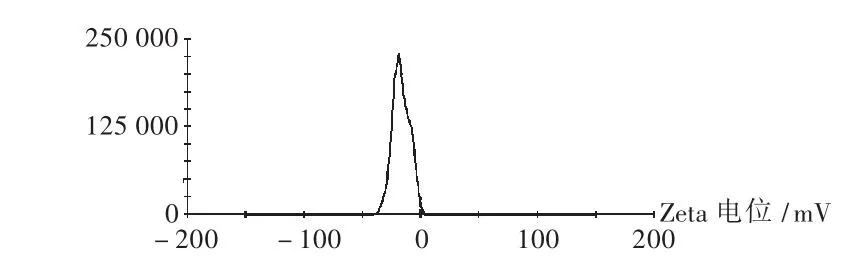
图4 新藤黄酸固体脂质纳米粒Zeta电位图
单硬脂酸甘油酯的熔点在55℃左右,在制备过程中反应温度应高于熔点,最终确定反应温度为(75±2)℃ 。制备初乳时,搅拌速率对反应过程有较大的影响:搅拌速率过低,反应不完全,有机溶剂挥发不完全,造成有溶剂残留;而转速过大,乳化时会产生大量泡沫,影响表面活性剂的效果,最终确定转速为1000 r/min。该方法固化的过程实际也是稀释的过程,故所得混悬液的固体含量较低,粒子比较分散。
试验中发现,固体脂质纳米粒稳定性不理想,放置一段时间后会有沉淀析出,可能是受周围光线、温度、湿度影响,造成晶型的改变[5],从β'转变成β1,使晶格转变,导致部分沉淀在混悬液中析出。期待进一步试验,将固体脂质纳米粒混悬液做成冻干粉,以加强它的稳定性。
[1]Schwarz C,Mehner W,Lucks JS,et al.Solid lipid nanopartieles(SLN)for controlled drug delivery.Production,characterization and sterilization[J].Control Release,1994,30:83-96.
[2]Zur Muhlen A,Schwarz C,Mehnert W.Solid lipid nanoparticles(SLN)for controlled drug delivery-drug release and release mechanism[J].Eur J Pharm Biopharm,1994,45:149-155.
[3]程 卉,彭代银,王效山,等.新藤黄酸体内外抗肿瘤作用研究[J].中草药,2008,3(2):236-240.
[4]张 洪,詹新安,成 蓓,等.联苯双酯固体脂质纳米粒的制备[J].广东药学院学报,2007,23(6):37-40.
[5]Freitas C,Muller RH.Stability determination of solid lipid nanoparticles(SLN)in aqueous dispersion after addition of electrolyte[J].J Microencapsul,1999,16(1):59-71.

