大鼠主动全身过敏试验方法的探讨
陈华英,李秀芳,金若敏,符胜光,姚广涛
(上海中医药大学药物安全评价研究中心,上海 201203)
主动全身过敏试验 (Active Systemic Anaphylaxis,ASA)是考察注射剂Ⅰ型过敏反应要求进行的试验项目之一。《药物研究技术指导原则》(以下简称“指导原则”)中推荐ASA的实验动物一般选用豚鼠,近年来发现临床前中药注射剂安全性评价过敏反应的高阴性率与临床出现较多过敏反应的结果有不一致的现象,促使思考如何提高临床前过敏性试验的灵敏度。有学者建议在进行中药注射剂犬长期毒性试验时密切关注相关的致敏反应出现情况,摸索能充分反映注射剂安全性的评价方法[1]。目前也有文献报道豚鼠对某些中药药源性的致敏原敏感性较差[2]。
近年来,在进行食品、蛋白质等的致敏性评价以及过敏症动物模型 (如哮喘、过敏性休克等)的研究时常采用大鼠作为实验对象[3-12]。这就提示在对中药注射剂的致敏性研究的主动全身过敏试验中,如果能筛选出敏感性较高的大鼠品系作为ASA的实验动物,对于提高中药注射剂临床前致敏性潜力预测将具有重要的现实意义。
在前期研究中发现,不同品系大鼠与过敏相关的一些细胞因子及免疫球蛋白水平在未致敏状态时已存在较大差异,鉴于此,课题组采用了 BN、F344、SD、Wistar 4种品系大鼠,以常用的阳性药卵白蛋白 (Ovalbumin,OVA)和天花粉蛋白(Trichosanthin,TCS)作为受试物,进行了不同品系大鼠ASA的研究。同时对清开灵注射液和注射用灯盏花素进行了豚鼠和4种品系大鼠的主动全身过敏试验。
1 材料
1.1 动物 Hartley豚鼠,清洁级,雌性,体质量300~340 g,购于上海生物制品研究所,许可证编号:SCXK(沪)2004-0003;BN、F344、 SD、Wistar大鼠,SPF级,雌雄各半,160~180 g,由上海西普尔-必凯实验动物有限公司提供,许可证编号:Scxk(沪)2008-0016。动物饲养于上海中医药大学实验动物中心,SPF级环境。
1.2 药物 卵白蛋白,Sigma产品,购于北京鼎国生物技术有限责任公司,批号:DHO15-4;天花粉蛋白 (1.2 mg/mL,1 mL/支),上海金山制药有限公司生产,批号: 070901;清开灵注射液 (10 mL/支),由某制药厂生产,批号:711901A;注射用灯盏花素 (50 mg/支),由某药业有限公司生产,批号:20080905。
2 方法
2.1 卵白蛋白、天花粉蛋白对动物的主动全身过敏试验[1]
2.1.1 给药剂量 根据“指导原则”规定:阳性对照组给予1~5 mg/只卵白蛋白或已知致敏阳性物质,激发剂量一般为致敏剂量的2~5倍量[1]。本实验在前期试验的基础上选择卵白蛋白的致敏剂量5 mg/只,天花粉蛋白致敏剂量0.6 mg/kg,激发剂量分别为致敏剂量的2倍。临用前用生理盐水配制。
2.1.2 致敏 分别取 Hartley豚鼠,BN、F344、SD、Wistar大鼠,按体质量随机分为阴性对照组、卵白蛋白组、天花粉蛋白组,每组6~10只。分别腹腔注射致敏剂量的卵白蛋白和天花粉蛋白,隔日1次,连续3次。阴性对照组注射等容量生理盐水。
2.1.3 激发 在末次致敏后第14天,动物静脉注射进行激发,各组激发剂量为致敏剂量的2倍,静脉快速注射。观察豚鼠注射后即刻至30 min内的过敏反应情况,并对动物过敏反应发生强度进行判断。豚鼠全身致敏性评价标准[1]为:“-”,过敏反应阴性 (症状:正常);“+”,过敏反应弱阳性(症状:躁动、竖毛、颤抖、搔鼻);“++”,过敏反应阳性 (症状:喷嚏、咳嗽、呼吸急促、排尿、排粪、流泪); “+++”,过敏反应强阳性(症状:呼吸困难、哮鸣音、紫癜、步态不稳、跳跃、喘息、痉挛、旋转、潮式呼吸);“++++”,过敏反应极强阳性 (症状:死亡)。计算过敏反应发生率,根据过敏反应发生率和发生程度进行综合判断。大鼠在激发后,除了参照豚鼠过敏反应症状表观察外,还应观察比较给药组与阴性对照组大鼠反应的不同。
2.1.4 补充试验 激发注射后,若发现有过敏反应症状时,取健康未致敏动物2只,自静脉快速注射激发剂量的受试物,观察受试物是否会引起的类似过敏反应症状,供结果判断时参考。
2.2 清开灵注射液、注射用灯盏花素的主动全身过敏试验[1]
2.2.1 给药剂量 卵白蛋白的致敏剂量及激发剂量同2.1.1项;清开灵注射液的致敏剂量为2.5 mL/kg;注射用灯盏花素:豚鼠的致敏剂量为62.5 mg/kg,大鼠的致敏剂量为25 mg/kg,激发剂量均为致敏剂量的2倍。
2.2.2 致敏 分别取 Hartley豚鼠,BN、F344、SD、Wistar大鼠,按体质量随机分为阴性对照组、卵白蛋白组、清开灵注射液组、注射用灯盏花素组,每组6~8只。腹腔注射致敏,阴性对照组给予等容量生理盐水,隔日1次,共3次。
2.2.3 激发 末次致敏后第14天,动物静脉注射进行激发,各组激发剂量为致敏剂量的2倍。同2.1.3项,观察豚鼠注射后即刻至30 min内的过敏反应情况,并对动物过敏反应发生强度进行判断,计算过敏反应发生率,根据过敏反应发生率和发生程度进行综合判断。大鼠在激发后,除了参照豚鼠过敏反应症状观察外,还应观察比较给药组与阴性对照组大鼠反应的不同。
2.2.4 补充试验 同2.1.4项。
3 统计学方法
实验所得数据采用SPSS13.0软件包进行统计学处理,过敏反应发生率采用卡方检验,过敏反应发生程度采用秩和检验。
4 结果
4.1 卵白蛋白、天花粉蛋白的主动全身过敏试验
4.1.1 过敏反应症状、发生率、发生程度 结果显示,豚鼠对卵白蛋白和天花粉蛋白的主动全身过敏反应症状以呼吸困难,步态不稳、紫癜,痉挛,潮式呼吸为主,偶见搔鼻、咳嗽症状;大鼠对卵白蛋白和天花粉蛋白的主动全身过敏反应症状以呼吸急促或呼吸困难、步态不稳、紫疳、四肢软瘫、活动减少为主,偶见喘息、痉挛。4种品系大鼠对卵白蛋白和天花粉蛋白所致主动全身过敏的阳性反应症状比较一致,且与豚鼠的症状大致相近。见表1。在试验结束后对大鼠进行解剖发现,不同品系大鼠的胃肠道均有不同程度的充血。

表1 卵白蛋白和天花粉蛋白致Hartley豚鼠和4种品系大鼠主动全身过敏反应症状Tab.1 Symptoms of Hartley guinea pig and four rat strains induced by ovalbumin or trichosanthin in ASA test
豚鼠和4种品系大鼠对卵白蛋白和天花粉蛋白过敏反应的发生率均为100%,与正常组比较,有极显著差异 (P<0.01),4种品系大鼠对卵白蛋白或天花粉蛋白的过敏反应发生率与豚鼠比较,未见明显差异。见表2。根据豚鼠全身致敏性评价标准对卵白蛋白和天花粉蛋白的过敏反应强度进行评价,豚鼠对卵白蛋白均有极强阳性反应;对天花粉蛋白有3只豚鼠产生阳性反应,3只产生极强阳性过敏反应;4种品系大鼠在本研究所使用剂量下,对两种抗原的主动全身过敏反应强度未见明显的差异,均表现为强阳性。见表3。

表2 卵白蛋白和天花粉蛋白致Hartley豚鼠和4种品系大鼠主动全身过敏反应发生率Tab.2 Incidence of allergic response induced by ovalbumin or trichosanthin in Hartley guinea pig and four rat strains
4.1.2 补充实验 取健康未致敏豚鼠及4种品系大鼠各4只,均分为两组,分别静脉注射激发剂量卵白蛋白和天花粉蛋白,给药后动物未出现类似过敏反应症状。
4.1.3 初步制定大鼠过敏反应症状表 以4种品系大鼠对两种过敏原的过敏反应症状为主要基础见表4、表5,参照豚鼠ASA过敏反应症状表对应观察,将大鼠的阳性反应归纳、汇总分析后,初步制定了大鼠ASA过敏反应症状表6。由于本研究中使用的动物样本数及受试物种类有限,故对大鼠ASA试验中过敏反应症状评价表的初步制定是在豚鼠ASA症状表的基础上补充了大鼠的活动减少、 四肢软瘫等重要症状。
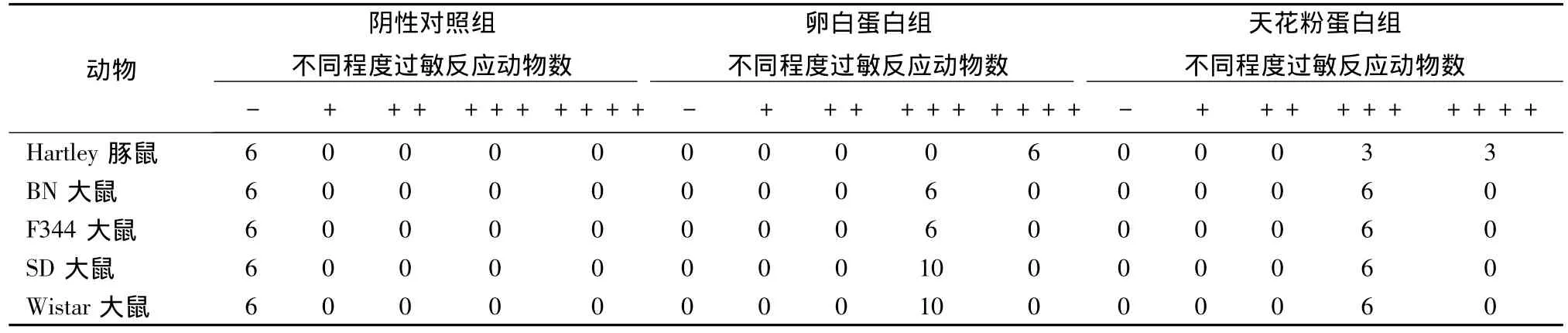
表3 卵白蛋白和天花粉蛋白致Hartley豚鼠和4种品系大鼠主动全身过敏反应程度Tab.3 Degree of allergic response induced by ovalbumin or trichosanthin in Hartley guinea pig and four rat strains
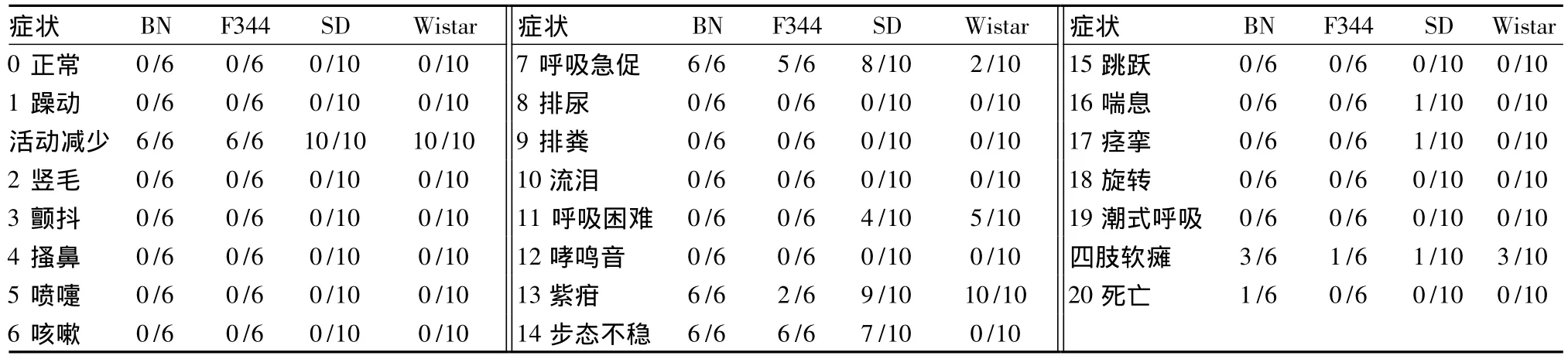
表4 卵白蛋白致4种品系大鼠主动全身过敏反应不同症状的发生率Tab.4 Positive ratio of each symptom induced by onalbumin of four rat strains in ASA test
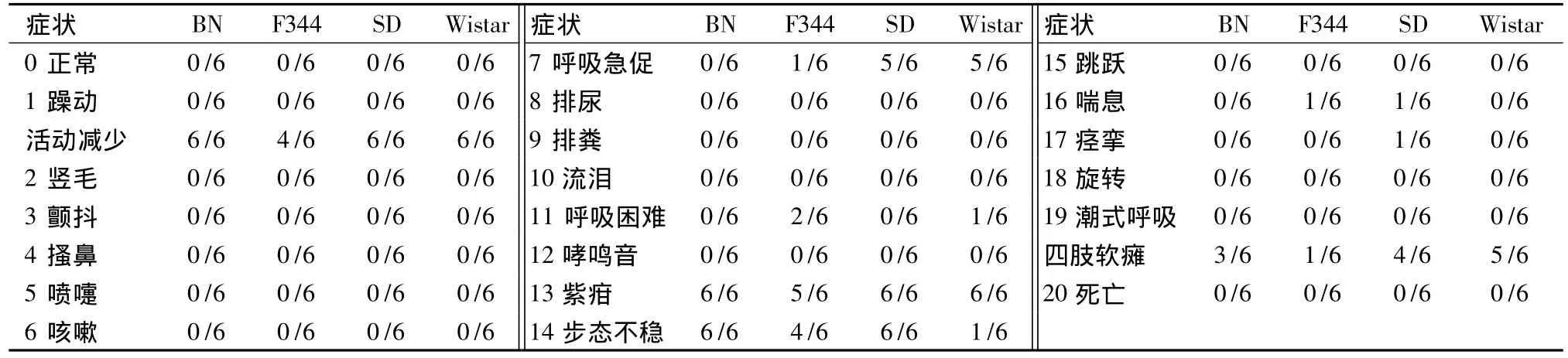
表5 天花粉蛋白致4种品系大鼠主动全身过敏反应不同症状的发生率Tab.5 Positive ratio of each symptom induced by trichosanthin of four rat strains in ASA test
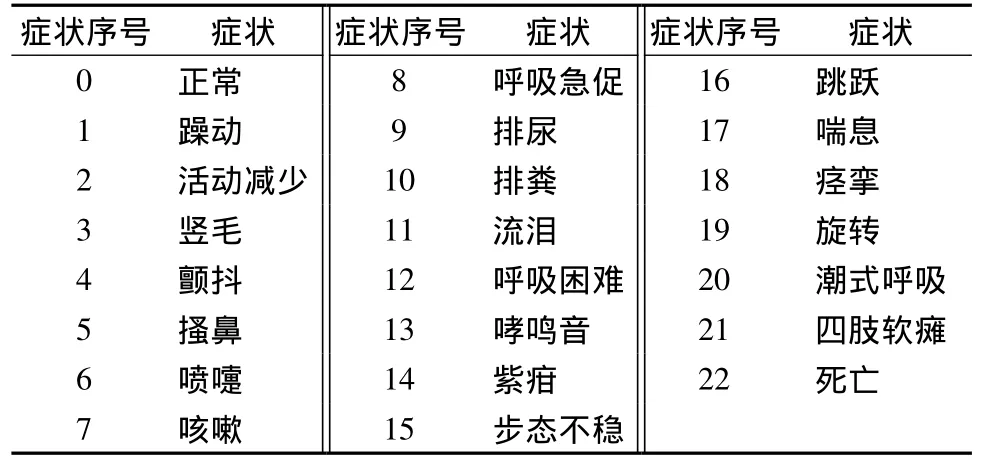
表6 大鼠过敏反应症状Tab.6 Symptoms of rat in ASA test
4.1.4 初步制定大鼠全身致敏性评价标准 将豚鼠与大鼠ASA评价标准及症状进行排序对比,在豚鼠评价标准的基础上,制定了大鼠全身致敏性评价标准,见表7。

表7 大鼠全身致敏性评价标准Tab.7 Evaluation criteria standard of rat in ASA test
4.2 清开灵注射液、注射用灯盏花素ASA试验研究
4.2.1 过敏反应症状、发生率、发生程度 以清开灵注射液攻击不同种类动物后,动物的表现也稍有不同。Hartley豚鼠过敏症状主要为颤抖、偶见双耳发红,BN大鼠出现躁动不安,SD大鼠偶见呼吸急促,F344和Wistar大鼠未见异常反应;注射用灯盏花素攻击动物后,Hartley豚鼠无明显过敏反应症状,BN大鼠出现躁动不安,F344大鼠出现搔鼻、躁动不安、紫疳的过敏反应症状,SD大鼠仅见活动减少,Wistar大鼠未见异常。见表8。在试验结束后,对动物解剖发现,清开灵注射液组的SD大鼠见胃肠道轻微充血,注射用灯盏花素组的BN、F344大鼠均见不同程度的胃肠道充血。

表8 清开灵注射液和注射用灯盏花素致Hartley豚鼠和4种品系大鼠过敏反应症状Tab.8 Symptoms of Hartley guinea pig and four rat strains induced by Qingkailing Injection or Breviscapine Injection in ASA test
清开灵注射液的过敏反应发生率从高到低依次为:BN大鼠 (100%)、Hartley豚鼠 (50%)、SD大鼠 (16.67%)、F344和Wistar大鼠 (0);注射用灯盏花素的过敏反应发生率从高到低依次为:BN大鼠 (100%)和F344大鼠 (100%)、SD大鼠 (83.33%)、Hartley豚鼠和 Wistar大鼠 (0)。见表9。

表9 清开灵注射液和注射用灯盏花素致Hartley豚鼠和4种品系大鼠过敏反应发生率Tab.9 Incidence of allergic response induced by Qingkailing Injection or Breviscapine Injection in Hartley guinea pig and four rat strains
根据豚鼠和大鼠的全身致敏性评价标准,对Hartley豚鼠和4种品系大鼠各组的过敏反应程度进行比较,发现清开灵注射液激发后,Hartley豚鼠、BN大鼠出现弱阳性过敏反应,SD大鼠仅有一只出现呼吸急促,判断为阴性,F344和Wistar大鼠均呈阴性反应;注射用灯盏花素激发后,F344大鼠出现强阳性过敏反应,BN大鼠过敏反应程度明显低于F344大鼠,为弱阳性过敏反应,SD大鼠也为弱阳性反应,而Hartley豚鼠和Wistar大鼠均呈阴性反应。见表10。
4.2.2 补充实验 对动物出现阳性过敏反应的注射剂,取健康未致敏BN大鼠4只,分两组,分别尾静脉注射激发剂量清开灵注射液和注射用灯盏花素,另取健康未致敏F344大鼠2只,尾静脉注射激发剂量注射用灯盏花素,给药后动物均未出现类似过敏反应症状。
5 讨论
大量资料显示[13-15],在中药注射剂所引发的不良反应中,以免疫毒性最为常见,变态反应为其主要毒性特征。在中文科技期刊数据库中1979年—2010年的相关文献的检索中发现,共有50多种已上市的中药注射剂在临床使用时有过敏反应的报道。虽然引起中药注射剂过敏反应的因素很多,如患者的过敏性体质,注射剂成分的复杂,原药材质量及生产工艺的不同,注射剂中相关物质如鞣质等的含有量以及药物的溶媒等都有可能导致过敏反应。考虑到中药注射剂上市前均做过过敏性安全评价,这从另一方面提示,现行的过敏反应试验对于全面评价中药注射剂的潜在致敏性可能存在一定的不足。

对表10 清开灵注射液和注射用灯盏花素致Hartley豚鼠和4种品系大鼠过敏反应发生程度Tab.10 Degree of allergic response induced by Qinghailing Injection or Breviscapine Injection in Hartley guinea pig and four rat strains
目前, “指导原则”中推荐ASA试验的动物“通常选用体质量为300~400 g的豚鼠”。但有文献报道,豚鼠模型在评价中药注射剂过敏反应中敏感性较差,郭姗姗等[16-17]用豚鼠和BN大鼠分别评价了双黄连注射液和清开灵注射液的过敏性,在ASA试验中,BN大鼠各组过敏反应发生率均等于或高于豚鼠各组。Li Zhonggang等[18-19]使用BN大鼠评价了不同剂量双黄连注射液的致敏性,并对其机制进行了初步研究,认为BN大鼠较好的模拟了双黄连注射液的过敏反应,是一个理想的动物模型。目前国内外关于大鼠用于ASA的报道越来越多。
为了进一步考察大鼠用于ASA试验的可行性,从以下几个方面进行了探讨。
首先,关于大鼠是否可以用于主动全身过敏试验:本实验研究结果显示,在较大剂量时,4种品系大鼠对两种阳性药的过敏反应症状、过敏反应发生率基本一致,品系间未见明显差异,且与豚鼠相近,而过敏反应发生程度4种品系大鼠间也基本一致,但略弱于豚鼠,未出现极强阳性的反应死亡。从阳性药定性的角度分析,初步认为大鼠也可以作为ASA的实验动物。
关于大鼠与豚鼠对致敏原敏感性的分析:阳性药剂量较大时,4种品系大鼠与豚鼠用于主动全身过敏试验时,过敏反应发生率和发生程度未见明显区别;在同样致敏和激发条件下的清开灵注射液,BN大鼠的过敏反应发生率高于豚鼠,BN大鼠和豚鼠过敏反应发生程度没有显著差异;对于注射用灯盏花素,豚鼠用大于大鼠的剂量,实验结果呈阴性,而BN、F344、SD大鼠则出现过敏反应。
其次,大鼠的不同品系对预测中药注射剂潜在致敏性的影响:课题组从动物遗传背景、T细胞尤其是辅助性T细胞1与辅助性T细胞2(Th1/Th2)细胞因子分布格局[20]、国内易得和前期研究结果等方面综合考虑,挑选了两个近交系大鼠 BN、F344和两个封闭群大鼠 SD、Wistar。结果显示,对于清开灵注射液,4种品系大鼠的过敏反应发生率从高到低依次为:BN大鼠>SD大鼠>F344、Wistar大鼠;对于注射用灯盏花素,过敏反应发生率为F344、BN大鼠>SD大鼠>Wistar大鼠,而且F344大鼠对注射用灯盏花素表现出了强阳性反应,发生程度显著高于其余3个品系大鼠。以上结果显示,不同中药注射剂对不同品系动物的敏感性存在差异,因此在选用大鼠评价中药注射剂的潜在致敏性时,应注意大鼠的品系。
本研究对结果判断中着重注意了对类过敏的排除:凡是在药物激发注射后,动物出现过敏反应症状时,均按“指导原则”推荐的方法,进行了补充试验,排除了由于受试物作用引起的类似过敏反应症状。
本实验为大鼠用于主动全身过敏试验评价中药注射剂提供了实验依据。研究初步提示,不同品系大鼠对不同中药注射剂潜在致敏能力的敏感性不同,可能与中药注射剂的复杂体系有关。对此我们将优化试验设计,增加更多的中药注射剂,进一步深入研究不同品系大鼠对注射剂敏感性不同的现象。
综合分析,主动全身过敏试验中补充大鼠作为实验动物能进一步提高对中药注射剂过敏反应评价的灵敏性与全面性,有助于更全面的预测药物潜在的致敏性。
[1]国家食品药品监督管理局.药物研究技术指导原则[M].北京:中国医药科技出版社,2005.
[2]黄芳华.从中药注射剂的不良反应浅析中药注射剂研发中的若干问题[J].世界科学技术-中医药现代化,2004,6(3):9-14.
[3]Guo P,Piao X,Cao Y,et al.Recombinant soybean protein betaconglycinin alpha'-subunit expression and induced hypersensitivity reaction in rats[J].Int Arch Allergy Immunol,2008,145(2):102-110.
[4]Akiyama H,Teshima R,Sakushima J I,et al.Examination of oral sensitization with ovalbumin in Brown Norway rats and three strains of mice[J].Immunol Lett,2001,78(1):1-5.
[5]Dewachter P,Raeth-Fries I,Jouan-Hureaux V,et al.A comparison of epinephrine only,arginine vasopressin only,and epinephrine followed by arginine vasopressin on the survival rate in a rat model of anaphylactic shock[J].Anesthesiology,2007,106(5):977-983.
[6]Shishehbor F,Behroo L,Ghafouriyan Broujerdnia M,et al.Quercetin effectively quells peanut-induced anaphylactic reactions in the peanut sensitized rats[J].Iran J Allergy Asthma Immunol,2010,9(1):27-34.
[7]Macedo S M,Vaz S C,Lourenco E L,et al.In vivo hydroquinone exposure impairs allergic lung inflammation in rats[J].Toxicology,2007,241(1-2):47-57.
[8]Jia Y,Xu L,Heisler S,et al.Airways of a hyperresponsive rat strain show decreased relaxant responses to sodium nitroprusside[J].Am J Physiol,1995,269(1 Pt 1):85-91.
[9]Skripuletz T,Schmiedl A,Schade J,et al.Dose-dependent recruitment of CD25+and CD26+T cells in a novel F344 rat model of asthma[J].Am J Physiol Lung Cell Mol Physiol,2007,292(6):1564-1571.
[10]Singh P,Daniels M,Winsett D W.et al.Phenotypic comparison of allergic airway responses to house dust mite in three rat strains[J].Am J Physiol Lung Cell Mol Physiol,2003,284(4):588-598.
[11]刘 婷,梁爱华,易 艳,等.BN大鼠与豚鼠用于药物致敏性评价的比较[J].中国中药杂志,2009,34(4):472-475.
[12]李中港,秦慧迪,汪怀山,等.BN大鼠与Wistar大鼠Ⅰ型超敏反应敏感性的比较[J].中国药理学与毒理学杂志,2010,24(1):30-34.
[13]邱水生,严国鸿.常见中药注射剂不良反应表现及原因探析[J].海峡药学,2007,19(9):114-116.
[14]丁玉峰.中药注射剂引起的变态反应及其影响因素[J].华中医学杂志,2007,31(4):244-246.
[15]黄小萍.中药注射剂不良反应54例临床分析[J].临床误诊误治,2008,21(1):87-88.
[16]郭姗姗,王意忠,张 毅,等.BN大鼠和豚鼠评价双黄连注射液的过敏反应[J].中国药理学与毒理学杂志,2009,23(2):128-133.
[17]郭姗姗,王意忠,张 毅,等.BN大鼠和豚鼠对清开灵注射液致速发型过敏反应的比较[J].药学学报,2009,44(8):852-857.
[18]Li Zhonggang,Gao Yan,Wang Huaishan,et al.A rat model of Shuang Huang Lian injection-induced anaphylaxis[J].Asian Pac J Allergy Immunol,2010,28:185-191.
[19]李中港.过敏反应动物模型的建立及在双黄连注射剂过敏反应检测中的应用[D].济南:山东大学,2010.
[20]Gillespie K M,Saoudi A,Kuhn J,et al.Th1/Th2 cytokine gene expression after mercuric chloride in susceptible and resistant rat strains[J].Eur J Immunol,1996,26(10):2388-2392.

