α-萘酚-硫酸法测定酒糟多糖含量
张世仙,刘 焱,朱 彬,金 茜,曾启华
(遵义师范学院化学化工学院,黔北特色资源应用研究实验室,贵州 遵义 563002)
多糖是由10个以上的单糖分子通过糖苷键结合而成的物质,多糖是一切有生命的有机体必不可少的成分,是构成动植物骨架结构的组成成分,多糖与维持生命的种种生理机能密切相关。研究发现多糖能控制细胞分裂和分化,调节细胞的生长与衰老,有些多糖具有抗肿瘤、抗病毒、降血糖、降血压、镇痛、抗辐射等药效[1-5]。贵州省是酿酒大省,大多数白酒是用当地生产的高粱和小麦为原料通过酒曲发酵而成,其最大副产物——酒糟中残存着大量的多糖、被富集的蛋白质、矿物元素等营养物质[6-7],是提取酒糟多糖的较好原料。
对多糖的定量测定可以采用两种方法[8-17]:一是利用多糖中的还原糖与试剂发生氧化还原反应显色测定,如3,5-二硝基水杨酸盐(DNS)比色法和Somogyi-Nelson法;二是将多糖在强酸性条件下脱水生成糠醛或其衍生物,再与酚类或胺类化合物缩合,生成有特殊颜色的物质进行测定,如苯酚-硫酸法和蒽酮-硫酸法。其中苯酚-硫酸法是常用的一种经典方法,但是苯酚毒性大、易氧化,其提纯操作较难控制,文献[18]报道用萘酚-硫酸法测定白果多糖的含量,方法可行和容易操作。本实验尝试用a-萘酚-硫酸法测定酒糟多糖的含量,以建立酒糟多糖含量的测定方法和实验技术。
1 材料与方法
1.1 材料、试剂与仪器
酒糟 贵州省某酒厂提供;α-萘酚(分析纯) 湘中化学试剂开发中心;葡萄糖(分析纯) 天津市大茂化学试剂厂;无水乙醇(分析纯)、浓硫酸(分析纯) 成都市科龙化工试剂厂。
722型分光光度计 上海精密科学仪器有限公司;TB-214型电子天平 北京赛多利斯仪器系统有限公司;pHS-2C型精密酸度计 上海大普仪器有限公司;RE-52型旋转蒸发仪 上海亚荣生化仪器厂;0412-1型离心机上海手术器械厂;真空冷冻干燥机 美国Labconco公司。
1.2 方法
1.2.1 酒糟多糖的提取工艺[19-22]
新鲜酒糟粉→在料水比1∶12条件下,用盐酸调pH值至5.0~5.5→控制温度用水解蛋白酶降解酒糟中的蛋白质→离心→pH值调至中性→浓缩→4倍体积95%乙醇沉淀→静置→过滤→冷冻干燥→酒糟多糖
1.2.2 溶液配制
葡萄糖标准溶液:精密称取105℃干燥至质量恒定的葡萄糖标准品20mg,用二次蒸馏水定容至500mL,即得葡萄糖标准贮备液。
样品溶液:精密称取样品0.2200g,用二次蒸馏水定容至50mL,移取10mL,用二次蒸馏水定容至100mL,即为0.44mg/mL待测样品溶液。
1.5g/100mLα-萘酚溶液:准确称取1.5gα-萘酚,用体积分数30%乙醇溶液溶解并定容至100mL,即为1.5g/100mLα-萘酚溶液,转移至棕色瓶,于4℃冰箱保存、备用。
1.2.3 最大吸收波长确定
准确移取1mL 0.1mg/mL葡萄糖标准溶液于25mL比色管中,加入1mL 1.5g/100mL的α-萘酚溶液,摇匀并迅速加入5mL浓硫酸,充分混合,室温放置至无气泡后(约20min),在410~710nm波长区域测定吸光度,并以试剂空白为对照。
1.2.4 标准曲线的绘制
准确移取葡萄糖标准溶液10、15、20、30、35、40、45mL于50mL容量瓶中定容,得系列质量浓度的标准溶液。按1.2.3节方法实验,于560nm波长处,以试剂空白为参比测吸光度。
1.2.5 换算因子的测定[12-14]
准确移取1.2.2节中的样品溶液1mL,用二次蒸馏水定容于10mL容量瓶中。取1.0mL溶液5份,按1.2.3节方法实验,测定吸光度,由回归方程计算多糖中葡萄糖平均含量,按下式(1)计算出换算因子f。

式中:m为多糖质量/mg;ρ为样品溶液中葡萄糖的质量浓度/(μg/mL);D为多糖的稀释倍数;V为体积/mL。
1.2.6 样品测定
准确移取1mL质量浓度为0.44mg/mL样品溶液3份,按1.2.3节方法实验,测定吸光度,由回归方程计算葡萄糖含量,按式(2)计算得出酒糟多糖含量。

式中:W为样品的质量/mg;其他量符号含义同式(1)。
2 结果与分析
2.1 最大吸收波长确定
取一定量的葡萄糖标准液,按1.2.3节方法实验所得的吸收曲线见图1。从图1可见,最大吸收峰波长为560nm。

图1 α-萘酚-硫酸法确定多糖最大吸收波长Fig.1 The maximum absorption wavelength for naphthol-vitriol photometric determination of polysaccharide
2.2 标准曲线的测定
根据1.2.4节方法,以葡萄糖质量浓度为横坐标、吸光度为纵坐标绘制标准曲线,标准曲线方程为A=0.0255ρ+0.0419,R2=0.9975,葡萄糖在6~36μg/mL之间呈良好的线性关系。
2.3 测定方法的考察
2.3.1 显色时间的确定
准确移取1mL样品溶液,按1.2.2节方法实验,每隔10min测定1次吸光度,连续测定50min,结果见图2。

图2 显色时间对吸光度的影响(n=3)Fig.2 Effect of coloration time on absorbance (n=3)
由图2可见,冷却至室温后的20min内吸光度很稳定,30min后吸光度虽然有所下降,但下降趋势不明显,因此按1.2.2节方法实验的时间控制在20min之内。
2.3.2α-萘酚溶液添加量的确定
在盛有1.0mL一定质量浓度的葡萄糖标准溶液的5支比色管中,各加入1.0mL二次蒸馏水和1.5g/100mL的α-萘酚溶液0.2、0.6、0.8、1.0、1.2mL,再分别加入2.5mL浓硫酸,另取一支比色管作空白,按1.2.2节方法实验并测定吸光度。结果表明,当1.5g/100mL的α-萘酚溶液加入量为1.0mL时,吸光度较大,见图3。

图3 α-萘酚添加量对吸光度的影响Fig.3 Effect of α-naphthol dosage on absorbance
2.3.3α-萘酚溶液质量浓度的确定
取6支比色管,分别加入1.0mL一定质量浓度的葡萄糖标准溶液,再分别加入质量浓度为0、0.500、0.750、0.875、1.500、1.750g/100mL的α-萘酚溶液,按1.2.2节方法实验并测定吸光度。结果表明,使用1.500g/100mLα-萘酚溶液,吸光度最大,见图4。
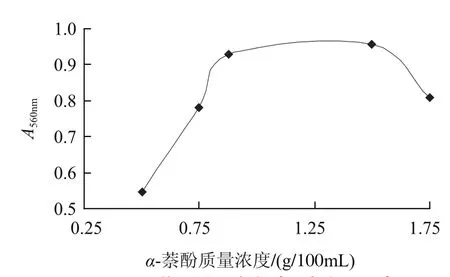
图4 α-萘酚质量浓度对吸光度的影响Fig.4 Effect of α-naphthol concentration on absorbance
2.4 方法学考察
2.4.1 精密度实验
准确移取1mL 一定质量浓度的葡萄糖标准溶液于11支比色管中,加双蒸水1.0mL,再加入1.0mL 1.5g/100mL的α-萘酚溶液,按1.4.3节方法实验,连续测定11次,得吸光度分别为0.904、0.898、0.900、0.900、0.898、0.899、0.901、0.900、0.899、0.900、0.899,计算RSD为0.18%。
2.4.2 重复性实验
准确量取1mL 0.44mg/mL的样品溶液于8支比色管,按1.2.2节方法实验,得吸光度分别为0.686、0.686、0.685、0.684、0.686、0.686、0.684、0.685,计算RSD为0.14%。
2.4.3 加标回收率实验
准确量取2mL 0.44mg/mL的样品溶液于10mL容量瓶中,用二次蒸馏水定容至刻度,取1mL按1.2.3节方法实验,测得吸光度,换算含糖量平均值为0.945μg/mL。再取4支10mL容量瓶,各加入2mL该样品溶液,并分别加入一定量的葡萄糖标准溶液,用二次蒸馏水定容至刻度,取1mL按1.2.3节方法进行实验,结果见表1。
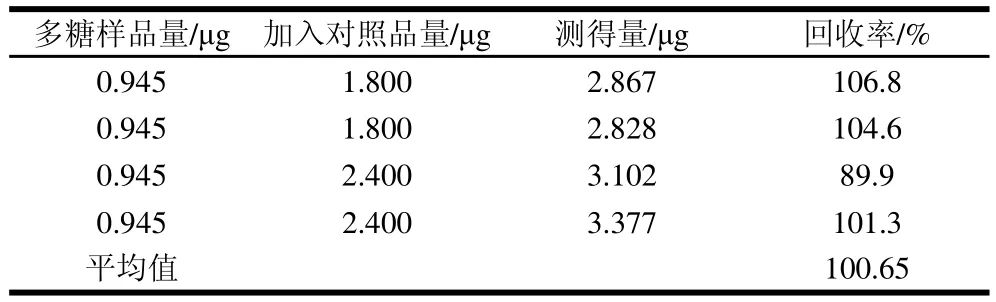
表1 回收率测定结果(n=4)Table 1 Recovery rates of glucose from spiked sample (n=4)
从表1可见,平均回收率为100.65%,RSD为6.5%。2.4.4 换算因子的测定
实验测得1.2.5节中样品溶液的吸光度为0.585、0.585、0.593、0.588、0.586。由回归方程计算出酒糟多糖中葡萄糖平均含量为21.392μg/mL,按换算因子公式计算出f=2.057(n=5)。
2.5 样品测定
将1.2.6节实验测得的吸光度代入回归方程计算葡萄糖含量,再通过多糖含量公式计算得出酒糟多糖平均含量为10.6%,RSD为4.0%(n=3)。
3 结 论
α-萘酚-硫酸法测定酒糟多糖含量实验表明:样品与5mL浓硫酸反应,用1.5g/100mLα-萘酚1.0mL显色,于560nm波长处测定其吸光度,实验结果较稳定,回收率较高。
α-萘酚-硫酸法与常用的苯酚-硫酸法相比,测定酒糟多糖含量的步骤基本一致,但是α-萘酚-硫酸法在操作、试剂消耗等方面更具优势,适合酒糟多糖含量的测定。
[1]张惟杰. 复合多糖生化研究技术[M]. 上海∶ 上海科学技术出版社,1987∶ 124-178.
[2]陈惠黎, 王克夷. 糖复合物的结构与功能[M]. 上海∶ 上海医科大学出版社, 1997∶ 324-341.
[3]王涛, 赵谋明. 多糖的研究进展[J]. 现代食品科技, 2007, 23(1)∶103-106.
[4]魏传晚, 曾和平, 王晓娟, 等. 多糖及其研究进展简述[J]. 广东化工,2004(1)∶ 36-40.
[5]赵国华, 陈宗道, 李志孝, 等. 活性多糖的研究进展[J]. 食品与发酵工业, 2001, 27(7)∶ 45-48.
[6]邢书涵, 连正兴, 孙勇藏, 等. 灵菇源干酪乳杆菌KL1胞外多糖抑制人结肠癌细胞增殖的研究[J]. 食品科学, 2012, 33(7)∶ 284-288.
[7]王肇颖, 肖敏. 白酒酒糟的综合利用及其发展前景[J]. 酿酒科技,2004(1)∶ 65-69.
[8]刘丹. 对多糖测定方法的探讨[J]. 四川文理学院学报∶ 自然科学版,2008, 18(2)∶ 49-51.
[9]武平, 赵文婧, 徐晓娇, 等. 测定葡萄酒中总糖方法的探讨[J]. 中国酿造, 2011, 227(1)∶ 158-161.
[10]赵凯, 许鹏举, 谷广烨. 3,5-二硝基水杨酸比色法测定还原糖含量的研究[J]. 食品科学, 2008, 29(8)∶ 534-536.
[11]孙延芳, 梁宗锁, 张欣, 等. 芒果多糖的纯化与光谱分析[J]. 食品科学, 2012, 33(7)∶ 93-95.
[12]邸明磊, 单晓菊, 马丽娜, 等. 苯酚-硫酸法测定苦豆子多糖含量[J].现代中药研究与实践, 2012, 26(1)∶ 59-61.
[13]钟岩, 潘浦群, 王艳红. 苯酚-硫酸法测定鲜人参中多糖含量[J]. 时珍国医国药, 2008, 19(8)∶ 1957-1958.
[14]夏秀华, 王海鸥. 银杏叶多糖两种测定方法的比较[J]. 食品研究与开发, 2007, 28(11)∶ 124-127.
[15]吴拥军, 刘洁, 吴予明, 等. 中药巴戟天多糖的测定及其微量元素分析[J]. 光谱学与光谱分析, 2005, 25(12)∶ 2076-2078.
[16]刘晓涵, 陈永刚, 林励, 等. 蒽酮硫酸法与苯酚硫酸法测定枸杞子中多糖含量的比较[J]. 食品科技, 2009, 34(9)∶ 270-272.
[17]吴亚军, 朱颖, 夏少秋, 等. 蒽酮-硫酸法测定六味地黄生物制剂中多糖含量的研究[J]. 时珍国医国药, 2011, 22(1)∶ 39-41.
[18]郑敏燕, 耿薇, 魏永生, 等. 萘酚-硫酸显色光度法测定白果多糖含量方法的研究[J]. 应用化工, 2010, 39(3)∶ 447-452.
[19]张世仙, 张素英, 曾启华, 等. 碱法提取茅台酒糟中水溶性膳食纤维的工艺研究[J]. 中国酿造, 2011, 30(10)∶ 126-128.
[20]张世仙, 从凯龙, 曾启华, 等. 酶法提取茅台酒糟中水溶性膳食纤维的工艺研究[J]. 中国酿造, 2012, 31(3)∶ 97-99.
[21]张桂香, 王元秀, 宋晓妍, 等. 响应面法优化啤酒酵母泥中β-1,3-葡聚糖提取工艺[J]. 食品科学, 2012, 33(6)∶ 92-95.
[22]毛磊, 李睿, 金慧芳. 酶解辅助法优选山药多糖的提取工艺[J]. 应用化工, 2009, 38(6)∶ 847-849.

