离子选择电极法测定高氟样品中氟的方法改进
盛晓风,郭莹莹,* ,尚德荣,3,赵艳芳,翟毓秀,宁劲松
(1.中国水产科学研究院黄海水产研究所,农业部海洋渔业资源可持续利用重点开放实验室,山东青岛266071;2.国家水产品质量监督检验中心,山东青岛266071;3.中国海藻工业协会,北京100125)
氟是参与人体正常代谢的一种微量元素,是牙齿和骨骼不可缺少的矿物质。人体摄入一定量的氟,能够促进骨骼发育、预防蛀牙。但若长期摄入过量氟,则对骨骼、肾脏、甲状腺和神经系统造成损害,严重者可形成氟骨症,导致关节疼痛、韧带钙化、骨质增生,甚至瘫痪等病症[1]。南极磷虾和茶叶是典型的高氟样品。南极磷虾作为可供人类利用的蕴藏量最为丰富的海洋生物资源,不仅营养丰富,且储量十分可观。据有关资料估计,南极磷虾的储量可达1 ×109~2 ×109t,是人类赖以生存的后备蛋白库[2]。在当今世界渔业资源日趋衰减的情况下,南极磷虾以其巨大的生物量和潜在的渔业资源价值越来越受到世界各国的重视。但是,由于南极磷虾的高氟含量对人体健康具有潜在的危害,已成为制约南极磷虾综合加工利用的重要瓶颈[3-4]。茶树是一种聚氟作物,饮茶是人体摄入氟的主要途径之一[5]。自从2005 年立顿红茶被曝出氟含量超标的消息以后,加上有报道称中国西南地区部分民族由于饮用高氟含量的砖茶,患上氟斑牙和氟骨病等[6-7],引起消费者对日常饮茶可能导致体内氟超标的担忧。因此,建立一种准确、简单、快速、稳定的测定高氟样品中氟含量的方法,并对南极磷虾和茶叶等高氟样品中氟含量进行监测分析,将为高氟样品的安全性评价和综合开发利用提供科学的研究基础。目前,食品中氟含量的测定方法主要有离子选择电极法(ISE)、离子色谱法(IC)、氟试剂比色法等[8-9]。其中离子色谱法具有准确度高、选择性好、检出限低、重复性好等优点,但离子色谱仪器稳定时间较长、分析成本较高,并且要求被测样品中的悬浮物<0.45μm(以防堵塞进样系统),影响其推广应用;氟试剂分光光度法样品前处理的扩散或灰化蒸馏操作较费时,氟试剂溶液及硝酸镧溶液不稳定,且南极磷虾中丰富的虾青素可能会影响吸光度值,此法一般适用于测定低氟(0.1~2mg/kg)样品;氟离子选择电极法因其选择性好、适用范围宽、快速准确、操作简便等优点而受到广泛的应用,是目前氟含量测定中最常用的方法[10-12]。但是GB/T 5009.18-2003《食品中氟的测定》中规定的氟离子选择电极法的线性范围很窄,将样品稀释后测定氟含量,结果误差较大,不适用于测定氟含量较高的南极磷虾和茶叶等样品。因此,本文对GB/T 5009.18-2003《食品中氟的测定》进行改进,将氟离子选择电极法的线性范围延伸至0.04 ~50.0μg/mL,建立了适合于高氟样品中氟含量的检测方法,并利用茶叶中氟成分分析标准物质(GBW08516)和两个能力验证样品CNCA-06-07-S24 紧压茶(边销茶)、CNCA-06-07-S95 紧压茶(边销茶)进行方法质控分析,检测结果均满意。
1 材料与方法
1.1 材料与仪器
南极磷虾 青岛福卡海洋生物科技有限公司;茶叶中氟成分分析标准物质(GBW08516) 国家标准物质研究中心;紧压茶(边销茶)(编号:CNCA-06-07-S24、CNCA-06-07-S95) 国家农副产品质检中心(湖南)和湖南省产商品质量监督检验所。
BP221S 电子分析天平 感量0.0001g,德国赛多利斯公司;85-1 型磁力搅拌器 上海沪西分析仪器厂有限公司;PHS-3C 数字酸度计 梅特勒-托利多(上海)有限公司;pF-1 型雷磁离子氟离子选择电极 上海精密科学仪器有限公司;232 型饱和甘汞电极 上海精科雷磁仪器厂。
乙酸钠溶液(3mol/L);柠檬酸钠溶液(0.75mol/L);总离子强度缓冲剂 将乙酸钠溶液和柠檬酸钠溶液等体积混合,临用时现配制;盐酸(1 +11);氟标准溶液1000μg/mL 国家标准物质研究中心;氟标准使用液浓度分别为1.0、10.0、100.0μg/mL 用氟标准溶液稀释至相应浓度,现用现配。
本方法所用水均为不含氟的去离子水,试剂为分析纯,全部试剂贮存于聚乙烯塑料瓶中。
1.2 原理

1.3 实验方法
1.3.1 样品制备 用匀浆机将南极磷虾绞碎混匀,备用;将茶叶中氟成分分析标准物质和紧压茶在80℃条件下烘干1h,备用。
1.3.2 标准曲线的绘制 分别吸取氟标准使用液(1.0μg/mL)0、1.0、2.0、5.0、10.0mL,置于50mL 容量瓶中,加入25mL 总离子强度缓冲液和10mL 盐酸溶液,加水至刻度,混匀,倒入标准系列塑料杯中。将电极电位仪接通,将清洗好的氟离子选择电极和甘汞电极插入塑料杯中,在磁力搅拌器上搅拌数分钟,待读数稳定后(即每分钟电极电位变化小于0.2mV)停止搅拌,静置30s,读取毫伏值,同时记录测定时的温度。标准系列测定从低浓度到高浓度逐个进行,以氟离子浓度对数(lgCF-)为横坐标,以电极电位(mV)为纵坐标,绘制一条浓度范围为0.02 ~0.20μg/mL 的标准曲线[13]。
分别吸取10.0μg/mL 氟标准溶液0.0、0.2、0.4、0.6、0.8、1.0、2.5mL 和100.0μg/mL 氟标准溶液0.5、1.0、1.5、2.0、2.5、5.0、10.0mL 以及1000μg/mL 标准溶液2.5mL,置于50mL 容量瓶中,加入25mL 总离子强度缓冲液,10mL 盐酸溶液,加水至刻度,混匀,倒入塑料杯中。按照上述步骤,读取电位值。以氟离子浓度对数(lgCF-)为横坐标,以电极电位(mV)为纵坐标,绘制一条浓度范围为0.04 ~50.0μg/mL 的标准曲线。
1.3.3 样品中氟含量的测定 分别称取1g(精确至0.0001g)虾肉样品、茶叶标物和紧压茶于50mL 容量瓶中,加入10mL 盐酸溶液,密闭浸泡提取1h(不时轻轻摇动),然后加入25mL 总离子强度缓冲剂,加水至刻度,混匀,过滤,备用。
方法一:分别移取0.5mL 虾肉提取液、1mL 紧压茶提取液和5mL 茶叶提取液,加入总离子强度缓冲剂25mL 和盐酸溶液10mL,用水定容至50mL,得到稀释液。将样品稀释液倒入塑料杯中,插入氟离子选择电极和甘汞电极,在磁力搅拌器上搅拌数分钟,待读数稳定后停止搅拌,静置30s,读取平衡电位值,查线性范围窄的氟标准曲线(0.02~0.20μg/mL),得到氟含量,每个样品平行测定6 次,考察方法的精密度。
方法二:分别移取25mL 南极磷虾、紧压茶和茶叶的提取原液,倒入塑料杯中,将电极电位接通,按照上述操作步骤,读取平衡电位值,查线性范围宽的氟标准曲线(0.04~50.0μg/mL),得到氟含量,每个样品平行测定6 次,考察方法的精密度。
1.3.4 结果计算 根据公式计算试样中氟含量:
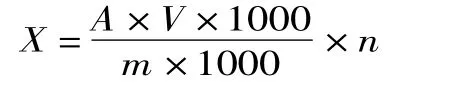
式中:X-试样中氟的含量(mg/kg);A-测定用样液中氟的浓度(μg/mL);m-试样的质量(g);V-样液总体积,单位为毫升(mL);n-稀释倍数。
1.3.5 回收率实验 分别称取1g(精确至0.0001g)南极磷虾、茶叶标准物质和紧压茶于50mL 容量瓶中,添加不同量的标准溶液(如表5 所示,加标量为样品中氟含量的0.5~2 倍,但加标后的总浓度应不超过方法的测定上限浓度值),加入10mL 盐酸溶液,密闭浸泡提取1h(不时轻轻摇动),然后加入25mL 总离子强度缓冲剂,加水至刻度,混匀,过滤,备用。
分别移取25mL 南极磷虾、紧压茶和茶叶的提取原液,倒入塑料杯中,测得电位值,查线性范围宽(0.04~50.0μg/mL)的标准曲线,得到氟含量,然后根据样品加标量计算回收率。
2 结果与讨论
2.1 标准曲线的绘制(标准系列的lgCF -与电极电位的线性关系)
以氟离子浓度对数(lgCF-)为横坐标,以电极电位(mV)为纵坐标,得到两条浓度范围分别为0.02~0.20μg/mL 和0.04 ~50.0μg/mL 的标准曲线,如图1和图2 所示。
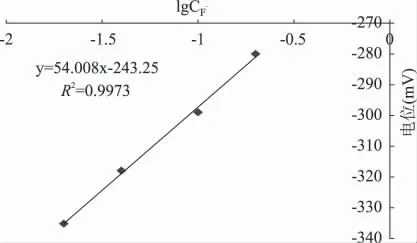
图1 氟标准曲线(0.02~0.20μg/mL)Fig.1 The standard curve of fluorine(0.02~0.20μg/mL)

图2 氟标准曲线(0.04~50.0μg/mL)Fig.2 The standard curve of fluorine(0.04~50.0μg/mL)
有文献报道,氟电极的测定范围在0.02 ~2000μg/mL,当标准溶液温度在20~25℃时,标准曲线的斜率应在58.1 ±2 之间,表明电极具有良好的性能[14]。本文测定的两条标准曲线其溶液温度均为23℃,由图1 可知,线性范围在0.02~0.20μg/mL 时,相关系数为R2=0.9973,线性一般,标准曲线为E =54.008 lgCF--243.25,电极斜率为54.008,不符合斜率要求58.1 ±2。这是由于在低浓度窄线性范围内,氟电极的响应值不稳定,受外界因素的影响较大,如待测液pH、温度、搅拌速度和测定的顺序等,且这种干扰随着氟离子浓度的降低而增大。由图2 可知,当线性范围在0.04~50.0μg/mL 时,曲线呈良好的线性关系,E =58.916lgCF--238.15,电极斜率为58.916,相关系数为R2=0.9998,完全符合测定要求。这是由于在高浓度宽线性范围内,氟电极在低浓度条件下受外界因素的干扰可忽略不计。但是并非线性越宽越好,线性范围的上限和下限是线性方程的可靠性或者准确性的一个区间表达,应根据所测样品中氟的实际浓度来决定线性范围,当标准曲线的相关系数大于0.998,而且所测样品中氟含量包括在范围中(最好位于上限和下限的中间),表明该线性范围合理。
2.2 查两条标准曲线得到的氟含量测定结果比较
将提取的样品原液稀释相应倍数后,按照氟离子选择电极法的操作步骤,读取平衡电位值,查线性范围窄的氟标准曲线(0.02~0.20μg/mL),得到南极磷虾、茶叶标物和紧压茶中的氟含量,结果如表1所示。
将提取的样品原液直接倒入塑料杯中,根据所得电位值,查线性范围宽的氟标准曲线(0.04 ~50.0μg/mL),得到南极磷虾、茶叶标物和紧压茶中氟含量,具体结果见表2。
采用线性范围窄的标准曲线进行氟定量时,由于样品中氟含量非常高,测定之前需要稀释相应倍数,由表1 和表2 可知,对氟含量较高的南极磷虾而言,样品提取液稀释与否,氟含量测定结果差别很大,分别为419.8mg/kg 和548.3mg/kg,相对偏差达到26.5%,而且在稀释100 倍的过程中明显增大了实验误差,测定结果不准确。将茶叶标准物质提取液稀释10 倍时,氟含量测定结果为70.1mg/kg,超出了标准值的范围(64.3 ±5.4)mg/kg。而应用线性范围宽的标准曲线时,不需要对样品稀释,测定结果为67.2mg/kg,符合标准值的范围,RSD 为2.5%。对能力验证样品紧压茶而言,采用线性范围宽的标准曲线定量时,测定结果分别为180.3mg/kg 和239.6mg/kg,RSD 分别为1.4%和1.8%,Z 值分别为0.47 和0.32,考核结果满意(评价原则:中位值分别为178 和238,Z≤2 为结果满意),然而将样品稀释50 倍,采用线性范围窄的标准曲线定量时,测定结果分别为189.0mg/kg 和253.1mg/kg,与中位值相比,具有显著性差异。
2.3 回收率实验
通过进行回收率实验,结果表明南极磷虾的回收率为88.7%~98.2%,茶叶标物的回收率为91.2%~105.3%,紧压茶的回收率为89.7%~104.0%(见表3)。通过采用延长工作曲线的方法,将线性范围扩展至0.04~50.0μg/mL,可以不必稀释样液,从而减少实验误差,而且加标回收率良好,表明线性范围宽的标准曲线(0.04~50.0μg/mL)适用于高氟样品中氟含量的测定。
2.4 氟测定时的注意事项
首先饱和甘汞电极在使用之前一定要用去离子水浸泡10~24h;氟离子选择电极和饱和甘汞电极组成电池,电位在-370mV 稳定后才能正常使用;氟离子选择电极在测定时,试样和标准溶液应在同一温度;在测量时,电极用蒸馏水清洗后,应用滤纸擦干后进行测试,以防止引起测量误差;在测量试样较多浓度相差较大时,建议用两支氟离子选择电极,以免引起误差;建议将氟标准溶液存放在清洗后的聚乙稀塑料瓶中,对使用的容量瓶、移液管和玻璃容器应及时清洗,酸缸浸泡过夜;氟电极在使用完毕后建议用去离子水清洗至-370mV 后干放,这样可以延长电极使用寿命,并且不会影响下一次测量。
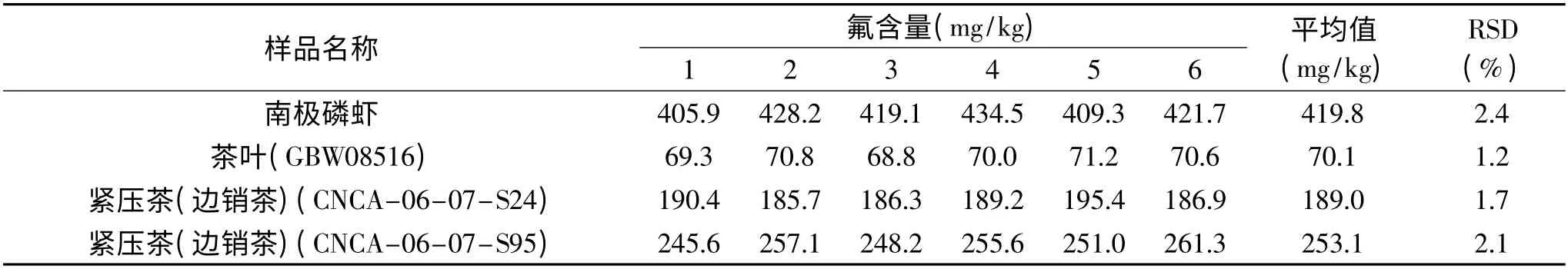
表1 查氟标准曲线(0.02~0.20μg/mL)得到的不同样品中氟含量Table 1 The obtained fluorine content in different samples by checking standard curve of fluorine(0.02~0.20μg/mL)
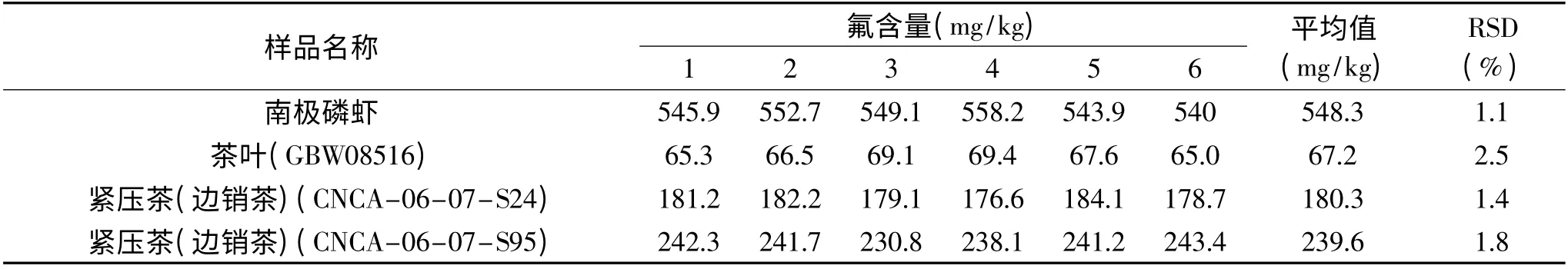
表2 查氟标准曲线(0.04~50.0μg/mL)得到的不同样品中氟含量Table 2 The obtained fluorine content in different samples by checking standard curve of fluorine(0.04~50.0μg/mL)

表3 不同样品中氟的回收率测定结果(n=3)Table 3 The results of fluoride recoveries in different samples(n=3)
3 结论
氟离子选择电极法具有抗干扰能力强,操作相对简单、结果准确可靠等优点,GB/T 5009.18-2003《食品中氟的测定》中氟离子选择电极法的线性范围为0.02~0.20μg/mL,适用于测定一般食品中氟含量。对于南极磷虾和茶叶等高氟样品,需对样液稀释50~100倍后方可测定,稀释过程中增大了实验误差,影响了测定结果的准确性。因此,本文对国标方法进行改进,将线性范围扩展至0.04~50.0μg/mL,建立了氟离子选择电极法测定南极磷虾和茶叶等高氟样品中氟含量的方法,通过精密度及回收率实验,南极磷虾中氟的回收率为88.7%~98.2%,茶叶标物的回收率为91.2%~105.3%,紧压茶的回收率为89.7%~104.0%,RSD 为1.1%~2.5%。结果表明该方法的稳定性好、精密度高、操作简便、检测结果准确可靠,便于推广应用。采用该方法对南极磷虾和茶叶等高氟样品中氟含量进行监测分析,将为高氟样品的食用安全性评价提供科学依据,为南极磷虾优质资源和茶叶资源的合理开发利用提供理论基础。
[1]李爱琴,李海涛.氟污染研究综述[J].甘肃环境研究与监测,1995,3(4):50-53.
[2]张海生,潘建明,刘小涯,等.南极磷虾富氟异常的原因及机理[J].海洋学报,1994,16(4):120-125.
[3]朱兰兰,赵晓军,周德庆,等.南极磷虾中氟的研究进展[J].农产品加工·学刊,2012,22(3):24-25.
[4]Bunji Yoshitomi,Ichiro Nagano.Effect of dietary fluoride derived from Antarctic krill(Euphausia superba)meal on growth of yellowtail(Seriola quinqueradiata)[J].Chemosphere,2012,86(9):891-897.
[5]汪禄祥,张云倩.茶叶中氟对人体的健康影响[J].云南科技管理,2006,12(4):51-52.
[6]Jin Cao,Sha Fei Luo,Juan Yi,et al.Safety evaluation on fluoride content in black tea[J].Food Chemistry,2004,88(10):233-236.
[7]黄文景,蒋贵发,黄明立,等.广西市售茶叶含氟量的调查[J].广西预防医学,2005,11(4):231-232.
[8]贾丽,范筱京.食品中氟离子的分析方法[J].食品科技,2006,21(9):250-252.
[9]马立锋,阮建云,石元值,等.茶叶中氟的测定方法研究[J].茶叶通报,2003,25(3):103-104.
[10]Marcel Langenauer,Urs Krähenbühl,Armin Wyttenbach.Determination of fluorine and iodine in biological materials[J].Analytica Chimica Acta,1993,274(2):253-256.
[11]黄会秋.微波消解-氟离子选择电极法测定海产品中氟的研究[J].中国卫生检验杂志,2005,15(9):1088-1090.
[12]王娅,陈伯涛,姚福荣,等.超声波萃取-离子选择电极法测定茶叶中氟含量[J].安徽农业科学,2012,40 (3):1445-1447.
[13]中华人民共和国卫生部,中国国家标准化管理委员会.GB/T 5009.18-2003《食品中氟的测定》[S].北京:中国标准出版社,2003.
[14]周定友.氟离子选择电极的影响因素及对策[J].中国卫生检验杂志,2001,11(6):746-747.

