以鸡蛋壳制备丙酸钙*
秦建芳,弓巧娟,姚陈忠,宁笑笑,谭俊民
1(运城学院 应用化学系,山西 运城,044000)2(康杰中学,山西 运城,044000)
由废弃鸡蛋壳制备丙酸钙的工艺[1],一般为高温煅烧法和直接反应法。高温煅烧法是将鸡蛋壳在高温下煅烧,使主要成分CaCO3转化为CaO,然后与丙酸反应制备丙酸钙。直接反应法是直接将经过壳膜分离后粉碎的鸡蛋壳与丙酸在水浴加热下制备丙酸钙。前一种方法需要高温煅烧,能耗大,成本高,而且在煅烧过程中产生大量CO2和粉尘污染;后一种方法直接采用水浴加热,降低了能耗成本,避免了高温煅烧蛋壳所造成的环境污染,是鸡蛋壳制备丙酸钙的发展方向[2]。本文以废弃鸡蛋壳为原料利用直接反应中和法制备丙酸钙。
1 仪器与药品
丙酸(AR),无水CaCl2(AR)(M = 110.99 g/mol),浓HCl(12 mol/L),废鸡蛋壳(学校食堂提供)。
SHZ-D(Ⅲ)循环水式真空泵(巩义市予华仪器有限责任公司);电热鼓风干燥箱(沈阳市节能电炉厂);85 -2 数显恒温磁力搅拌器;TAS -990AFG 型原子吸收分光光度计(北京普析通用仪器有限责任公司)。
2 实验方法
2.1 蛋壳预处理
用自来水清洗蛋壳,去除表面的杂质,晾干,放入烘箱干燥,研碎、备用。
2.2 壳膜分离
称取50 g 蛋壳放入烧杯中,加入20 mL 浓HCl、150 mL 蒸馏水作为壳膜分离剂[4],室温下搅拌1 h,使壳膜完全分离,静置、回收水面上的蛋壳膜,将蛋壳烘干(在预处理中已研碎)。
2.3 中和反应制备丙酸钙
称取5 g 蛋壳粉,以固液比为1∶10(g∶mL)的量加水,保持反应温度为60℃,在不断搅拌下,缓慢加入理论值150%的丙酸,反应6.5 h 后,得到所需溶液。将溶液抽滤,除去不溶物,然后将滤液转移到蒸发皿中蒸发、浓缩,80℃干燥、得白色粉末状产品,产率为70.35%。
2.4 产品纯度的测定
2.4.1 钙标准溶液的配制
准确称取0.276 9 g 无水CaCl2溶于100 mL 容量瓶内,用二次蒸馏水稀释至刻度,充分摇匀后得到1 mg/mL 钙标准溶液。稀释后得到一系列钙标准溶液2、4、6、8、10、12、14 μg/mL。
2.4.2 待测溶液的配制
为了防止结晶水对实验结果的干扰,取适量的产品放入马福炉中350℃煅烧5 h,准确称取煅烧产物0.249 7 g,溶于100 mL 的容量瓶中,稀释至刻度、摇匀、待用。
2.4.3 测定
在波长422.7 nm 处,测定空白液、上述一系列标准溶液、待测溶液的吸光度,绘制标准曲线,得出回归方程,然后根据回归方程计算出待测溶液中Ca2+的浓度,得出产品的纯度。
2.5 正交试验设计
为确定中和反应的最佳条件,将影响反应的4 个因素:反应温度、反应时间、固液比、丙酸用量设置不同的水平(见表1)进行正交实验。

表1 正交试验的因素和水平L9(34)Table 1 Factors and levels of orthogonal experiment L9(34)
3 结果与讨论
3.1 正交试验结果分析
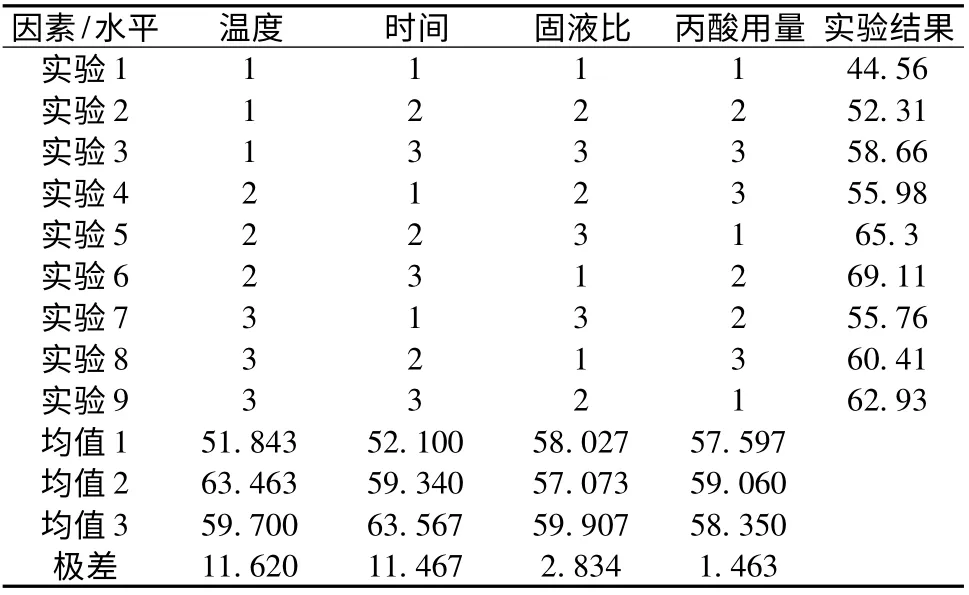
表2 正交试验结果及极差分析Table 2 Orthogonal test results and range analysis
由表2 极差分析可知:影响丙酸钙产率的因素大小依次为反应温度>反应时间>固液比>丙酸用量。主要因素应取最好的水平,而次要因素可以选取适当的水平。以蛋壳为原料制备丙酸钙按现有的因素和水平,最佳工艺条件为:温度50℃,时间5 h,固液比1∶18,丙酸用量150%。但该组合在正交表中没有出现,按照前面的实验方法进行反应,得出该条件下,丙酸钙的产率为70.03%,稍高于正交试验结果。
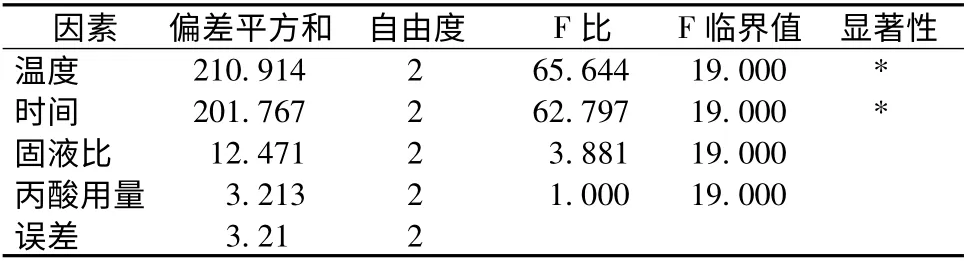
表3 方差分析表Table 3 Analysis of variance table
由表3 可以看出,影响因素的主次顺序与上述分析相同,温度、时间的F 比>19.000,即温度、时间对试验结果影响极显著;固液比、丙酸用量的F 比<19.000,即固液比和丙酸用量的影响程度相对较小。结论与极差分析法相同。
在利用极差和方差分析法分析正交试验结果后,由于所得的最佳搭配只是相对于被选因素和水平而言的,因此通常需作进一步讨论,根据成本、时间、收益、能耗等方面的统筹考虑选取适当的水平[4](本实验中固液比选取1 ∶10,丙酸用量为理论用量的150%)。而主要因素则根据效应曲线图进行详细分析:对温度而言,温度太高或太低,丙酸钙的产率都不高,在单因素试验中,可细化实验条件,选取适当温度45、50、55、60、65℃,观察丙酸钙的产率变化情况;对时间而言,效应曲线随着时间的增加,丙酸钙的产率也在增加,分别设定反应时间为4.5、5.5、6.5、7.5 h。观察丙酸钙的产率变化。
3.2 单因素实验
3.2.1 固液比对丙酸钙产率的影响
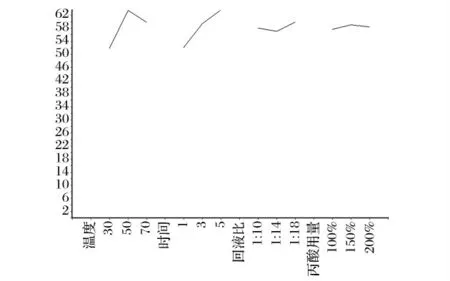
图1 效应曲线图Fig.1 Effect curve
从效应曲线图1 可知,固液比为1∶18 时产率最高,1∶10 时次之。丙酸和蛋壳的反应属于多相反应体系,既有固相又有液相,且生成的产物是易溶于水的,反应后进入了液相,固液比太小会导致丙酸钙的浓度太大,使溶液极易达到饱和,不利于反应向右进行[6]。但固液比太大会造成后续的蒸发、浓缩时间变长,从而使能耗增加。所以从时间、收益等方面的统筹考虑,固液比1∶10 为最佳条件。
3.2.2 丙酸用量对丙酸钙产率的影响
丙酸用量为理论用量的150%时,丙酸钙的产率最大(见图1)。这是因为丙酸是弱酸,部分解离,量少时,溶液中H+的浓度小,使得反应不完全,导致产率较低。随着丙酸用量逐渐增大,丙酸浓度增大,使得溶液中H+浓度增加,有利于丙酸钙的生成[6]。但是随着丙酸的继续过量,丙酸钙的产率却略有降低。而且此时体系中有大量的丙酸剩余,不仅增加了后处理的难度,也造成原料的浪费。所以选择丙酸用量为理论用量的150%为最佳反应条件。
3.2.3 中和反应温度的确定
由图2 可知,丙酸钙的产率随着温度的升高而逐渐增大,在60℃时,达到最大值。随着温度的升高,分子的运动速度加快,CO2气体溢出速度加快,反应速率很大,但温度太高时,丙酸和水的蒸发速度太快导致丙酸钙的浓度大大增加,不利于反应的进行。因此,反应的最佳温度为60℃。
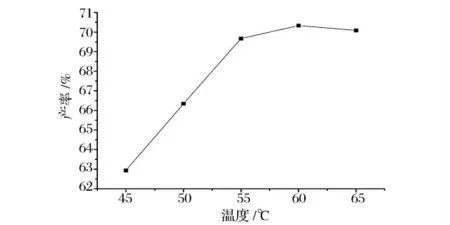
图2 反应温度对产率的影响Fig.2 The influence of reaction temperature on the yield
3.2.4 中和反应时间的确定
弱酸丙酸和弱碱碳酸钙的反应速度相对较慢,反应时间太短,反应不完全,丙酸钙的产率较低。由图3 可知,随着反应时间的延长,丙酸钙的产率增加。但是在6.5 h 以后增加的不太明显。这是因为此时反应已基本达到动态平衡,再增加反应时间只是徒劳。因此,最佳反应时间为6.5 h。
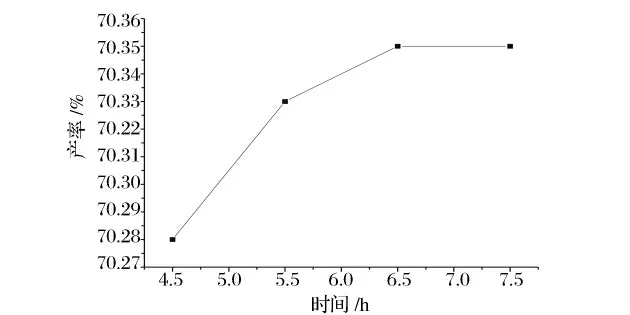
图3 反应时间对产率的影响Fig.3 The influence of reaction time on the yield
3.3 产品的纯度的测定
3.3.1 绘制钙标准工作曲线
在波长422.7 nm 处,测定空白液、一系列标准溶液、待测溶液的吸光度,得到钙标准工作曲线A =0.005c+0.01,R =0.999 47,表明浓度在2 ~14 μg/mL 范围内,线性关系良好。
3.3.2 产品纯度的测定
通过原子分光光度计平行测定3 组待测试液的吸光度平均值为0.056。可知Ca2+浓度为9.2 μg/mL,产品的纯度为96%。
4 结论
本文以废弃鸡蛋壳为原料采用直接反应中和法制备食品防腐剂丙酸钙。采用正交试验和单因素试验相结合的方法,确定了制备丙酸钙的最佳工艺条件为:反应温度60℃,反应时间6.5 h,固液比为1∶10 (g∶mL),丙酸用量为理论用量的150%,丙酸钙的产率70.35%,用原子吸收光谱法测定产品的纯度为96%。
[1] 李涛,马美湖,蔡朝霞,等. 废弃鸡蛋壳中碳酸钙制取丙酸钙的工艺条件[J]. 环境化学,2010,29(3):508 -512.
[2] 李涛,马美湖,蔡朝霞. 蛋壳中碳酸钙转化为有机酸钙的研究[J]. 四川食品与发酵,2008,44(5):8 -12.
[3] 郝素娥,宁明华. 利用蛋壳制备丙酸钙的研究[J]. 化学研究与应用,1999,11(1):105 -107.
[4] 滕海英,祝国强,黄平,等. 正交试验设计实例分析[J].药学服务与研究,2008,8(1):75 -76.
[5] 陈雪,孙超,赵玉娥. 以蛋壳为原料用水热法制备丙酸钙的工艺研究[J]. 畜牧与饲料科学,2010,31(1):1-2.
[6] 李涛,马美湖,蔡朝霞,等. 鸡蛋壳中CaCO3制备C6H10O4Ca 的研究[J]. 食品工业,2009(5):48 -51.

