米糠中阿魏酸提取工艺的优化①
姜 帅,刘翠娟,慎爱民,张 磊,佟德成,宋琳琳,赵 岩,杨治伟,吕玉光
(佳木斯大学药学院生物药制剂黑龙江省重点实验室,黑龙江 佳木斯 154007)
0 引言
米糠是指稻谷脱壳后依附在糙米上的表面层,其由外果皮、中果皮、交联层、种皮和糊层组成,化学成分为糖类、脂肪、蛋白质、维生素和灰分.黑龙江是中国的米都,富产水稻,其占全国产量的三分之一.近年来,科学工作者在米糠深加工、副产品综合利用上取得了丰硕成果和收益.在米糠中的阿魏酸含量较高,对米糠中阿魏酸的提取分离研究具有较好的前景[1].
阿魏酸(Ferulic acid)的化学名称为4-轻基-3-甲氧基肉桂酸,其广泛存在于植物细胞壁中,多以酯的形式存在,与碳水化合物以共价键连接,游离态的阿魏酸含量很低[2].阿魏酸有顺式和反式两种,顺式为黄色油状体,反式为白色至微黄色结晶体.反式阿魏酸常作为一些药的活性化合物,被广泛应用于食品和药品行业中[3].研究表明阿魏酸是阿魏、川芎、当归、升麻、木贼等多种中药的有效成分之一.随着对阿魏酸广泛深入地研究,发现阿魏酸及其衍生物具有多方面的生物活性,如抗血小板聚集、促进血小板解聚、降血脂、抗血栓、抗氧化、抗自由基、抗炎、抗肿瘤抗突变、增强免疫功能以及增强人体精子活力和运动性等,且毒性很低,激起有关学者的兴趣[4].
近些年,超声强化提取法已被广泛应用于各个领域,特别是医药行业的中药提取中[5].本试验将这一技术应用于阿魏酸的提取,优化提取条件以期获得较高产率和纯度的阿魏酸,为今后产业化提供理论依据.
1 仪器与试剂
1.1 仪 器
VERTEX70傅里叶红外光谱仪(德国布鲁克公司);SHB-III循环水式多用真空泵(郑州长城科工贸有限公司);DT-LNS集热式恒温加热磁力搅拌器(河南省予华仪器有限公司);KQ-500DE型数控超声波清洗器(昆山市超声仪器有限公司);BS110型电子天平(北京赛多利斯天平有限公司);PHS-3C精密pH计(上海雷磁创益仪器代表有限公司);UV757CRT紫外可见分光光度计(上海精密科学仪器有限公司);101-1电热鼓风干燥箱(上海实验仪器有限公司);DZG-6050真空干燥箱(上海森信实验仪器有限公司);UV757CRT紫外可见分光光度计(上海精密科学仪器有限公司).
1.2 实验试剂
新鲜米糠(庆安鑫利达米业公司),阿魏酸(标准品贵州迪大科技有限责任公司)正己烷(分析纯天津市凯通化学制剂有限公司),乙醚(分析纯天津市北方天医化学试剂厂),石油醚(90-120℃)(分析纯哈尔滨市新达化工厂),无水乙醇(分析纯天津市凯通化学制剂有限公司),乙酸乙酯(分析纯哈尔滨市新达化工厂),氢氧化钠(分析纯天津市北方天医化学试剂厂),无水碳酸钠(分析纯齐齐哈尔轻工学院试剂厂),亚硫酸钠(分析纯天津市凯通化学制剂有限公司),蒸馏水(分析纯佳木斯市化学试剂厂),盐酸(分析纯佳木斯市化学试剂厂).
2 实验方法
(1)将500g新鲜米糠置于烘箱中,在105℃下活化20min,冷却后用正己烷(l:3,w/v)浸泡5h脱脂2次,再于真空干燥箱中干燥5h.
(2)提取法①:参照文献[6],分别量取3份各40g预处理后的米糠放入置于集热式恒温加热磁力搅拌器中的1000ml圆底烧瓶中,以1:8(w/v)的比例分别各加入1%氢氧化钠-乙醇(4:1,v/v)、0.2g/L的亚硫酸钠,各在80℃下加热回流6h,挤压过滤,浓盐酸调pH值为1左右,抽滤,减压蒸馏出乙醇,各取10mL上清液,3000r/min离心分离3min,上清液置于分液漏斗中,分别用乙酸乙酯萃取三次,每次10mL,合并萃取液,2%碳酸钠萃取三次,每次10mL,分别合并碱液,乙醚洗涤碱液至澄清,弃去乙醚,碱液加浓盐酸调pH=1左右.减压蒸馏出乙酸乙酯,残渣溶于10mL乙醇,精密量取0.1mL,乙醇定容至 10mL.所得三个样品分别标注为A1,A2,A3.剩余液回流蒸出乙醇精制提纯.
(3)提取法②:另外分别量取3份40g预处理后的米糠放入置于超声波清洗器中的1000ml圆底烧瓶中,以1:8(w/v)的比例分别各加入1%氢氧化钠 - 乙醇(4:1,v/v)、0.2g/L的亚硫酸钠,各在80℃下加热回流4h,挤压过滤,浓盐酸调pH值为1左右,抽滤,减压蒸馏出乙醇,各取10mL上清液,3000r/min离心分离3min,上清液置于分液漏斗中,分别用乙酸乙酯萃取三次,每次10mL,合并萃取液,2%碳酸钠萃取三次,每次10mL,分别合并碱液,乙醚洗涤碱液至澄清,弃去乙醚,碱液加浓盐酸调pH=1左右.减压蒸馏出乙酸乙酯.残渣溶于10mL乙醇,精密量取0.1mL,乙醇定容至10mL.所得三个样品分别标注为 B1,B2,B3.剩余液回流蒸出乙醇精制提纯.
(4)采用VERTEX 70型傅里叶红外光谱仪对产物结构表征,KCr压片,扫描范围4000 cm-1~400 cm-1.
(5)核磁共振波谱的测定和解析
将样品阿魏酸溶解于DMSO-d6中,以TMS为内标测试其1H-NMR和13C-NMR谱图,并进行解析.结构式为:
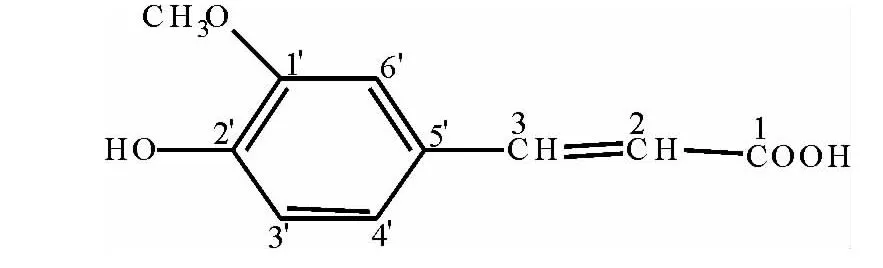
图1
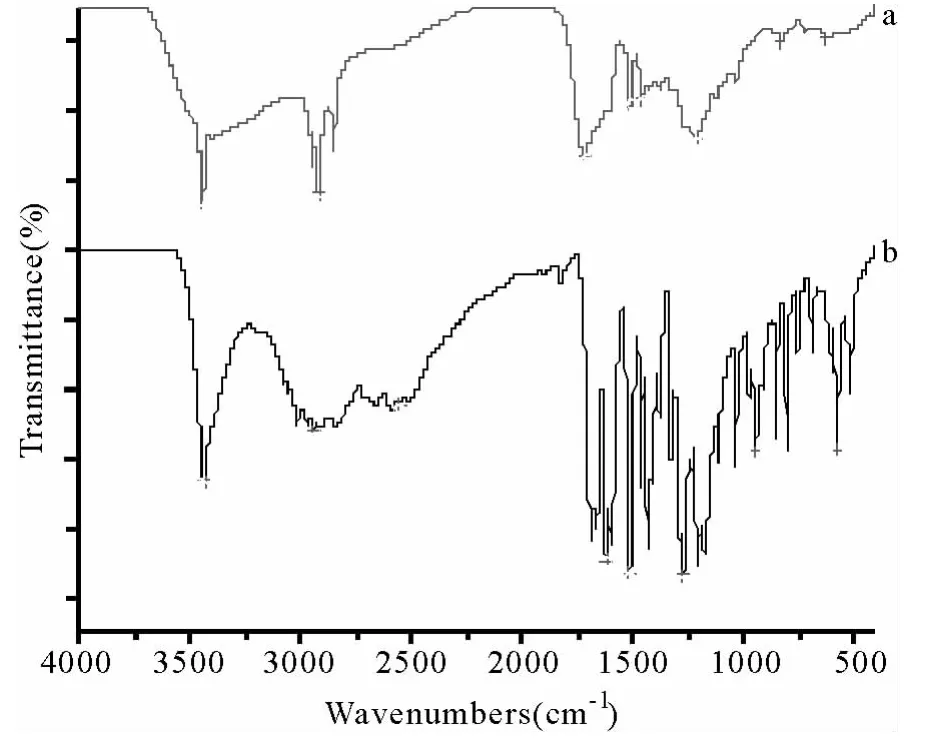
图2 阿魏酸标准品与提取法①的红外光谱

图3 阿魏酸标准品与提取法②的红外光谱
仪器 Bruker AVANCE-400MHz超导核磁共振波谱仪;样品 超声强化提取精制真空烘干后的阿魏酸;溶剂 氘代二甲基亚砜DMSO-d6(含0.1%内标物TMS);试样的制备:将超声强化提取精制真空烘干后的样品阿魏酸约5mg溶解在0.5ml DMSO-d6溶剂中制成溶液,装于5mm样品管中待测定.
(6)采用紫外分光光度法进行阿魏酸含量的测定.
3 结果分析
3.1 样品的红外表征分析
提取法①样品的红外光谱与阿魏酸标准品的红外光谱基本一致.由图1可见:3444cm-1,示有羟基;2920cm-1,示有甲氧基;1718cm-1,示有羧基存在;1463cm-1,834cm-1,为芳环特征吸收;1211cm-1,示有酚的结构存在.

图4 阿魏酸的1H-NMR谱
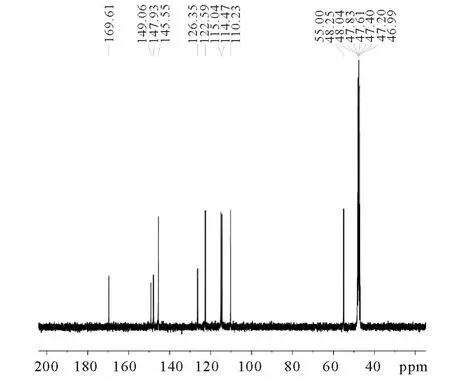
图5 阿魏酸的13C-NMR谱
提取法②样品的红外光谱与阿魏酸标准品的红外光谱基本一致.由图2可见:3399cm-1,示有羟基结构;2920cm-1,示有甲氧基结构;1718cm-1,示有羧基存在;1515cm-1,1429cm-1,为芳环特征吸收;1211cm-1,示有酚的结构存在.
3.2 核磁共振谱图解析
3.2.1 阿魏酸1H-NMR的解析
阿魏酸的1H-NMR谱见图3,其相关数据及归属列于表1.
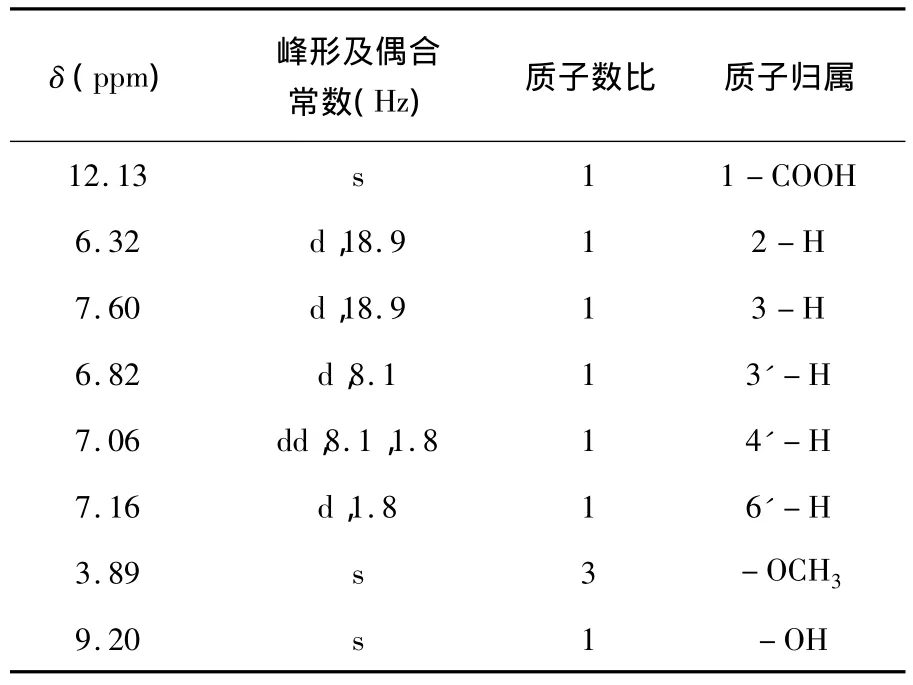
表1 阿魏酸的1H-NMR数据
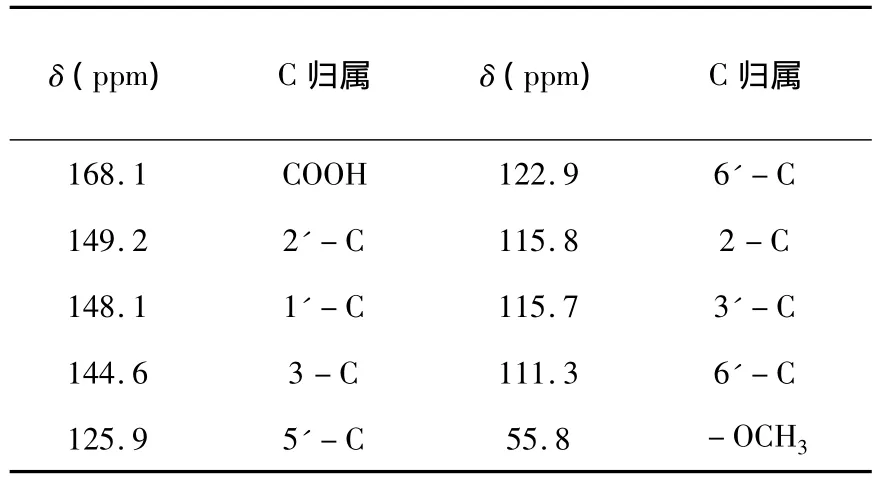
表2 阿魏酸的13C-NMR数据
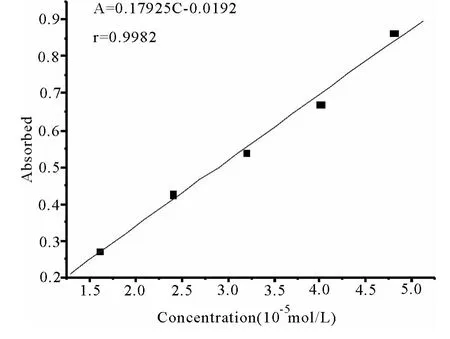
图6 阿魏酸标准曲线
阿魏酸分子中存在三个独立的自旋系统,各部分之间可以认为不存在偶合作用.甲氧基呈现单峰,不和任何氢发生偶合关系.各氢的化学位移见表1,2-H和3-H的化学位移值相差较大,是因为这两个烯氢处于苯环和羰基的大共轭系统中,2-H处于负电区,而3-H处于正电区,同时3-H也处于苯环的去屏蔽区.-COOH和-OH两个活泼氢的化学位移分别为12.13和9.56ppm,这和测定条件例如温度、浓度以及所用溶剂等有关.
3.2.2 阿魏酸的13C-NMR的解析:
阿魏酸的13C-NMR谱见图4,其相关数据及归属列于表2.
阿魏酸的碳信号可以为三组:第一组δ 168.1为α,β-不饱和酸的基碳信号.在常见官能团中,羰基的碳原子由于共振位置在最低场,因为很易被识别.羰基的碳原子共振之所以在最低场,从共振式可以看出羰基的碳原子缺少电子,故共振在最低场.如羰基与杂原子或不饱和基团相连,羰基的碳原子的电子短缺得以缓解,因此共振移向高场方向.由于上述原因酮、醛共振位置在最低场,一般δ>195ppm,酰氯、酰胺、酯、酸酐等相对酮、醛共振位置明显地移向高场方向,一般δ<185ppm.α,β-不饱和酮、醛的δ也减少,但不饱和键的高场位移作用较杂原子弱.第二组 δ 111.3~ δ 149.2为烯碳和苯环上的碳信号.取代烯烃的碳信号一般为100~150ppm.苯环的δ值的因素很多,如取代基电负性、重原子效应、中介效应和电场效应等.第三组δ 55.8为连氧碳信号.连氧碳信号的化学位移值一般在50~90ppm.
3.3 阿魏酸含量的测定
采用紫外分光光度法测定测定两类样品中阿魏酸的百分含量,来说明工艺优化的效果.
(1)配制五个不同浓度的100mL的阿魏酸标准品溶液,溶剂为乙醇.根据中国药典2005年版第一部可查阿魏酸最大吸收波长为323nm处,分别测得其吸光度A值见表3.作出阿魏酸的标准曲线如图5.根据线性回归方程为A=0.17925 C -0.0192得出阿魏酸的吸光系数为E=0.17925(r=0.9982).(2)取上述实验方法①提取的阿魏酸样品A1,A2,A3分别各精取1mL乙醇定容为100mL的待测液.测得其紫外吸光度值分别为 0.393,0.385,0.397.其吸光度平均值A=0.391.根据朗伯比尔定律A=ECL可以求得待测液的浓度,进而求得①提取法所得阿魏酸的含量为87.1%.同理,取上述实验方法②提取的阿魏酸样品 B1,B2,B3分别各精取1mL乙醇定容为100mL的待测液.测得其紫外吸光度值分别为 0.419,0.416,0.420.其吸光度平均值A=0.418.进而求得②提取法所得阿魏酸的含量为92.3%.

表3 不同浓度的阿魏酸在乙醇溶剂中的吸光度值
采用超声强化提取法提取米糠中阿魏酸,收率提高5.2%.
4 结论
采用超声强化提取的方法,对米糠中提取反式阿魏酸的工艺条件进行优化处理,所得样品的收率提高5.2%.
[1]张国升.从米糠中提取阿魏酸的研究[J].安徽中医学院学报,1997,16(6):56 -57.
[2]Rosazza,J P N,Z.Huang,L.Dostal,et al.Biocatalytic Transformations of Ferulic acil:An Abundant Aromatic Natural Product[J].Indust.Microbiol,1995,15:457 -467.
[3]欧仕益,包惠燕,篮志东.阿魏酸及其衍生物的药理作用研究进展[J].中药材,2001,24(3):220 -221.
[4]李全斌,何开勇,吴建萍.阿魏酸含量测定方法研究进展[J].中医药导报2011,17(3):117 -119.
[5]刘翠娟,杨治伟,慎爱民.超声化学的发展与应用[J].佳木斯大学学报(自然科学版).2005,23(2):273 -277.
[6]廖律,周明达,肖劲,等.米糠中阿魏酸的提取及高效液相色谱法测定[J].食品工业科技.2007,28(2):216 -219.

