白蛋白发酵液大孔树脂法脱色过程研究
李辰雨,战伟超,单守水,林 剑,徐世艾*
(1.烟台大学 化学化工学院,山东 烟台 264005;2.烟台大学 生命科学学院,山东 烟台 264005)
人血清白蛋白(human serum albumin,HAS)是临床应用较多的一种蛋白质,目前临床使用的人血清白蛋白大多来自人类血浆[1]。80年代以来,人们通过基因工程技术使人血清白蛋白在细菌等宿主中得到表达[2-5],其中,毕赤酵母表达系统应用最广,在白蛋白纯化方面,目前多采用超滤法、离子交换法[6]等方法。由于分离纯化过程中色素难以除去,为白蛋白分离纯化增加难度,对于发酵液中色素除去的基础理论方面的研究则鲜见报道。选用LS-305、LS-610B、SP-207、HP-20和DM-21五种大孔吸附树脂,进行树脂预选、静态吸附试验和动态吸附试验。研究了发酵液中的色素在大孔树脂上的静态吸附动力学和动态吸附动力学行为,讨论了发酵液中的色素在Langmuir方程和Freundlich方程拟合程度的热力学过程,一阶动力学模型、二阶动力学模型和粒子内扩散模型对静态吸附动力学过程的影响,及动态吸附过程的脱色率,并检测整个吸附过程的蛋白质的损失率,为树脂吸附法除去发酵液中的色素从而为从发酵液中分离纯化白蛋白的工程应用提供依据。
1 材料与方法
1.1 材料与试剂
毕赤氏酵母(Pichia pastoris):山东大学;8万u分子质量聚砜超滤膜:上海摩速科学器材有限公司;牛血清蛋白:北京索莱宝科技有限公司;LS-305树脂、LS-610B树脂:陕西蓝深特种树脂有限公司;SP-207、HP-20树脂:日本三菱化学公司;DM-21树脂:山东鲁抗立科药物化学有限公司;各树脂的物理结构参数见表1。
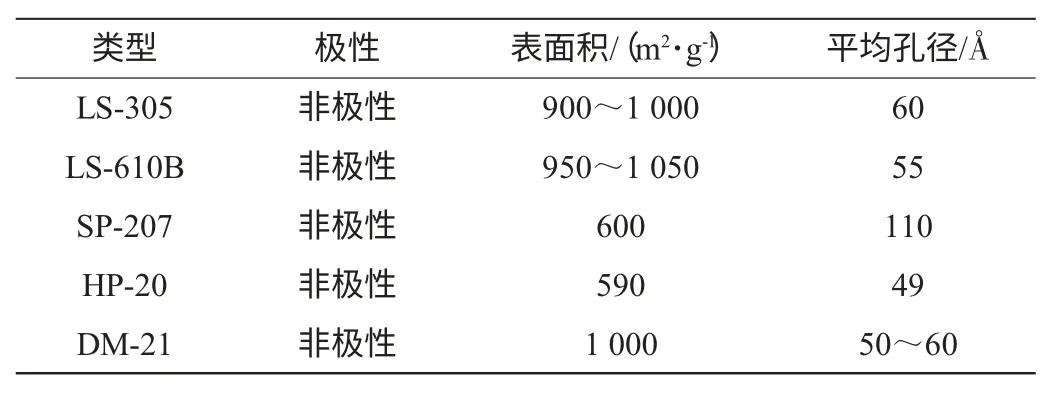
表1 树脂的物理结构参数Table 1 Physical structure parameters of resins
1.2 仪器与设备
YC-2层析实验冷柜:北京博医康实验仪器有限公司;RO-NF-VF-40实验室用膜分离设备:上海摩速科学器材有限公司;UV-5100紫外可见分光光度计:上海元析仪器有限公司;AR1530电子天平:奥豪斯仪器有限公司;SPH-2102B振荡培养器:上海智械仪器制造有限公司;Anke TDL-5-4台式离心机:上海安亭科学仪器厂。
1.3 实验方法
1.3.1 发酵液的预处理
首先将发酵液离心处理20 min,转速为5 000 r/min;然后将上清液超滤处理,将透过分子质量为8万u膜的液体作为树脂脱色的溶液。
1.3.2 树脂的预处理
首先将树脂用体积分数为95%的乙醇浸泡24 h,用去离子水洗几次;然后将树脂用1 mol/L氢氧化钠浸泡5 h,用蒸馏水洗至中性;随后将树脂用1 mol/L盐酸浸泡5 h;用蒸馏水洗至中性;最后用滤纸吸去树脂表面的水,将这种处理的树脂称为滤纸片干(filter paper dried,FPD)树脂。FPD树脂经过80 ℃恒温干燥12 h,树脂质量恒定时称为干树脂。研究全部使用FPD树脂的质量为基准,计算全部使用干树脂的质量为基准。
1.3.3 发酵液中色素特征吸收波长的测定
首先将发酵液稀释10倍,然后将稀释后的发酵液在350~900 nm波长范围内进行扫描,确定发酵液中色素的特征吸收波长λt。
1.3.4 蛋白质含量的测定
用考马斯亮蓝法作为蛋白质含量的测定方法。牛血清蛋白标准曲线的制备见参考文献[7]。以牛血清蛋白质含量(x)为横坐标,吸光度值(y)为纵坐标得标准曲线方程为:y=188.26x-1.647 3(R2=0.998 6),根据回归方程计算样品中蛋白质含量。
1.3.5 树脂的预选
预先称取5 种FPD 树 脂LS-610B、LS-305、SP-207、HP-20、DM-21(5.35 g、5.45 g、4.85 g、4.35 g、4.27 g)(相当于1 g干树脂)分别加入到具塞锥形瓶(300 mL)中,并加入初始浓度(以吸光度值计)相同(1.704)发酵液到锥形瓶中各100 mL,然后放入到振荡培养器(20 ℃、220 r/min)进行吸附8 h,用紫外分光光度计测定发酵液中色素的吸光度值,并测定蛋白质的吸光度值(在595 nm波长条件下测定),评估其色素脱色率和蛋白质损失率。色素脱色率和蛋白质损失率计算公式如下:
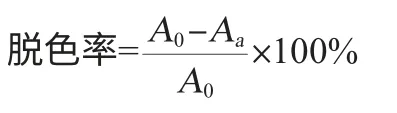
式中:A0是发酵液脱色前的吸光度值;Aa发酵液脱色后的吸光度值。
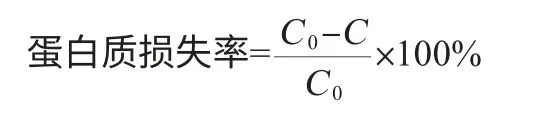
式中:C0、C分别为脱色前后蛋白质含量,μg。
1.3.6 不同pH值对吸附性能的试验
预先称取2 种FPD 树 脂LS-610B、LS-305(5.35 g、5.45 g),分别加入到具塞锥形瓶(300 mL)中,并加入100 mL不同pH值(2.0、4.0、6.0、8.0、10.0)初始浓度(0.276)相同的发酵液,然后放入到振荡培养器(20 ℃、220 r/min)进行吸附8 h,用紫外分光光度计测定发酵液中色素的吸光度值,并测定蛋白质的吸光度值,评估其色素脱色率和蛋白质损失率。
1.3.7 静态吸附等温线试验
预先称取2 种FPD 树 脂LS-610B、LS-305(5.35 g、5.54 g),分别取pH值为6.0不同初始浓度(0.732、1.303、1.643、1.911、2.201)的发酵液100 mL加入到具塞锥形瓶(300 mL)中。然后将锥形瓶放入到振荡培养器(20 ℃、220 r/min)中,充分吸附8 h。用紫外分光光度法测吸光度值,并用以下公式计算色素吸附容量。
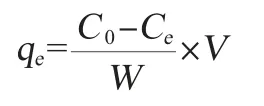
式中:qe是平衡时树脂的吸附容量,△AV/g;C0是料液初始浓度(以吸光度值计);Ce是料液平衡浓度(以吸光度值计);V是料液的体积,mL;W是干树脂质量,g。
1.3.8 静态吸附动力学试验
预先称取2 种FPD 树 脂LS-610B、LS-305(5.35 g、5.54 g),分别加入到具塞锥形瓶(300 mL)中,并加入pH值为6.0,初始浓度(1.704)相同发酵液各100 mL,然后将锥形瓶放入到振荡培养器(20 ℃、220 r/min)中,在不同时间取样,并用紫外分光光度法测定色素吸光度值,考马斯亮蓝法测定蛋白质含量,直至吸附平衡。树脂吸附容量按以下公式计算:
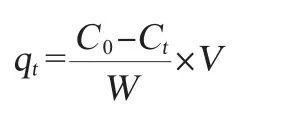
式中:qt是时间t树脂的吸附容量,△AV/g;C0是料液初始浓度(以吸光度值计);Ct是料液在时间t的浓度(以吸光度值计);V是料液的体积,mL;W是干树脂质量,g。
1.3.9 动态吸附试验
根据静态试验,树脂LS-610B被选择进行动态试验。动态吸附试验按以下方法:
预处理好的大孔树脂被装入到玻璃柱(20 cm×1.6 cm)中,为20 mL,然后用去离子水以3倍柱床体积(bed volumn,BV)洗脱大孔树脂。然后上样pH为6.0,用紫外分光光度计检测发酵液色素吸光度值和蛋白质含量。
2 结果与分析
2.1 最大吸收波长的确定
发酵液中色素在350~900 nm 波长范围内的扫描结果如图1所示,图1表明发酵液在波长380 nm处有特征吸收,故将波长380 nm作为测定发酵液中色素的吸光度的最佳波长。

图1 发酵液中色素紫外可见光吸收曲线Fig.1 UV absorption curve of pigment in the fermentation broth
2.2 树脂的预选
5种FPD树脂LS-610B、LS-305、SP-207、HP-20、DM-21吸附量及蛋白质损失率结果见表2。

表2 不同树脂的吸附性质Table 2 Adsorption properties of different resins
由表2可以看出,LS-610B树脂与LS-305树脂吸附容量相对高于另外3种树脂,且蛋白损失率相对较低,故选取LS-610B和LS-305作为发酵液静态吸附脱色树脂。
2.3 不同pH值对吸附性能的影响
不同pH值下LS-610B和LS-305树脂的吸附容量与蛋白质损失率,结果见表3。由表3可知,2种树脂pH 6.0时较其他pH值时,色素吸附效果好,蛋白损失率较低。故以LS-610B和LS-305树脂脱色时,发酵液pH 6.0为宜。
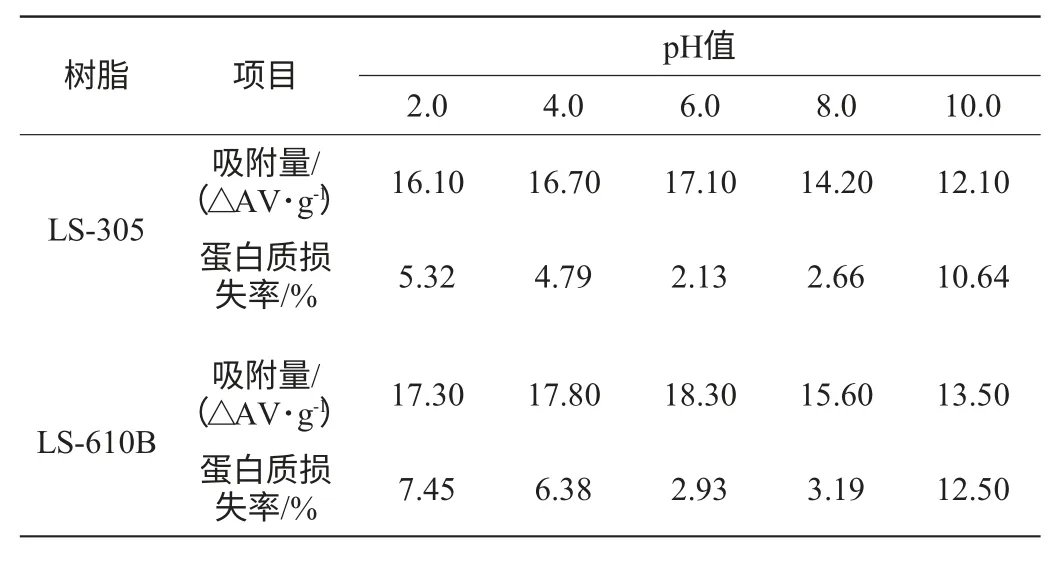
表3 不同pH值的大孔树脂吸附参数Table 3 Adsorption parameters of macroporous resins with different pH
2.4 静态吸附等温线
两种普遍的理论模型(Langmuir模型和Freundlich模型)被用来比较大孔树脂的等温吸附[8]。
Langmuir方程:
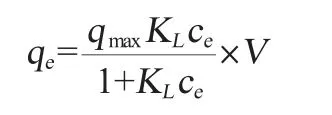
Freundlich模型:

式中:qe是平衡吸附量,△AV/g;qmax是最大吸附容量,△AV/g;ce是平衡时发酵液中色素浓度(以吸光度值计);KL是Langmuir常数;KF和n 是Freundlich常数。
图2表示两种树脂在20 ℃下发酵液中色素静态吸附等温线,Langmuir模型中的KL和qmax通过ce/qe和ce的线性关系拟合得到。Freundlich模型中的KF和n通过log(qe)和log(ce)的线性拟合得到。实验数据的统计处理及相关系数R2的值见表4。
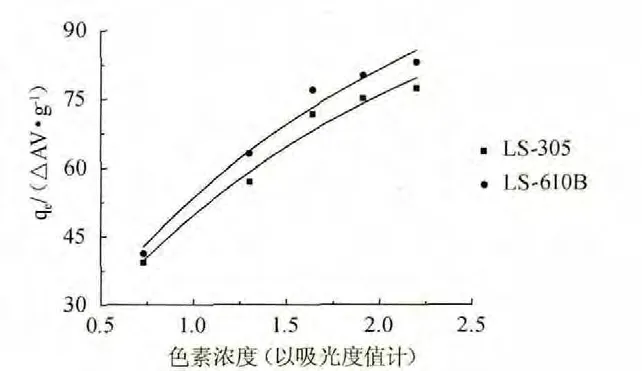
图2 两种树脂在20℃下对发酵液中色素的静态吸附等温线Fig.2 Static adsorption isotherms of pigment in the fermentation broth by two kinds of resins at 20℃
由表4可知,比较相关系数R2,实验数据较好符合Langmuir模型,比较最大吸附容量qmax(Langmuir模型)LS610B>LS305,原因可能是LS610B的比表面积大于LS305的比表面积。所以两种树脂的吸附等温线更符合Langmuir模型,LS610B的最大吸附量计算值为123.00△AV/g。

表4 在20℃下Langmuir和Freundlich吸附等温方程参数Table 4 The parameters of adsorption isothermal equation from Freundlich and Langmuir at 20℃
2.5 静态吸附动力学性质
LS305和LS610B两种树脂在20 ℃下吸附容量(qt)随时间(t)的变化趋势,结果见图3。由图3可以看出,在8 h之内LS305和LS610B两种树脂达到吸附平衡。LS610B吸附容量比LS305的吸附容量高10△AV/g左右,LS610B在吸附过程中蛋白质的损失率比LS305吸附过程中蛋白质的损失率高0.5%左右。
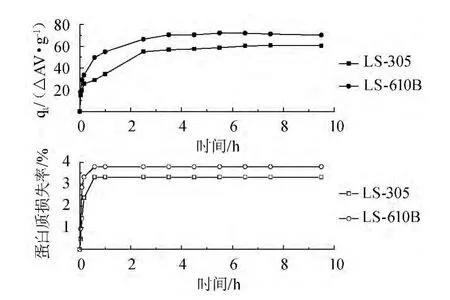
图3 两种树脂在20℃下对发酵液中色素的吸附动力学曲线及蛋白质损失率Fig.3 Kinetic curves of the pigment in the fermentation broth and the protein loss rate by two kinds of resins at 20℃
吸附容量与时间的数据按照一阶动力学模型[9]、二阶动力学模型[10]和颗粒内扩散模型[11]进行处理。
一阶动力学模型:

动力学参数计算结果见表5。由表5可知,从二阶动力学模型中的相关系数(R2)略高于一阶动力学模型中的相关系数(R2),而且二阶动力学模型qe的计算值比一阶动力学模型的计算值更接近与实验数据值。结果表明,发酵液中的色素在这两种树脂中的吸附动力学更好的符合二阶动力学模型,相似的结果已经被其他作者所报道[12-14]。
按照二阶动力学模型的速率常数k2,两种树脂的吸附速率大小为:LS610B>LS305。
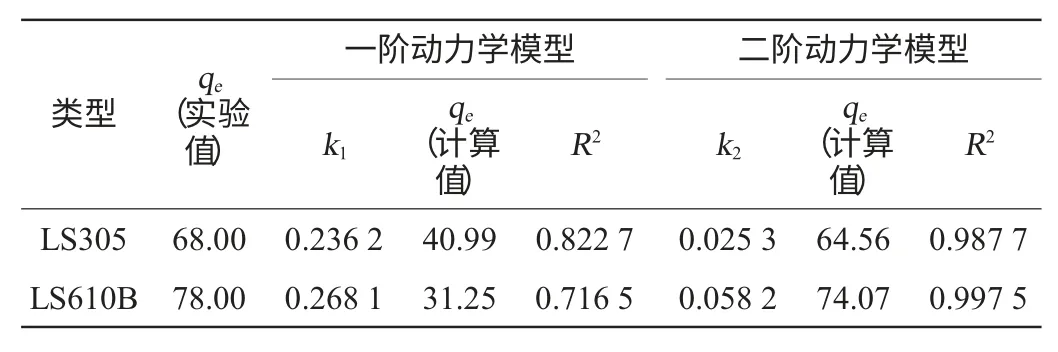
表5 在20℃下两种树脂动力学参数Table 5 Kinetic parameters from two resins at 20℃
一阶动力学模型和二阶动力学模型主要考虑粒子外膜扩散,内部扩散和吸附过程的相互作用。虽然粒子扩散动力学模型不能代表整个吸附过程,但可用来解释一定的吸附原理,且在吸附过程中会造成一定量的蛋白质损失,但损失率相对较低,故选取LS-610B作为发酵液动态吸附脱色树脂。
将吸附容量qt与时间t1/2进行拟合,结果见图4。由图4可知,颗粒内扩散是吸附速率的控制步骤,因为这条线如果经过原点,且为直线,说明该过程是单一的颗粒扩散速控步骤。由图4可知,颗粒扩散图形不经过原点,也不是直线,证明该过程不是唯一的颗粒扩散速控步骤,液膜扩散也在一定程度上影响吸附过程。吸附过程包括两个阶段,第一阶段(0~2.5 h)属于逐渐吸附阶段,颗粒扩散速率很小;第二阶段(2.5~8.0 h)被认为是最终的平衡吸附阶段。因此,颗粒扩散与液膜扩散交互影响色素在LS305和LS610B树脂上的吸附[15-16]。
二阶动力学模型:

颗粒扩散动力学模型:
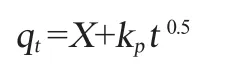
式中:qe和qt分别是平衡时的吸附容量和时间t的吸附容量,△AV/g;k1是一阶动力学模型的速率常数,h-1;k2是二阶动力学模型的速率常数,g/(△AV·h);kp是颗粒内扩散速率常数,△AV/(g·h1/2);X是常数。
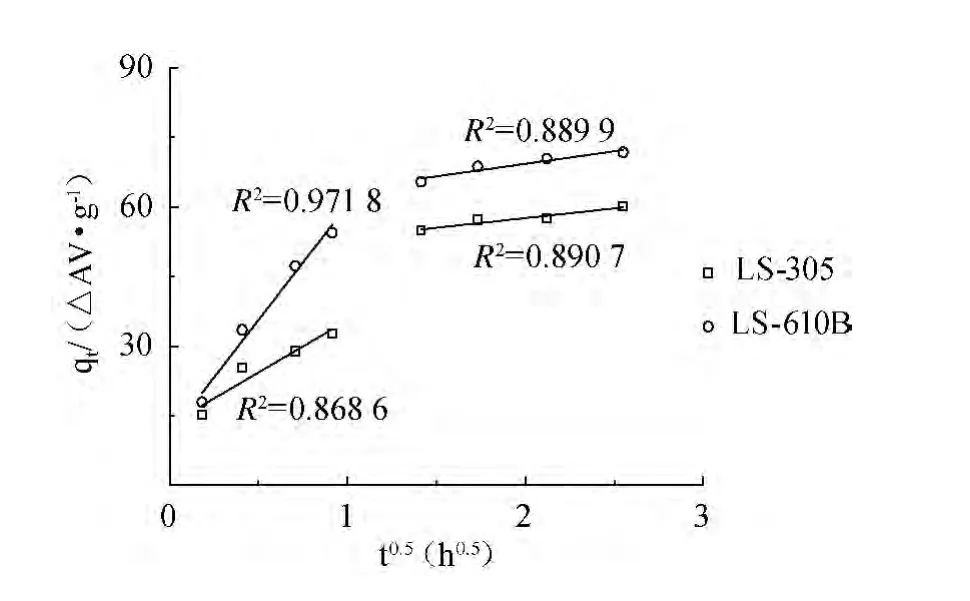
图4 两种树脂吸附发酵液中色素的颗粒扩散模型Fig.4 Particle diffusion model for adsorption of pigment in fermentation broth by two resins
2.6 动态吸附试验
由图5可以看出,4 BV/h的流速脱色率(进料10 BV时约为68%)小于2 BV/h的脱色率(进料10 BV时约为81.5%),原因可能是吸附物质没有足够的时间与发酵液中色素进行相互作用[17]。两种流速的蛋白质损失率相对较低(进料4 BV时蛋白质损失率约为1%)。故LS-610B可以用于发酵液分离白蛋白的脱色预处理。

图5 不同流速的脱色率及蛋白质损失率Fig.5 Decolourization ratio and protein loss rate at different flow rates
3 结论
通过预选5种大孔树脂LS-305、LS-610B、SP-207、HP-20和DM-21,得到大孔树脂LS305和LS610B吸附容量较大且蛋白损失率较低。又在不同pH值下对大孔树脂LS305和LS610B进行静态吸附试验,得出发酵液在pH=6.0下脱色为宜。静态吸附等温线试验表明,试验数据在Langmuir 吸附等温线模型有较高的相关系数,静态吸附试验表明,试验数据在二阶动力学模型有较高的相关系数。颗粒内扩散模型能较好的描述发酵液中色素在这两种树脂上的吸附动力学,说明颗粒内扩散不是唯一的控制步骤,吸附速率还受液膜扩散的影响。最后对大孔树脂LS610B进行动态吸附试验,试验表明,在上柱液pH值为6.0,流速2 BV/h,进料体积10 BV条件下,发酵液脱色率约81.5%,蛋白质损失率约3%。因此,大孔树脂LS610B可以用于白蛋白发酵液脱色处理。
[1]VERMEULEN J N,MEIJER D K,OVER J,et al.A phase I/IIa study with succinylated human serum albumin (Suc-HSA),a candidate HIV-1fusion inhibitor[J].Antivir Ther,2007,12(2):273-278.
[2]LAWN R M,ADELMAN J,BOCK S C,et al.The sequence of human serum albumin cDNA and its expression inE.coli[J].Nucleic Acids Res,1981,22(9):6103-6114.
[3]QUIRK A V,GEISOW M J,WOODROW J R,et al.Production of recombinant human serum albumin fromSaccharomyces cerevisiae[J].Biotechnol Appl Biochem,1989,11(3):273-287.
[4]张必武,邬小兵,乐国伟,等.人血清白蛋白基因工程研究进展[J].生物技术,2002,12(1):28-29.
[5]杨 喆,刘红岩,马 波,等.重组人血清白蛋白在汉逊酵母中的高密度发酵表达[J].云南大学学报:自然科学版,2007,29(S1):446-450.
[6]朱家文,武 斌,陈 葵,等.离子交换层析分离纯化重组人血清白蛋白[J].华东理工大学报:自然科学版,2002,28(4):341-345.
[7]冯 昕,王吉中,尧俊英,等.考马斯亮蓝法测定乳与乳制品中蛋白质含量[J].粮食与食品工业,2010,17(3):57-59.
[8]DI M A,ARENA E,FALLICO B,et al.Recovery of anthocyanins from pulp wash of pigmented oranges by concentration on resins[J].J Agr Food Chem,2002,50(21):5968-5974.
[9]CHANG X L,WANG D,CHEN B Y,et al.Adsorption and desorption properties of macroporous resins for anthocyanins from the calyx extract of roselle (Hibiscus sabdariffaL.)[J].J Agr Food Chem,2012,60(9):2368-2376.
[10]HO Y S,MCKAY G.Pseudo-second order model for sorption processes[J].Process Biochem,1999,34(5):451-465.
[11]GUIBAL E,MILOT C,TOBIN J M.Metal-anion sorption by chitosan beads:equilibrium and kinetic studies[J].Ind Eng Chem Res,1998,37(4):1454-1463.
[12]ZHOU C C,YAN J,CAO Z N,et al.Postcrosslinking of macroporous styrene-divinylbenzene copolymers via pendant vinyl groups:Effect of the starting copolymers on the pore structure of the postcrosslinked products[J].J Appl Poly Sci,2002,83(8):1668-1677.
[13]LIN L,ZHAO H,DONG Y,et al.Macroporous resin purification behavior of phenolics and rosmarinic acid fromRabdosia serra(Maxim.)hara leaf[J].Food Chem,2012,130(2):417-424.
[14]WAWRZKIEWICZ M,HUBICKI Z.Equilibrium and kinetic studies on the sorption of acidic dye by macroporous anion exchanger[J].Chem Eng J,2010,157(1):29-34.
[15]LORENC-GRABOWSKA E,GRYGLEWICZ G.Adsorption of lignitederived humic acids on coal-based mesoporous activated carbons[J].J Colloid Interface Sci,2005,284(2):416-423.
[16]胡洋叶,王玉蓉,韩振蕴.大孔树脂吸附知母总皂苷的动力学与热力学研究[J].中医药信息,2011,28(5):36-39.
[17]MA C Y,TAO G J,TANG J,et al.Preparative separation and purification of rosavin inRhodiola roseaby macroporous adsorption resins[J].Sep Purif Technol,2009,69(1):22-28.

