甲烷在活性炭上的吸附平衡研究
朱子文,郑青榕,冯玉龙,曾斌
(集美大学轮机工程学院福建省船舶与海洋工程重点实验室,福建厦门361021)
甲烷在活性炭上的吸附平衡研究
朱子文,郑青榕*,冯玉龙,曾斌
(集美大学轮机工程学院福建省船舶与海洋工程重点实验室,福建厦门361021)
以吸附式天然气(ANG)的工程应用为目的,展开甲烷在活性炭上吸附平衡研究。首先,在温度区间-10℃~40℃、压力范围0~8MPa,测试甲烷在比表面积为1916m2/g SAC-02活性炭上的吸附平衡数据,并在不同压力区域比较DA方程、Toth方程和Ono-Kondo方程的预测精度。其次,选用Clausius-Clapeyron方程,分别通过过剩吸附量和绝对吸附量的等量线标绘以及DA方程计算甲烷在活性炭上的等量吸附热。结果表明,平衡压力高于1MPa时,Toth方程和DA方程预测结果累计误差的平均值分别为0.3%和0.5%;过剩吸附量和绝对吸附量标绘、DA方程确定的等量吸附热为17.31kJ/mol~20.24kJ/mol、16.49kJ/mol~18.81kJ/mol、15.29kJ/mol~21.58kJ/mol,但DA方程计算值随温度变化。ANG工程应用可选择Toth方程和DA方程用于模型分析和等量吸附热计算。
吸附式天然气(ANG);活性炭;吸附模型;吸附热
在吸附式天然气(ANG)技术研发中,实验室一般通过静态容积法测定甲烷在吸附剂上的吸附等温线来评价其对天然气的吸附容量。试验测定的为甲烷在吸附剂上的过剩吸附量,而更具有工程应用意义的为绝对吸附量,过剩吸附量与绝对吸附量之间的换算极为关键。此外,ANG储存系统容量及其循环性能受充放气过程热效应的影响明显,准确确定甲烷在吸附剂上的等量吸附热为优化热效应管理措施的另一重要方面[1,2]。
甲烷在常温下处于超临界区域,其在ANG工程应用范围内的吸附相不可能为液相,过剩吸附等温线在一定的平衡压力下出现最大点,并呈现出微孔内单分子层吸附的特点,无法直接运用描述吸附质在亚临界温度区域的吸附平衡模型[3-6]。将超临界温度气体的吸附相态作准液态或者过热液体近似后,根据Gibbs关于吸附的定义,可由过剩吸附量计算绝对吸附量,但对吸附相态所作的假设具有局限性[5-8]。相对而言,源于Langmuir单层吸附理论的Toth等半经验方程,可不预先对吸附相态作假设,通过实验数据拟合方程参数后,就可较高精度地预测绝对吸附量[8-10]。在计算甲烷在活性炭上的等量吸附热时,普遍采用Clausius-Clapeyron方程并由等量吸附线标绘确定,但标绘确定的吸附热往往基于理想气体、吸附相为液相且等量吸附热不随温度变化的假设,吸附平衡数据跨越较大温度区间的标绘结果具有不确定性[11]。
针对上述问题,本研究依据ANG储存条件范围内测定的甲烷在活性炭上的吸附平衡数据,分析DA方程、Toth方程、格子理论Ono-Kondo方程预测甲烷在活性炭上吸附平衡的适用性,比较由过剩吸附量与绝对吸附量标绘以及由吸附模型确定的甲烷在活性炭上的等量吸附热。
1 试验
试验选用福建宁德鑫森炭业公司提供的椰壳活性炭SAC-02。由Micromeritics ASAP2020M全自动吸附仪于液氩浴中测定吸附等温线,运用BJH法及Horvath-Kawazoe法计算确定的孔大小及分布(PSD)和BET法标绘确定的比表面积结果见图1和表1。

表1 SAC-02活性炭结构参数
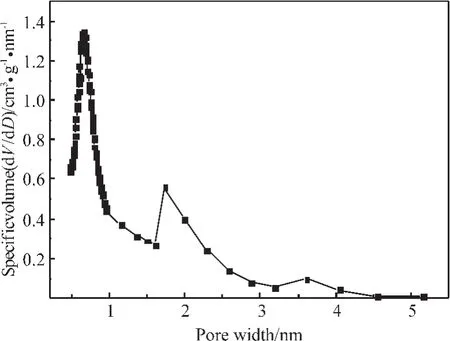
图1 87K液氩确定SAC-02活性炭孔大小及分布(PSD)
甲烷在活性炭上的吸附平衡数据由法国Seteram Pro-E&E高压气体吸附仪测得,其中平衡时过剩吸附量的大小由该仪器自动计算所得。考虑到工程应用时ANG的存储环境为常温中压(-10℃~40℃、5MPa左右)[12],本次测试的温度和压力范围分别选择为-10℃~40℃(间隔10℃)、0~8MPa。SAC-02活性炭试样的测试量为0.4323g,试样在装载入吸附池前须在真空干燥箱内、150℃下真空干燥24h。测试用气体均为厦门林德气体公司提供的高纯气体,其中φ(CH4)>99.999%。测试结果如图2所示,更多实验信息可参阅文献[13]。从图2可看出,过剩吸附等温线体现了超临界温度气体的吸附特征,在较高温度区域属于Ⅰ型等温线;温度较低时,则呈现出最大点。
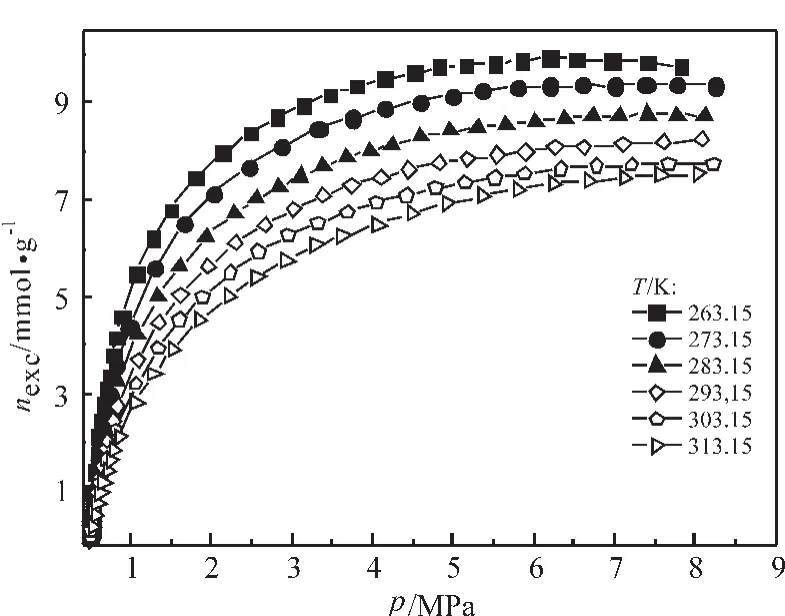
图2 甲烷在SAC-02活性炭上的过剩吸附等温线
2 吸附平衡模型
根据Gibbs关于吸附的定义,有如下关系式:

式中,nexc为过剩吸附量;nabs为绝对吸附量;Va为吸附相体积;ρg为气体的气相密度。甲烷的气相密度由8参数BWR方程确定[14]。从式(1)可得:

式中,ρa为吸附相密度。
2.1 DA方程
考虑到活性炭具有能量不均匀表面,选用含有吸附相比容修正项的DA方程[15]:
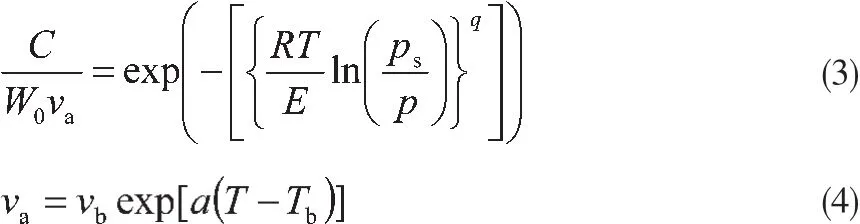
式中:C为甲烷在SAC活性炭上吸附的总量;W0为甲烷在样品上饱和吸附相体积;E为甲烷在活性炭上的特征吸附能;q为反映吸附剂表面能量不均匀性的指数;va为吸附相比容;a为吸附相膨胀系数;Tb为101.325kPa下甲烷所对应的沸点温度,又被称为泡点温度;vb为泡点温度下甲烷的比容。ps为甲烷的饱和蒸汽压,采用Dubinin推荐的公式计算[5]:

W0、E、q通过测试数据的非线性拟合确定,结果见表2。

表2 DA方程参数拟合值
2.2 Toth方程
Toth方程表达式为:

式中:n0为吸附质在吸附剂上的饱和吸附量;f为与平衡压力对应的逸度,对于实验范围内的甲烷逸度f采用SRK方程计算[14];t为反映吸附剂表面能量不均匀性的系数[15]。将式(6)代入式(2),得:
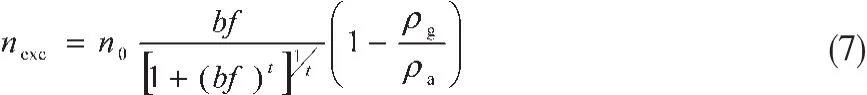
n0、b、t、ρa通过Matlab对吸附平衡数据非线性拟合确定,结果见表3。
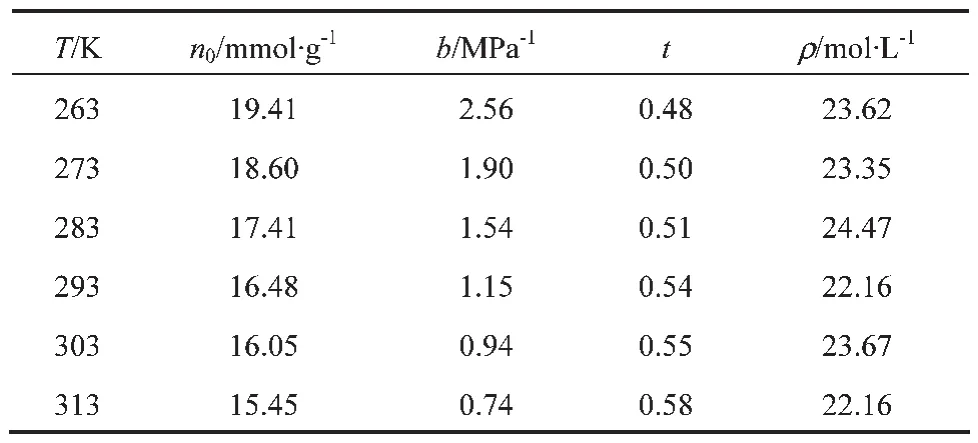
表3 Toth方程参数拟合值
2.3 格子理论Ono-Kondo方程
基于Ono和Kondo发展的格子理论,通过作边界势场的平均近似,在推导出描述气体吸附平衡Ono-Kondo方程的基础上,忽略吸附质分子间的作用,同时考虑到吸附空间的对称性(x1=xN),依据Gibbs关于吸附的定义,可得过剩吸附量与Ono-Kondo方程的关系式[16]:
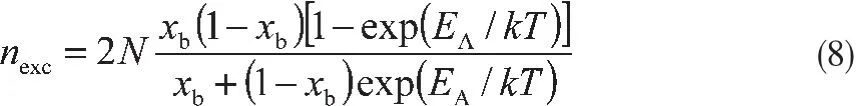

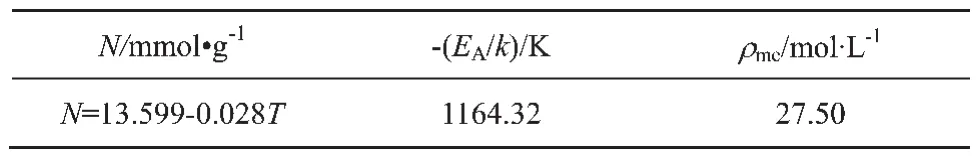
表4 Ono-Kondo方程参数拟合值
2.4 误差分析
累积误差可由下式计算:
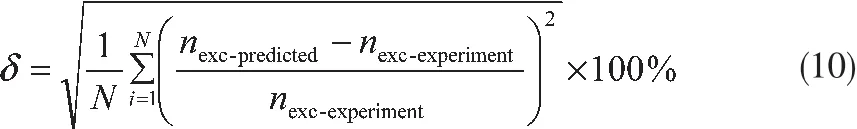
式中:nexc-predicted为过剩吸附量预测值;nexc-experiment为过剩吸附量实验值。累积误差如图4所示,在测试范围内,DA方程、Toth方程以及Ono-Kondo方程的累计误差平均值分别为4.5%、1.6%和21%;平衡压力大于1MPa时,DA方程、Toth方程以及Ono-Kondo方程的累计误差平均值分别为0.5%、0.3%和3.01%。显然,Toth方程在整个试验范围内具有最高的预测精度,DA方程在压力大于1MPa区域的预测精度与Toth方程相近。
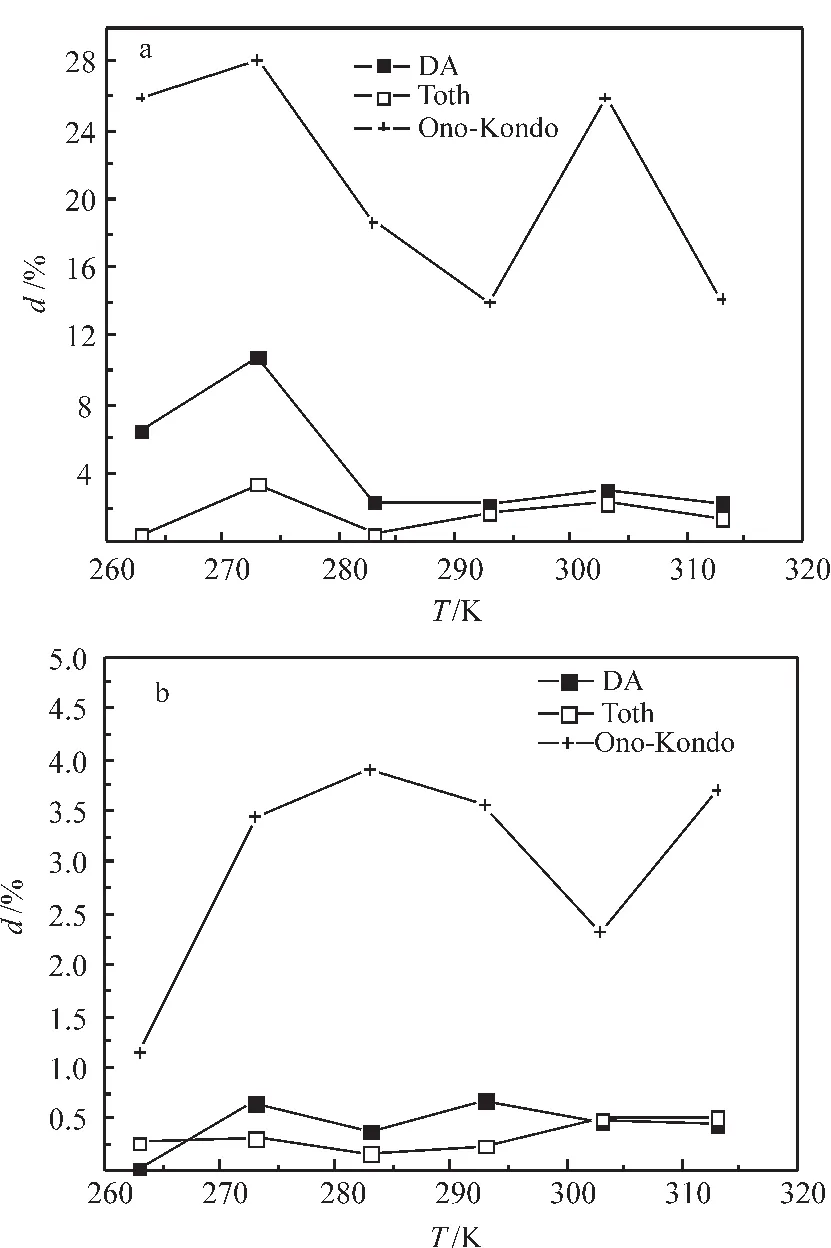
图3 模型预测甲烷在SAC-02活性炭上不同压力区域吸附平衡数据的累积误差
3 等量吸附热
根据文献[19],忽略固体表面在吸附过程中的能量变化,将传热过程简化为气相变为吸附相的相变过程和吸附相附着于固体表面的放热过程,则有:
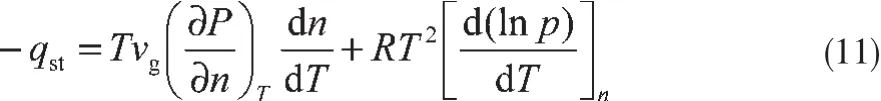
式中,qst为等量吸附热;式(11)等号左侧第一项代表气相状态,超临界温度区域的气体吸附可只考虑吸附相;vg为吸附质分子的气相比容;n为吸附质在单位质量吸附剂上的吸附量;第二项为Clausius-Clapeyron方程,等量吸附热也可由此项进行等量吸附线标绘确定。在实际状态下,应用与压力p对应的逸度以减少误差,则有:
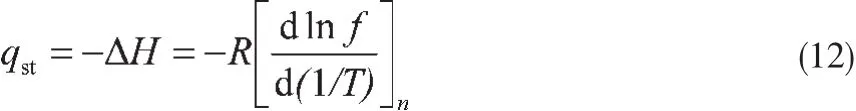
式中,ΔH为气相与吸附相的摩尔焓差;f为与平衡压力对应的逸度。在吸附量为0.5mmol/g~7mmol/g之间以0.5mmol/g为间隔取14个过剩(绝对)吸附量值,在不同吸附量下以ln f对1/T进行标绘,得到一组等量吸附线后由式(12)计算的等量吸附热如图4所示。从图4中可看出,由过剩吸附量确定的甲烷在SAC-02活性炭上的等量吸附热为17.31kJ/mol~20.24kJ/mol,平均值为17.93kJ/mol;由绝对吸附量确定的甲烷在SAC-02活性炭上的等量吸附热为16.49kJ/mol~18.81kJ/mol,平均值为17.09kJ/mol。极限吸附热应用不同温度时的亨利常数求得[20],结果如图5所示,其平均值约为21.28kJ/mol。
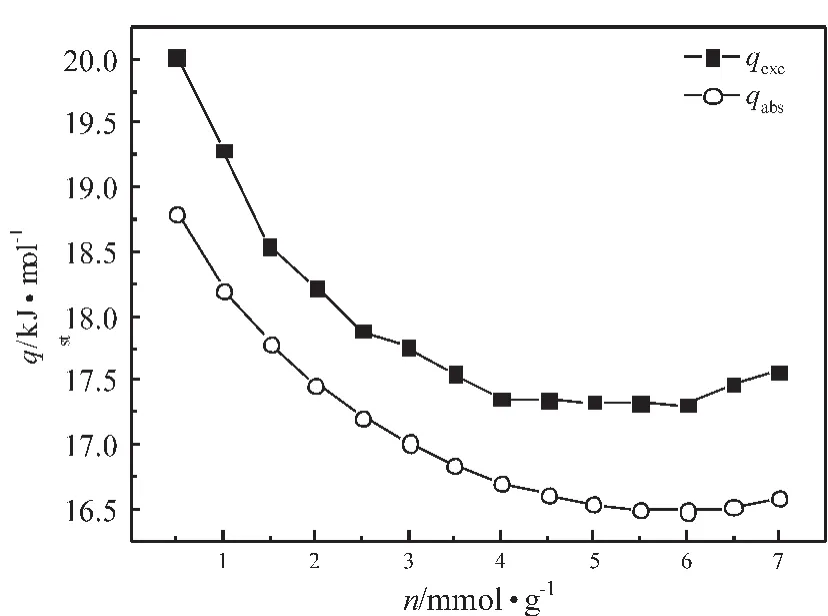
图4 甲烷在SAC-02活性炭上的等量吸附热
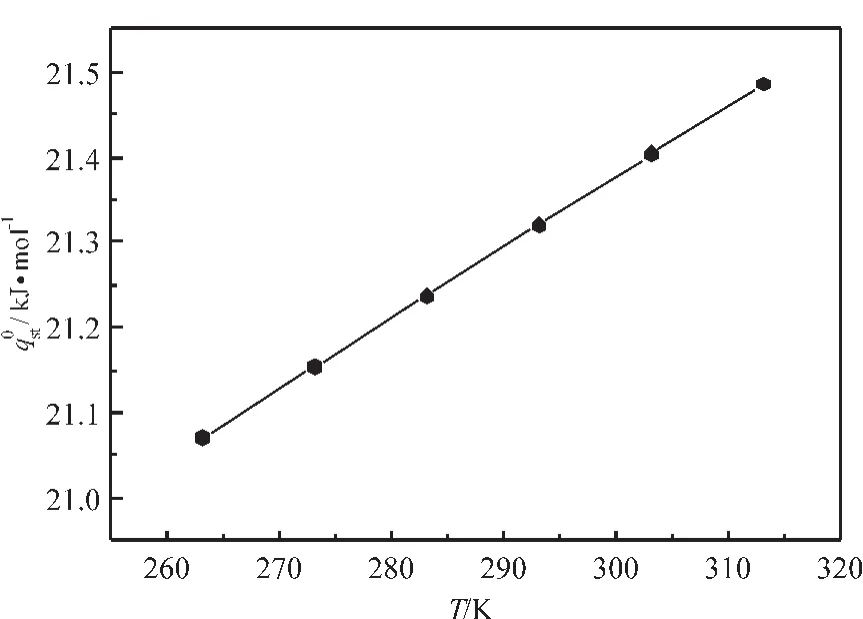
图5 甲烷在SAC-02活性炭上的极限吸附热

由式(13)计算得到吸附热随吸附量的变化曲线如图6所示,其中θ=C/C0。从图6中可发现,不同温度的等量吸附热是变化的,且随着温度的升高而升高;吸附热随着吸附量的增大先增大后减小,这一变化趋势与图4中过剩吸附量和绝对吸附量标绘得到的等量吸附热随吸附量变化趋势相似。测试范围内,等量吸附热约在15.29kJ/mol~21.58kJ/mol,最大值略大于图5所示的极限吸附热,这与DA方程在低压区域预测精度较低有关。考虑到具有工程应用背景的ANG系统处于较高压力范围,等量吸附热也可以由DA方程确定。
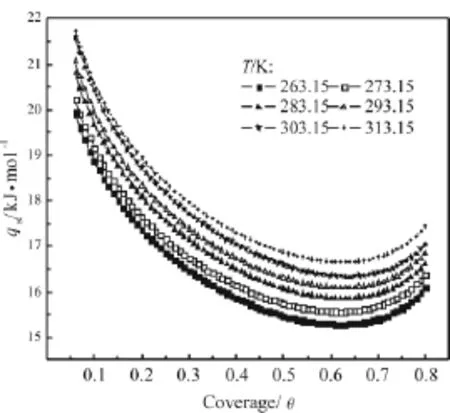
图6 DA方程计算确定的甲烷在SAC-02活性炭上的等量吸附热
4 结语
为选择适用于ANG工程应用的预测模型,基于甲烷在比表面积为1916m2/g活性炭上的吸附平衡数据,依据Gibbs关于吸附的定义,在不同平衡压力范围比较了DA方程、Toth方程、Ono-Kondo方程的预测精度,同时分别由过剩吸附量和绝对吸附量标绘和DA方程计算了甲烷在活性炭上的等量吸附热,得到如下结论:
(1)Toth方程适合于作为ANG工程应用的预测模型。在测试范围内,DA方程、Toth方程以及Ono-Kondo方程的累计误差平均值为4.51%、1.62%和21.04%;平衡压力大于1MPa时,DA方程、Toth方程以及Ono-Kondo方程的累计误差平均值为0.51%、0.34%和3.04%。
(2)三种方式确定的等量吸附热数值相近,但DA方程确定值反映了温度变化的影响。在试验范围内,由过剩吸附量和绝对吸附量标绘、DA方程确定的等量吸附热为17.31kJ/mol~20.24kJ/mol、16.49kJ/ mol~18.81kJ/mol、15.29kJ/mol~21.58kJ/mol。在ANG的存储条件下,DA方程和Toth方程预测精度相近,但DA方程确定的等量吸附热反映了随温度变化的特点,与ANG的实际工程应用更为接近。
[1]Rahman K A,Chakrabort y A,Saha B B.On thermodynamics of methane+carbonaceous materials adsorption[J].Int JHeat Mass Tran,2012,55(4):565-573.
[2]郑青榕,Birkett G,Do D D.甲烷在活性炭上吸附的实验及理论分析[J].天然气化工(C1化学与化工),2009, 34(1):41-45.
[3]周理,李明,周亚平.超临界甲烷在高比表面活性炭上的吸附测量及理论分析[J].中国科学(B辑),2000,30 (1):49-56.
[4]周理,吕昌忠,王怡林,等.述评超临界温度气体在多孔固体上的物理吸附[J].化学进展,1999,11(3):222-226.
[5]Dubinin M M.The Potential theory of adsorption of gases and vapors for adsorbents with energetically nonuniform surfaces[J].Chem Rev,1960,60(2):235-241.
[6]Ozawa S,Kusumi S,Ogino Y.Physical adsorption of gases at high pressure[J].JColloid.Interface Sci 1976, 56(1):83-91.
[7]李明,顾安忠,鲁雪生,汪荣顺.吸附势理论在甲烷临界温度以上吸附中的作用[J].天然气化工(C1化学与化工),2003,28(5):28-31.
[8]D D Do,Do H D.Adsorption of supercritical fluids in non-porous and porous carbons:Analysis of adsorbed phase volume and density[J].Carbon,2003,41(9):1777-1791.
[9]Li M,Gu A Z,Lu X S,et al.Determination of the adsorbate density from supercritical gas adsorption equilibrium data[J].Carbon,2003,41(3):585-588.
[10]高帅,郑青榕.甲烷在活性炭上吸附平衡模型的研究[J].燃料化学学报,2013,41(03):380-384.
[11]Nicholson D,Parsonage N G.Computer simulation and the statistical mechanics of adsorption[M].London: Academic Press,1982.
[12]Menon V C,Komarneni S.Porous adsorbents for vehicular natural gas storage:A review[J].JPorous Mater,1998,5 (1):43-58.
[13]解晨.甲烷在活性炭上的吸附平衡及充放气研究[D].集美大学,2012.
[14]童景山.流体热物性学:基本理论与计算[M].北京:中国石化出版社,2008:20-55.
[15]Do D D.Adsorption analysis:Equilibria and kinetics[M].Imperial College Press:London,1998.
[16]Benard P,Chahine R.Modeling of high-pressure adsorption isotherms above the critical temperature on microporous adsorbents:application to methane[J].Langmuir,1997,13(4):808-813.
[17]Aranovich G L,Donohue M D.Adsorption isotherms for microporous adsorbents[J].Carbon,1995,33(10):1369-1375.
[18]郑青榕,廖海峰,解晨,等.超临界甲烷在活性炭上的吸附平衡分析[J].燃料化学学报,2012,40(7):892-896.
[19]Chakraborty A,Saha B B,Koyama S.On the thermodynamic modeling of the isosteric heat of adsorption and comparison with experiments[J].Appl Phys Lett,2006,89(17):171901.
[20]Meeks O R,Rybolt T R.Correlations of adsorption energies with physical and structural properties of adsorbatemolecules[J].JColloid Interface Sci,1997,196 (1):103-109.
[21]Ragman K A,Loh W S,Yanagi H,et al.Experimental adsorption isotherm of methane onto activated carbon at sun-and supercritical temperatures[J].JChem Eng Data, 2010,55(11):4961-4967.
Adsorption equilibrium ofmethane on activated carbon
ZHU Zi-wen,ZHENGQing-rong,FENG Yu-long,ZEN Bin
(Provincial Key Laboratory of Naval Architecture and Ocean Engineering,Institute of Marine Engineering,JimeiUniversity,Xiamen 361021,China)
The adsorption equilibrium of methane on the activated carbon was studied for practical application of adsorbed natural gas(ANG)technology.Activated carbon SAC-02 was selected as an adsorbent,six isotherms of excess adsorption amount of methane weremeasured at temperature from-10℃to 40℃and pressure up to 8 MPa.Parameters of DA equation,Toth equation and Ono-Kondo equation were set by nonlinear fit of adsorption data.Accuracies of the predicted results were evaluated in terms of the relative error between the experimental data and those determined by the equations.Isosteric heats ofmethane adsorption on the activated carbon were respectively caculated by adsorption isotheres on the absolute amounts and excess amount as well as from DA equation.It showed that the accumulated relative error from Toth equation and DA equation was respectively less than 0.3%and 0.5%where the pressure was higher than 1 MPa.Results also revealed that the isosteric heat of adsorption calculated by DA equation was temperature dependent,and the isosteric heat of adsorption determined by adsorption isosteres from the absolute amountand excess amountaswell as the DA equation was about 16.49-18.81kJ·mol-1,17.31-20.24kJ·mol-1and 15.29-21.58kJ·mol-1, respectively.Conclusions were drawn that Toth equation was suitable for analyzing adsorption equilibrium of methane on the activated carbon,and DA equation was recommendable for calculating the isosteric heat of methane adsorption on the activated carbon.
adsorbed natural gas(ANG);activated carbon;adsorptionmodel;adsorption heat
O647.3;TK16
A
1001-9219(2015)02-39-05
2014-06-03;基金来源:福建省高等学校新世纪优秀人才计划支持计划(编号:Z80136)和福建省教育厅产学研项目(编号:JA12185)资助;作者简介:朱子文(1991-),男,硕士研究生,主要从事新能源材料研发;*
郑青榕(1967-),男,博士,教授,主要从事吸附理论及工艺方面的研究,电邮zhengqr@jmu.edu.cn,电话0592-6183533,传真0592-6180332。

