荷叶中化学成分的分离与鉴定(Ⅲ)*
夏明辉,彭 双,赵 晶,韩立峰,张 祎,王 涛
·中药研究·
荷叶中化学成分的分离与鉴定(Ⅲ)*
夏明辉1,彭双2,赵晶1,韩立峰1,张祎1,王涛1
(1.天津市中药化学与分析重点实验室,天津300193;2.青海省青海湖药业有限公司,西宁810000)
[目的]研究荷叶中的化学成分,为进一步开发利用荷叶资源提供依据。[方法]采用正相硅胶、反相ODS、SephadexLH-20等柱色谱及制备型高效液相色谱法(HPLC)等方法进行分离纯化,并通过理化性质、质谱、核磁以及文献比对等方法,对化合物的结构进行鉴定。[结果]从荷叶体积分数为70%的乙醇提取物中分离鉴定了6个化合物,分别为:sarmentol F(1);(3S,5R,6S,7E,9R)-7-megastigmene-3,6,9-triol(2);(3S,5R,6R,7E)-3,5,6-trihydroxy-7-megastigmen-9-one(3);3S,5R-dihydroxy-6R,7-mestigmadien-9-one(4);3S,5R-dihydroxy-6S,7-mestigmadien-9-one(5);R-(-)-去氢催吐萝芙叶醇(6)。[结论]化合物1~6均为首次从莲属植物中分离得到。
荷叶;化学成分;结构鉴定
荷叶(Nelumbinis Folium)为睡莲科莲属植物莲(NelumbonuciferaGaertn.)的干燥叶。其具有清暑化湿、升发清阳、凉血止血之功效[1]。现代药理研究表明,荷叶具有调脂降脂[2-4]、抗氧化[5]、抗衰老[5]及抑菌[6]等作用。荷叶中主要含有生物碱[7]、黄酮、降倍半萜、木脂素等化学成分,笔者对其化学成分进行了系统研究[8-9],本文继续报道从该属植物中首次分离得到了6个化合物。它们分别为:sarmentol F(1);(3S,5R,6S,7E,9R)-7-megastigmene-3,6,9-triol(2);(3S,5R,6R,7E)-3,5,6-trihydroxy-7-megastigmen-9-one(3);3S,5R-dihydroxy-6R,7-mestigmadien-9-one(4);3S,5R-dihydroxy-6S,7-mestigmadien-9-one(5),以及R-(-)-去氢催吐萝芙叶醇(6)。
1 仪器与材料
Agilent 6520系列Q-TOF质谱仪(美国Agilent公司),安捷伦1200制备型高效液相色谱仪(G1361A prep pump,G1365D 1260 MWD,美国Agilent公司),安捷伦1200分析型高效液相色谱仪(G1314A VWD串联Alltech 3300 ELSD,温度:45℃;气流量:1.5 L/min;gain:4;美国Agilent公司),HPLC用分析型色谱柱及制备型色谱柱:安捷伦zorbax C18色谱柱、安捷伦Eclipse XDB-C18色谱柱(250 mm× 21.2 mm,7 μm及 250 mm×4.6 mm,5 μm),Bruker 500 MHz超导核磁共振波谱仪(瑞士Bruker公司)。
柱色谱硅胶(200~300目,青岛海洋化工厂);ODS(50 μm,日本YMC公司);Sephadex LH-20(美国GE公司);薄层色谱硅胶预制板GF254(青岛海洋化工厂);展开剂:氯仿-甲醇-水(下层,系列体积比例);薄层显色剂:10%的硫酸乙醇溶液(V/V);甲醇、乙醇、正丁醇、乙酸乙酯、石油醚等(分析纯或色谱纯,天津市康科德科技有限公司)、二氯甲烷,氨水(分析纯,天津市北方天医化学试剂厂)、冰乙酸(分析纯,天津市化学试剂三厂)。
所用药材荷叶(Folium Nelumbinis)购自河北安国药材市场,经天津中医药大学张丽娟教授鉴定为睡莲科植物莲(Nelumbo mucifera Gaertn.)的干燥叶。植物标本现保存于中医药研究院。
2 提取与分离
取干燥荷叶药材20 kg,用70%的乙醇水溶液(V/V)加热回流提取两次,合并滤液,减压浓缩回收有机溶剂后,50℃真空干燥,得浸膏约2 394 g,取其中2 280 g,用适量水悬浮后,用4种有机溶剂萃取,分别得石油醚层32 g,二氯甲烷层137 g,乙酸乙酯层77 g和正丁醇层364 g。取二氯甲烷部分(100 g)经硅胶柱层析 [先用石油醚-乙酸乙酯-氨水10∶1∶0→3∶1∶0→1∶1∶0.002→1∶5∶0.006→1∶10∶0.011(V/V/V)为流动相进行梯度洗脱,然后再用乙酸乙酯、甲醇进行洗脱],合并得到12组流分(Fr.1-12)。取其中Fr.7(6.0 g),经ODS柱色谱,MeOH-H2O体积比30∶70→40∶60→50∶50→60∶40→100∶0梯度洗脱,合并得到15组流分(Fr.7.1-15)。其中Fr.7.2(277 mg)、Fr.7.7(96.8 mg)经Sephadex LH-20以及制备型高效液相色谱法(HPLC)等手段分离,分别得到化合物6(58mg)和化合物1(13mg)。取Fr.9(5.2 g),经ODS柱色谱,MeOH-H2O体积比30∶70→40∶60→50∶50→60∶40→100∶0梯度洗脱,合并得到14组流分(Fr.9.1-14)。其中Fr.9.3(289 mg)、Fr.9.4(249 mg)、Fr.9.5(448 mg)经Sephadex LH-20及制备HPLC等手段分离,分别得到化合物3(12mg)、化合物4(14mg)、化合物2(31mg)、化合物5(15mg)。化合物1~6结构见图1。
3结构鉴定
化合物1:棕色油状物。TLC板上,10%的硫酸乙醇溶液(V/V)显色呈棕色。HR-MS给出其准分子离子峰m/z 211.136 8[M-H]-,得出分子式为C13H24O2(Calc.C13H23O2,211.170 4)。1H-NMR(500 MHz,CDCl3)谱的低场区有2组dd峰:δ 5.29(1H,dd,J= 15.5,9.5 Hz,H-7)和5.50(1H,dd,J=15.5,6.5 Hz,H-8),为反式烯氢质子信号;在高场区可观察到四组甲基峰,其中有2个单峰:δ 0.84(3H,s,H-11)和0.88(3H,s,H-12),1个dd峰:δ 1.27(3H,dd.J=6.5,1.5 Hz,H-10),1个d峰:δ 0.82(3H,d,J=7.0 Hz,H-13);此外,高场区及中低场区还有几组多重峰:δ 1.74(1H,ddd,J=13.0,4.0,2.0 Hz,H-2a)、1.12(1H,m,H-2b)、3.79(1H,m,H-3)、2.10(1H,ddd,J=12.0,6.0,4.0 Hz,H-4a)、0.93(1H,m,H-4b)、1.53(1H,m,H-5)、1.31(1H,m,H-6)、4.30(1H,m,H-9)。13C-NMR(125 MHz,CDCl3)谱中显示有13个碳信号,结合DEPT谱可知化合物1包括1个季碳,2个仲碳,6个叔碳,4个甲基。在低场区只有2个碳信号:δ 130.6和137.3,即为反式双键上的碳信号。中高场区的2个叔碳信号δ 69.0和66.9,从化学位移值可知各连有一个羟基。结合HSQC,知低场区的δ 31.3、23.7、21.4、21.1为4个甲基碳信号。核磁数据(见表1)与参考文献[10]对照后,数据基本一致,确定化合物1为sarmentolF。
化合物2:无定形粉末。TLC板上,体积分数为10%的硫酸乙醇溶液(V/V)显色呈棕色。HR-MS给出其准分子离子峰m/z 251.163 5[M+Na]+,得出分子式为C13H24O3(Calc.C13H24O3Na,251.161 8)。1H-HMR(500 MHz,CD3OD)谱的低场区有2组特征信号:δ 5.72(1H,dd,J=16.0,6.0 Hz,H-8)和5.55(1H,d,J= 16.0 Hz,H-7),知该化合物中有一个反式双键;在高场区可明显观察到4组甲基峰:δ 1.24(3H,d,J=6.5 Hz,H-10)、0.89(3H,s,H-11)、0.98(3H,s,H-12)、0.81(3H,d,J=7.0 Hz,H-13)及几组多重峰:δ 1.93(1H,m,H-5)、1.67(1H,m,H-2a)、1.38(1H,m,H-2b)、1.66(1H,m,H-4a)、1.40(1H,m,H-4b);在中高场区也有2组明显的多重峰:δ 3.80(1H,m,H-3)和4.29(1H,m,H-9)。13C-NMR(125 MHz,CD3OD)谱中显示有13个碳信号,结合HSQC谱可知该化合物有2个仲碳,5个叔碳、2个季碳和4个甲基。其中δ 135.5(C-8)和133.9(C-7)为反式双键的2个碳信号;而δ 25.9(C-11)、25.2(C-12)、24.2(C-10)和16.5(C-13)则为4个甲基碳信号。核磁数据与参考文献[11]相对照,基本一致(见表1),确定化合物2为(3S,5R,6S,7E,9R)-7-megastigmene-3,6,9-triol。
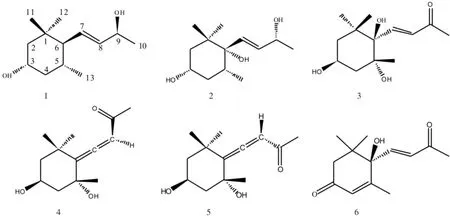
图1 化合物1~6的结构
化合物3:无色油状物。TLC板上,紫外灯(254nm)下有一暗斑,10%的硫酸乙醇溶液(V/V)显色呈桔红色。HR-MS给出其准分子离子峰m/z 277.121 3[M+ Cl]-,确定其分子式为 C13H22O4(Calc.C13H22O4Cl,277.121 2)。1H-NMR(500 MHz,CDCl3)谱的低场区有2组特征信号:δ 7.29(1H,d,J=16.0 Hz,H-7)和6.37(1H,d,J=16.0Hz,H-8),知为反式双键上的质子信号;在高场区可观察到4组甲基单峰:δ 2.32(3H,s,H-10)、1.28(3H,s,H-11)、0.87(3H,s,H-12)、1.17(3H,s,H-13);此外,还有几组多重峰:δ 4.18(1H,m,H-3)、1.61(1H,m,H-2)、1.88(1H,ddd,J=13.0,5.0,1.5 Hz,H-4a)、1.78(1H,dd,J=13.0,11.5 Hz,H-4b)。13C-NMR(125 MHz,CDCl3)谱中显示12个碳信号,从HMBC谱中知,有一个碳信号与溶剂峰重叠。结合DEPT谱可知该化合物有4个季碳,2个仲碳,3个叔碳和4个甲基。最低场区的δ 198.0(C-9)为α,β-酮羰基信号;δ 148.7(C-7)和131.2(C-8)为反式双键的2个碳信号:而δ 26.6(C-10)、25.6(C-11)、27.7(C-12)和27.5(C-13)为4个甲基碳信号。上述核磁数据与参考文献[12]相对照,基本一致(见表1),确定化合物3为(3S,5R,6R,7E)-3,5,6-trihydroxy-7-megastigmen-9-one。
化合物4:无色油状物。TLC板上,紫外灯(254nm)下有一暗斑,10%的硫酸乙醇溶液(v/v)显色呈棕色。HR-MS给出其准分子离子峰m/z 247.130 7[M+Na]+,推测其分子式为C13H20O3(Calc.C13H20O3Na,247.1305)。1H-NMR(500 MHz,CDCl3)谱的低场区有1个明显的单峰:δ 5.85(1H,s,H-8);中高场区有1个多重峰,根据峰面积知为1个次甲基质子信号:4.34(1H,m,H-3);在高场区有4组明显的单峰,均为甲基峰:2.18(3H,s,H-10)、1.43(3H,s,H-11)、1.38(3H,s,H-13)、1.16(3H,s,H-12)和2组亚甲基信号:2.30(1H,d,J=7.0Hz,H-4a)、1.44(1H,m,H-4b)、1.99(1H,d,J=7.0Hz,H-2a)、1.35(1H,m,H-2b)。13C-NMR(125 MHz,CDCl3)谱中共13个碳信号。结合DEPT谱可知该化合物有5个季碳信号,2个仲碳信号,2个叔碳信号以及4个甲基信号。上述核磁数据与参考文献[13]对照,基本一致(见表1),确定化合物4为3S,5R-dihydroxy-6R,7-mestigmadien-9-one。
化合物5:无色油状物。TLC板上,紫外灯(254nm)下有一暗斑,10%的硫酸乙醇溶液(V/V)显色呈淡棕色。HR-MS给出其准分子离子峰m/z 247.132 3[M+ Na]+,推测其分子式为C13H20O3(Calc.C13H20O3Na,247.130 5)。1H-NMR(500 MHz,CDCl3)谱的低场区有1个明显的单峰:δ 5.99(1H,s,H-8);中高场区有1个多重峰,根据峰面积知为1个次甲基质子信号:4.31(1H,m,H-3);在高场区有4组单峰,均为甲基峰:2.27(3H,s,H-10)、1.42(3H,s,H-11)、1.39(3H,s,H-13)、1.11(3H,s,H-12)和2组亚甲基信号:2.23(1H,ddd,J=2.0,3.5,13.0 Hz,H-4a)、1.36(1H,m,H-4b)、1.93(1H,ddd,J=2.0,4.0,12.5 Hz,H-2a)、1.35(1H,m,H-2b)。13C-NMR(125 MHz,CDCl3)谱中可见13个碳信号,结合DEPT谱可知有5个季碳,2个仲碳,2个叔碳和4个甲基。碳谱数据与化合物4比较,非常相近,碳谱中除8、9、10相差值分别为0.4、1.2、1.1 ppm之外,其余的差值不超过0.2 ppm,说明化合物5和化合物4为同分异构体。上述核磁数据与参考文献[13-14]相对照,基本一致(见表1),确定化合物5为3S,5R-dihydroxy-6S,7-mestigmadien-9-one。
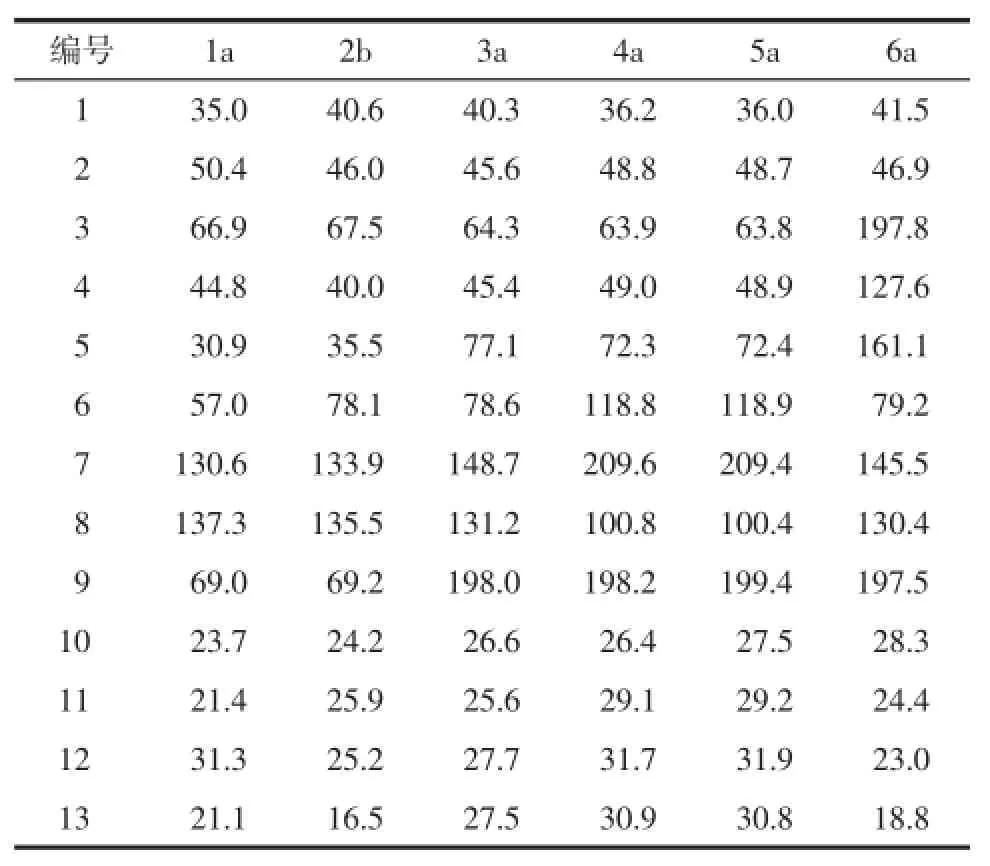
表1 化合物1~6的碳谱数据
化合物6:棕色油状物。TLC板上,紫外灯(254nm)下有一明显的暗斑,10%的硫酸乙醇溶液(V/V)显色呈黄绿色。HR-MS给出其准分子离子峰m/z 245.115 4[M+Na]+,确定其分子式为C13H18O3(Calc. C13H18O3Na,245.114 8)。1H-NMR(500 Hz,CDCl3)谱的低场区有3组峰,其中2组为d峰:δ 6.85(1H,d,J= 15.5 Hz,H-7)和6.48(1H,d,J=15.5 Hz,H-8).提示存在一对反式耦合的烯氢;另一组为s峰:δ 5.96(1H,s,H-4),知化合物中还存在一个双键;高场区可观察到4个单峰:δ 2.31(3H,s,H-10)、1.90(3H,s,H-13)、1.11(3H,s,H-11)和1.03(3H,s,H-12),知为甲基信号;中高场区的2组信号δ 2.50(1H,d,J=17.5 Hz,H-2a)和2.34(1H,d,J=17.5 Hz,H-2b)为饱和碳上的同碳耦合质子。13C-NMR(125MHz,CDCl3)谱结合DEPT谱知该化合物有4个季碳,4个伯碳,1个仲碳和4个叔碳。在最低场区观察到有δ 197.8和197.5,知该化合物含2个α,β-酮羰基。低场区的其余4个碳:δ 161.1、145.5、130.4、127.6,为氢谱中所推出的两个双键的碳信号。而高场区的δ 28.3、24.4、23.0、18.8为4个甲基的碳信号。上述核磁数据与参考文献[15]对照,基本一致,确定化合物6为R-(-)-去氢催吐萝芙叶醇[R-(-)-dehydrovomifoliol]。
[1]国家药典委员会.中华人民共和国药典[M].北京:中国医药科技出版社,2010:258-259.
[2]赵骏,高岚,齐召朋.荷叶总生物碱及其盐的提取和降脂作用的比较[J].天津中医药,2005,22(2):161-162.
[3]李玉红,张德芹,刘虹,等.糖脂清对四氧嘧啶糖尿病小鼠糖、脂代谢的影响[J].天津中医药大学学报,2009,28(4):185-187.
[4]李玉红,刘虹,王茜,等.糖脂清过柱前后对KK-Ay小鼠血糖血脂药效学影响对比实验[J].天津中医药,2012,29(4):384-388.
[5]王蓉,杨柳青.荷叶抗氧化活性的初步研究[J].科技信息,2011,32:3-4.
[6]孙晔,戴妙妙,缪存铅,等.荷叶挥发油对肉类抑菌活性的影响因素研究[J].食品工业,2009,6(1):12-14.
[7]朱晓月,刘虹,郝彧,等.市售荷叶药材中荷叶碱含量调查[J].天津中医药大学学报,2010,29(1):36-37.
[8]彭双,韩立峰,刘二伟,等.荷叶中化学成分的分离和鉴定[J].沈阳药科大学学报,2012,29(7):519-524.
[9]马迪,彭双,韩立峰,等.荷叶中化学成分的分离与鉴定(II)[J].沈阳药科大学学报,2014,31(5):355-359.
[10]Morikawa T,Zhang Y,Nakamura S,et al.Bioactive constituents from Chinese natural medicines.XXII.Absolute structures of new megastigmane glycosides,sedumosides E1,E2,E3,F1,F2 and G from Sedum sarmentosum(Crassulaceae)[J].Chem Pharm Bull,2007,55(3):435-441.
[11]Susumu K,Katsuyoshi M,Hideaki O,et al.Crotonionosides A-G:Megastimane glycosides from leaves of Croton cascarilliodes Rauschel[J].Phytochemistry,2011,72:147-153.
[12]Seng TT,Alistair LW,Patrick TH.Isolation and x-ray crystal structure of(E)-4-(r-1′,t-2′,c-4′-Trihydroxy-2′,6′,6′-trimethylcyclohexyl)but-3-en-2-one,a constituent of new zealand thyme honey[J].Aust J Chem,1989,42:1799-1804.
[13]崔锡强,李杏翠,王磊,等.蚕沙中化学成分研究[J].中国中药杂志,2008,33(21):2493-2494.
[14]Terje B,Gerhard E,Kurt B,et al.Claimed 6R/6S allene isomerization in carotenoids is geometrical 9-trans/9-cis isomerization[J].Tetrahedron Letters,1989,30(19):2577-2580.
[15]Stefano S,Assem B,Claudio F.Chemoenzymatic resolution of cis-and trans-3,6-dihydroxy-a-ionone.Synthesis of the enantiomeric forms of dehydrovomifoliol and 8,9-dehydrotheaspirone[J].Tetrahedron:Asymmetry,2007(18):2573-2580.
Isolation and identification of chemical constituents from Nelumbinis Folium(Ⅲ)
XIA Ming-hui1,PENG Shuang2,ZHAO Jing1,HAN Li-feng1,ZHANG Yi1,WANG Tao1
(1.Key Laboratory of Traditional Chinese Medicinal Chemistry and Analytical Chemistry of Tianjin,Tianjin 300193,China 2.Qinghai Lake Pharmaceutical Company Limited,Xining 810000,China)
[Objective]To investigate the chemical constituents of the lotus leaf for futher research and development.[Methods]The chemical components were obtained by using several chromatographies,such as silica gel,ODS,Sephadex LH-20 and PHPLC,and their structures were identified by the physico-chemical methods,MS,NMR spectra and comparing with literatures.[Results]Six compounds were isolated from 70%ethanol extract of lotus leaves and identified as sarmentol F(1);(3S,5R,6S,7E,9R)-7-megastigmene-3,6,9-triol(2);(3S,5R,6R,7E)-3,5,6-trihydroxy-7-megastigmen-9-one(3);3S,5R-dihydroxy-6R,7-mestigmadien-9-one(4);3S,5R-dihydroxy-6S,7-mestigmadien-9-one(5),and R-(-)-dehydrovomifoliol(6).[Conclusion]Compounds 1~6 are obtained from Nelumbo Adans.for the first time.
Nelumbinis Folium;chemical constituents;structure identification
R285.5
A
1673-9043(2015)02-0096-04
10.11656/j.issn.1673-9043.2015.02.08
天津市高等学校科技发展基金一般资助项目(2012 0203);高等学校博士学科点专项科研基金(20121210110007)。
夏明辉(1990-),女,硕士研究生,主要从事中药药效物质基础研究。
王涛,E-mail:wangt@263.net。
(2014-12-14)

