原料药粒径对头孢地尼颗粒体外溶出行为的影响
刘为中,李志云,查晓雁
(合肥医工医药有限公司,安徽合肥 230088)
头孢地尼(Cefdinir)属第三代头孢类抗生素,由日本藤泽药品工业公司(现日本Astellas制药株式会社)研制开发,于1991年首次在日本上市,随后分别在美国、韩国及我国上市[1]。头孢地尼在0.1 mol·L-1磷酸盐缓冲液中略溶,在水、乙醇或乙醚中不溶[2]。该药属水难溶性药物,原料药的粒径可能会影响其溶出度,因此,本研究以日本安斯泰来制药株式会社生产的头孢地尼颗粒(商品名为Cefzon®)为参比制剂,考察不同粒径的原料药对头孢地尼颗粒溶出行为的影响,为确定制备头孢地尼颗粒最佳原料粒径提供一定的依据。
1 仪器与试药
1.1 仪器 ZR-8G智能溶出仪(天津天大天发有限公司),AS5150超声波清洗器(北京华博科技制造有限公司),UV-2550紫外分光光度计(日本岛津),QM-16X2球磨机(天津市新渤海制药设备有限责任公司),BT-2001激光粒度分布仪(丹东百特仪器有限公司)。
1.2 试药 头孢地尼原料(浙江永宁药业股份有限公司,批号为:130702),头孢地尼对照品(中国药品生物制品检定所,纯度98.3%,批号:130948-200501),Cefzon®(安斯泰来制药株式会社,规格:每袋50 mg,批号:024850),自制颗粒D90:142.90 μm、D50:30.25 μm、D10:3.47 μm(100 目筛);D90:51.21 μm、D50:10.71 μm、D10:2.25 μm(200 目筛);D90:35.62 μm、D50:6.98 μm、D10:1.66 μm(微粉化),磷酸二氢钾、氢氧化钠等试剂均为分析纯。
2 方法与结果
2.1 溶出度方法学的建立
2.1.1 检测波长的确定 精密称取头孢地尼原料适量,用pH=6.8磷酸盐缓冲液超声溶解,0.8μm微孔滤膜滤过,配成每1 mL中约含头孢地尼10μg的溶液,在200~400 nm波长范围扫描,在287 nm波长处有最大吸收,故选定检测波长为287 nm。
2.1.2 辅料空白干扰试验 按处方配比量称取空白辅料,混合均匀后,称取1 袋量,按“2.1.1”项下的试验方法配制溶液,并在287 nm波长处测定吸光度,结果显示吸光度仅为0.002,故空白辅料无干扰。
2.1.3 标准曲线绘制及线性范围的考察 取头孢地尼对照品约50 mg,精密称定,置200 mL量瓶中,用0.1 mol·L-1磷酸盐缓冲液超声溶解后,稀释至刻度,摇匀,精密量取 2.0、3.0、4.0、5.0、6.0 mL 分别置100 mL量瓶中,用pH=6.8磷酸盐缓冲液稀释至刻度,摇匀,作为供试品溶液。取上述溶液,照紫外—可见分光光度法(中国药典2010年版二部附录IV A)[2],在最大吸收波长287 nm处分别测定吸光度。以吸光度对浓度进行线性回归,回归方程为 A=5.636 ×10-2C+1.378 ×10-2,相关系数 r=0.999 5,标准曲线见图1。结果表明,头孢地尼颗粒在4.91 ~14.73 mg·L-1浓度范围内,浓度与吸光度的线性关系良好。
2.1.4 回收率试验 分别精密称取头孢地尼25、40、50 mg及处方量的相应辅料各9份,置200 mL量瓶中,加0.1 mol·L-1磷酸盐缓冲液超声溶解,用pH=6.8磷酸盐缓冲液稀释至刻度,摇匀,用0.8 μm微孔滤膜滤过,弃去初滤液,精密量取续滤液并稀释成含头孢地尼 5、8、10 mg·L-1的溶液,作为供试品溶液;在最大吸收波长287 nm处分别测定吸光度,代入“2.1.3”项下的标准曲线,计算样品浓度并求得回收率,结果见表1。结果RSD均小于2%,表明该方法准确可靠。

表1 回收率测定结果(n=9)
2.1.5 稳定性试验 取10 mol·L-1供试品溶液一份,分别于 0、2、4、8、12、24 h 测定吸光度值,考察其稳定性,结果见表2。结果显示RSD小于2.0%,说明样品溶液在24 h内稳定性良好,该方法准确可靠,误差在允许范围内。
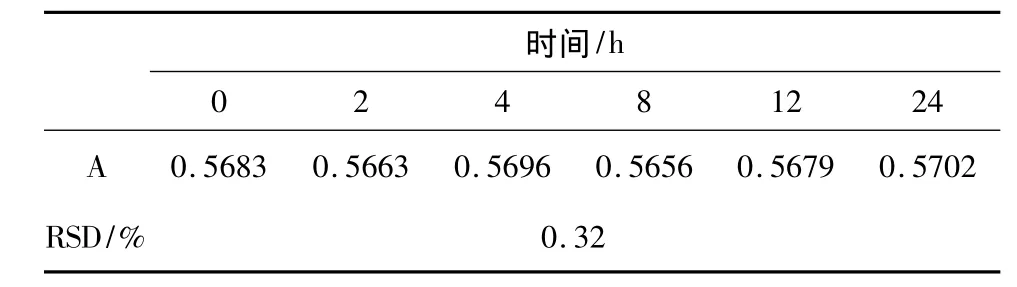
表2 稳定性试验结果
2.2 不同原料药粒径对溶出行为的影响 虽然优化处方也是促进难溶性药物溶出的有效方法之一[3],但由于本制剂中处方影响因素较少,故不做重点考察。另外,溶出介质的pH值对难溶性药物的溶出有一定的影响[4],因此,本研究重点考察在4种溶出介质中原料粒径对头孢地尼颗粒溶出行为的影响。
取同一批头孢地尼原料,两份用标准筛筛分法得到 D90:142.90 μm、D50:30.25 μm、D10:3.47 μm(100 目筛)和 D90:51.21 μm、D50:10.71 μm、D10:2.25μm(200目筛)粒径的原料,另取一份经球磨粉碎机微粉化以后用粒度分析仪得到粒径分布为D90:35.62 μm、D50:6.98 μm、D10:1.66 μm 的微粉化原料(粒径分布图见图2),根据已经确定的基本处方,分别称取三种粒径的原料和处方量的辅料,制备头孢地尼颗粒。
取3种自制头孢地尼颗粒与参比制剂,按中国药典2010年版二部附录XC溶出度测定第二法(桨法)[2],以 pH=6.8 磷酸盐缓冲液、水、pH=1.2 盐酸盐缓冲液、pH=4.0醋酸盐缓冲液900 mL为溶出介质,转速为50 r·min-1,依法操作,分别于5、10、15、30、45、60 min 取溶液10 mL,用0.8 μm 微孔滤膜滤过,同时补充溶出介质10 mL,精密量取续滤液适量,配制成每1 mL中约含头孢地尼10μg的溶液,摇匀,作为供试品溶液;另精密称取头孢地尼对照品适量,置容量瓶中,用0.1 mol·L-1磷酸盐缓冲液溶解、pH=6.8磷酸盐缓冲液稀释成含头孢地尼10 mg·L-1的溶液作为对照溶液,UV法在287 nm处测定吸光度,计算不同时间点的累积溶出百分率。以相似因子f2作为指标,对比自制制剂与参比制剂的溶出特性,结果见图3、表3。
由溶出曲线图3可知,同一批次的头孢地尼原料药,当粒径不同时,溶出度有一定差异。原料粒径为 D90:142.90 μm、D50:30.25 μm、D10:3.47 μm(100目筛)和 D90:51.21 μm、D50:10.71 μm、D10:2.25μm(200 目筛)时,制剂在pH=6.8 磷酸盐缓冲液中15 min溶出度达到85%以上,在水、pH=1.2盐酸盐缓冲液、pH=4.0醋酸盐缓冲液三种介质中f2<50,因此这两种粒径制备的颗粒与参比制剂的溶出行为均存在差异;粒径(微粉化)为D90:35.62 μm、D50:6.98 μm、D10:1.66 μm(微粉化)原料制得的颗粒在pH=6.8磷酸盐缓冲液中15 min溶出度达到85%以上,在水、pH=1.2盐酸盐缓冲液、pH=4.0醋酸盐缓冲液三种介质中f2>50,说明溶出行为与参比制剂相似。由以上结果可知,减小原料粒径能够有效地提高头孢地尼颗粒的溶出度。

表3 在4种溶出介质中不同粒径样品相对于原研的溶出曲线相似性评价
3 讨论与结论
近年来,越来越多的难溶性药物被相继开发,提高药物的溶出特性已成为开发该类药物的研究重点。影响难溶性普通口服固体制剂溶出特性的物理因素主要是药物的晶型和粒度[5],对于多晶型药物,因晶格结构不同,某些物理性溶解度可能不同,对难溶性药物的固体口服制剂而言,溶解度不同会影响制剂的溶出特性。原料药粉末的粒径是影响其制剂溶出度的另一重要物理因素[6]。因此,在制剂过程中,减小原料药粒径,提高药物离子的表面积可以有效地提高药物的溶出表面积和溶出度[7]。
目前,已出现一些制剂技术能够提高难溶性药物的溶出度,比如药物微粉化[8]、制备固体分散体[9]、制备环糊精包合物[10]、制备粉状溶液和溶剂沉积物等,对提高难溶性药物固体制剂的溶出度效果显著[11]。
本研究建立在可靠的头孢地尼颗粒溶出度测定方法基础上,考察了头孢地尼原料粒径对制剂溶出的影响,结果表明,当头孢地尼原料粒径分别为D90:142.90 μm、D50:30.25 μm、D10:3.47 μm 和D90:51.21 μm、D50:10.71 μm、D10:2.25 μm 时,自制头孢地尼颗粒的溶出行为与参比制剂有较大差异,但粒径减小到 D90:75μm、D50:45μm、D10:18 μm时溶出有所改善;当粒径减小至D90:35.62μm、D50:6.98 μm、D10:1.66 μm 后,药物的溶出有显著提高,与原研溶出行为相似,这说明对于难溶性药物来说,减小原料粒径能够有效提高难溶性药物的溶出度。据文献报道[12],并不是原料的粒径越小好,过度微粉化可能会导致过细的粉末周围形成一层气泡囊,阻碍水分进入颗粒,从而阻碍药物的溶出;对于有刺激性的药物,粒径愈小,刺激性愈大;稳定性差的药物,粒子太细,分解速度会加快;对于某些长效制剂而言,要求药物在较长时间内缓慢释放和吸收,需要较大的粒度。因此,并非所有的药物都需要微粉化,选择合适的粒径对于制剂的质量至关重要。
[1]周永健,边 颖,蔡 毅.第三代口服头孢菌素 -头孢地尼[J].天津药学,2003,15(2):66 -68.
[2]国家药典委员会.中国药典(二部)[S].北京:中国医药科技出版社,2010:177 -178,附录 IVA,XC.
[3]张梅君,王志强,黄学荪.固体制剂溶出度的研究进展[J].中国药业,2009,18(8):58 -60.
[4]刘小燕,金 涌,臧洪梅.不同溶出介质中头孢地尼胶囊溶出曲线的相似性比较[J].安徽医药,2013,17(5):749 -751.
[5]曾凡彬.影响难溶性药物口服固体制剂溶出特性的理化因素-晶型和粒度[J].中国新药杂志,2002,11(7):507-509.
[6]曹 林,解爱莉.不同粒径苯磺酸氨氯地平原料对制剂工艺的影响[J].黑龙江科技信息,2014,17(2):2.
[7]Rasenack N,Muller BW.Micron -size drug particles:common and novelmicronization techniques[J].Phram Dev Technol,2004,9(1):1-13.
[8]张定堃,林俊芝,秦春凤,等.微粉化对穿心莲内酯粉体学性质和溶出度的影响[J].中国医药工业杂志,2014,45(4):325-329.
[9]张 维,张志云,张志丽,等.超临界流体技术制备固体分散体的研究进展[J].安徽医药,2013,17(6):903 -905.
[10]管咏梅,张 妮,陈振华,等.固体分散技术和包合技术对白头翁总皂苷增溶作用研究[J].中国中药杂志,2013,38(23):4061-4066.
[11]Saleh MA,Mohammed SA,Abdullah EC,et al.Enhancement the Dissolution Rateand Solubility of Poorly Soluble Drugs:Review[J].Advanced Materials Research,2013,701:234 -238.
[12]张可擎.头孢地尼胶囊的制备及提高其溶出度的研究[D].广州:广州中医药大学,2011.

