探析氯气制备实验的考查方式
江苏 印志林
探析氯气制备实验的考查方式
江苏 印志林
氯气的性质活泼,用途广泛,氯气的制备和性质是设计实验试题的“发源地”之一。下面在分析氯气制备实验要点的基础上,探析该实验的常见考查方式。
一、氯气实验室制法的实验要点
氯气的实验室制法是重要的气体制备实验,复习时如果能对该实验进行多角度的发散思维,掌握实验的要点和细节,则可以在后续复习中触类旁通,事半功倍。
1.实验原理
实验室制氯气利用的是氧化还原反应原理,用氧化剂将盐酸中的Cl-氧化为Cl2。教材实验中使用的氧化剂是在这个反应中,盐酸既表现了还原性,又表现了酸性,反应中HCl只有一半被氧化。
若无浓盐酸,则可以用食盐和浓硫酸来代替:

若无MnO2,则可用K2Cr2O7、KMnO4、KClO3、Ca(ClO)2等更强的氧化剂来代替:
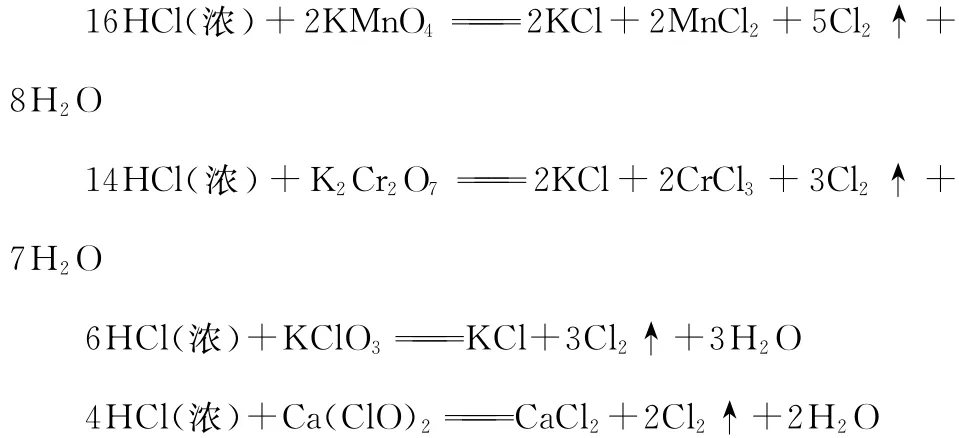
2.反应条件
MnO2的氧化性较弱,跟浓盐酸的反应需加热,但浓盐酸的挥发性较强,加热温度过高过快会加快盐酸的挥发,使收到的气体不纯,故要缓缓加热。
3.反应的进程
盐酸中Cl-还原性的强弱,与盐酸浓度有关,故该实验成败的关键在于浓盐酸的浓度。当盐酸的浓度小于7mol·L-1时,Cl-浓度小,还原性弱,化学反应将不能发生,故实验中必须选用浓盐酸。
4.反应装置
该反应为固体和液体反应且需加热,故发生装置使用烧瓶、分液漏斗、酒精灯等。因为在加热条件下浓盐酸更易挥发,为保持其浓度,并减少HCl的挥发,所以浓盐酸必须由分液漏斗慢慢加入。
5.气体的收集
因为Cl2密度大于空气且能溶于水,所以常用向上排空气法收集Cl2。Cl2在饱和食盐水中的溶解度大大减小,也可用排饱和食盐水法收集Cl2。
6.气体的净化
用以上方法制得的Cl2中常混有少量HCl和水蒸气,若需收集纯净、干燥的Cl2,可将所制得的气体依次通过盛有饱和食盐水和浓硫酸的洗气瓶。
7.检验与验满
因为Cl2是黄绿色气体,故可以用观察法判断Cl2是否收集满。实验中常用淀粉碘化钾试纸检验Cl2,若将润湿的淀粉碘化钾试纸靠近集气瓶口,试纸变蓝,表明Cl2已收集满。
8.尾气吸收
Cl2具有毒性,制Cl2的装置应密闭,多余的Cl2应使用碱液吸收。和Ca(OH)2相比,NaOH易溶于水,其溶液浓度可以大一些,更适合于吸收装置中多余的Cl2。需要注意的是,吸收余气所用的NaOH溶液浓度不能太大,若用浓NaOH溶液则会导致倒吸现象发生。
二、有关氯气制备实验的综合方式
从近年来的高考试题看,与氯气有关的综合实验题是考试的热点题型。
1.将氯气的制备实验与物质制备实验进行综合
【例1】(2015·海南卷)工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实验。
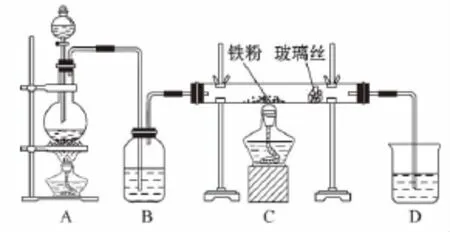
回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为_______________,装置B中加入的试剂是_____________。
(2)制取无水氯化亚铁的实验中,装置A用来制取_______________。尾气的成分是________。若仍用D的装置进行尾气处理,存在的问题是________、________。
(3)若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是________。欲制得纯净的FeCl2,在实验操作中应先________,再________。
【解析】(1)在制取无水氯化铁的实验中,A装置为Cl2的制备装置,实验室通常用MnO2和浓盐酸共热制取Cl2,Cl2中混有HCl和水蒸气,需要用浓硫酸干燥混合气体以除去水蒸气。D装置中应盛NaOH溶液,用于吸收多余的Cl2。
(2)HCl与铁共热可制得无水氯化亚铁,则A装置是HCl的制备装置,HCl和Fe反应生成FeCl2的同时还生成H2,故尾气的成分是没有反应的HCl和反应生成的H2。HCl极易溶于水,H2不能与NaOH溶液反应。若仍用D的装置进行尾气处理,则D中液体会发生倒吸,可燃性的H2也不能被吸收。
(3)检验FeCl3,常用的试剂是KSCN。欲制得纯净的FeCl2,需防止装置中氧气的干扰,在实验操作中应先点燃A处的酒精灯,利用产生的HCl气体排出装置中的空气,然后再点燃C处酒精灯。
【答案】(1)MnO2+4HCl(浓)MnCl+Cl↑+222H2O 浓硫酸
(2)HCl HCl和H2发生倒吸 可燃性气体H2不能被吸收
(3)KSCN溶液 点燃A处的酒精灯 点燃C处的酒精灯
2.将氯气的制备实验和性质实验进行综合
【例2】某研究性学习小组同学查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为Ca(ClO)2+他们设计了如下图所示的制取氯气并验证其性质的实验装置:

请回答下列问题:
(1)该实验中A部分的装置是__________(填写装置的序号)。
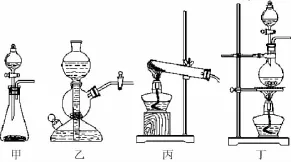
(2)A中发生反应一段时间后,B中的现象是________ _______________________,B中发生反应的离子方程式为___________________________。整套实验装置存在的明显缺陷是________________。
(3)写出D装置中发生反应的离子方程式:___________ ________________。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):__________________。
【解析】(1)固体和液体加热制备气体时,应选用加热的圆底烧瓶配分液漏斗装置。
(2)Cl2通入KI溶液时置换出I2,I2遇淀粉溶液变蓝。实验中可能有剩余的Cl2,最后应加尾气吸收装置,以防止Cl2逸出污染环境。
(3)D装置中,Cl2与水反应生成HCl和HClO,盐酸能与NaHCO3反应放出CO2。
(4)C中的Na2SO3被氧化后生成Na2SO4,向该溶液中加入足量盐酸后再加BaCl2溶液,如果生成白色沉淀,则可证明其中含有。
【答案】(1)丁
(2)溶液变蓝色 2I-+Cl2===2Cl-+I2无尾气吸收装置
(3)Cl2+H2OH++Cl-+HClO、HCO3-+H+===H2O+CO2↑
(或Cl2+===Cl-+HClO+CO2↑)(4)取少量溶液置于洁净的试管中,向其中加入稀HCl至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,则证明亚硫酸钠被氧化
3.将氯气的制备实验和化学反应原理知识进行综合
【例3】经常性地对环境进行消毒,是预防各种传染性疾病的有效措施。某研究小组为制备消毒液(主要成分是NaClO)设计了A、B两套装置(B装置中电极材料均为石墨)。并查阅到下列资料:“在加热的情况下卤素单质和碱液发生如下反应:

请回答下列问题:
(1)写出装置A烧瓶中发生反应的离子方程式:______ ______________________________________________________。
(2)若去掉装置A中盛浓硫酸的洗气瓶,能否达到预期目的?________(填“能”或“不能”)。
(3)装置A中盛冰水的烧杯的作用是________________ ______________________________________________________。
(4)利用装置B制备消毒液时有关反应的化学方程式为____________________________________________________。
(5)装置B中a端应接电源的_______________极,理由是____________________________________________________。
【解析】(1)MnO2具有氧化性,浓盐酸中的Cl-具有还原性,加热时MnO2能将Cl-氧化为Cl2,+4价锰元素被还原为+2价。
(2)Cl2与NaOH溶液反应时不需要干燥,若去掉装置A中盛浓硫酸的洗气瓶,对反应不产生影响。
(3)Cl2与NaOH溶液反应时放热,为了防止受热时反应生成NaClO3,需用冰水降温。
(4)电解饱和食盐水生成的Cl2和NaOH发生反应,可以得到含有NaClO的消毒液。
(5)装置B中,b端所连的碳棒旁有便于氢气逸出的玻璃导管,所以b是电源的负极,与之相连的碳棒是阴极,H+在阴极发生还原反应。
【答案】(1)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O
(2)能
(4)Cl2+2OH===-Cl-+ClO-+H2O
(5)正 因为a端所连的碳棒上Cl-发生氧化反应,是电解池的阳极
分析以上解题过程可以看出,解答与气体制备有关的综合实验题时,应注意以下问题:
(1)明确实验的原理和目的,搞清楚各实验装置的作用,根据“制备气体—除杂干燥—主体实验—尾气吸收”的基本流程连接实验装置,同时注意实验的细节问题,如洗气瓶中导管的长短、分液漏斗中玻璃塞的开合等。
(2)选择的除杂试剂应在除去杂质气体的同时,减少原气体的溶解量,故一般采取通入相关饱和溶液的方法。如Cl2中混有HCl,可通过饱和食盐水;SO2(或CO2)中混有HCl,则可通过饱和NaHSO3(或NaHCO3)溶液。
(3)设计实验检验物质时应防止干扰,除去杂质气体时应验证是否除尽。
(4)制备物质时,应控制温度、浓度等反应条件,防止副反应的发生。制备在空气中能与水蒸气发生反应的物质时,应保证制取装置前后均有除水装置,以确保实验前后均无水蒸气引入,提高产物的纯度。
(作者单位:江苏省常州市横山桥高级中学)

