苏教版选修四“化学反应原理”教学
郑碧芬
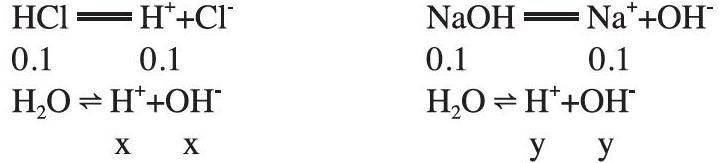
一、注重夯实基础
由于各学生之间的智力差异和学习基础不同,学生对化学知识的掌握能力不同,应针对学生实际情况因材施教。 在教学中,教师可通过习题形式让学生回顾、理解所学知识,而不是教师一味讲授。教学设计如下:
1.温故而知新
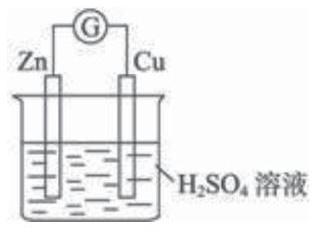
该装置为 池,Zn是 极,Cu是 极,电子从 经 流向 ,电流从 流向 ,离子从 流向 ,电极反应式分别是 总反应式 。
该习题可以让学生上课马上作答,教师根据学生回答情况及时调整,学生能够很好地回忆、理解原电池的工作原理。
2.设置问题情境,引出盐桥
在实验中,为什么Zn、Cu附近都有气泡产生?学生进行各种猜想,教师一一进行评价,提出解决办法,引入盐桥。盐桥的作用是平衡两极的电荷。
二、注重实验教学
化学是一门实验学科,要让学生真正了解每个实验涉及的化学反应原理、装置原理和操作原理,多给机会让学生动手做实验。以“强电解质和弱电解质的区分”这一教学目标为例,教学设计如下。
1.学生分组实验
(1)测定浓度均为0.1mol/L的盐酸、醋酸溶液的PH;(2)两支试管中分别放入形状相同的镁条,取浓度均为0.1mol/L的盐酸、醋酸溶液各10ml于气球中,并将气球扣在试管口,同时迅速加入到试管中,观察现象。
2.现象
(1)盐酸的PH小于醋酸的PH;(2)盐酸中气球涨得比较快,但最终两气球大小一样。
3.解析
(1)盐酸是强酸,醋酸是弱酸,当物质的量浓度相同时,由于盐酸完全电离,醋酸部分电离导致盐酸中氢离子浓度大。酸性越强,PH越小。(2)反应开始时,盐酸中氢离子浓度大于醋酸中氢离子浓度,离子浓度大,反应速率就越快。但由于镁条足量,促进醋酸往电离的方向进行,最终完全电离出氢离子,所以两者产生的氢气一样多。
4.拓展思考
(1)比较物质的量浓度相同的氢氧化钠溶液和氨水的PH大小;(2)比较PH相同的氢氧化钠溶液和氨水的物质的量浓度大小;(3)物质的量浓度、体积均相等的盐酸与醋酸,分别和足量的Zn反应,比较反应开始时的速率和产生氢气的物质的量;(4)PH、体积均相等的盐酸与醋酸,分别和足量的Zn反应,比较反应开始时的速率和产生氢气的物质的量。
三、注重分析、对比能力培养
很多学生上课时,感觉所学内容不难,但是真正碰到习题时,却不知道如何下手,眼高手低的现象十分普遍,甚至出现所学知识混淆不清的现象。在教学中,如果能采用分析对比的方法,可以大大提高学习效率。
1.题目
常温下,分别计算浓度均为0.1mol/L的盐酸、氢氧化钠溶液的PH。
2.解题思路
知道PH与氢离子浓度之间的关系,分析盐酸、氢氧化钠溶液中存在的电离过程,认识水电离出的氢离子与氢氧根离子浓度一定相等。
3.具体解析
假设盐酸、氢氧化钠溶液中水电离出的氢离子浓度分别是x、y。
从电离方程式看出,酸和碱中水的电离受到抑制。
计算酸PH的时候,把水电离出的氢离子忽略掉,因此PH=-lg0.1=1;计算碱PH的时候,把水电离出的氢氧根离子忽略掉,因此溶液中氢氧根离子浓度为0.1mol/L,根据Kw计算出氢离子浓度(来自水的电离),再算PH。C(H+)=10-14/0.1=10-13,mol/L,PH=-lg10-13=13。
四、注重构建知识网络
化学知识点比较零散,尤其是在元素和有机化学当中,很多的特性是无规律可循的却存在规律性,学生容易混淆。因此,构建知识网络体系显得十分重要。教师要提高学生的学习效率,增强知识链中的薄弱环节,实现基础知识到位,逻辑思维到位,分析问题和解决问题的能力到位,就要注重方法的探索。
五、注重教学方法
“化学反应原理”这部分内容知识跨越大、难度大,教师在教学中要认真分析学生的学情,摸清他们的知识储备,针对不同模块的知识采取不同的教学方法,才能获得良好的教学效果。在教学活动中,教师要关注和反思教学行为,注意教学方法的灵活多样性,调动学生学习积极性手段的有效性,教师在课堂所有活动的取向性,学生在课堂教学活动的参与性等诸多方面。
参考文献:
赵华,高峰.“化学反应原理”模块的学习情况调查和认知策略研究[J].化学教育,2011(3).

