ZrO2/Al2O3复合载体镍基催化剂CO甲烷化反应本征动力学
沈叶婷, 张海涛, 房鼎业, 李 涛
(华东理工大学大型工业反应器工程教育部工程研究中心,上海 200237)
ZrO2/Al2O3复合载体镍基催化剂CO甲烷化反应本征动力学
沈叶婷,张海涛,房鼎业,李涛
(华东理工大学大型工业反应器工程教育部工程研究中心,上海 200237)
采用固定床反应器,研究了复合载体镍基催化剂上的CO甲烷化反应。在温度为250~440 ℃,压力为0.1~2.5 MPa,原料气配比(nH2/nCO)为1.0~4.5的情况下,考察了操作条件对复合载体镍基催化剂甲烷化反应的影响。实验结果表明:CO转化率、CH4的选择性均随着反应温度、反应压力的升高而增加;当反应温度达到340 ℃时,CO转化率最高;当nH2/nCO=3.0时,具有较高的CO转化率和CH4的选择性。通过正交法设计实验,测定了甲烷化反应动力学数据。以双曲型动力学方程建立了以各组分逸度表示的CH4和CO2反应动力学模型,并用最大继承法对参数进行估值,获得动力学参数。残差分析及统计检验表明动力学模型是适宜的。
本征动力学; CO甲烷化; ZrO2/Al2O3载体; 镍基催化剂
天然气是一种高效的清洁能源。随着生活水平和环保要求的提高,国内对天然气的需求与日俱增,天然气供应的缺口正逐年加大,对外依存度快速上升。我国煤炭资源丰富,利用煤制气将丰富的煤炭资源转化成天然气,对我国节能减排、促进能源的可持续发展意义重大[1]。
目前工业应用的甲烷化镍基催化剂大多以γ-Al2O3为载体,而ZrO2/Al2O3复合载体表面和内部均易产生氧空位,所以金属组分的分散度更高[2]。文献[3-4]制备了ZrO2/Al2O3复合载体镍基催化剂,发现ZrO2的引入有助于减小Ni颗粒的尺寸,增加活性中心数目,从而表现出更好的催化性能; 而且相比单一Al2O3载体催化剂,复合载体催化剂更易还原。Mn助剂的加入可以进一步加强Ni与载体的相互作用。文献[5-6]研究了Mn对Ni/γ-Al2O3催化剂催化活性的影响,发现Mn助剂可促进Ni的还原,加强Ni与载体的相互作用,从而提高催化剂的催化活性。
反应动力学研究在工艺开发、工业反应器设计与过程优化中起重要作用。国内外众多学者对甲烷化催化剂的反应动力学进行了以幂函数和双曲动力学模型为主的研究[7-17]。于建国等[12-14]研究耐硫甲烷化催化剂得到的幂函数模型,具有表达式简明、数据处理方便等优点,但其应用的操作条件范围较窄。基于不同反应机理的双曲动力学模型[15-17]包含了所有基元反应的速率常数和反应涉及的物质的吸附平衡常数,适用的操作条件范围较宽。目前动力学研究主要是基于γ-Al2O3载体,而对ZrO2/Al2O3复合载体镍基催化剂双曲型动力学的研究则鲜见报道。
本文考察了反应温度、反应压力、原料气配比等对CO转化率和CH4选择性的影响。以双曲型动力学方程形式建立了以各组分逸度表示的动力学模型,采用最大继承法进行参数估值,获得动力学的模型参数。
1 实验流程
1.1催化剂制备
通过浸渍法制备Al2O3-ZrO2复合载体,将硝酸锆(Zr(NO3)45H2O,分析纯)溶于去离子水,与γ-Al2O3混合,静置6 h,在旋转蒸发仪中快速蒸干,110 ℃下干燥12 h,550 ℃下焙烧6 h,得到ZrO2-Al2O3复合载体。将以Ni(NO3)2·6H2O为Ni源和质量分数为50.0%的Mn(NO3)2为Mn源配制的混合溶液在相同条件下干燥焙烧,得到复合载体镍基催化剂。
1.2实验流程
图1所示为固定床CO甲烷化反应实验流程图。进行反应前,在N2保护条件下以2 ℃/min的升温速率升温至450 ℃,再切换H2,常压下还原镍基催化剂3 h。原料气为预先配置好的一定组成的混合气,经减压阀后得到实验所需的压力,通过脱氧器去除原料气中微量的氧气后进行反应,反应生成的H2O在冷凝器中冷凝,进行气液分离,尾气由皂膜流量计测量后放空。

1-Gas cylinder; 2-Pressure gauge; 3-Filter; 4-One-way valve; 5-Ball valve; 6-Pressure controller; 7-Reducing valve; 8-Mass flow controller; 9-Temperature controller; 10- Deaerator; 11-Mixer; 12- Heating furnace; 13- Reaction tube; 14- Condenser; 15- Gas-liquid separator; 16- Holding tank; 17- Back pressure valve; 18- Soap film flowmeter; 19- Gas chromatography; 20- Needle valve
图1固定床CO甲烷化反应实验流程图
Fig.1Experimental flow sheet of CO methanation in fixed-bed reactor
不凝性气体通过背压阀后经气相色谱(Aglient 7890B)在线分析。以N2为载气,采用毛细管HP-AL/S柱(25 m×320 μm×8 μm)和氢火焰离子检测器(FID)分析C1~C6烃类; 以He为载气,填充柱PROAPAK Q与0.5 nm分子筛色谱柱和热导率检测器(TCD)分析N2、CO、CO2的含量; 以N2为载气,0.5 nm分子筛色谱柱和热导率检测器(TCD)分析H2的含量。用归一化法计算尾气中各组分的含量。
2 操作条件对反应的影响
2.1温度对反应的影响

图2 温度对CO转化率和甲烷选择性的影响Fig.2 Effect of reaction temperature on the conversion of CO and selectivity of CH4表1 CO甲烷化产物气湿基组成 Table 1 Wet basis composition of CO methanation production
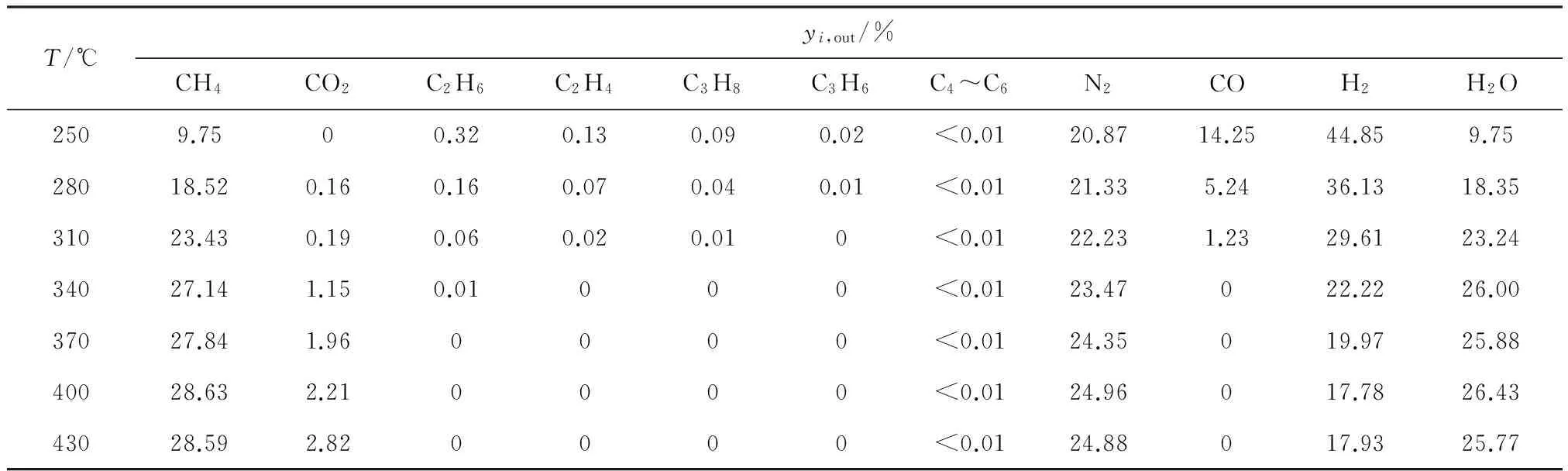
T/℃yi,out/%CH4CO2C2H6C2H4C3H8C3H6C4~C6N2COH2H2O2509.7500.320.130.090.02<0.0120.8714.2544.859.7528018.520.160.160.070.040.01<0.0121.335.2436.1318.3531023.430.190.060.020.010<0.0122.231.2329.6123.2434027.141.150.01000<0.0123.47022.2226.0037027.841.960000<0.0124.35019.9725.8840028.632.210000<0.0124.96017.7826.4343028.592.820000<0.0124.88017.9325.77
2.2压力对反应的影响
甲烷化反应是分子数减少的反应,压力升高对平衡有利,在空速为8 L/(gh),反应温度为340 ℃,压力为0.1~2.5 MPa,原料气中H2、CO、N2的摩尔分数分别为65.70%、19.74%、15.22%条件下考察压力变化对反应的影响,实验结果如图3所示。随着压力升高,CO转化率和CH4选择性都有所提高,当压力从0.1 MPa升高到1.7 MPa,CO转化率从92.7%升高到100%,继续提高压力,转化率保持100%。当压力从0.1 MPa升高到2.5 MPa,CH4选择性从90%升高到95.1%。压力升高对反应有利,可以通过升高压力来提高甲烷的产率。
2.3nH2/nCO对反应的影响
从煤炭或者生物质中获得的合成气具有不同的nH2/nCO,研究反应工艺中原料气配比的影响也很重要。图4所示为nH2/nCO对CO转化率及CH4选择性的影响。从图4可以看出,在340 ℃、1.7 MPa下,随着nH2/nCO的增大,催化剂的催化性能呈现提高的趋势。nH2/nCO的变化对CO转化率的影响较小,当nH2/nCO为1.0~3.0时,CO转化率基本维持在95.0%以上。nH2/nCO对CH4选择性影响较大。当nH2/nCO=1.0时,其选择性仅为60.0%; 随着nH2/nCO的升高,选择性迅速提高; 当nH2/nCO达到3.0时,转化率与选择性均达到最大,转化率达到99%以上,选择性达到93.9%以上;nH2/nCO再增加,选择性和转化率基本不变化。因此,适宜的nH2/nCO为3.0,此时,催化剂对CO甲烷化的催化性能较高,这是因为富氢条件下,不仅能促进甲烷化反应,而且能够抑制副反应的发生。
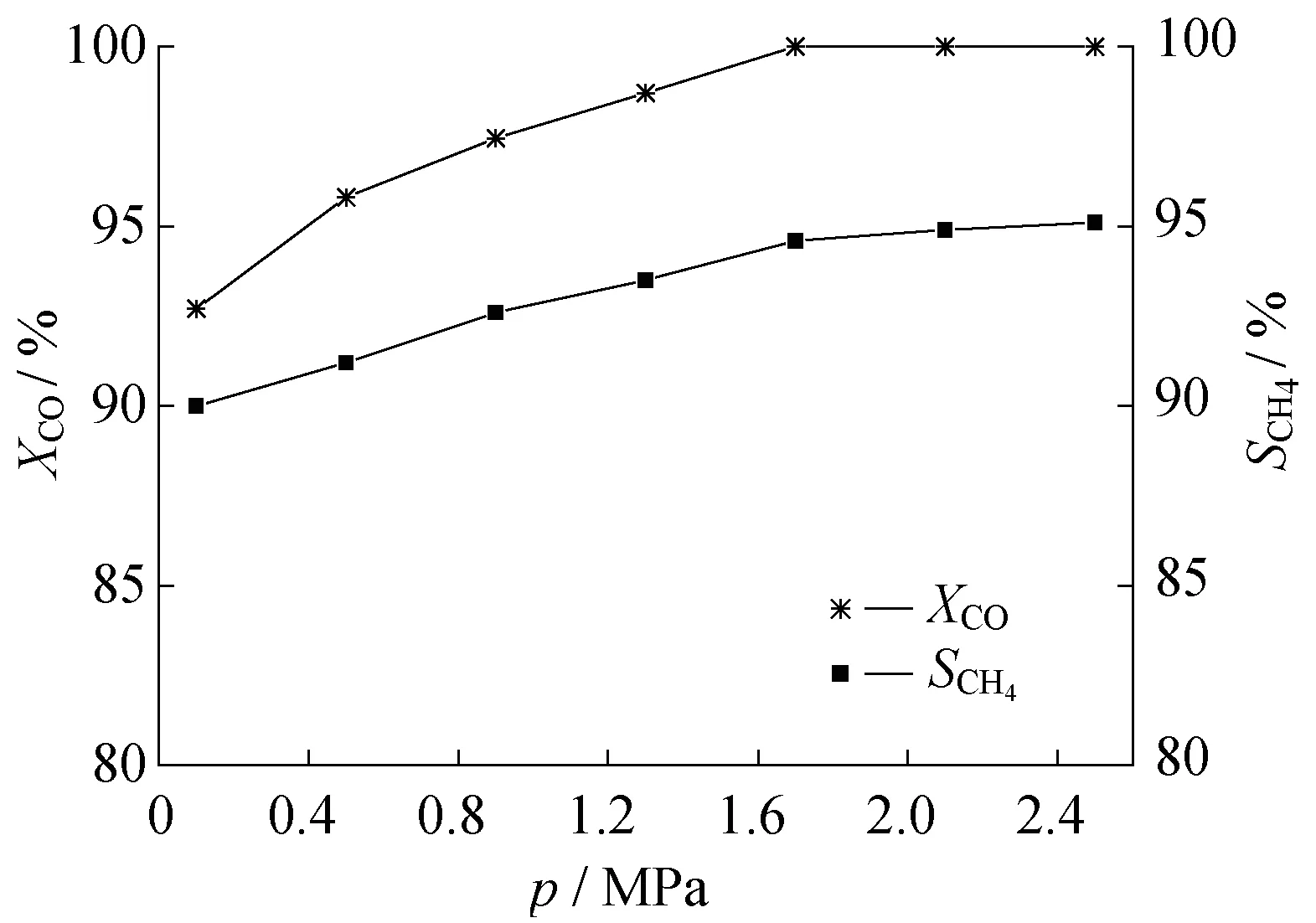
图3 压力对CO转化率和甲烷选择性的影响Fig.3 Effect of reaction pressure on the conversion of CO and selectivity of CH4
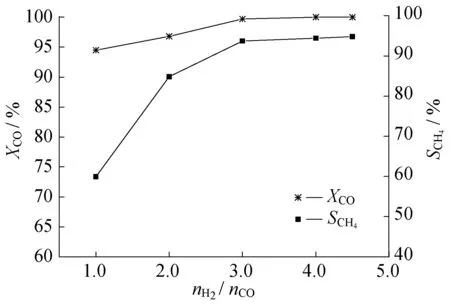
图4 nH2/nCO 对CO转化率和甲烷选择性的影响Fig.4 Effect of nH2/nCO on the conversion of CO and selectivity of CH4
3 反应动力学
3.1消除内扩散和外扩散
采用相同的催化剂用量和原料气流速,通过改变催化剂粒径来消除内扩散影响。在400 ℃、2.1 MPa、40 L/(gh)下,CO转化率与粒径的关系如表2所示。催化剂粒径小于0.30 mm时,CO的转化率基本保持不变,说明已无内扩散的影响,因此,在测定动力学数据时,粒径可选定为0.20~0.15 mm。
采用相同的催化剂用量,催化剂粒径为0.20~0.15 mm,在400 ℃、2.1 MPa下,当气体空速大于20 L/(gh)时,CO的转化率稳定在96.5%左右(见表3),表明加大原料气的空速后,气体的湍流程度提高,大大降低了气膜的阻力,从而消除了外扩散的影响。因此,测定动力学数据时,空速固定在30 L/(gh)。

表2 粒径与CO转化率的关系

表3 空速与CO转化率的关系
3.2动力学实验数据
原料气中H2、CO摩尔分数分别为60%~70%与18%~20%,其余为N2。在压力为0.5~2.1 MPa,反应温度280~400 ℃,空速为30 L/(gh)条件下,采用正交设计法测定了25组动力学数据,如表4所示。
甲烷化反应系统中共有6种组分,分别是CO、CO2、H2、CH4、H2O和N2。yi,in,yi,out分别表示气体组分i(CO、CO2、H2、CH4、 H2O、N2)的进、出口摩尔分数。各组分及总物料衡算关系见表5。
表5中NT,in,NT分别表示气体总进、出口摩尔流量。物料衡算选取CO甲烷化和变换反应作为独立反应,CO2、CH4为关键组分,yCO2、yCH4分别表示CO2和CH4的出口摩尔分数,其他组分的出口摩尔分数可以通过yCO2、yCH4来表示。
由物料衡算得:
(1)

表4 固定床CO甲烷化动力学实验数据

表5 物料衡算
(5)
3.3动力学模型
在甲烷化过程中,主要涉及以下反应:
CO+3H2CH4+H2O
(6)
CO+H2OCO2+H2
(7)
2COC+CO2
(8)
CO甲烷化的反应机理主要是CO直接解离和氢助解离两种。目前普遍认可的机理是氢助解离。本文采用氢助解离机理,选取CO甲烷化反应(式(6))和水汽变换反应(式(7))为独立反应,CH4反应速率方程采用工业上常用的基于Xu&Froment催化剂反应速率模型[20],而水汽变换反应速率方程直接引用文献[21],其中涉及的基元反应以及速率控制步骤见表6。其中fi表示CO,CH4,H2,H2O,CO2等组分的逸度;θv为催化剂表面活性吸附位的分数;θi为各气体组分以及中间产物在催化剂表面上所占吸附位的分数;KAi为各中间产物的吸附平衡常数;ka,ka′,kb,kb′分别为速率控制步骤正、逆反应速率常数; rds表示速率控制步骤。通过对速率控制步骤关键组分速率方程进行化简,得到如下甲烷化反应速率模型:
(9)
(10)
DEN=
(11)
式中,反应速率常数ki和吸附常数Kj表示如下:
(12)
(13)
K1=10 266.76×exp(-26 830/T+30.11)
(14)
K2=exp(4 400.0/T-4.063)
(15)


表6 甲烷化反应基元反应
*:Active site
3.4参数估值与模型检验
以yCH4,yCO2为独立变量,参数估值的目标函数S0见式(16)。
(16)
式中:下标e,c分别表示实验测得值和模型计算值。灵敏性分析证实H2,CH4,H2O,CO的吸附平衡常数对反应速率影响很小,所以采用文献[21]中的参数作为初值,用Runge-Kutta法求解微分方程,将25组动力学实验数据代入动力学方程式(9)、式(10),用最大继承法对参数进行估值,得到模型参数见表7,其中H2、CH4、H2O的吸附平衡常数未调整,CO吸附活化能参数微调为-44.65 kJ/mol。

表7 动力学参数
对所得到的本征动力学模型进行统计检验,结果如表8所示。表8中M表示实验次数;Mp表示参数个数;ρ2表示相关系数;F0.05(10,14)表示方差检验显著水平5%。ρ2越接近1表示所得的模型适应性越好,其表达式如下:
(17)
方差检验F是回归均方与模型残差均方和的比,表达式为:
(18)
对于非线性回归,一般要求F>10F0.05(Mp,M-Mp-l),模型才是高度显著的。
将CH4和CO2反应器出口浓度实测值与模型计算值标绘于图5。
由表8可知,ρ2>0.99,F>10F0.05(10,14),即表明在本文的压力、温度以及原料气组成范围内所得到的双曲动力学模型是适用的。从图5可以看出CH4和CO2出口摩尔分数的实测值和双曲动力学模型计算吻合良好。CH4和CO2出口浓度的相对误差绝对值的平均值分别为4.11%,8.50%。

表8 动力学模型统计检验

图5 CH4 ,CO2出口浓度实测值与模型计算值Fig.5 Experimental values and model calculated values of CH4,CO2 concentration of outlet
4 结 论
(1) 复合载体镍基甲烷化催化剂,在温度为250~440 ℃,压力为0.1~2.5 MPa,原料气配比(nH2/nCO)为1.0~4.5的情况下,在中低温区域 (340~430 ℃)内具有较高的转化率和选择性。CO的转化率和CH4选择性随温度、压力升高而增大,随着nH2/nCO增加而增大。在nH2/nCO=3.0的情况下,可以通过升高压力、温度来提高CH4的产率。
(2) 建立双曲型本征动力学模型,采用正交设计法设计实验,通过最大继承法进行参数估值,获得动力学模型参数。统计检验表明,在实验条件下动力学模型是适宜的,所得到的实验结果可以用于甲烷化过程开发和反应器设计。
[1]李茂华,杨博,鹿毅.煤制天然气甲烷化催化剂及机理的研究进展[J].工业催化,2014,22(1):10-24.
[2]杨霞,田大勇,孙守理.ZrO2-Al2O3复合载体对镍基催化剂甲烷化性能的影响[J].化工进展,2014,33(3):673-678.
[3]胡雪娟,石秋杰,谌伟庆.Ni/ZrO2-Al2O3制备表征及催化性能的研究[J].化学研究与应用,2008,20(4):378-381.
[4]CAI M,WEN J,CHU W.Methanation of carbon dioxide on Ni/ZrO2-Al2O3catalysts:Effects of ZrO2promoter and preparation method of novel ZrO2-Al2O3carrier[J].Journal of Natural Gas Chemistry,2011,20(3):318-324.
[5]高晓庆,王永钊,李海涛.Mn 助剂对 Ni/r-A12O3催化剂CO2甲烷化性能的影响[J].分子催化,2011,25(1):49-54.
[6]王承学,龚杰.二氧化碳加氢甲烷化镍锰基催化剂的研究[J].天然气化工,2011,36(1):4-6.
[7]KOPYSCINSKI J,SCHILDHAUER T J,VOGEL F.Applying spatially resolved concentration and temperature measurements in a catalytic plate reactor for the kinetic study of CO methanation[J].Journal of Catalysis,2010,271(2):262-279.
[8]ALSTRUP I.On the kinetics of CO methanation on nickel surfaces[J].Journal of Catalysis,1995,151(1):216-225.
[9]JENS S,SØREN D,JOACHIM J,etal.Methanation of CO over nickel:Mechanism and kinetics at high H2/CO ratios[J].Journal of Physical Chemistry B,2004,109(6):2432-2438.
[10]ZHANG J,FATAH N,CAPELA S.Kinetic investigation of carbon monoxide hydrogenation under realistic conditions of methanation of biomass derived syngas[J].Fuel,2013,111(3):845-854.
[11]EFSTATHIOU A M,BENNETT C O.The CO/H2reaction on Rh/Al2O3:I.Steady-state and transient kinetics[J].Journal of Catalysis,1989,120(1):118-136.
[12]于广锁,于建国,孙杏元.KD-306型耐硫甲烷化催化剂本征动力学[J].华东理工大学学报(自然科学版),1999,25(1):19-22.
[13]于建国,于广锁.KD306耐硫甲烷化催化剂宏观动力学测试[J].华东理工大学学报(自然科学版),1997,23(5):510-514.
[14]于建国,于遵宏,孙杏元.SDM-1型耐硫甲烷化催化剂宏观动力学[J].化工学报,1994,45(1):120-124.
[15]HAYES R E,THOMAS W J,Hayes K E.A study of the nickel-catalyzed methanation reaction[J].Journal of Catalysis,1985,92 (2):312-326.
[16]SUGHRUE E L,BARTHOLOMEW C H.Kinetics of carbon monoxide methanation on nickel monolithic catalysts[J].Applied Catalysis,1982,2(4-5):239-256.
[17]KLOSE J,BAERNS M.Kinetics of the methanation of carbon monoxide on an alumina-supported nickel catalyst[J].Journal of Catalysis,1984,85(1):105-116.
[18]赵安民.合成气甲烷化镍基催化剂的研究[D].上海:华东理工大学.
[19]GAO J,WANG Y,PING Y A.Thermodynamic analysis of methanation reactions of carbon oxides for the production of synthetic natural gas[J].RSC Advances,2012,2(6):2358-2368.
[20]PARLIKKAD N R,CHAMBREY S,FONGARLAND P,etal.Modeling of fixed bed methanation reactor for syngas production:Operating window and performance characteristics[J].Fuel,2013,107(9):254-260.
[21]XU J,FROMENT G F.Methane steam reforming,methanation and water-gas shift:I.Intrinsic kinetics[J].AIChE Journal,1989,35(1):88-96.
Intrinsic Kinetics of CO Methanation over ZrO2/Al2O3Supported Ni-Based Catalyst
SHEN Ye-ting,ZHANG Hai-tao,FANG Ding-ye,LI Tao
(Engineering Research Center of the Large Scale Reactor Engineering and Technology,Ministry of Education,East China University of Science and Technology,Shanghai 200237,China)
CO methanation reaction over Ni-based complex-support catalyst for synthetic natural gas production was systematically investigated in a fixed-bed reactor.The influence of operating conditions on the methanation reaction was explored at reaction temperature of 250~440 ℃,pressure of 0.1~2.5 MPa andnH2/nCOof 1.0~4.5.The experimental results indicated that the conversion of CO and selectivity of CH4increased with the increase of reaction temperature and pressure.The highest conversion of CO was achieved at 340 ℃.WhennH2/nCO=3.0,a relatively high conversion of CO and high selectivity of CH4were obtained.The experimental data of intrinsic kinetics of CO methanantion over Ni-based catalyst were measured by orthogonal experiments.Hyperbolic type kinetic models were developed in terms of the reaction rates of CO2and CH4in form of the fugacity of the reactants.The parameters of the models were obtained through max inherit optimization.It was proved by residual analysis and statistical test that the kinetic models are reliable and acceptable.
intrinsic kinetics; CO methanation; ZrO2/Al2O3carrier; Ni-based catalyst
1006-3080(2016)04-0446-08
10.14135/j.cnki.1006-3080.2016.04.002
2015-11-06
沈叶婷(1989-),女,江苏南通人,硕士生,研究方向为碳一化工。E-mail:stylesyt@163.com
通信联系人:李涛,E-mail:tli@ecust.edu.cn
TQ032.41
A

