TiO2/MgFe2O4磁性纳米材料的制备及其光催化降解性能研究
王宇航
(陕西学前师范学院化学与化工系,陕西 西安 710100)
TiO2/MgFe2O4磁性纳米材料的制备及其光催化降解性能研究
王宇航
(陕西学前师范学院化学与化工系,陕西 西安 710100)
通过水热法制备MgFe2O4磁性纳米微球,并以其为核包覆TiO2制备新型磁性纳米光催化剂TiO2/MgFe2O4;利用扫描电镜(SEM)、透射电镜(TEM)、X-射线衍射仪(XRD)、振动样品磁强计(VSM)表征TiO2/MgFe2O4磁性纳米材料的形貌、结构、包覆情况和磁性,并考察了该催化剂在紫外灯照射下对甲基橙模拟废液的脱色效果。结果表明,TiO2/MgFe2O4是一种大粒径、中空结构且易于通过磁场回收的光催化剂,TiO2均匀地包覆在MgFe2O4微球表面,其粒径为300~400 nm,比饱和磁化强度高达45.0 emu ·g-1;以甲基橙水溶液为模拟废液,紫外光照射120 min后TiO2/MgFe2O4对甲基橙的脱色率达到96%。
TiO2/MgFe2O4;光催化降解性能;磁性;甲基橙;脱色率
掺杂镁的铁氧体磁性纳米微球(MgFe2O4)由于其特有的性质,在靶向给药[1]、气敏原件材料[2]、催化剂[3]、半导体存储介质[4]等领域有着广泛应用。目前,制备MgFe2O4磁性纳米微球(以下简称MgFe2O4微球)的方法有:共沉淀法[5]、溶胶-凝胶法[6]、超声化学法[7]。不同方法制备的MgFe2O4微球在形貌、结构、比饱和磁化强度、结晶形状等方面差别很大。近年来,一步水热法[8-10]以环保、省料优势制备粒径均一 、比饱和磁化强度大、分散性较好的MgFe2O4微球成了研究热点。
纳米TiO2具有无毒、抗化学和光腐蚀、光催化活性高等优点,是典型的光催化材料[11],在治理污水[12]、降解染料[13]等方面有较好的应用前景,但存在量子效率低等不足,因而限制了其应用。越来越多的科研工作者通过改性TiO2制备新型的TiO2光催化剂。将MgFe2O4微球与TiO2结合形成核-壳结构粒子,既保持了TiO2特有的光催化活性,在外界磁场刺激下,又可快速分离回收,有望用于制备高效稳定且可回收利用的新型光催化剂。
作者首先采用一步水热法制备MgFe2O4微球,然后通过水热高温使其结晶,最后水解将TiO2包覆在MgFe2O4微球外制备核-壳结构的新型磁性纳米光催化剂TiO2/MgFe2O4;利用扫描电镜(SEM)、透射电镜(TEM)、X-射线衍射仪(XRD)、振动样品磁强计(VSM)表征TiO2/MgFe2O4磁性纳米材料的形貌、结构、包覆情况和磁性,并考察了该催化剂在紫外光照射下对甲基橙模拟废液的脱色效果。
1 实验
1.1 试剂与仪器
氯化铁(FeCl3·6H2O)、氯化镁(MgCl2·6H2O)、尿素、乙醇、柠檬酸钠、钛酸丁酯(TBOT)、聚乙烯吡咯烷酮(PVP),均为分析纯。
荷兰Philips PW3040/60型X-射线衍射仪;德国JSM-6700F型扫描电子显微镜;日本Hitachi H-600型透射电子显微镜;美国湖滨7307型振动样品磁强计;日本岛津UV-2501PC/2550型紫外可见分光光度计。
1.2 TiO2/MgFe2O4磁性纳米材料的制备
首先采用一步水热法制备MgFe2O4微球:称取FeCl3·6H2O 1.0 mmol、MgCl2·6H2O 0.7 mmol、柠檬酸钠适量、尿素适量于80 mL蒸馏水中;待完全溶解后置于装有聚四氟乙烯内衬的反应釜中,200 ℃下反应12 h,得到MgFe2O4微球,用乙醇和蒸馏水反复冲洗。
然后取2.0 mg MgFe2O4微球溶解在200 mL乙醇与0.02 g PVP混合溶液中,超声30 min至完全分散,加入2.0 mL TBOT室温水解;于水热釜中160 ℃下反应24 h,得到TiO2/MgFe2O4磁性纳米材料,用磁铁分离,清洗后烘干保存。
1.3 光催化降解性能评价
以100 mL初始浓度为100 mg·L-1的甲基橙水溶液作为模拟废液。将装有100 mL模拟废液的三口瓶固定于紫外灯下,加入新型磁性纳米光催化剂TiO2/MgFe2O4,待其在黑暗环境中吸附平衡后,打开紫外灯,机械搅拌,每隔一定时间从上口取上清液10 mL,离心,取上清液5 mL摇匀,用紫外可见分光光度计测定490 nm处吸光度A(初始吸光度用A0表示),以脱色率(D)评价降解效果:
2 结果与讨论
2.1 MgFe2O4微球中空结构形成分析
为了更好地吸附污染物,一步水热法制备TiO2/MgFe2O4磁性纳米材料是利用尿素作为碱源以得到中空结构的微球。当体系中加入尿素时,其在高于33 ℃时会缓慢分解,产生CO2和NH3,其中NH3和水结合提供了碱性环境,而CO2则在体系中形成小气泡,这些气泡具有较大的比表面积,可使MgFe2O4纳米晶粒在其表面聚集,形成初级松散的微球。所以说,反应过程中气泡的存在对中空结构的形成起着很重要的作用。
Ostwald熟化作用[4-15]是MgFe2O4微球中空致孔机理的重要依据。反应分为2步:一是碱性环境下初级松散微球的形成;二是微球从松散结构向良好结晶形态的中空结构的转换。体系首先生成无定形的纳米颗粒,随后纳米颗粒在高比表面能的气泡表面成核以降低体系比表面能,其中较低浓度的Fe3+可以保证微球的松散结构。而微球内部的纳米颗粒比表面能较高,受到Ostwald熟化作用的驱动,纳米颗粒会在微球外表面重新结晶,因此微球会呈现中空结构。
2.2 SEM分析与TEM分析(图1)
从图1a可以看出,水热法制得的MgFe2O4微球粒径均一且都在200~220 nm范围内;微球表面并不光滑,说明微球从松散结构向良好结晶形态转变是一步一步堆积得到的,与Ostwald熟化作用分析结论一致。从图1b可以看出,TiO2已成功包覆在MgFe2O4微球表面,粒径明显增大(300~400 nm)。从图1c、d可以看出,MgFe2O4微球是中空结构,TiO2确实已成功包覆在MgFe2O4微球表面上;TiO2/MgFe2O4纳米材料磁性高,自然条件下容易发生自吸导致团聚(图1d)。

a.MgFe2O4的SEM照片 b.TiO2/MgFe2O4的SEM照片 c,d.TiO2/MgFe2O4的TEM照片
图1 样品的SEM和TEM照片
Fig.1 SEM and TEM images of the samples
2.3 XRD分析(图2)

a.MgFe2O4 b.TiO2/MgFe2O4(2.0 mL TBOT) c.TiO2/MgFe2O4(1.0 mL TBOT)
图2 样品的XRD图谱
Fig.2 XRD patterns of the samples
为了进一步分析样品的晶形结构,将样品的XRD图谱与标准晶格参数理论值对比发现,TiO2/MgFe2O4光催化剂的结构并没有发生改变。从图2a可以看出,(220)晶面、(311)晶面、(400)晶面、(511)晶面和(204)晶面衍射峰与尖晶石型Fe3O4(JCPDS No.19-629)衍射峰完全一致。这是因为,镁掺杂量较低,所以体系的晶型基本上是尖晶石型Fe3O4。从图2b、c可以看出,(101)晶面、(200)晶面、(105)晶面、(220)晶面和(215)晶面衍射峰与锐钛矿型TiO2(JCPDS 21-1272)衍射峰吻合。当TiO2的复合量较少时(图1c),特征峰不明显,且TiO2的晶相不完整,结晶度较低;随着TiO2复合量的增加,TiO2的特征峰强度增强(图1b),且光催化剂TiO2/MgFe2O4中MgFe2O4的各个晶面的衍射峰强度减弱,结晶度降低。表明,TiO2的存在抑制了尖晶石型MgFe2O4晶体的生长。
2.4 VSM分析(图3)
从图3可以看出,MgFe2O4微球和TiO2/MgFe2O4磁性纳米材料均具有较高的比饱和磁化强度,分别为60.0 emu·g-1和45.0 emu·g-1,可能是因为大粒径微球是由纳米颗粒堆积组成的二次结构所致。而TiO2/MgFe2O4磁性纳米材料因为体系外包覆了一层没有磁性的TiO2外壳,其比饱和磁化强度较MgFe2O4微球低。从图3还可以看出,2条曲线所对应的磁矫顽力几乎都可以忽略,表明MgFe2O4微球和TiO2/MgFe2O4磁性纳米材料都具备超顺磁特性。
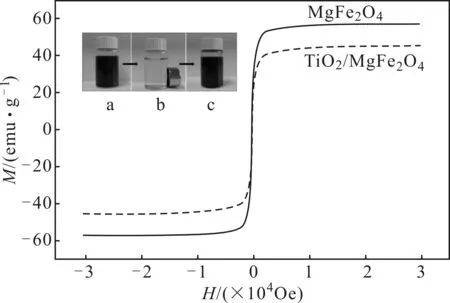
图3 样品的磁滞回线
Fig.3 Magnetic hysteresis curves of the samples
与其它方法相比[16-17],一步水热法制备的MgFe2O4微球和TiO2/MgFe2O4磁性纳米材料不但具有较高的比饱和磁化强度,同时还具有良好的水分散性。在没有外界磁场刺激的情况下,小瓶中的溶液呈均一黑色液态(图3a);当添加外界磁场后,磁性微球能够快速从水中分离,水呈无色透明状态(图3b),表明所有磁性微球均具备较好的磁响应性;当外界磁场消失时,轻微晃动小瓶,其中的溶液呈现均一黑色状态(图3c),表明磁性微球具备良好的水分散性。
2.5 TiO2/MgFe2O4磁性纳米材料的光催化降解性能
相同用量的自制的TiO2/MgFe2O4磁性纳米材料与P25(商品TiO2)在紫外灯照射下对甲基橙模拟废液的脱色率随光照时间的变化曲线如图4所示。
从图4可以看出,在相同用量和光照时间(120 min)下,P25对甲基橙模拟废液的脱色率达到92%,而TiO2/MgFe2O4磁性纳米材料对甲基橙模拟废液的脱色率达到96%。虽然相同质量的TiO2/MgFe2O4磁性纳米材料中所含活性TiO2的量低于P25中活性TiO2的量,但其催化效率却高,这可能与掺杂的Mg2+半径有关。在TiO2晶体中,Ti4+的O2-配位数为6,Ti4+的半径为74.5 pm,而Fe3+和Mg2+的半径分别为69 pm和72 pm,均与Ti4+半径相近,因而Fe3+和Mg2+容易取代TiO2晶体中的Ti4+或者进入晶格间隙。而Mg2+的掺杂会给晶体带来额外的电子,导致掺杂部位的束缚空穴,从而使电子和空穴得到有效的分离,进一步提高光催化活性[18]。

图4 脱色率随光照时间的变化曲线
Fig.4 Change curves of decolorization rate with irradiation time
除此之外,自制的TiO2/MgFe2O4磁性纳米材料具有可回收性。当光催化反应完成后,在外界磁场的刺激下,利用TiO2/MgFe2O4高的比饱和磁化强度便可分离回收甲基橙脱色溶液中的TiO2/MgFe2O4磁性纳米光催化剂,从而达到重复使用的目的。
3 结论
通过一步水热法制备了新型磁性纳米光催化剂TiO2/MgFe2O4,用SEM、TEM、XRD、VSM 分析了该磁性纳米材料的形貌、结构、包覆情况和磁性。结果表明,TiO2均匀地包覆在MgFe2O4微球表面,TiO2/MgFe2O4磁性纳米材料粒径为300~400 nm,比饱和磁化强度高达45.0 emu·g-1。镁的掺杂使材料的光催化活性提高,紫外照射120 min后对甲基橙模拟废液的脱色率达到96%。TiO2/MgFe2O4具有良好的磁性,易于通过磁场进行分离回收,是一种大粒径、中空结构且可重复使用的新型光催化剂。
[1] WASEEM S,ALI Z,BIBI M,et al.Magnetic nanobeads:synthesis and application in biomedicine[J].Nanomedicine Journal,2016,3(3):147-154.
[2] LIU Y L,LIU Z M,YANG Y,et al.Simple synthesis of MgFe2O4nanoparticles as gas sensing materials[J].Sensors and Actuators B:Chemical,2005,107(2):600-604.
[3] ZHOU H Y,HU L,WAN J Z,et al.Microwave-enhanced catalytic degradation ofp-nitrophenol in soil using MgFe2O4[J].Chemical Engineering Journal,2016,284:54-60.
[4] NABIYOUNI G,GHANBARI D,GHASEMI J,et al.Microwave-assisted synthesis of MgFe2O4-ZnO nanocomposite and its photo-catalyst investigation in methyl orange degradation[J].Journal of Nanostructures,2015,5(3):289-295.
[5] CHEN Q,RONDINONE A J,CHAKOUMAKOS B C,et al.Synthesis of superparamagnetic MgFe2O4nanoparticles by coprecipitation[J].Journal of Magnetism and Magnetic Materials,1999,194(1/2/3):1-7.
[6] 王清成,王雪梅,庄稼.MgFe2O4/Fe2O3纳米粉的溶胶-凝胶法合成及电磁波吸收特性[J].功能材料,2005,36(12):1839-1841.
[7] 徐波,王树林,李生娟,等.超声强化合成MgFe2O4纳米颗粒及其机理研究[J].物理学报,2012,61(3):124-128.
[8] GHANBARI D,SALAVATI-NIASARI M.Hydrothermal synthesis of different morphologies of MgFe2O4and magnetic cellulose acetate nanocomposite[J].Korean Journal of Chemical Engineering,2015,32(5):903-910.
[9] KIM J,LEE D.Core-shell metal-ceramic microstructures:mechanism of hydrothermal formation and properties as catalyst materials[J].Chemistry of Materials,2016,28(8):2786-2794.
[10] SAEZ-PUCHE R,FERNANDEZ M J T,BLANCO-GUTIÉR-REZ V,et al.Ferrites nanoparticles MFe2O4(M=Ni and Zn):hydrothermal synthesis and magnetic properties[J].Boletín de la Sociedad Espaola de Cerámicay Vidrio,2008,47(3):133-137.
[11] GREEN I X,TANG W,NEUROCK M,et al.Spectroscopic observation of dual catalytic sites during oxidation of CO on a Au/TiO2catalyst[J].Science,2011,333(6043):736-739.
[12] CHOI H,STATHATOS E,DIONYSIOU D D.Photocatalytic TiO2films and membranes for the development of efficient wastewater treatment and reuse systems[J].Desalination,2007,202(1):199-206.
[13] WEI B L,CHEN Y P,YE M J,et al.Enhanced degradation of gaseous xylene using surface acidized TiO2catalyst with non-thermal plasmas[J].Plasma Chemistry and Plasma Processing,2015,35(1):173-186.
[14] VOORHEES P W.The theory of Ostwald ripening[J].Journal of Statistical Physics,1985,38(1/2):231-252.
[15] LIU B,ZENG H C.Symmetric and asymmetric Ostwald ripening in the fabrication of homogeneous core-shell semiconductors[J].Small,2005,1(5):566-571.
[16] GHELEV C,KOUTZAROVA T,KOLEV S,et al.Magnetic pro-perties of nanosized MgFe2O4powders prepared by auto-combustion[J].Journal of Physics:Conference Series,2012,356(1):597-604.
[17] 唐宏志,徐波,王树林,等.MgFe2O4纳米颗粒制备及其电磁性能研究[J].功能材料,2013,44(6):776-779.
[18] 陈建华,王晓林,张培新,等.纳米二氧化钛粉末离子掺杂研究[J].广西大学学报(自然科学版),2005,30(1):44-50.
Preparation and Photocatalytic Degradation Performance of Magnetic TiO2/MgFe2O4Nanocomposites
WANG Yu-hang
(DepartmentofChemistryandChemicalEngineering,ShaanxiXueqianNormalUniversity,Xi′an710100,China)
In this paper,magnetic MgFe2O4nanoparticles were successfully prepared through a hydrothermal method,then MgFe2O4nanoparticles were coated by TiO2to prepare a novel magnetic nano-photocatalyst TiO2/MgFe2O4.The morphology,structure,coating condition and magnetism of the photocatalyst were characterized by SEM,TEM,XRD,and VSM analysis.The decolorization effect of the photocatalyst against methyl orange simulated wastewater under UV irradiation was investigated.Results indicated that,TiO2/MgFe2O4was one kind of photocatalyst with larger size,hollow structure and recyclable by magnetic fields.TiO2dispersed uniformly and enwrapped the core MgFe2O4,the particle size of composite TiO2/MgFe2O4was 300~400 nm,and the saturation magnetization was 45.0 emu ·g-1.Using methyl orange aqueous solution as a simulated wastewater,the photocatalytic decolorization rate was up to 96% under UV irradiation for 120 min.
TiO2/MgFe2O4;photocatalytic degradation performance;magnetism;methyl orange;decolorization rate
陕西省基础教育科研“十二五”规划2014年度课题资助项目(SGH140716),陕西学前师范学院2016年度校级科研基金资助项目(2016YBKJ069)
2016-09-06
王宇航(1986-),女,陕西咸阳人,讲师,在读博士,研究方向:无机功能材料,E-mail:yuhangwang0912@163.com。
10.3969/j.issn.1672-5425.2016.12.011
王宇航.TiO2/MgFe2O4磁性纳米材料的制备及其光催化降解性能研究[J].化学与生物工程,2016,33(12):51-54.
O 614
A
1672-5425(2016)12-0051-04

