高浓度过氧乙酸的制备
马洪宇, 封禄田, 张晓青, 魏瀚林
高浓度过氧乙酸的制备
马洪宇, 封禄田, 张晓青, 魏瀚林
(沈阳化工大学 应用化学学院, 辽宁 沈阳 110142)
高浓度过氧乙酸是强氧化剂,用途广泛,但是化学性质不稳定,易分解,易爆炸。介绍了高浓度过氧乙酸的制备方法。制备高浓度的过氧乙酸首先需要得到高浓度的过氧化氢。通过制备高浓度的过氧化氢,得到了适宜的优化工艺:在真空度为10 mmHg, 在恒温为85 ℃,以2 s/滴的滴加速度,提纯2次即可得到70%的过氧化氢。通过制备高浓度过氧乙酸制备的条件选择性试验,考察了反应物料比、催化剂用量、温度等过氧乙酸浓度的影响。制备高浓度过氧乙酸的适宜条件为:70%的过氧化氢与冰乙酸质量比为4∶5时,滴加总质量为3%的浓硫酸,密封搅拌1 h后,避光静置12 h后,过氧乙酸的含量最大为40.8%。提出了高浓度过氧乙酸制备、贮存和使用的适宜条件。
高浓度过氧化氢;安全制备;高浓度过氧乙酸
过氧乙酸(peroxyacetic acid) 又名过醋酸[1], 因为它是通过冰醋酸的氧化而形成的过氧基分子而得名, 它是在1902年首次被合成的, 其分子式为 C2H4O, 相对分子质量为 76.051 8。通过研究表明, 它不仅是一种广谱、高效、速效、廉价的灭菌剂, 而且还是化工工业生产中的良好氧化剂。过氧乙酸不仅被广泛使用在医疗器械清洗、灭菌、消毒而且在灾区、隔离区、疫区等地的消毒和预防性消毒中被使用[2]。
过氧乙酸的液体是无色透明,气味是刺激性酸味。它容易挥发, 在水和有机溶剂中易溶。熔点是 0.1 ℃, 沸点是110 ℃, 比重为 1.226。腐蚀性很强, 具有漂白作用。它的化学性质不是很稳定。过氧乙酸遇到重金属离子、大量热、大多数有机物、强碱等易分解。高浓度溶液的质量分数大于 45%时,如果遇到剧烈的碰撞或加热即可能发生爆炸( 闪点 40.5 ℃)。由于市场销售的过氧乙酸浓度一般在 20%左右,主要用于消毒,因此不会发生爆炸的危险。过氧乙酸是一个强氧化剂,尤其是浓度高的的过氧乙酸。因为它是具有良好的氧化性、反应副产物较少等优点,现在已经成为有机合成和药物合成中特别重要的化学氧化剂。但是过氧乙酸也存在一些缺点,比如稳定性不好,温度越高、浓度越高时他就越不稳定,而且它的贮存的条件也是问题,高浓度过氧乙酸不宜长期储存,所以要使用高浓度过氧乙酸时一定要现配现用为好[3]。到目前为止,国内市场销售过氧乙酸含量主要多在20%左右,很少有销售高浓度(35%~40%)过氧乙酸。本论文运用冰乙酸和浓度为70%的过氧化氢反应,得到浓度为 40%的过氧乙酸。实验方法主要分为两步:第一步为制备高浓度过氧化氢;第二步为高浓度过氧乙酸的合成。
1 高浓度过氧化氢制备
要合成高浓度的过氧乙酸,第一要做的是制备高浓度的过氧化氢,而现在30%浓度的过氧化氢作为主要产品在国内各大市场上销售,百分之七八十浓度的过氧化氢在市场上是很难购买到的,能购买的产品价格也是非常昂贵。因为当过氧化氢的浓度超过74%时,过氧化氢遇到重金属或者受热就容易发生爆炸的危险[4]。所以在制备高浓度过氧化氢时一定要特别注意实验安全。
1.1 高浓度过氧化氢的工作原理和试验方法
它的工作原理如图1所示。装置图由恒压滴液漏斗、蛇形冷凝管、克氏蒸馏头、圆底烧瓶、直形冷凝管、真空尾接管以及空气干燥塔等玻璃仪器组成。蛇形冷凝管连接恒温水槽,分别在恒温水槽中设定温度为65、75、85 ℃。使蛇形冷凝管中保持温度的稳定。右边的空气干燥塔的接入旋片式真空泵,使体系的真空度维持在10 mmHg。恒压滴液漏斗放入30%的过氧化氢,以2 s/滴的滴速滴入蛇形冷凝管,通过蛇形冷凝管的水产生部分气化,水蒸气通过克氏蒸馏头被抽进直形冷凝管,进入右边的圆底烧瓶。左边的圆底烧瓶得到的是提纯后高浓度的过氧化氢。在不同的温度下,分别多次提纯得到最终高浓度的过氧化氢。
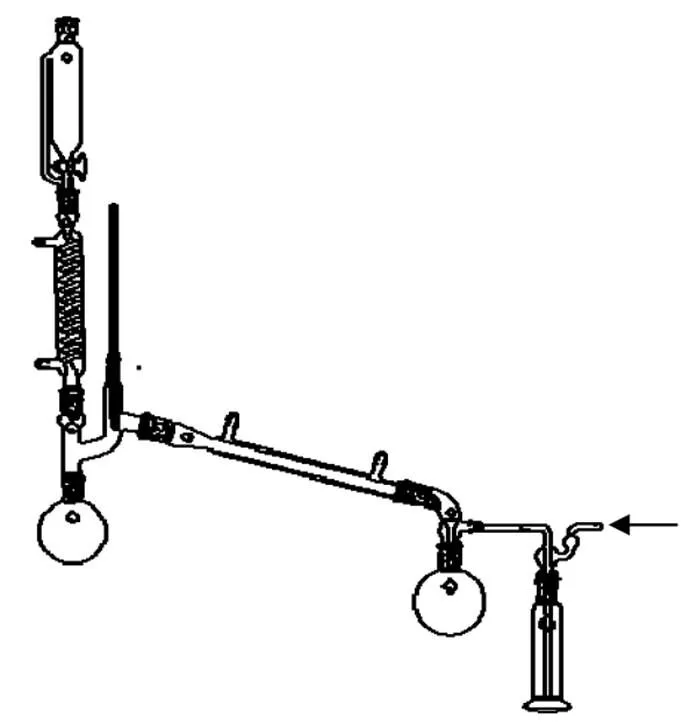
图1 制备高浓度过氧化氢的装置图
1.2 结果与讨论
经过多次的的实验得到结果如表1。

表1 过氧化氢浓度与次数关系
由表1可知在蛇形冷凝管中的温度为65 ℃,需要提纯的次数为5次,而且时间较长。温度为75℃,需要提纯的次数为3次,时间次之。温度为85℃,需要提纯的次数为2次,时间最短。而且操作过程中安全性很好。所以,制备高浓度的过氧化氢的适宜的条件为:在恒温为85 ℃,以2 s/滴的滴加速度,提纯2次即可得到70%的过氧化氢。
2 过氧乙酸的合成与制备
2.1 过氧乙酸合成方法的概述
过氧乙酸的合成方法主要以下几种:
(1)过氧化氢和乙酸酐反应
(CH3CO)2O + H2O2—→ CH3COOOH + CH3COOH
该方法生成的过氧乙酸中含有不少乙酸,但却不含有水,因此可以稳定地使用和保存。但是此方法反应是放出的热量比较多而且剧烈,所以操作时一定要特别注意安全。
(2)过氧化氢和乙酸的反应
CH3COOH + H2O2—→ CH3COOOH + H2O
该合成的方法生成的过氧乙酸过程时间较长,反应较温和,可以预先制备和贮存。
(3)乙醛的氧化
CH3CHO + O2—→ CH3COOOH
该合成方法的反应过程比较复杂,如果想要得到浓度过氧乙酸的收率,需加入合适的催化剂促进反应[5]。反应需要注意实验安全。
综上所述,本文采用了第二种方法过氧化氢和乙酸即双氧水法。由于第一种方法和第三种方法反应放热剧烈,反应复杂。由于双氧水法工艺简单,故在过氧乙酸的实际应用中,其制造方法以双氧水法为主。所以我们采用第二种方法。
2.2 试验方法
称取40 g浓缩的后的70%过氧化氢放入250 mL的烧杯中,分别加入30, 40, 50, 60 g的冰乙酸。将其放入磁力搅拌中,边搅拌边滴加两者总质量的3%的浓硫酸。滴加完毕,密封搅拌1 h后避光放置4, 8, 12, 16 h分别检测过氧乙酸的含量。并按文献[6]检测过氧乙酸的含量公式如下:
过氧乙酸样品的质量分数为:
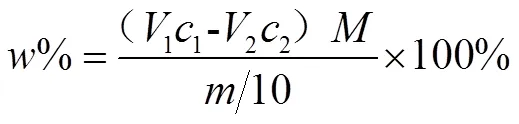
式中:—自制过氧乙酸的质量分数的数值,%;
1— 硫代硫酸钠标准滴定溶液浓度的准确数值,mol/L
1—硫代硫酸钠标准溶液的体积数值,mL;
2— 高锰酸钾标准滴定溶液浓度的准确数值,mol/L
2—高锰酸钾标准溶液的体积的数值,mL;
—检测试样的质量的数值,g;
—过氧乙酸毫摩尔质量二分之一的数值,即= 0.038 03。
最终的检测结果是两次平行检测结果的算术平均值,而且这两次平行检测结果的绝对差值不大于0.3%。
2.3 结果与讨论
2.3.1 冰乙酸的量对过氧乙酸含量的影响
冰乙酸和过氧化氢反应制备过氧乙酸时,按上述实验分别加料搅拌结束后静置12 h后,测定过氧乙酸的含量如图1所示来确定适宜的反应物料比。
由图1可知,由于冰乙酸和过氧化氢的反应是可逆反应,在保证过量过氧化氢且量不变的情况下,随着冰乙酸量的增加,过氧乙酸的含量的增加并不呈线性。由图可知,当冰乙酸为50 g即过氧化氢与冰乙酸质量比为4∶5时,过氧乙酸的含量最大。

图2 冰乙酸的量对过氧乙酸含量的影响
2.3.2 时间对过氧乙酸含量的影响
冰乙酸和过氧化氢反应制备过氧乙酸时,按70%过氧乙酸的质量40 g和冰乙酸的质量50 g滴加1 mL的浓H2SO4搅拌1 h结束后,分别取静置4, 8, 12, 16 h的过氧乙酸样品测定过氧乙酸的含量。如图2所示来确定适宜的反应时间。
由图2可知,由于冰乙酸和过氧化氢的反应是可逆反应,在确定反应物的物料比保持不变的情况下,随着反应时间的增加,过氧乙酸的含量的增加而增加。当避光静置时间12 h后过氧乙酸的含量保持在40.8%。
3 结 论
(1)制备高浓度过氧化氢的适宜条件是:在真空度为10 mmHg, 在恒温为85 ℃,以2 s/滴的滴加速度,提纯2次即可得到70%的过氧化氢。

图3 时间对过氧乙酸含量的影响
(2)制备高浓度过氧乙酸的适宜条件为:70%的过氧化氢与冰乙酸质量比为4∶5时,滴加总质量为3%的浓硫酸,密封搅拌1 h后,避光静置12 h后,过氧乙酸的含量最大为40.8%。
[1]刘吉起, 李书建, 王竫. 过氧乙酸的性质、制备和应用[J]. 河南预防医学杂志, 2004, 03: 171-173.
[2]韩双战,赵彦丽. 过氧乙酸的合成和应用[J].河北化工, 2008, 06: 41-43.
[3] 姚菊英, 吴玉萍, 夏克坚. 实验室高浓度过氧乙酸的制备[J]. 江西教育学院学报, 2007, 03: 26-28.
[4]王东升, 卓超, 吴达俊. 过氧乙酸的制备及其在药物合成中的应[J]. 合成化学, 2000, 01: 22-28+33.
[5]于国庆. 高浓度过氧乙酸的实验室制备方法[J]. 天津化工, 2012, 04: 41-43.
[6]GB 19108-2003, 过氧乙酸溶液过氧乙酸含量的测定[S]
Preparation of High Concentration Peracetic Acid
,,,
(Shenyang University of Chemical Technology, Liaoning Shenyang 110142,China)
High concentration of peracetic acid is a strong oxidant, itis widely used, but its chemical nature is unstable. In this paper, the preparation method of peracetic acid with high concentration was introduced. At first, in order to prepare high concentration peracetic acid, high concentration hydrogen peroxide need be prepared. Through analysis on the preparation process of high concentration hydrogen peroxide, the optimum process condition was obtained as follows: constant temperature 85 ° C , vacuum degree 10 mmHg, dropping rate 2s/drop , purifying times 2.Under above conditions, 70% high concentration hydrogen peroxide can be prepared. The effect of the ratio of reactants, the amount of catalyst and the temperature on the concentration of prepared peracetic acid was investigated by the conditional selectivity test. The optimum conditions for the preparation of peracetic acid with high concentration were determined as follows: mass ratio of 70% hydrogen peroxide and glacial acetic acid 4: 5, concentrated sulfuric acid dosage 3%, sealing and agitating time 1 h, standing time away from light 12 h.Under above conditions, the maximum content of prepared peracetic acid can reach to 40.8%. The suitable conditions for the preparation, storage and use of peracetic acid with high concentration were put forward.
high concentration hydrogen peroxide; safe preparation; high concentration peracetic acid
2016-12-01
马洪宇(1990-),男,研究生,辽宁大连人,2017毕业于沈阳化工大学化学专业,研究方向:精细化学品合成。
封禄田(1961-),男,教授,博士,研究方向:精细化学品合成。
TQ 111
A
1004-0935(2017)01-0030-03

