TiO2纳米管阵列的制备及光催化活性
胡亚微, 王晓芳, 柯 钰
(陕西科技大学 化学与化工学院, 陕西 西安 710021)
0 引言
TiO2是一种新型多功能无机半导体材料,由于其具有无毒害性、物理和化学性质稳定等优良的特性,在光电材料、纳米材料、光催化材料以及无机抗菌材料方面都有非常广泛的应用[1-4].与其它形态的纳米TiO2相比,TiO2纳米管具有更大的比表面积和更强的吸附能力,而且高度有序的纳米管阵列取向性好,更易于电子的传输,减少光生电子-空穴对的复合,使得TiO2纳米管在光催化降解有机污染物方面被广泛地研究[5-9].然而,目前的光催化剂多为粉末,难以回收,不利于其重复使用.因此,发展易回收的TiO2纳米管光催化剂成为备受关注的焦点.
此外,由于TiO2光催化剂带隙较宽(3.2 eV),只能吸收波长小于387 nm的紫外辐射,不能充分利用太阳光.因此,为了扩大TiO2的光谱响应范围,许多研究是通过掺杂或者与窄带系半导体复合提高其光催化性能.胡军成等[10]采用光化学还原法制备了Au-Ag共掺杂的TiO2光催化材料,由于共掺杂的协同效应,其紫外可见光谱的吸收带比纯的TiO2的吸收带明显红移.VanManh Nguyen等[11]采用脉冲电沉积法和SILAR法制备出CdS/ZnSe/TiO2三元复合光催化剂,通过窄带系半导体的共敏化作用,增加了其可见光下的光谱响应范围.然而单独研究二氧化钛纳米管可见光下光催化性能的研究相对较少.
近年来,制备TiO2纳米管的方法有很多种,如模板合成法、高温水解法(水热法)和电化学法等[12,13].采用阳极氧化法制备的二氧化钛纳米管直接生长在钛基体上,结合牢固,并且制备的二氧化钛纳米管结构有序排列,使其在光催化方面具有更加优良的特征[14,15].基于此,本文通过阳极氧化法制备TiO2纳米管阵列,并对其可见光下的光催化性能进行了研究.
1 实验部分
1.1 纳米TiO2的制备
1.1.1 基片预处理
用蒸馏水冲洗钛箔试样片(纯度99.5% ,尺寸1.5 cm×1 cm×0.3 mm),并用化学抛光液浸泡钛箔试样片1 min后,去离子水清洗,室温晾干备用.化学抛光液是体积比为1∶3∶10的HF、HNO3和蒸馏水的混合溶液[16].
1.1.2 TiO2纳米管阵列的制备
选用恒压直流阳极氧化法,以处理后的钛箔试样片为阳极,Pt电极为阴极,0.5 wt%的NH4F和2 vol% H2O的乙二醇混合液为电解液,在40 V电压下,两电极间距为2 cm,氧化1 h、3 h和5 h.整个阳极氧化过程在室温(25 ℃左右)下进行,且伴随磁力搅拌.将阳极氧化后的试样用去离子水冲洗、冷风吹干后放于马弗炉中,以5 ℃/min分别升温至450 ℃和550 ℃后保温4 h,最后随炉冷却至室温,制得TiO2纳米管阵列.
1.2 表征和测试
采用X射线粉末衍射仪(XRD,D/Max-3c型,Rigaku,铜靶,电压40 kV,电流35 mA,扫描范围:20 °~70 °)对样品进行物相与结构分析;采用扫描电子显微镜(SEM,JSM-6700F,JEOL,加速电压15 kV,电流10μA)对样品进行形貌分析,采用紫外-可见漫反射光谱仪(Lambda 950, PerkinElmer)测定样品的吸收光谱进行.
使用上海佳鹏科技有限公司生产的CHX系列光化学反应仪对样品的光催化性能进行测定,采用500 W的氙灯作为光源,并安装滤光片以获得λ>420 nm范围的光.光照前,将制得的样品浸入到5 mL 5 mg/L的亚甲基蓝溶液中,并以商用P25粉(德国赛,其中锐钛矿相占80%,金红石相占20%)作为对比,在黑暗下静置30 min使其达到吸附-脱附平衡.随后采用紫外-可见分光光度计(UV-2100型,Shimadzu),每隔30 min光照后测量其吸收曲线并记录其在λ= 664 nm处的吸光度.通过Ct/C0来评价对亚甲基蓝(MB)的光降解程度.Ct代表时间t时MB的浓度,C0代表MB的初始浓度.
2 结果与讨论
对在40 V电压下氧化不同时间得到的样品进行表观分析,1 h获得的样品表面成膜差,几乎没有氧化层形成;3 h获得的样品表面形成灰白色膜层,并且颜色均匀;5 h获得的样品表面形成暗灰色膜层,但在后期试验中该膜层由于较厚易于从基体表面脱落.因此选择氧化时间为3 h,且以下结果分析均为氧化时间为3 h所得样品测试所得.
2.1 XRD分析
图1为不同煅烧温度所制备TiO2纳米管阵列和p25粉末的XRD图谱.从图1可以看出,所制备样品的XRD谱图中不仅有TiO2的衍射峰而且含有Ti的衍射峰.Ti的衍射峰来自于钛基体.450 ℃所制备样品的TiO2衍射峰为锐钛矿结构,与标准数据文件(JCPDS卡文件,21-1272)一致.而550 ℃所得样品TiO2衍射峰主要为锐钛矿(A)结构,同时在2θ为27.5 °处有个微弱的小峰,表明有少量的金红石相(R)生成(JCPDS卡文件,21-1276).商用P25的衍射峰主要为锐钛矿结构的TiO2和少量的金红石结构,与商业提供的数据一致.
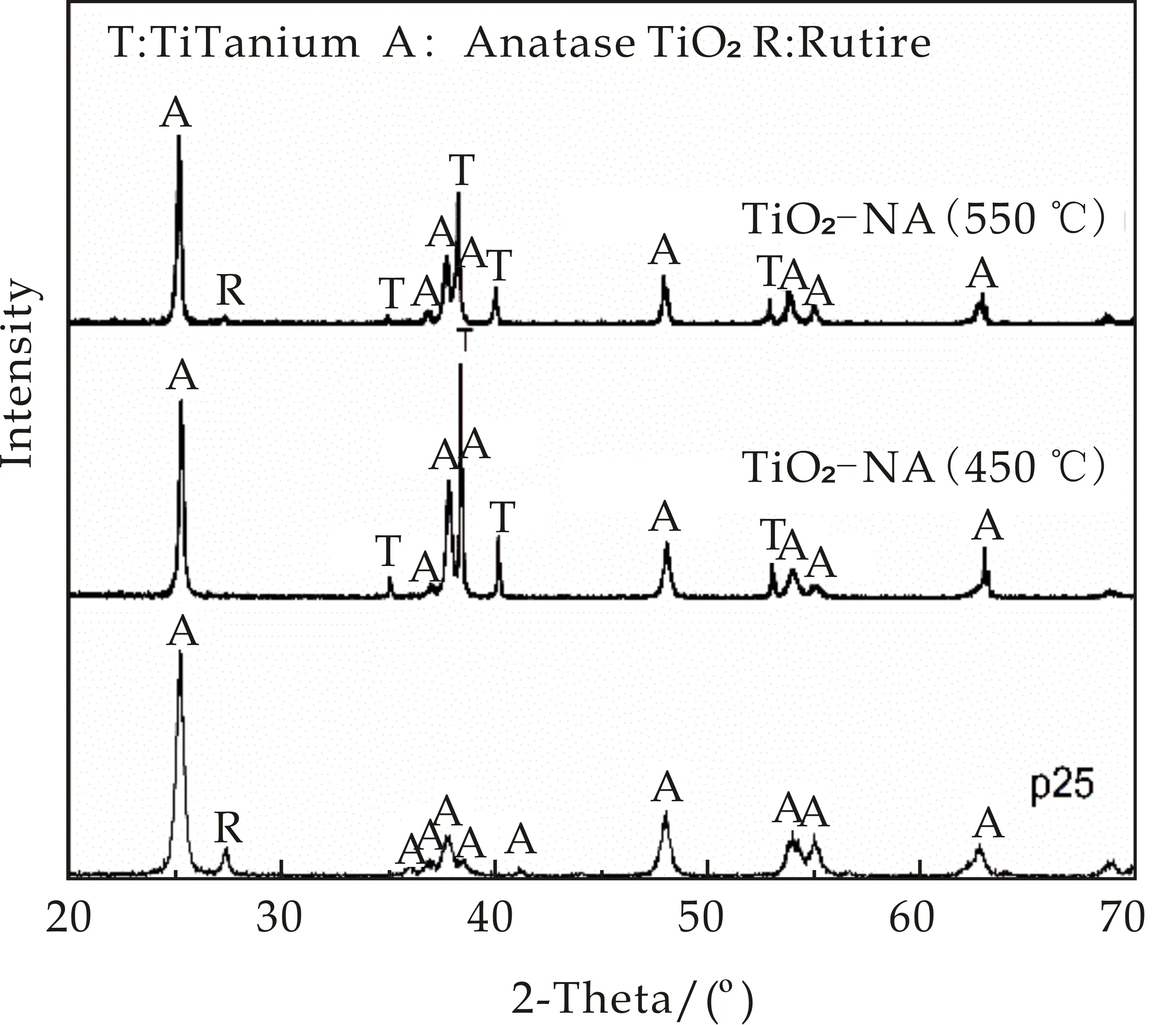
图1 TiO2纳米管阵列的XRD图
2.2 SEM分析
图2(a)~(c)为550 ℃煅烧所得TiO2纳米管阵列表面和断面SEM图.可以观测到所制备的样品是TiO2纳米管阵列.TiO2纳米管阵列排列整齐,并且管径比较均匀,管径大约为50 nm左右,管长约为6 um.图2(d)为450 ℃煅烧所得TiO2纳米管阵列表面SEM图,其形貌和550 ℃所得样品没有显著区别.商用P25粉末的SEM图(图2(e)所示)结果显示TiO2平均粒径为30 nm左右,但团聚比较严重.

(a) TiO2(550 ℃)表面

(b) TiO2(550 ℃)断面

(c) TiO2(550 ℃)裂缝

(d) TiO2(450 ℃)表面

(e) P25表面图2 TiO2 纳米管阵列和P25的SEM照片
2.3 光催化性能分析
图3为亚甲基蓝的光催化降解图,其中 “-30 min”代表染料在黑暗下静置30 min使其达到吸附-脱附平衡.在没有催化剂的情况下,纯染料在可见光下降解很少(如图3(a)所示),可以忽略不计;而以商用P25 TiO2粉末作为光催化剂在可见光下降解染料分子时,黑暗下平衡30 min后亚甲基蓝的去除率约13%,这是由于P25 TiO2粉末对染料的吸附作用,而在随后的可见光照射下对亚甲基蓝几乎没有降解(如图3(b)所示),说明P25在可见光下几乎没有光催化活性.
而对于在450 ℃和550 ℃煅烧所制备的TiO2纳米管阵列而言,其对亚甲基蓝也具有一定的吸附作用,黑暗下平衡30 min后,其对亚甲基蓝的吸附率基本相同,约为22%,其吸附率明显高于商用P25 TiO2粉末.这是因为所制备的TiO2纳米管阵列的比表面积大,有利于有机染料的吸附.并随着可见光照射时间的延长,亚甲基蓝在664 nm 处的吸收峰强度逐渐降低,光照120 min后,450 ℃所制备的样品对亚甲基蓝的降解率可达35.8%,550 ℃所制备的样品对亚甲基蓝的降解率可达52%,表明TiO2纳米管阵列在可见光下具有较好的光催化性能,而且550 ℃所制备的样品的光催化活性优于450 ℃所制备的样品.
同时,将550 ℃所制备的TiO2纳米管阵列从基体上剥离,研究其光催化活性,结果如图3(e)所示,光照120 min后,剥离得到的纳米管对亚甲基蓝的降解率大约为36.6%,低于TiO2纳米管阵列的光催化活性.

(a) 纯染料
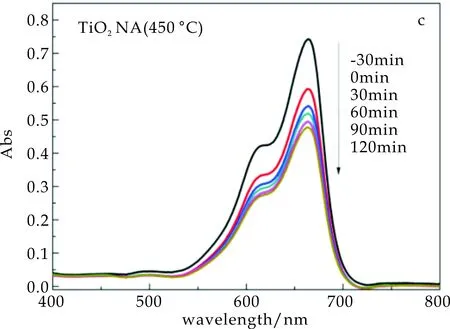
(c) TiO2纳米管阵列(450 ℃)

(d) TiO2纳米管阵列(550 ℃)
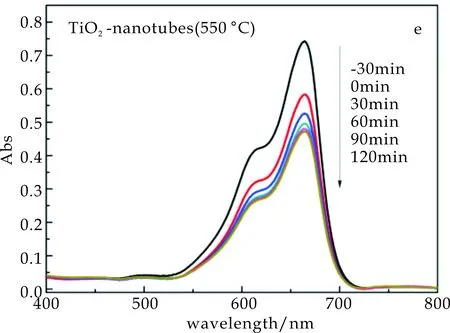
(e) 基体剥离的TiO2纳米管(550 ℃)

(f) MB的催化降解曲线图
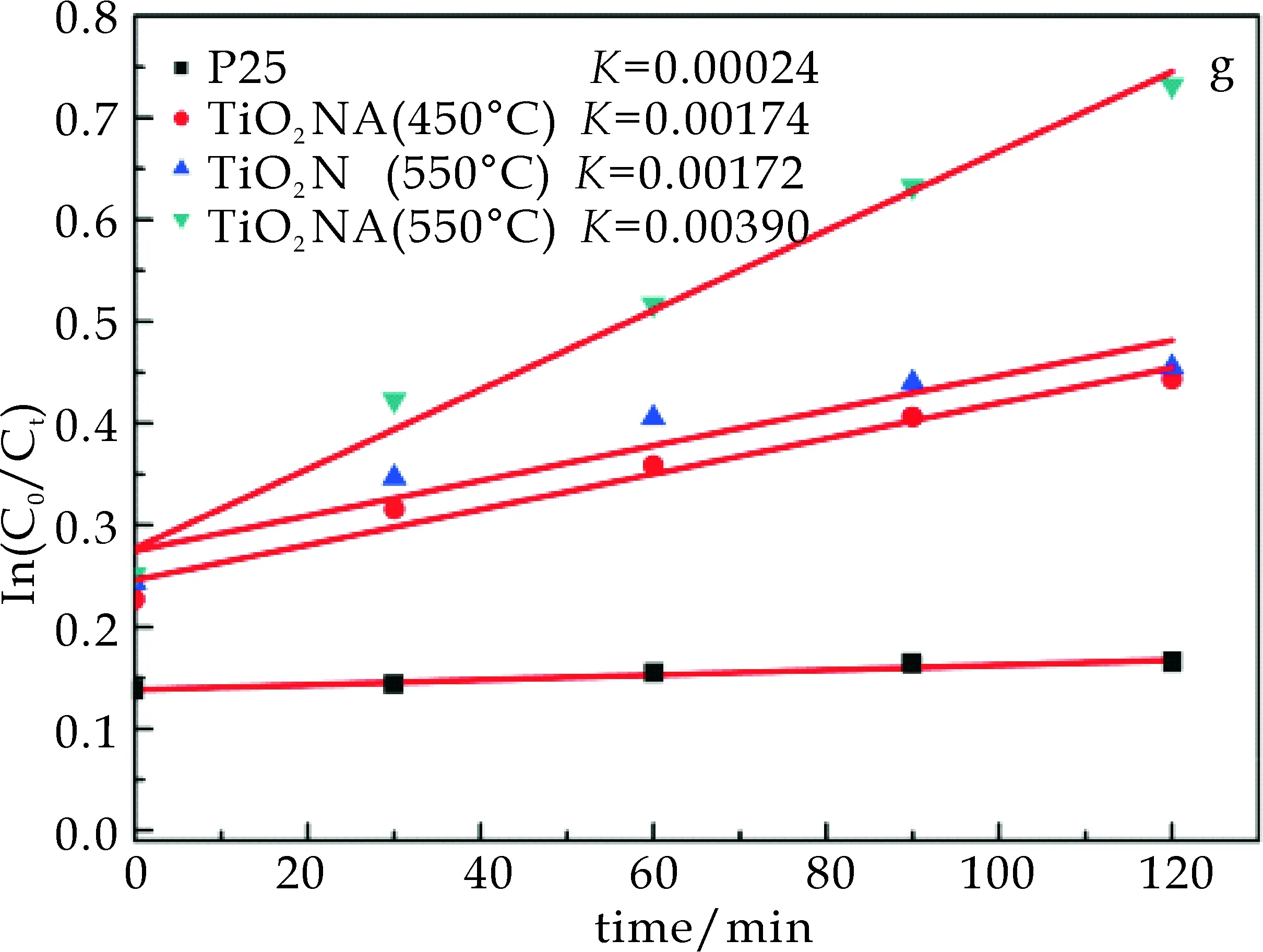
(g) MB的降解活性曲线图图3 亚甲基蓝在可见光照下的光催化降解曲线图
在非均相光催化时,一般认为光催化降解满足Langmuir- Hinshelwood动力学方程,且光催化氧化反应符合一级反应动力学特征,其特征方程为:
ln(Ct/C0)=-Kt[17]
(1)
式(1)中:C0是亚甲基蓝的起始浓度;Ct是经过光照时间t后亚甲基蓝的浓度;K是一级反应速率常数,可以用K来衡量样品催化性能的强弱.
以ln(C0/Ct)对t做图并进行拟合,发现浓度的对数与时间呈现线性关系,在可见光下550 ℃所制备的TiO2纳米管阵列降解MB的速率是0.003 90 min-1,剥离基体后的TiO2纳米管降解速率为0.001 72 min-1,450 ℃所制备的TiO2纳米管阵列降解MB的速率是0.001 74 min-1,而 P25 TiO2粉末的降解速率只0.000 24 min-1,550 ℃所制备的TiO2纳米管阵列降解MB的速率约为商用P25 TiO2粉末的16倍,明显优于商用P25 TiO2粉末,而且是剥离基体后TiO2纳米管降解速率的2.27倍,这是由于TiO2纳米管阵列的高比表面积和高度有序性,更有利于电子的传输,从而减少了电子-空穴对的复合,增加了其可见光光催化活性.
2.4 UV-Vis结果分析
图4是商用P25 TiO2粉末和TiO2纳米管阵列的紫外-可见漫反射谱.由图4可知,对于商用P25 TiO2粉末,只对400 nm以下的紫外光具有强的吸收,这与TiO2带隙比较宽(3.2 eV)只能吸收位于紫外区的光相一致.而用本实验方法制备TiO2纳米管阵列其吸收边有明显的红移,在可见光区有吸收.450 ℃和550 ℃所得样品的吸收边分别为480 nm和511 nm,根据公式Eg=1 240/λ可以估算出其禁带宽度分别为2.58 eV和2.42 eV,这也是550 ℃所得样品比450 ℃所得样品可见光催化活性高的原因.

图4 TiO2 纳米管阵列和P25的紫外-可见漫反射谱
由于二氧化钛的表面形貌会影响其对光线的捕获能力和对不同波长的吸收[18],所制备的TiO2纳米管阵列能够吸收可见光,产生电子-空穴对,光生电子与空穴对迅速向TiO2半导体粒子表面迁移扩散,与表面吸附的粒子(OH-、O2、有机物等)发生一系列反应,进而生成羟基自由基(·OH)等强氧化自由基将有机物彻底氧化降解,矿化为无机小分子[19].而且本方法制备的TiO2纳米管阵列高度有序利于电子的传输,从而减少了电子-空穴对的复合,具有较高的可见光催化活性.
3 结论
采用阳极氧化法制备出管径均匀且高度有序的TiO2纳米管阵列.该方法制备的TiO2纳米管阵列在可见光下具有良好的光催化活性,可见光照射120 min后,550 ℃所制备的TiO2纳米管阵列对亚甲基蓝的降解率可达到52%,降解速率约为商用P25 TiO2粉末的16倍,而且是该样品剥离基体后的TiO2纳米管降解速率的2.27倍,表明TiO2纳米管阵列的高比表面积和高度有序性更有利于电子传输,减少电子-空穴对的复合,增加其可见光光催化活性.
[1] Han S,Jing S,Chen S.Fabrication of TiO2nanoube arrays by rectified alternating current anodization[J].Journal of Materials Science & Technology,2015,31(1):23-29.
[2] Wang M,Sun L,Lin Z,et al.p-n Heterojunction photoelectrodes composed of Cu2O-loaded TiO2Nanotube arrays with enhanced photoelectro chemicaland photoelectron catalytic activities[J]. Energy & Environmental Science,2013,6(4):1 211-1 220.
[4] 张丽娜,计亚军,吴大辉,等.阳极氧化法制度有序TiO2纳米管阵列材料的研究进展[J]. 机械工程材料,2015,39(9):1-5.
[5] Zhou D,Chen Z,Yang Q,et al.In-situ construction of all-solid-state Z-scheme g-C3N4/TiO2,nanotube arrays photocatalyst with visible-light-induced properties[J].Solar Energy Materials & Solar Cells,2016,157:399-405.
[6] Nguyen V,Li W,Pham V,et al.A CdS/ZnSe/TiO2nanotube array and its visible light photocatalytic activities[J].Journal of Colloid & Interface Science,2016,462:389-396.
[7] 邓安平,黄应平,方艳芬,等.TiO2纳米管的制备和光催化降解有毒有机污染物[J].环境化学,2009,28(2):202-205.
[8] Roy P,Berger S,Schmuki P.TiO2,Nanotubes: Synthesis and applications[J].Angewandte Chemie International Edition,2011,50(13):2 904-2 939.
[9] 苏钰丰.TiO2纳米管阵列表面修饰及光催化降解有机污染物研究[D].厦门:厦门大学,2016.
[10] 胡军成,陈盛焕,刘 勇,等.Au-Ag共掺杂TiO2纳米片的制备及其光催化性能[J].中南民族大学学报(自然科学版),2010,29(3):1-5.
[11] Nguyen V,Li W,Pham V,et al.A CdS/ZnSe/TiO2nanotube array and its visible light photocatalytic activities[J].Journal of Colloid & Interface Science,2016,462:389-396.
[12] 王亚云,邵 谦.TiO2纳米管制备修饰及应用研究进展[J].新技术新工艺,2013(9):69-73.
[13] Pang Y L,Lim S,Ong H C,et al.A critical review on the recent progress of synthesizing techniques and fabrication of TiO2based nanotubes photocatalysts[J].Applied Catalysis A:General,2014,481:127-142.
[14] Samran B,Krongkitsiri P,Pimmongkol S,et al.Preparation and microstructure of titania (TiO2) nanotube arrays by anodization method[J].Advanced Materials Research,2013,802:104-108.
[15] Lan S.Progress on fabrication,modification and applications of titania nanotube arrays[J].Chinese Journal of Inorganic Chemistry,2007,23(11):1 841-1 850.
[16] Fan X,Fan J,Hu X,et al.Preparation and chara-cterization of Ag deposited and Fe doped TiO2nanotube arrays for photocatalytic hydrogen produ ction by water splitting[J].Ceramics Internationnal,2014,40(10):15 907-15 917.
[17] 徐小勇,施卫国,胡学兵,等.氮掺杂二氧化钛光催化降解亚甲基蓝的动力学研究[J].硅酸盐通报,2009,28(2):332-335.
[18] 张飞白.二氧化钛纳米管的制备及光催化降解亚甲基蓝的研究[D].天津:南开大学,2009.
[19] 章 丹,徐 斌,朱培娟,等.TiO2光催化降解亚甲基蓝机理的研究[J].华东师范大学(自然科学版),2013(5):35-42.

