硬脂酸酰胺丙基二甲基烷基季铵盐的合成及性能研究
高臣臣,许虎君*,陈丹丹,徐源鸿,方银军
(1.江南大学化学与材料工程学院,江苏 无锡 214122; 2.浙江赞宇科技集团股份有限公司,浙江 杭州 310030)
脂肪酰胺类表面活性剂具有耐水解性强,毒性低、低刺激,良好的生物降解性[1]等优点。脂肪酰胺基叔胺广泛用于表面活性剂中间体的制备,并与季铵化试剂反应生成酰胺型季铵盐阳离子表面活性剂[2]。
阳离子表面活性剂含有带正电荷的亲水基和烷基的疏水基[3],氮原子上的正电荷与多数物体表面的负电荷相互吸引,受静电作用而稳定的附在其表面。疏水链缠绕在细胞膜外形成薄膜,阻碍了微生物的新陈代谢,以及渗透进入细胞膜内,与蛋白质中的氨基酸相互作用,从而破坏微生物,达到抑菌的目的[4]。此外,酰胺键的加入有利于提高表面活性剂的抗菌活性和生物相容性[5-6,14]。郭志强等[7]通过测定烷基氯化铵对微生物的最低抑制浓度(MIC),确定了烷基氯化铵的最低使用量和最佳杀菌浓度范围。Cornellas等[8]报道了含有酰胺基团的咪唑和吡啶阳离子表面活性剂能显著增强其抗菌性。Franklin等[9]和Dizman等[10]研究表明随着烷基链的增长,抗菌能力增强。但达到一定程度,抗菌力下降。笔者以硬脂酸、N,N-二甲基-1,3-丙二胺制备了硬脂酸酰胺基叔胺中间体,并与环氧氯丙烷、苄溴、溴丁烷、苄氯、溴癸烷、氯代甘油等季铵化试剂反应,制备得到一系列硬脂酸酰胺型季铵盐。通过IR,1H NMR,ESI-MS等表征手段确定了中间体及目标产物的结构,并对季铵盐产物的表面化学性能及抗菌性能等进行了测定。
1 实验部分
1.1 主要原料及仪器
硬脂酸、环氧氯丙烷、苄溴、溴丁烷、苄氯、溴癸烷、氯代甘油,均为化学纯,国药集团化学试剂有限公司;N,N-二甲基-1,3-丙二胺,工业级,纯度≥99.5%,江苏飞翔化工股份有限公司;氮气(气体钢瓶)。IR400红外光谱仪,加拿大BOMEM公司;WATERS Platform ZMD 400质谱仪,美国Waters公司;核磁共振波谱仪,瑞士Bruker公司;光学接触角测量仪(OCA 40),北京东方德菲仪器有限公司。
1.2 实验方法
1.2.1硬脂酸酰胺丙基二甲基叔胺的合成[11]
将硬脂酸(20.15 g,70.8 mmol)加入150 mL三口圆底烧瓶中,用氮气保护,升温至120 ℃,缓慢滴加N,N-二甲基-1,3-丙二胺(10.78 g,105.5 mmol),并用分水器接收反应生成的水,于155 ℃下反应8 h。反应结束后,减压蒸馏,除去过量的N,N-二甲基-1,3-丙二胺,得到淡黄色固体。用丙酮—石油醚多次洗涤产品,真空干燥,即得到白色固体产物硬脂酸酰胺丙基二甲基叔胺(C18AMPM),合成如图1所示。
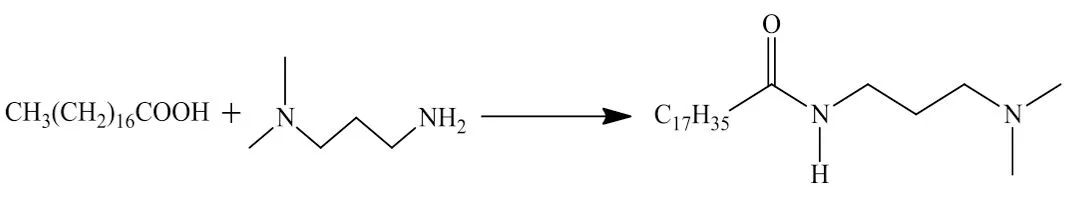
图1 硬脂酸酰胺丙基二甲基叔胺的合成路线
1.2.2硬脂酸酰胺丙基二甲基烷基季铵盐的合成[12]
将制备好的中间体硬脂酸酰胺丙基二甲基叔胺与环氧氯丙烷、苄溴、溴丁烷、苄氯、溴癸烷、氯代甘油等季铵化试剂反应,得到一系列硬脂酸酰胺型季铵盐,按顺序依次标记为C18AMPM-1、C18AMPM-2、C18AMPM-3、C18AMPM-4、C18AMPM-5、C18AMPM-6。
以环氧氯丙烷和氯代甘油为例,合成路线如图2所示。具体步骤如下:将硬脂酸酰胺丙基二甲基叔胺(8.37 g,22.7 mmol),环氧氯丙烷(2.34 g,25.3 mmol),甲醇20 mL加入150 mL三口圆底烧瓶中,升温至甲醇回流,反应6~8 h,取量滴定胺值,直至转化率不变时停止反应,旋蒸除去过量甲醇,选用合适的溶剂重结晶,真空干燥,得到白色固体产物。采用同样方法制备其他季铵盐,提纯并得到目标产物(C18AMPM-1)。

图2 硬脂酸酰胺季铵盐的合成路线
1.3 性能测定
表面张力γ:制备产品均为酰胺型季铵盐类阳离子表面活性剂,采用光学接触角测量仪(OCA 40)测定其表面张力。
Krafft点:质量分数1%的硬脂酸酰胺型季铵盐水溶液,边搅拌边升温至溶液透明,记录此时温度。
抗菌性:采用GB 15979-2002测定硬脂酸酰胺型季铵盐水溶液(5 mmol/L)对大肠杆菌EC、金黄色葡萄球菌SA、海氏肠球菌EH、铜绿假单胞菌PA等菌种的抑制效果。
2 结果与讨论
2.1 结构表征
2.1.1C18AMPM的IR、1HNMR谱
图3为C18AMPM的IR谱。如图3所示,3 402 cm-1吸收峰为典型的酰胺N—H伸缩振动;1 653 cm-1为酰胺中的羰基伸缩振动,它比一般的羰基低;1 550 cm-1为酰胺N—H弯曲振动。结果证明了硬脂酸与N,N-二甲基-1,3-丙二胺发生反应生成了中间体C18AMPM。

图3 C18AMPM的IR谱
图4为C18AMPM的1H NMR谱。图4中,δ 4.87,3.31是MeOD的溶剂峰。1H NMR (400 MHz,MeOD) ,δ:3.21 (t,J=6.9 Hz,2H),2.37 (dd,J=8.9,6.7 Hz,2H),2.26 (s,6H),2.19 (t,J=7.5 Hz,2H),1.75~1.65 (m,2H),1.65~1.56 (m,2H),1.32 (d,J=10.0 Hz,28H),0.92 (t,J=6.8 Hz,3H)。
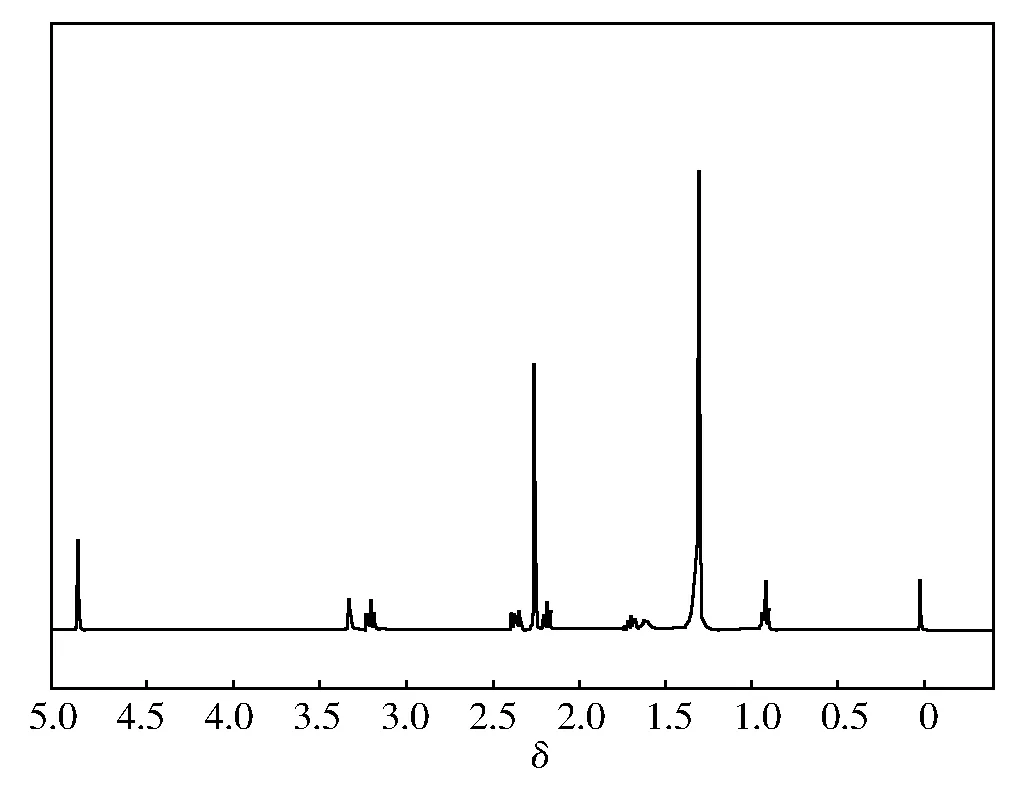
图4 C18AMPM的1H NMR谱
C18AMPM采用正离子模式进行ESI-MS分析(图5)。其中,C18AMPM(标记为M)的理论质荷比(m/z)为368.4,[M+H]+为369.3,具体解析结果与理论预测相符。

图5 C18AMPM的ESI-MS谱
2.1.2系列硬脂酸酰胺型季铵盐的核磁、质谱结果
C18AMPM-1。1H NMR (400 MHz,CDCl3),δ:8.29~7.63 (m,1H),7.13~5.84 (m,2H),5.83~4.66 (m,1H),4.59~4.11 (m,2H),4.07~3.75 (m,2H),3.45~3.32 (m,6H),3.22~2.56 (m,2H),2.25 (dd,J=27.2,19.5 Hz,2H),2.16~1.88 (m,2H),1.59 (s,2H),1.24 (dd,J=19.0,5.7 Hz,28H),0.89 (t,J=6.7 Hz,3H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2CH2CHCH2O]+([M-Cl]+) 425.2(100%);[C17H35CONH(CH2)3]+([M-N(CH3)2CH2CHCH2OCl]+) 324.2(75%)。
C18AMPM-2。1H NMR (400 MHz,CDCl3),δ:7.76 (t,J=5.5 Hz,1H),7.58 (d,J=6.6 Hz,2H),7.52~7.39 (m,3H),4.81 (s,2H),3.92~3.77 (m,2H),3.18 (s,6H),2.32~2.26 (m,2H),2.21 (d,J=10.5 Hz,4H),1.57 (dd,J=14.0,6.9 Hz,2H),1.25 (t,J=13.4 Hz,28H),0.86 (t,J=6.8 Hz,3H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2CH2C6H5]+([M-Br]+) 459.3(100%); [C17H35CONH(CH2)3]+([M-N(CH3)2CH2C6H5Br]+) 324.3(8%)。
C18AMPM-3。1H NMR (400 MHz,CDCl3),δ:7.80 (t,J=5.6 Hz,1H),3.85~3.75 (m,2H),3.42~3.33 (m,2H),3.26 (s,6H),2.28 (dd,J=18.3,10.5 Hz,2H),2.06 (d,J=17.0 Hz,4H),1.78~1.65 (m,2H),1.58 (dd,J=14.3,7.0 Hz,2H),1.41 (dq,J=14.7,7.3 Hz,2H),1.22 (t,J=8.9 Hz,28H),0.99 (t,J=7.3 Hz,3H),0.86 (t,J=6.8 Hz,3H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2C4H9]+([M-Br]+) 425.5(100%);[C17H35CONH(CH2)3N(CH3)2H]+([M-C4H9Br+H]+) 369.4(18%); [C17H35CONH(CH2)3]+([M-N(CH3)2C4H9Br]+) 324.4(15%)。
C18AMPM-4。1H NMR (400 MHz,MeOD),δ: 8.13 (s,1H),7.69~7.37 (m,5H),4.56 (s,2H),3.32~3.25 (m,4H),3.06 (s,6H),2.24~2.15 (m,2H),2.15~2.01 (m,2H),1.65~1.53 (m,2H),1.30 (s,28H),0.91 (t,J=6.8 Hz,3H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2CH2C6H5]+([M-Cl]+) 459.4(100%);[C17H35CONH(CH2)3N(CH3)2H]+([M-CH2C6H5Cl+H]+) 369.4(11%); [C17H35CONH(CH2)3]+([M-N(CH3)2CH2C6H5Cl]+) 324.4(10%)。
C18AMPM-5。1H NMR (400 MHz,MeOD),δ:3.32~3.25 (m,6H),3.09 (s,6H),2.22 (t,J=7.6 Hz,2H),2.03~1.89 (m,2H),1.76 (s,2H),1.62 (s,2H),1.46~1.18 (m,42H),0.91 (t,J=6.6 Hz,6H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2C10H21]+([M-Brl]+) 409.6(100%);[C17H35CONH(CH2)3N(CH3)2H]+([M-C10H21Br+H]+) 369.4(16%)。
C18AMPM-6。1H NMR (400 MHz,CDCl3)δ:7.85 (s,1H),4.90 (s,2H),4.32 (s,1H),3.52 (dd,J=69.2,30.3 Hz,6H),3.29 (s,6H),3.22~2.74 (m,1H),2.27 (dd,J=31.5,7.3 Hz,2H),2.11 (d,J=39.5 Hz,2H),1.57 (s,2H),1.24 (s,28H),0.87 (t,J=6.7 Hz,3H)。ESI-MS,m/z:[C17H35CONH(CH2)3N(CH3)2CH2CH(OH)CH2OH]+([M-Cl]+) 443.4(100%);[C17H35CONH(CH2)3N(CH3)2H]+([M-CH2CH(OH)CH2OHCl+H]+) 369.4(30%); [C17H35CONH(CH2)3]+([M-N(CH3)2CH2CH(OH)CH2OHCl]+) 324.4(15%)。
2.2 性能研究
2.2.1表面化学性能
图6为系列硬脂酸酰胺型季铵盐的表面张力。根据图6可以求出系列硬脂酸酰胺型季铵盐的cmc、γcmc及pC20。

图6 系列硬脂酸酰胺型季铵盐的表面张力
表面最大吸附量Γmax及平均每个分子占有的最小面积Amin可以用下式计算[13-14]:
(1)
(2)
式中:γ为表面张力,mN/m;c为表面活性剂溶液浓度,mol/L;T为热力学温度,K;R=8.314 J/(mol·K);NA为阿伏加德罗常数。Γmax、Amin的单位分别为μmol/m2、nm2。n为常数(受反离子影响),未添加NaCl时n=2,NaCl摩尔浓度较高时,反离子浓度视为不变,n=1。
如表1所示,对比C18AMPM-1和C18AMPM-6发现,环氧基开环后降低了其cmc和γcmc,这可能是由于环氧基开环后羟基数目增加,亲水性增强,更容易与水结合[15]。降低表面张力的效能受到界面饱和吸附量的影响,由于疏水基等条件相同,亲水基不同,C18AMPM-6在界面上的吸附量大于C18AMPM-1,表明C18AMPM-6具有更强的降低表面张力的能力。C18AMPM-3的结构类似双子表面活性剂,因而具有较低的cmc和γcmc,而C18AMPM-5因为季铵化试剂为溴癸烷,krafft点较高,两侧的疏水链增大了界面吸附的空间位阻,吸附量减少,故具有较低的γcmc。C18AMPM-2与C18AMPM-4因为反离子的不同,而且还是同一主族元素,故相差不大。
2.2.2抗菌性
采用GB 15979—2002 《一次性使用卫生用品卫生标准》对制备的硬脂酸酰胺型季铵盐做抗菌性能测试。统一配制5 mmol/L的水溶液。并与同浓度下的杀菌剂1227(十二烷基二甲基苄基氯化铵)作对照,结果见表2、表3。

表1 系列酰胺型季铵盐的表面化学性能(T=25 ℃)
对比C18AMPM-1与C18AMPM-6,可以得到环氧基具有较强的杀菌性,开环后杀菌性减弱。对比C18AMPM-2与C18AMPM-4,得到当季铵盐中正离子均一致时,负离子为Br-和Cl-,结果显示Cl-具有较强的杀菌效果。硬脂酸酰胺型季铵盐中正离子强烈吸附在细胞膜上,负离子Br-和Cl-破坏了膜的选择渗透性。具有酰胺基团的C18AMPM-4杀菌效果堪比1227,但硬脂酸酰胺型季铵盐具有较好的生物降解性,这是1227无法取代的。对比C18AMPM-3与C18AMPM-5,可以得到随着季铵化试剂疏水链的增长,抗菌活性降低,这个结果与Shaban等[16]得出的结论一致。可能是由于静电吸引附着在细胞壁上,长链疏水基干扰细胞膜,导致细胞内物质泄漏而死亡[17]。
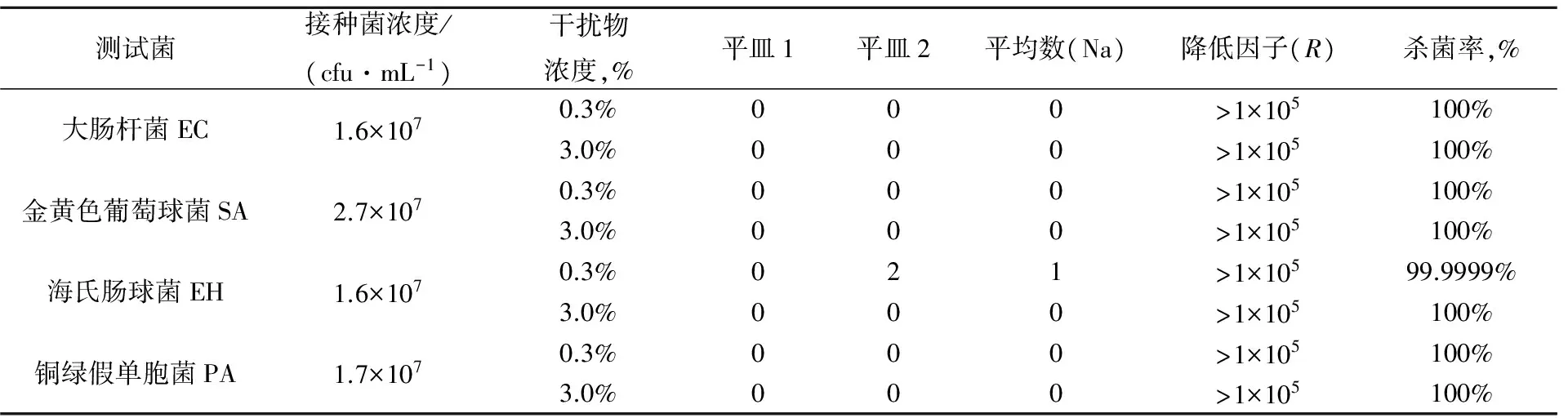
表2 杀菌剂1227抗菌条件及抗菌效果

表3 硬脂酸酰胺型季铵盐的抗菌结果
3 结 论
a.通过IR光谱,1H NMR,ESI-MS等表征手段确定了合成物质即为目标产物。
b.测定了系列硬脂酸酰胺型季铵盐的表面化学性能,对比了不同季铵化试剂下反应产物的性能,均具有较好的表面化学性能。
c.合成得到的硬脂酸酰胺型季铵盐具有较好的杀菌效果。与杀菌性1227做对比,C18AMPM-3与C18AMPM-4均满足杀菌要求;C18AMPM-1与C18AMPM-6对大肠杆菌EC效果不佳,对其他三种菌种均有效;C18AMPM-2对海氏肠球菌EH效果不佳,对其他菌种有效;当干扰物浓度在3.0%时,C18AMPM-5对金黄色葡萄球菌SA和海氏肠球菌EH效果变弱。
[1] 常致成. 脂肪酰胺和脂肪酸酯类非离子表面活性剂的开发与应用[J]. 表面活性剂工业,2000(2):5-8.
[2] 郭祥峰. 阳离子表面活性剂及应用[M]. 化学工业出版社,2002:102-106.
[3] 赵国玺,朱步瑶. 表面活性剂作用原理[J]. 日用化学工业信息,2003(17):16-16.
[4] Castillo J A,Pinazo A,Carilla J,et al. Interaction of antimicrobial arginine-based cationic surfactants with liposomes and lipid monolayers[J]. Langmuir,2004,20(8): 3379-3387.
[5] Zhang S,Ding S,Yu J,et al. Antibacterial Activity,in Vitro Cytotoxicity,and Cell Cycle Arrest of Gemini Quaternary Ammonium Surfactants[J]. Langmuir,2015,31(44): 12161-12169.
[6] Hoque J,Akkapeddi P,Yarlagadda V,et al. Cleavable cationic antibacterial amphiphiles: synthesis,mechanism of action,and cytotoxicities[J]. Langmuir,2012,28(33): 12225-12234.
[7] 郭志强. 烷基氯化铵季铵盐的抗菌性能研究[J]. 日用化学品科学,2004,27(2):20-22.
[8] Cornellas A,Perez L,Comelles F,et al. Self-aggregation and antimicrobial activity of imidazolium and pyridinium based ionic liquids in aqueous solution[J]. Journal of Colloid and Interface Science,2011,355(1): 164-171.
[9] Franklin T J,Snow G A. Biochemistry of antimicrobial action[M]. Springer,2013.
[10] Dizman B,Elasri M O,Mathias L J. Synthesis and antibacterial activities of water-soluble methacrylate polymers containing quaternary ammonium compounds[J]. Journal of Polymer Science Part A: Polymer Chemistry,2006,44(20): 5965-5973.
[11] Chu Z,Feng Y. Empirical correlations between Krafft temperature and tail length for amidosulfobetaine surfactants in the presence of inorganic salt[J]. Langmuir,2011,28(2): 1175-1181.
[12] 王一尘. 阳离子表面活性剂的合成[M]. 轻工业出版社,1984:51-58.
[13] Li F,Rosen M J,Sulthana S B.Surface properties of cationic gemini surfactants and their interaction with alkylglucoside or -maltoside surfactants [J]. Langmuir ,2001,17(4):1037-1042.
[14] 赵国玺.表面活性剂物理化学[M].修订版.北京:北京大学出版社,1984:85-88.
[15] 赵国玺,朱步瑶. 表面活性剂作用原理[M].北京:中国轻工业出版社,2003:250-252.
[16] Shaban S M,Fouda A S,Elmorsi M A,et al. Adsorption and micellization behavior of synthesized amidoamine cationic surfactants and their biological activity[J]. Journal of Molecular Liquids,2016,216:284-292.
[17] Garcia M T,Ribosa I,Perez L,et al. Self-assembly and antimicrobial activity of long-chain amide-functionalized ionic liquids in aqueous solution[J]. Colloids and Surfaces B: Biointerfaces,2014,123: 318-325.

