Ⅰ群4型禽腺病毒卵黄抗体实验室产品制备
于洪涛,赵 丽,王 昊
( 哈药集团生物疫苗有限公司,哈尔滨 150069)
腺病毒是全球家禽和野禽常见的传染病原之一[1-3]。多数腺病毒可在健康禽体内存在并复制,不表现临床症状或临床症状非常轻微,但可成为混合感染时的条件性病原;腺病毒有时也可作为原发性病原,引起禽类的多种病症[4-6]。
腺病毒可分为A、B、C、D、E 5个种12个血清型,我国主要流行A、B、C 3种基因型,共6个血清型(火鸡1型、1型、4型、5型、8a/b型),但是近期在豫南、皖北、苏北、鲁西北和胶东地区流行的禽腺病毒主要是血清4型和8a/b型,造成鸡群的死亡率较高,并且发病急,有蔓延的趋势。安卡拉病(心包积水-肝炎综合征)就是由Ⅰ群腺病毒,血清4型引起来的。该病多发于肉鸡,近期也开始感染麻鸡以及产蛋鸡的育成鸡,并且育成鸡发病死亡率还非常高。
Ⅰ群禽腺病毒的12个血清型交叉保护性较差,因此在防控上必须选用与流行株匹配的疫苗株和卵黄抗体才能有效遏制疫情的蔓延。并目前市场上没有商品化的疫苗或卵黄抗体,我公司通过自行分离的Ⅰ群4型禽腺病毒HY株,制备免疫原免疫蛋鸡,制备了3批Ⅰ群4型禽腺病毒卵黄抗体实验室制品,并且经过检验,该3批制品有较好的安全性及效力,为公司下一步申报该产品的新兽药注册证书奠定基础。
1 材料与设备
Ⅰ群4型禽腺病毒F5代生产种毒:批号为FAVHY-SS-01,病毒含量为107.22TCID50/0.1 mL,规格为2.0 mL·瓶-1。Ⅰ群4型禽腺病毒检验用强毒:批号为FAV-HY-QS-03-1,病毒含量为107.22TC ID50/0.1 mL,规格为2.0 mL·瓶-1。Ⅰ群4型禽腺病毒琼扩抗原:批号为FAV-HY-K-01;效价≥1:2;规格为2.0 mL·瓶-1。Ⅰ群4型禽腺病毒阳性血清:批号为FAV-HY-Y-01;效价≥1:64;规格为2.0 mL·瓶-1。Ⅰ群4型禽腺病毒阴性血清:批号为HY-Y-01,规格为2.0 mL·瓶-1。均由哈药集团生物疫苗有限公司制备、鉴定、保管和供应。
鸡肝癌细胞:21、42日龄SPF鸡,由哈药集团生物疫苗有限公司实验动物中心提供。
试验用产蛋鸡:120日龄产蛋鸡,由哈药集团生物疫苗有限公司实验动物中心提供,达到《生产用产蛋鸡质量标准》要求。
超滤膜包:采用Biomax 50 ku,改良聚醚砜材料,0.5 m2膜面积,购自Millipore公司。
注射用白油:符合《中华人民共和国兽药典》(2010年版)中兽用注射用白油标准要求。
试剂:醋酸钠(AR)、冰醋酸(AR)、正辛酸(AR)、氨水、甲醛,均购自国药集团化学试剂有限公司。
仪器:离心机(RC12BP型,德国产);超滤膜包:采用Biomax 100 ku,改良聚醚砜材料,0.5 m2膜面积,购自Millipore公司。
2 试验方法
2.1 卵黄抗体的制造及半成品检验
高免蛋鸡群应符合下列标准:应具有商品蛋鸡的良好生产性能。无禽白血病、网状内皮增生病和鸡传染性贫血病,按0.5%抽样,血清抗体结果应全部为阴性。监测鸡白痢、鸡毒支原体,二者阳性率≤0.1%。应适时接种禽流感、鸡新城疫、鸡传染性支气管炎、鸡传染性法氏囊病、鸡马立克氏病、减蛋综合症(EDS76)及大肠杆菌病等疫苗,并做好球虫病药物预防。
2.2 Ⅰ群4型禽腺病毒灭活疫苗(HY株)免疫程序
基础免疫:开产前2~3周健康产蛋鸡,颈部皮下或肌肉注射Ⅰ群禽腺病毒灭活疫苗(4型,HY株)(简称免疫原),1.0 mL·只-1。
加强免疫:在基础免疫后21日进行第2次接种,肌肉多点注射免疫原,1.0 mL·只-1。
强化免疫:在加强免疫后21日进行第3次接种,肌肉多点注射免疫原,1.0 mL·只-1。
维持免疫:在强化免疫接种后,跟踪测定抗体水平,抗体AGP效价<1:64时,进行加强免疫,1.0 mL·只-1。
高免蛋收集:产蛋鸡强化免疫接种结束后第10天开始,每隔5 d抽样测定卵黄中的抗体琼扩效价。当效价≥1:64时,收集鸡蛋,置2~8℃贮存,贮藏时间应≤10 d。
2.3 Ⅰ群4型禽腺病毒卵黄抗体制备
蛋壳消毒:将鸡蛋浸入1‰二氯异氰尿酸钠水溶液中消毒15 min。卵黄分离采用手工或机械打蛋,打蛋时应充分除去蛋清、胚盘和系带,收集卵黄。酸化:量取卵黄体积,加入卵黄体积8倍的醋酸缓冲液(0.12 mol·L-1,pH 5.0)充分搅拌,使其呈均匀膏状。调至pH 5.2,2~8℃静置5~15 h。萃取吸取上清液,缓慢加入辛酸至终浓度为1.5%,2~8℃静置6~20 h。取上清液过滤,滤液调至pH为7.2。过滤、浓缩:取萃取的卵黄液用孔径为1和0.45 mm的筒式滤芯过滤澄清,再经截留分子量为100 ku超滤膜包浓缩。灭活:加入终浓度为0.05%甲醛溶液,充分搅拌均匀,置室温灭活24 h。效价测定:将灭活后的抗体进行抗体效价测定,抗体琼扩效价应≥1:4。稀释:根据测定的抗体效价,将浓缩灭活后的卵黄抗体用磷酸盐缓冲液(0.01 mol·L-1,pH 7.2)适当稀释,再经孔径为0.22 mm滤膜过滤除菌。
2.4 半成品检验
性状为淡黄色澄明液体,久置后有少量白色沉淀。无菌检验:按2010版《中国兽药典》附录进行检验。抗体效价测定:按规程附注1方法测定琼扩效价。分装:定量分装,加盖密封,贴标签,置2~8℃保存。
2.5 卵黄抗体成品检验
性状:随机抽样肉眼观察。装量检查:按2010版《中国兽药典》附录进行检查。无菌检验:按2010版《中国兽药典》附录进行检验。支原体检验:按2010版《中国兽药典》附录进行检验。外源病毒检验:将腺病毒卵黄抗体2~3瓶混合,取20 mL倒入透析袋,放入400 g·L-1的PEG20 000中浓缩,浓缩后的液体用PBS(0.01 mol· L-1,pH 7.2)恢复至20 mL作为检品。鸡胚检查法:经尿囊腔接种检品0.1~0.2 mL。经绒毛尿囊膜接种检品0.1~0.2 mL。细胞检查法:取上述检品1.8 mL加入0.2 mL 10倍工作浓度的M-199浓缩培养液,作为处理的检品,每瓶鸡胚成纤维细胞(CEF)接种处理的检品0.2 mL。禽淋巴白血病病毒ELISA检测法:取上述检品1.8 mL加入0.2 mL 10倍工作浓度的M-199浓缩培养液,作为处理的检品,每瓶CEF接种处理的检品0.5 mL。禽网状内皮组织增生症病毒荧光染色检测法:取上述检品1.8 mL加入0.2 mL 10倍工作浓度的M-199浓缩培养液,作为处理的检品,每瓶CEF接种处理的检品1 mL。按现行《中国兽药典》附录进行检验。安全检验:用21日龄SPF鸡10只,每只颈部皮下分点注射本品2.0 mL,观察14日,记录鸡的存活情况。抗体效价测定:测定琼扩抗体效价。
SPF鸡攻毒检验:取21日龄SPF鸡30只,随机分为3组,每组10只。第1组经颈部皮下或肌肉注射本品,1.0 mL·只-1;第2组为攻毒对照组,经颈部皮下或肌肉注射生理盐水1.0 mL·只-1;第3组为健康对照组,不注射任何物品,3组隔离饲养。注射后24 h,第1、2组鸡各肌肉注射I群4型禽腺病毒HY株病毒液(含106.0TCID50/0.1 mL),0.1 mL·只-1。连续观察10日,记录鸡发病及死亡情况。
辛酸残留量测定:按辛酸含量检测方法(一次提取比色法)进行测定。甲醛残留量测定:按现行《中国兽药典》附录进行测定。
3 试验结果
3.1 半成品制备及检验结果
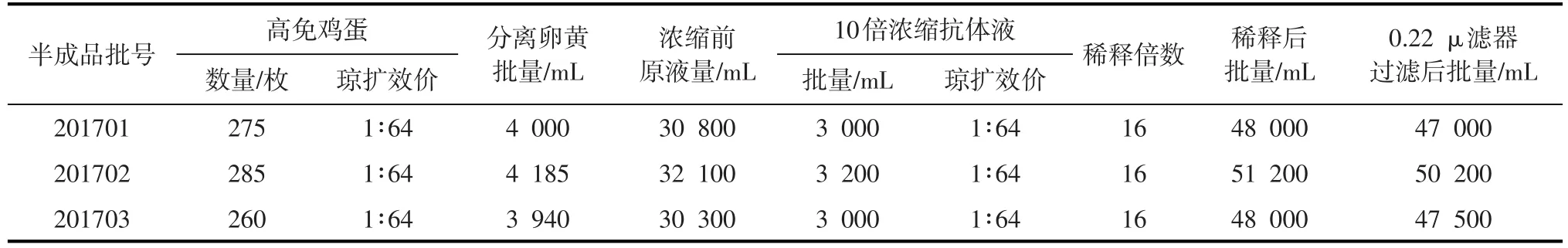
表1 Ⅰ群4型禽腺病毒卵黄抗体半成品制备结果
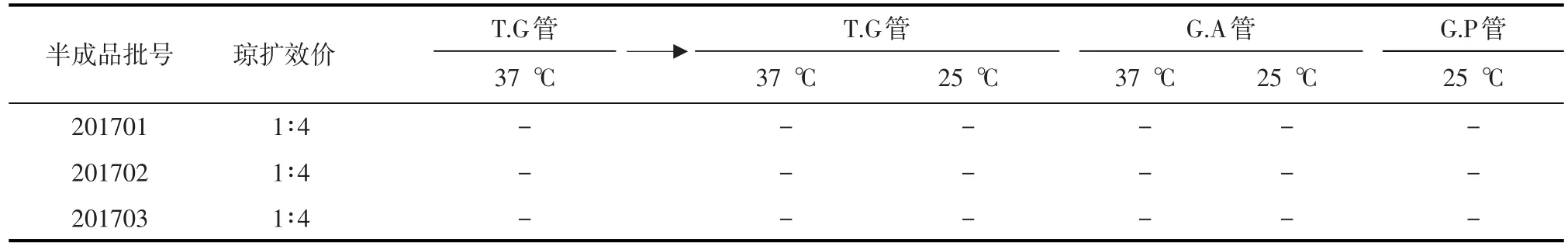
表2 Ⅰ群4型禽腺病毒卵黄抗体半成品检验结果
半成品制备及检验结果见表1~2。
从表1~2结果可知,实验室试制的3批Ⅰ群4型禽腺病毒卵黄抗体半成品量分别为47 000、50 200和47 500 mL,经检验Ⅰ群4型禽腺病毒卵黄抗体琼扩效价均≥1:4;无细菌、霉菌污染,达到Ⅰ群4型禽腺病毒卵黄抗体半成品质量标准要求。
3.2 卵黄抗体成品制备及检验结果
将检验合格的Ⅰ群4型禽腺病毒卵黄抗体半成品按100 mL·瓶-1无菌分装,制成成品,并从中试产品抽样按本产品《质量标准》检验,结果见表3~11。
从表3~11结果可知,3批Ⅰ群4型禽腺病毒卵黄抗体均为淡黄色的澄明液体;3/3装量均≥101 mL·瓶-1,符合现行《中国兽药典》附录要求;抗体无细菌、霉菌、支原体及外源病毒污染,纯净;注射21日龄SPF鸡,在观察期内,鸡全部健活,精神状态良好,行为、采食和饮水正常,无其他全身不良反应;注射局部吸收良好,无红肿和硬块,安全。3批Ⅰ群4型禽腺病毒卵黄抗体琼扩效价均≥1:4;用动物效检中,3批抗体对鸡攻毒保护率为100%,攻毒对照组发病率为90%,剖检发病鸡,均呈心包积水肝炎综合征的典型病理变化;健康对照组均100%健活;甲醛残留量为0.008 4%~0.008 6%,抗体样品A440-蛋黄氯仿萃提液A440<0.1%辛酸标准溶液A440,符合规定标准要求。
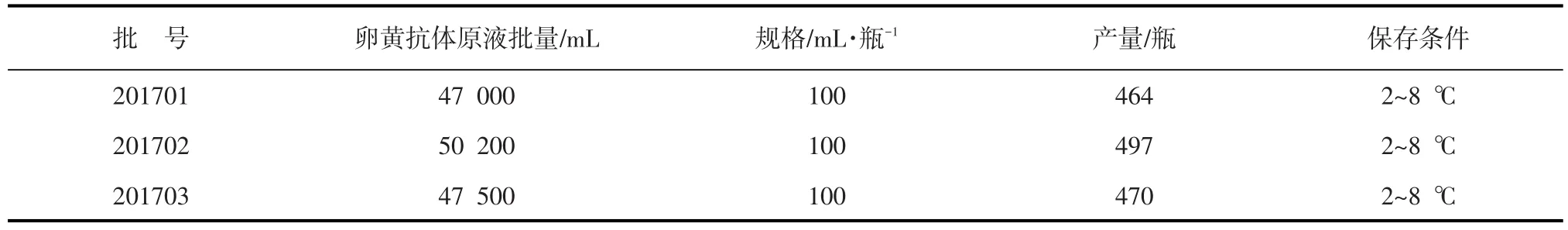
表3 3批实验室产品制备结果
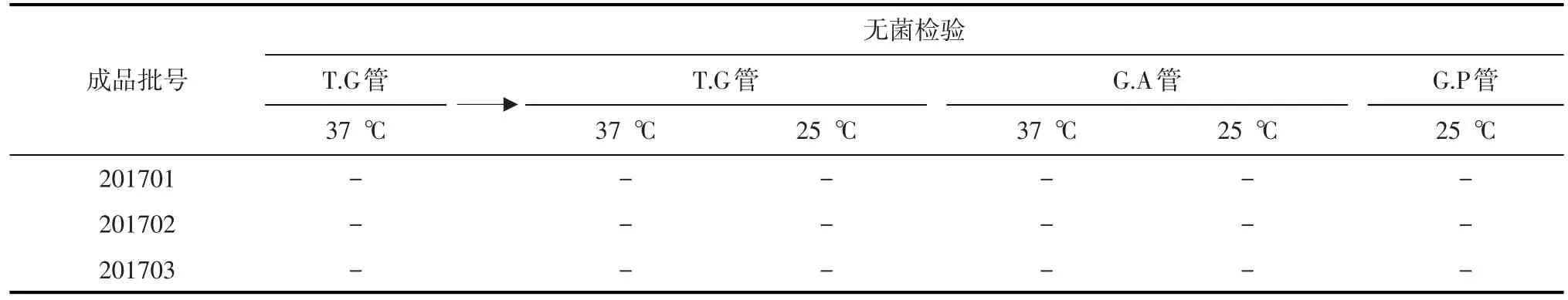
表4 3批成品无菌检验结果
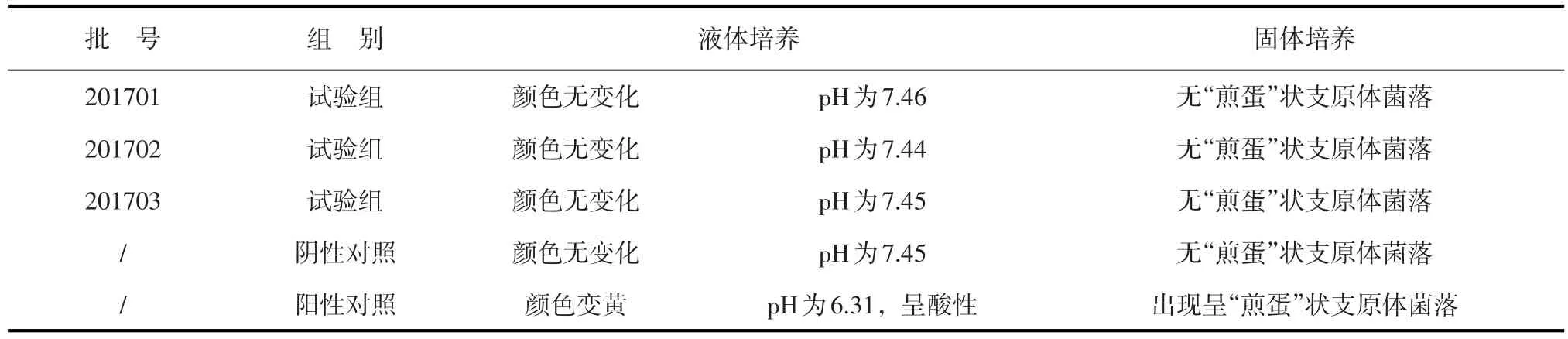
表5 3批成品支原体检验结果
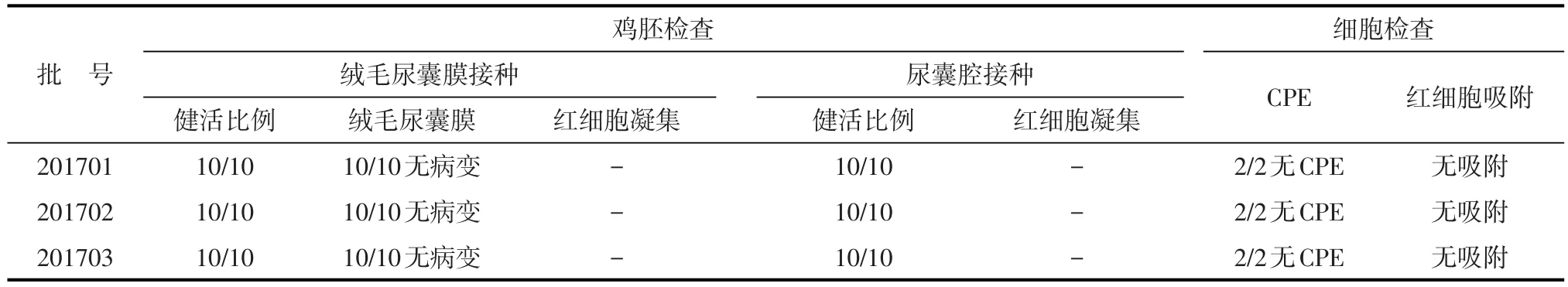
表6 3批成品外源病毒(鸡胚、细胞)检验结果
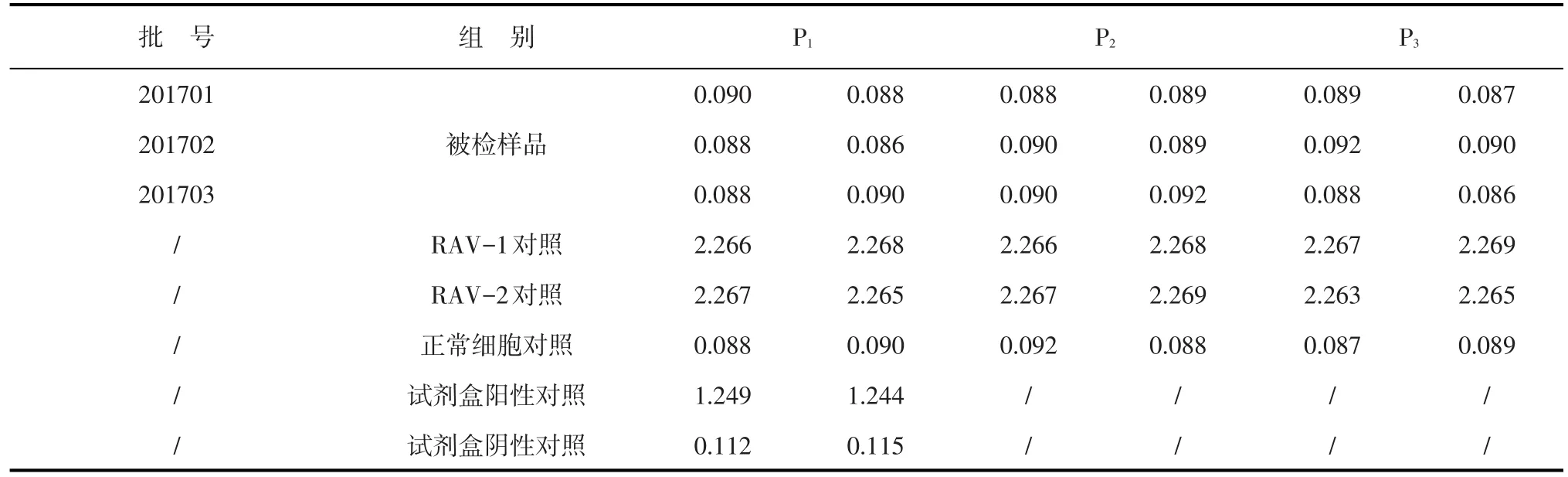
表7 3批成品禽白血病病毒(ALV)检验结果
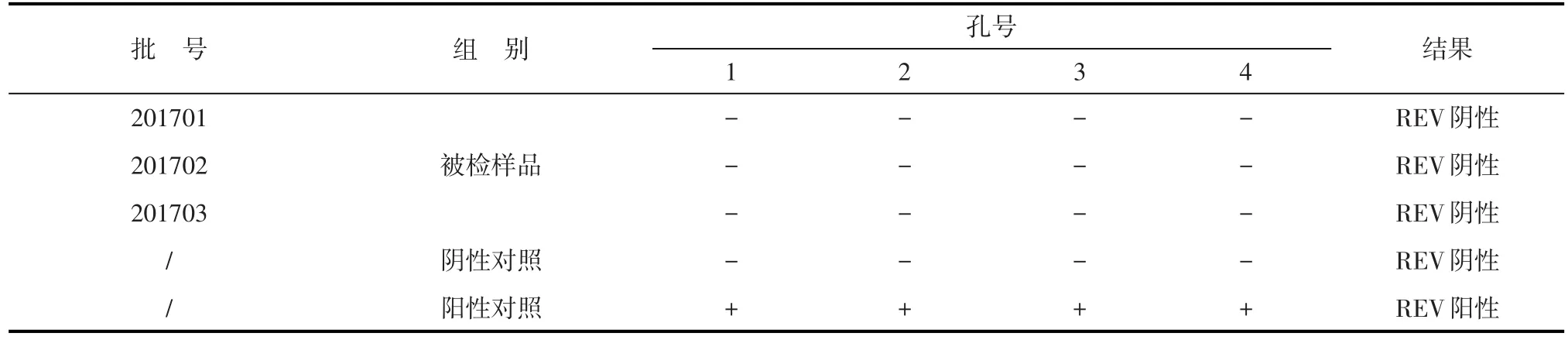
表8 3批成品禽网状内皮组织增生症病毒(REV)检验结果

表9 3批成品鸡安全检验结果
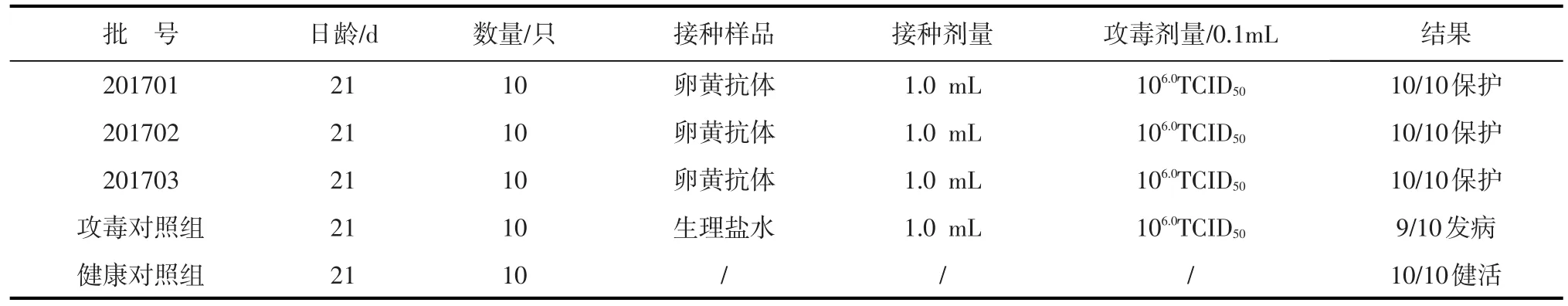
表10 3批成品鸡效力检验结果
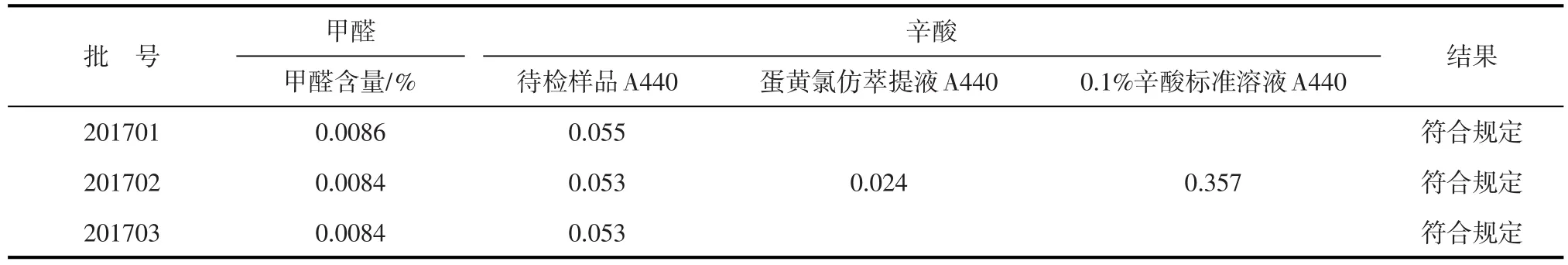
表11 3批成品甲醛和辛酸残留量测定结果
4 结论
按照《I群4型禽腺病毒卵黄抗体制造及检验试行规程(草案)》制备了3批实验室产品,并按照本产品《质量标准》对试制的3批卵黄抗体进行了性状、装量、无菌、支原体、外源病毒、安全、效力、辛酸和甲醛残留等检验,结果均符合本产品《质量标准》要求。研究制定的卵黄抗体生产工艺适于卵黄抗体的产业化生产。
[参考文献]
[1] 韦悠,谢芝勋,范晴,等.Ⅰ群禽腺病毒双价油乳剂灭活苗的研究[J].南方农业学报,2011,42(12):1 550-1 554.
[2] 赵继勋.Ⅰ群禽腺病毒感染的流行病学探究与防控认识[J].北方牧业,2017(6):18.
[3] 楚电峰,刘相娥,薄智勇,等.Ⅰ群禽腺病毒的流行病学和防控研究现状[J]. 中国动物检疫,2017,34(5):86-89.
[4] 王亚楠,韩涛,李纯玲,等.禽腺病毒Ⅰ群的研究现状[J].中国动物保健,2017,19(1):61-64.
[5] 李晓林,王相芹,罗济冠,等.Ⅰ群禽腺病毒的分离鉴定及其致病性研究[J]. 中国动物检疫,2016,33(8):86-89.
[6] 李海英,尹燕博,徐守振,等.I群禽腺病毒12个血清型毒株Hexon蛋白全基因序列测定和酶切位点分析[J].中国兽医学报,2012,32(1):33-37.

