miR-582-5p通过调控Wnt通路影响胃癌AGS细胞的增殖和耐药
刘 栋,王建华△,段降龙,孙学军,刘 斌,武 敏,刘思达,毛智军,张 涛,薛飞,普彦淞,李晓帆,高增战*,龙延滨
(1陕西省人民医院普外二科,西安 710068;2西安交通大学第一附属医院普外科;3陕西省人民医院内分泌科;△共同第一作者;*通讯作者,E-mail:gaoxi8004@163.com)
胃癌是常见的消化道恶性肿瘤之一,由于临床表现缺乏特异性导致诊断时往往处于晚期、恶性程度高导致预后差。在我国发病率居于恶性肿瘤的第2位,死亡率居恶性肿瘤第3位[1]。根治性手术术后辅助化疗可以延长生存期,但是由于有些患者对化疗耐药,疗效有限,传统生物标志物在胃癌的诊治中缺乏理性的特异性及敏感性,所以临床迫切需要寻找新的胃癌生物学标记物,提高血清标记物在胃癌诊治中的诊断及实时监测。microRNA(miRNA)是一类长度为21-25个核苷酸的小型非编码RNA,并在转录水平调控基因的表达,参与多种生理病理过程[2]。miRNA-582作为近年来参与肿瘤发展中的重要角色的微小RNA成员之一,目前研究表明miRNA-582涉及到膀胱癌[3]和结直肠癌[4]等肿瘤细胞生长及侵袭迁移的多种生物学进程中,但是结果仍有相互矛盾之处,前期我们的研究结果也表明miRNA-582与胃癌的发生、发展、侵袭有关,但是在化疗耐药中的机制尚未明确。LGR5是一种跨膜受体,属于G蛋白偶联受体家族成员,已经证实在多种人类实体肿瘤中高度表达,通过增强Wnt信号通路的活性,加速癌细胞的增殖及肿瘤形成[5]。本研究拟检测miR-582-5p在胃癌细胞AGS中调控胃癌细胞增殖能力、化疗药物奥沙利铂耐药性、细胞周期变化,探讨miR-5825p作为胃癌治疗靶点的可能性。
1 材料与方法
1.1 主要试剂和仪器
反转录试剂盒购自美国Thermo Scientific公司;real-time PCR试剂购自日本TaKaRa公司,Trizol试剂购自美国Invitrogen公司;miR-582-5p、U6引物由广州锐博生物科技有限公司设计并合成;RPMI-1640、胎牛血清、OPTI-MEN购自美国Gibco公司;LipofectamineTM2000购自美国Invitrogen公司;Annexin Ⅴ-FITC试剂盒购自美国BD公司;MTT购自美国Sigma公司;miR-582-5p mimic和Negative Control(NC)由上海吉玛公司生产;LGR5、cyclinD1、c-myc、surviven、MDR1和GAPDH抗体购自美国Santa Cruz公司。real-time PCR检测仪器为美国Bio-Rad公司生产的CFX96TMreal-time PCR Detection System;凝胶成像仪购自美国Bio-rad公司。
1.2 细胞培养
胃癌AGS细胞(西安交通大学医学院中心实验室馈赠)接种于RPMI1640培养基(含10%胎牛血清),置于37 ℃、5% CO2+95%空气培养箱中培养,定期观察并每隔2 d更换细胞培养液1次,待细胞长满约80%时用0.25%胰蛋白酶消化传代,取生长状态良好的对数期细胞进行后续实验。
1.3 real-time PCR检测miR-582-5p
用Trizol试剂按照操作说明对AGS细胞进行总RNA提取,各组细胞分别取2 μg RNA反转录成cDNA,行real-time PCR。反应条件:95 ℃预变性30 s;然后95 ℃ 5 s,60 ℃ 30 s,40个循环。以每个样本的U6作为内参,基因相对表达量采用2-ΔΔCt方法进行计算分析。实验重复3次。
1.4 细胞转染
将对数生长期AGS细胞经0.25%胰酶消化,取2×104个接种于6孔板,按实验设计分实验组(转染miR-582-5p mimics)、阴性对照组(转染negative control)和空白对照组(untreated cell)。用250 μl OPTI-MEN稀释LipofectamineTM2000转染试剂5 μl室温下静置5 min,再用250 μl OPTI-MEN稀释miR-582-5p mimics或Negative Control 5 μl,两者混合室温下静置20 min,每孔加入500 μl转染复合液,在37 ℃含5%的CO2培养箱中孵育6 h,用新鲜的含血清1640培养基替换含有转染复合物的培养基,供后续实验使用。实验重复3次。
1.5 细胞增殖实验
采用MTT法,取对数生长期的胃癌AGS细胞按5×103个/孔接种于96孔板,实验分组同上,每组设置4个复孔;未接种细胞孔中加入RPMI 1640培养基作为调零孔,放置含有5% CO2的37 ℃培养箱中,检测miR-582-5p mimics本身对细胞增殖的影响,细胞贴壁后分别更换含不同浓度的Oxaliplatin(奥沙利铂)培养基继续培养,换液后24,48,72,96 h各检测1次,每孔加入MTT 20 μl继续培养箱中孵育4 h用酶标仪检测其490 nm处吸光值。实验重复3次。
1.6 细胞周期检测
取胃癌AGS细胞按照2×105个/孔接种于6孔板,实验分组同上。转染后24 h换成无血清培养24 h,然后再换成含10%胎牛血清的RPMI 1640培养基培养24 h,用胰酶收集各组细胞,所收集细胞用预冷的PBS洗涤3次,1 000 r/min,5 min/次,弃上清。加入-20 ℃预冷的75%冰乙醇1 ml固定细胞,置于4 ℃冰箱过夜;检测前离心(1 000 r/min,5 min),用PBS洗涤2次;加入100 μl PBS并将细胞吹悬;用含0.01% RNase和0.5%碘化丙啶(PI)4 ℃处理细胞20 min。过300目尼龙网。送流式细胞仪检测。
1.7 Western blot检测LGR5的表达水平
将AGS细胞按照2×105个/孔接种于6孔板中,分为实验组、阴性对照组和空白对照组,收集转染72 h的各组细胞,加入细胞裂解液,提取细胞总蛋白,BCA法检测总蛋白浓度,每组样本取10 μl进行10% SDS-PAGE垂直电泳,湿转法将胶中蛋白水平转移至PVDF膜上,5%脱脂牛奶在37 ℃摇床上封闭1 h,加入TBST稀释后的一抗,4 ℃过夜;取出后TBST洗膜3次再加入二抗,孵育1 h,再洗膜3次,添加ECL发光液反应底物,凝胶成像系统扫描,采用相关图像分析软件(Bio-rad Quantity One,CA)进行条带灰度分析实验采用GAPDH作为参照蛋白。
1.8 双荧光素报告基因检测
将AGS细胞按105个/孔接种于24孔培养板,用含10%FBS的RPMI 1640培养液培养,使细胞融合率达到70%左右,将内参质粒Renilla、荧光素酶报告基因质粒pGL3-LGR5-3′UTR以及miR-582-5p mimics共转染,继续培养24 h,裂解细胞,利用双荧光素酶活性检测试剂盒检测荧光素酶活性的变化。
1.9 统计学分析
采用SPSS18.0统计软件进行分析,两组间比较采用两样本t检验,多组间差异采用单因素方差分析(One-way ANOVA),P<0.05为差异有统计学意义。
2 结果
2.1 胃癌AGS细胞转染miR-582-5p mimics后miR-582-5p的表达水平
与阴性对照组比较,实验组miR-582-5p的表达水平显著升高,差异有统计学意义(P<0.05),而阴性对照组和空白对照组之间差异无统计学意义(P>0.05,见图1)。
2.2 上调miR-582-5p对胃癌细胞增殖的影响
MTT结果显示,与阴性对照组比较,转染了miR-582-5p mimics的人胃癌细胞AGS,在转染24,48 h生长速度差异没有统计学意义(均P>0.05),但是在转染72,96 h明显抑制,随着OD值减小,细胞增殖能力明显降低(P<0.05,见图2),而阴性对照组和空白对照组间没有统计学差异(P>0.05)。结果表明上调miR-582-5p具有抑制胃癌细胞增殖的作用。
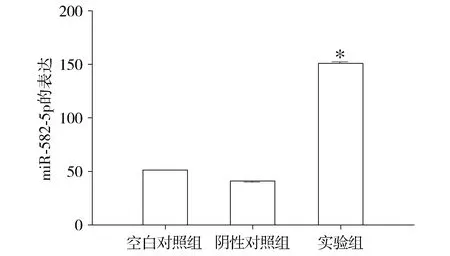
与其余两组比较,*P<0.05图1 Real-time PCR验证实验组转染效率Figure 1 miR-582-5p mimics transfection efficiency verified by real-time PCR
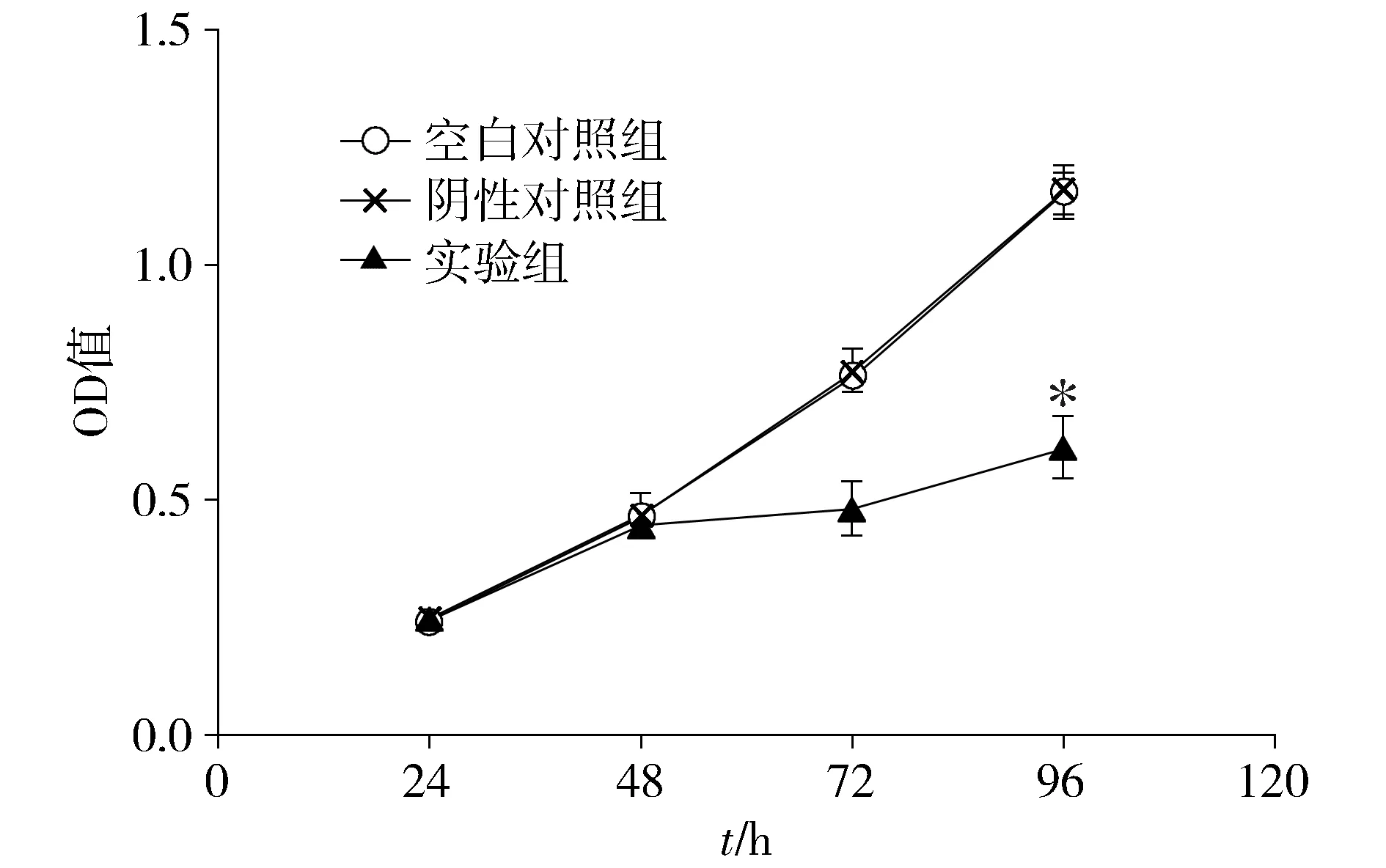
与其余两组比较,*P<0.05图2 MTT法检测上调miR-582-5p对胃癌细胞增殖的影响Figure 2 The proliferation ability of up-regulation of miR-582-5p in AGS cells by MTT
2.3 上调miR-582-5p对胃癌细胞周期的影响
流式细胞仪检测结果见图3。相对于阴性对照组,实验组人胃癌细胞AGS中G0/G1期细胞比例明显增多(61.6%±1.32%vs50.87%±2.77%,P<0.05),S期细胞比例减少(21.93%±1.49%vs30.03%±1.71%,P<0.05),G2/M期细胞比例无统计学差异(11.03%±0.61%vs11.61%±0.88%,P>0.05),而阴性对照组和空白对照组间没有统计学意义(P>0.05)。结果表明上调miR-582-5p具有抑制胃癌细胞G1/S转化的作用。
2.4 上调miR-582-5p对胃癌细胞耐药性的影响
细胞计数实验显示,药物维持时间在48 h,随着奥沙利铂浓度增高(1,2,4μg/ml),相比空白对照组,实验组AGS细胞转染miR-582-5p mimics以后对奥沙利铂的敏感性增加,生长明显抑制,差异具有统计学意义(见图4A)。在2 μg/ml和4 μg/ml浓度时,空白对照组和阴性对照组细胞活力无明显差异,所以选择浓度较低的2 μg/ml进行后续试验,奥沙利铂浓度维持在2 μg/ml,随着药物维持时间增加(24,48,72 h),相比阴性对照组,实验组AGS对奥沙利铂敏感性增加,生长明显抑制,差异具有统计学意义(见图4B)。上述结果表明,上调miR-582-5p具有增加胃癌细胞对奥沙利铂的敏感性,降低耐药性。
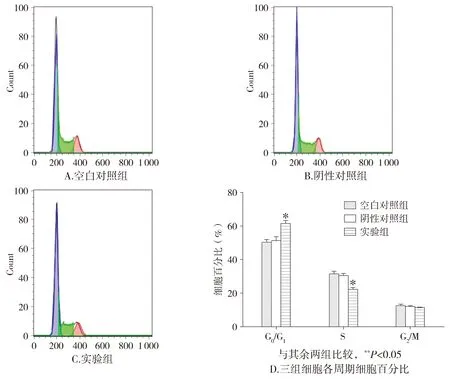
图3 流式细胞仪法检测上调miR-582-5p对胃癌细胞周期的影响Figure 3 Effect of up-regulation of miR-582-5p in AGS cells by FCM
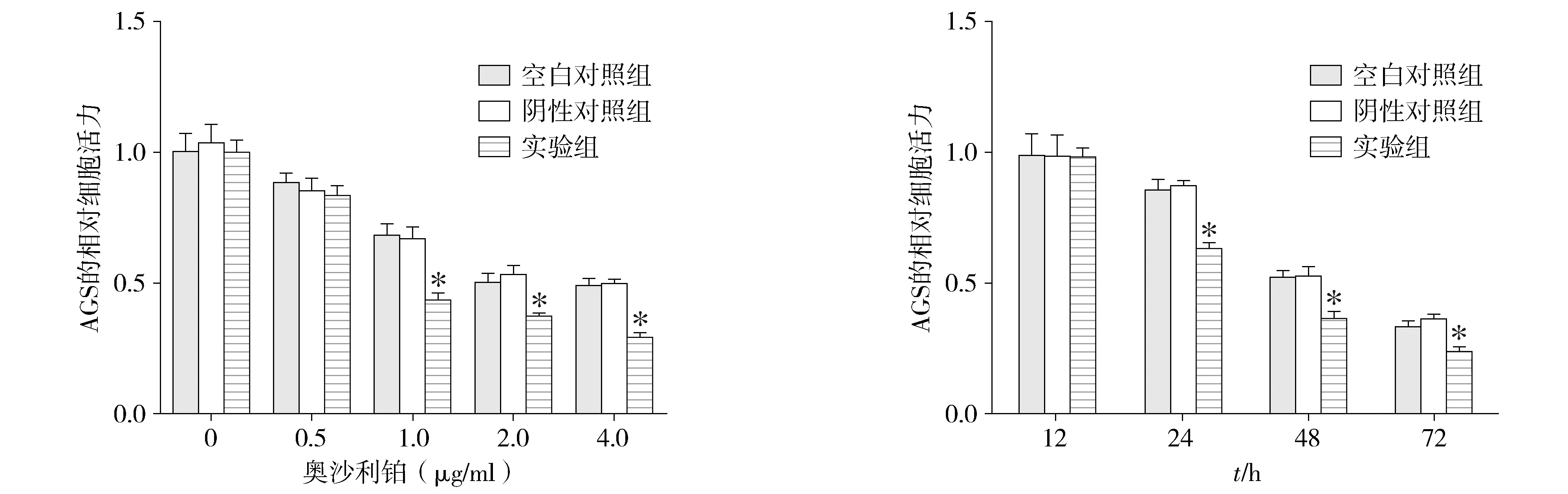
A.随着奥沙利铂浓度增加,miR-582-5p mimics敏感性增强B.2 μg/ml奥沙利铂在不同时间对各组细胞活力的影响与其余各组比较,*P<0.05图4 MTT法检测上调miR-582-5p对胃癌细胞化疗耐药性的影响Figure 4 Chemotherapy resistance of drugs to AGS cells after up-regulation of miR-582-5p by MTT
2.5 miR-582-5p调控的靶基因并验证
通过靶基因预测软件PicTar、TargetScan和microRNA.org预测并分析,LGR5基因可能是miR-582-5p的靶基因之一。双荧光素报告基因检测结果发现转染miR-582-5p mimics后,含有LGR5基因3′UTR的荧光素酶活性受到明显抑制(P<0.05,见图5A)。Western bolt结果显示转染miR-582-5p mimics后,实验组较阴性对照组和空白对照组LGR5的蛋白表达水平明显受到抑制(0.41±0.38vs0.91±0.08,1.01±0.02,见图5B、5C),差异有统计学意义,而LGR5的mRNA表达水平没有统计学差异(见图5D)。
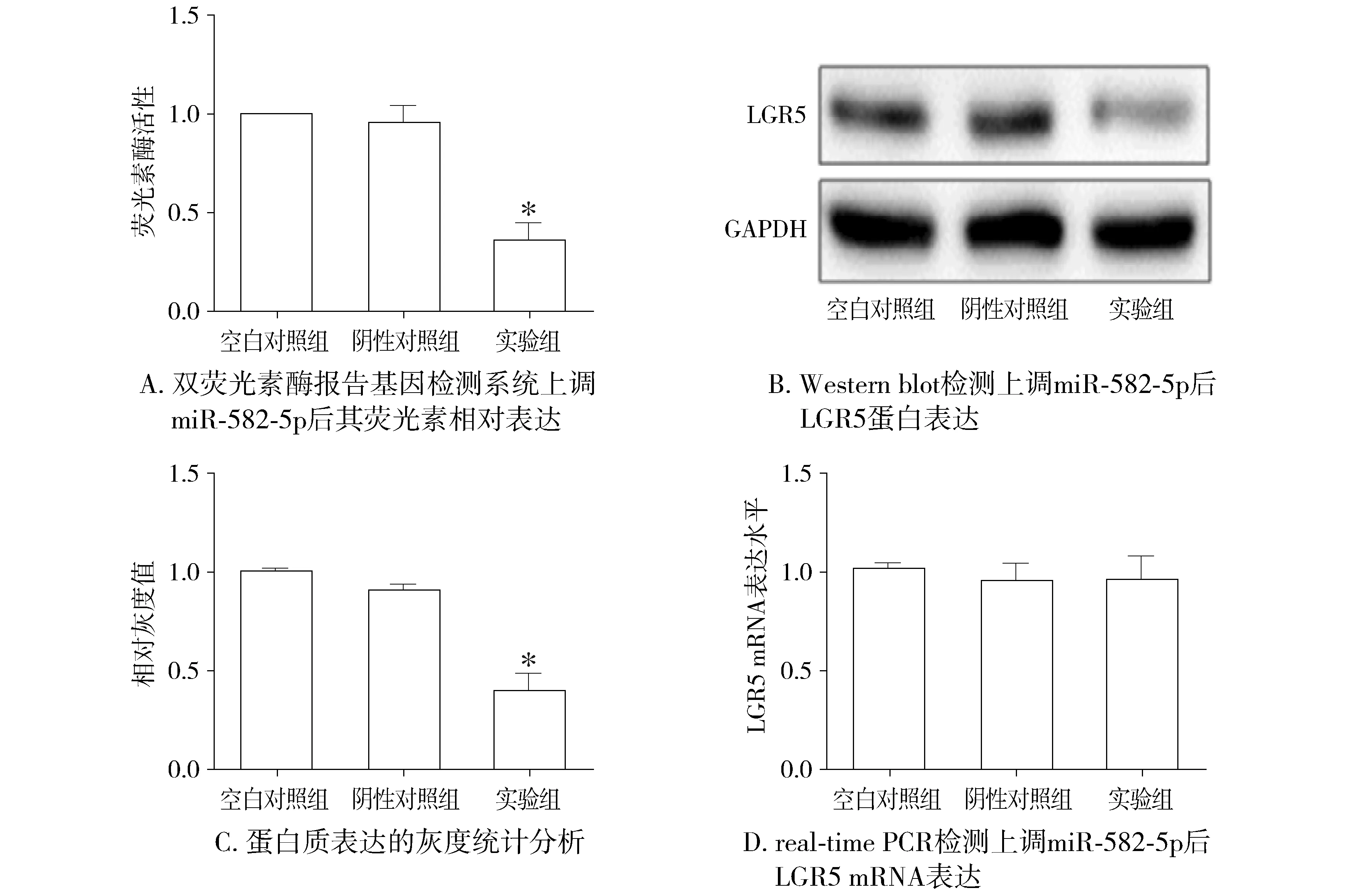
与其他两组比较,*P<0.05图5 预测miR-582-5p调控的靶基因并验证Figure 5 Prediction of miR-582-5p regulatory target genes and verification
2.6 上调miR-582-5p对Wnt/β-catenin下游相关靶基因的影响
与阴性对照组比较,实验组的AGS细胞cyclinD1,c-myc,survivin、MDR1表达明显降低(均P<0.05)。阴性对照组和空白对照组之间比较差异没有统计学意义(P>0.05,见图6)。
3 讨论
大量的研究表明,多种肿瘤中miRNA的高表达或低表达,miRNA可能扮演原癌基因和抑癌基因的角色[6]。根据既往研究,在胃癌中多种miRNA异常表达,提示在胃癌的发生发展中miRNA的表达差异性是普遍的现象,miRNA的异常表达与胃癌细胞增殖活性、药物敏感性和侵袭迁移能力密切相关[7]。miR-582-5p已被证实在人的多种肿瘤发生发展中发挥作用。本课题组前期的工作表明miR-582在胃癌中低表达[8],但是关于miR-582-5p在胃癌中的作用的机制研究至今少有报道。
LGR5是G蛋白偶联受体家族成员之一,已经被认为是小肠、结肠[9]和毛囊[10]的干细胞标志之一。有文献报道在许多实体肿瘤中检测到LGR5表达增高,如肺癌[11]、结直肠癌[12]、卵巢癌[13]和基底细胞癌[14]等,高表达LGR5与肿瘤发生、侵袭和迁移有关,提示LGR5可能在肿瘤形成过程中发挥作用。Wnt信号通路作为一个高度保守的系统,在调节干细胞和肿瘤方面发挥重要作用,其异常激活往往与肿瘤形成相关[15]。越来越多研究结果表明LGR5参与到Wnt/β-catenin信号通路中[16],通过募集结合了Wnt配体的LRP-Frizzled受体复合物从而导致LRP的磷酸化和下游一系列分子的激活,包括β-catenin的聚集,转入核,与TCF/LEF转录因子协调激活相关基因的表达,如cylinD1、c-myc、survivin、MDR1等[16]。
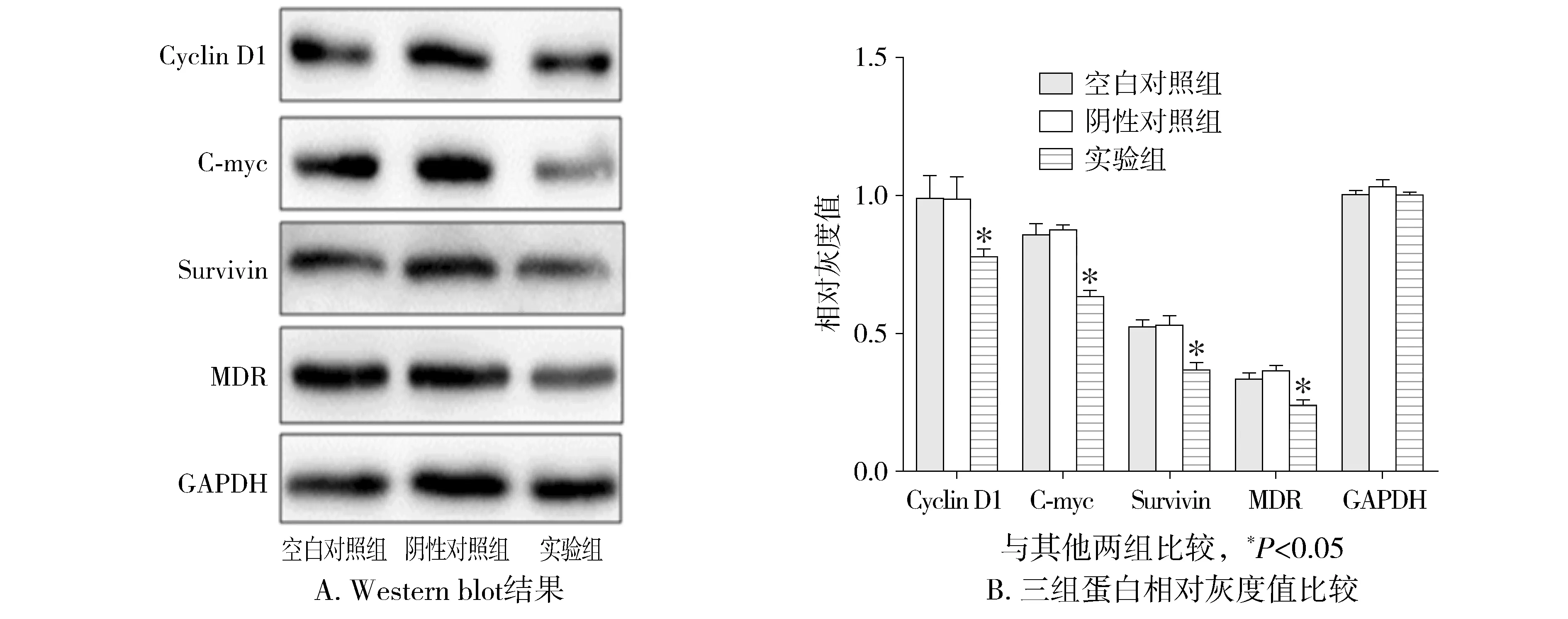
图6 Western blot检测上调miR-582-5p对Wnt/β-catenin下游相关靶基因的影响Figure 6 The effects of up-regulation of miR-582-5p on downstream target of Wnt/β-catenin by Western blot
本研究得出LGR5可能作为miR-582-5p在胃癌细胞的靶基因之一,上调miR-582-5p能够通过降低LGR5的表达而抑制胃癌细胞的增殖和周期,降低细胞对奥沙利铂的耐药性。因此,本研究提示miR-582-5p在胃癌的肿瘤形成过程中扮演着抑癌基因的角色。其他肿瘤的相关研究报道,miRNA-582-5p在肝癌组织和肝癌细胞系的表达降低,上调miR-582-5p能抑制肝癌细胞的生长,能直接靶向CDK1和AKT3且间接抑制cyclinD1来调节肝癌的进程[18]。在膀胱癌中利用miR-582-5p通过靶向PGGT1B、LRRK2和DIXDC1相关基因的机制实现肿瘤的治疗效应[3]。在人前列腺癌细胞和脑胶质瘤细胞中miR-582-5p表达上调且促进细胞增殖,在去势抵抗前列腺癌异体移植模型中miR-582-5p靶向下调增殖相关基因EFNB2[19],而胶质瘤中靶向下调凋亡相关基因caspase 3、caspase 9和Bim[20]。在人结直肠癌细胞中,miR-582-5p上调并通过靶向Rab27a[21]来抑制细胞周期,同时存在靶向APC来促进细胞增殖[22]的不一致的研究结果。在此,本研究得出miR-582-5p通过LGR5调控Wnt通路,导致cyclinD1,c-myc,survivin和MDR1蛋白表达下调,从而抑制胃癌细胞的增殖和周期,导致细胞的耐药。
综上所述,上调miR-582-5p能够抑制胃癌细胞的增殖活性和细胞周期,增加胃癌细胞化疗药物敏感性,预测其在胃癌中可能扮演致抑癌基因的角色,可能通过靶基因LGR5发挥生物学功能。
参考文献:
[1] Chen J, Kong Y, Weng S,etal. Outcomes of surgery for gastric cancer with distant metastases: a retrospective study from the SEER database[J]. Oncotarget, 2017,8(3):4342-4351.
[2] Qi M, Liu D, Zhang S. MicroRNA-21 contributes to the discrimination of chemoresistance in metastatic gastric cancer[J]. Cancer Biomarke, 2017, 18(4):1-8.
[3] Uchino K,Takeshita F,Takahashi RU,etal. Therapeutic effects of microRNA-582-5p and-3p on the inhibition of bladder cancer progression[J]. Mol Ther, 2013, 21(3):610-619.
[4] Tamura G.Alterations of tumor suppressor and tumor-related genes in the development and progression of gastric cancer[J]. World J Gastroenterol, 2006, 12(2):192-198.
[5] Miao J, Jiang Y, Wang D,etal. Trichosanthin suppresses the proliferation of glioma cells by inhibiting LGR5 expression and the Wnt/β-catenin signaling pathway[J]. Oncol Rep,2015,34(6):2845-2852.
[6] Leva GD, Garofalo M, Croce CM. MicroRNAs in cancer[J]. Annu Rev Pathol, 2014, 9(1):287-314.
[7] Shi Z, Wei Q, She J. MicroRNAs in gastric cancer metastasis[J]. Crit Rev Eukaryot Gene Expr, 2014, 24(1):39-53.
[8] 刘栋,王建华,宋斌,等.miR-582在胃癌组织中的表达及其作用机制[J].山西医科大学学报,2017,48(4):316-321.
[9] Barker N, van Es JH, Kuipers J,etal. Identification of stem cells in small intestine and colon by marker gene Lgr5[J]. Nature, 2007, 449(7165):1003-1007.
[10] Jaks V, Barker N, Kasper M,etal. Lgr5 marks cycling, yet long-lived, hair follicle stem cells[J]. Nat Genet, 2008, 40(11):1291-1299.
[11] Gao F, Zhou B, Xu J C,etal. The role of LGR5 and ALDH1A1 in non-small cell lung cancer: Cancer progression and prognosis[J]. Biochem Biophys Res Commun, 2015, 462(2):91-98.
[12] Ding H, Wang C. Role of Lgr5-positive cells in colorectal cancer[J]. Tumour Biol, 2015, 36(9):6759-6764.
[13] Ng A, Tan S, Singh G,etal. Lgr5 marks stem/progenitor cells in ovary and tubal epithelia[J]. Nat Cell Biol, 2014, 16(8):745-757.
[14] Tanese K, Fukuma M, Yamada T,etal. and tumor formation[J]. Am J Pathol, 2008, 173(3):835-843.
[15] Dravid G, Ye Z, Hammond H,etal. Defining the role of Wnt/β-catenin signaling in the survivl, proliferation, and self-renewal of human embryonic stem cells[J]. Stem Cells, 2010, 23(10):1489-1501.
[16] Carmon KS, Lin Q, Gong X,etal. LGR5 interacts and cointernalizes with Wnt receptors to modulate Wnt/β-catenin sigaling[J]. Mol Cell Biol, 2012, 32(11):2054-2064.
[17] Carmon KS, Gong X, Lin Q,etal. R-spondins function as ligands of the orphan receptors LGR4 and LGR5 to regulate Wnt/beta-catenin signaling[J]. Proc Natl Acad Sci U S A, 2011,108(28): 11452-11457.
[18] Yi Z, Wei H, Yan R,etal. miR-582-5p inhibits proliferation of hepatocellular carcinoma by targeting CDK1 and AKT3[J]. Tumour Biol, 2015, 36(11):8309-8316.
[19] Maeno A, Terada N, Uegaki M,etal. Up-regulation of miR-582-5p regulates cellular proliferation of prostate cancer cells under androgen-deprived conditions[J]. Prostate, 2014, 74(16):1604-1612.
[20] Floyd DH, Zhang Y, Dey BK,etal. Novel anti-apoptotic microRNAs 582-5p and 363 promote human glioblastoma stem cell curvival via direct inhibition of caspase 3, caspase 9, and Bim[J]. PLoS One, 2014, 9(5):e96239.
[21] Zhang X, Zhang Y, Yang J,etal. Upregulation of miR-582-5p inhibits cell proliferation, cell cycle progression and invasion by targeting Rab27a in human colorectal carcinoma[J]. Cancer Gene Ther, 2015, 22(10):475-480.
[22] Shu Z, Chen L, Ding D. miR-582-5P induces colorectal cancer cell proliferation by targeting adenomatous polyposis coli[J]. World J Surg Oncol, 2016, 14(1):239-246.

