石墨烯-碳纳米管三维结构吸附分离CO2/H2S/CH4三元混合物的分子模拟
雷广平,羊光耀
(1.中北大学 能源动力工程学院,山西 太原 030051;2. 重庆大学 动力工程学院 低品位能源利用技术及系统教育部重点实验室,重庆 400030)
天然气作为一种清洁、经济的化石能源,2013年全球消耗量已经超过3.3×1012m3。根据产地不同,新开采出的天然气中通常含有不同含量的CO2和H2S等酸性气体。例如我国川东地区开采的天然气中H2S含量(φ,下同)高达15%,CO2含量接近10%[1]。酸性气体的存在会对设备及输送管道造成严重腐蚀。因此,在输送与使用前必须进行脱硫脱碳处理。目前化学工业中多采用有机胺溶液吸收的方法进行[1],但该方法具有能耗高、污染大和吸收剂再生困难的缺点。而以膜分离[2]和吸附分离[3]为代表的新型分离方法得到了越来越多的关注。
近年来,分子筛[4]、金属有机骨架[5]以及活性炭[6]等多孔固体材料已被用于 H2、CH4、CO2以及气体混合物吸附性能的研究中。碳纳米管[7]及石墨烯[8]等无机碳材料具有高比表面积、耐腐蚀、高化学稳定性及热稳定性等优点,可作为一种理想的吸附材料。近年,被成功合成的石墨烯-碳纳米管三维结构(GNHS)[9]同样表现出优良的吸附性能。研究发现锂掺杂GNHS的储氢能力高达41 g/L[10]。GNHS 对 H2S/CH4[11]以及 CO2/CH4[12]二元混合物也同样具有良好的吸附分离能力。
本工作采用蒙特卡洛(GCMC)模拟方法探讨压力对CO2/H2S/CH4三元混合物在GNHS内吸附分离性能的影响,并研究了气相混合物中H2S或CO2的存在对其他组分分离的影响。
1 模拟方法
GNHS 的模拟结构图见图 1[13]。GNHS 尺寸为4.064 nm×4.401 nm×2.656 nm,碳纳米管在x,y方向的距离分别为2.032 nm和2.198 nm,石墨烯狭缝宽度保持为0.664 nm。吸附剂材料保持刚性结构,x,y,z 3个方向均采用周期性边界条件。为了提高计算精度,CH4[14],CO2[14],H2S[15]均采用全原子模型,短程范德华力采用Lennard-Jones模型,截断半径选取1.2 nm。各势能模型参数如表1所示。

图1 GNHS的模拟结构图Fig.1 Simulated structure diagram of the graphene-nanotube hybrid structure(GNHS).
采用Music软件进行GCMC模拟[16],根据普光气田所开采天然气的实际组成情况[1],模拟中CO2和H2S的气体含量分别取9%和15%。气相中各组分的逸度采用Peng-Robinson状态方程计算[17],CO2-H2S,CO2-CH4,H2S-CH4间的相互作用因子分别为0.097,0.0919,0.08,忽略三元相互作用因子。每次计算共运行1×108步,其中前5×107步用于体系平衡计算,后5×107步用于统计相关数据。
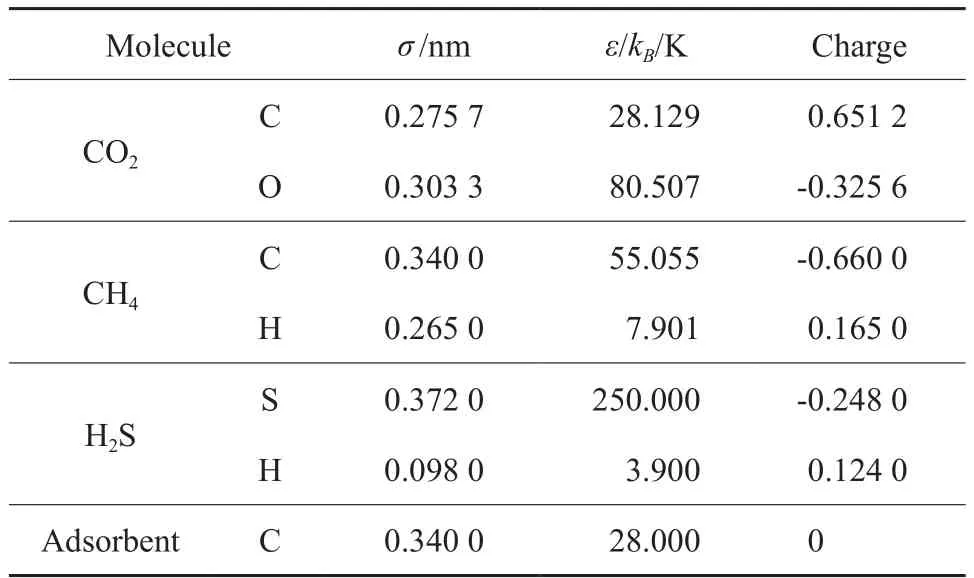
表1 各势能模型参数Table 1 Lennard-Jones parameters and charges of various models
通过GCMC模拟可得到各组分的吸附量、吸附选择性等参数,其中相对吸附选择性(S)的计算如式(1)所示[17]。

式中,x,y分别表示气相主体及吸附相中组分1和组分2的摩尔分数。
2 结果与讨论
2.1 压力对CO2/H2S/CH4三元混合物分离性能的影响
温度为300 K时3组分在GNHS内部的吸附等温线见图2。由图2可见,各组分间存在着明显的吸附竞争关系。随压力的升高,三组分的吸附量均呈现先增加后稳定的趋势。虽然H2S与CO2在气相中的含量较低,但两者在GNHS内部的吸附量明显高于CH4。为解释该现象,计算了吸附质分子之间以及吸附质与吸附剂间的相互作用能随压力的变化关系,如图3所示。由图3可见,CO2和H2S分子与吸附剂及其他吸附质分子间的相互作用明显高于CH4。当压力较低时,随着压力的升高,吸附质分子与吸附剂间的相互作用呈现降低趋势,而吸附质间的相互作用则逐渐增强,这是因为随着气体吸附量的升高,吸附质分子间距逐渐减小所致。进一步升高压力,吸附质分子之间以及吸附质与吸附剂之间的相互作用能则基本不再变化。
GNHS吸附材料可同时高效地分离天然气混合物中的CO2与H2S组分。CO2与H2S相对于CH4的吸附选择性随压力的变化关系见图4。由图4可见,两组分相对于CH4的选择性均高达100左右。随压力的升高,CO2的选择性快速上升至最大值后逐渐下降;而H2S的选择性则逐渐升高至一稳定值,直至压力升高至3.8 MPa后,出现下降趋势。当压力低于1.8 MPa时,GNHS对CO2的选择性高于H2S,而随着压力的继续升高,情况则发生反转。

图2 300 K时CO2/H2S/CH4三元混合物中各组分的吸附等温线Fig.2 Adsorption isotherms of different components of CO2/H2S/CH4 ternary mixture at 300 K.

图3 三元混合物中吸附质-吸附剂(a)和吸附质-吸附质(b)间的相互作用能随压力的变化Fig.3 Variations of interaction energy between adsorbate and adsorbent(a) and that between adsorbate and adsorbate(b)in the ternary mixture with pressure.
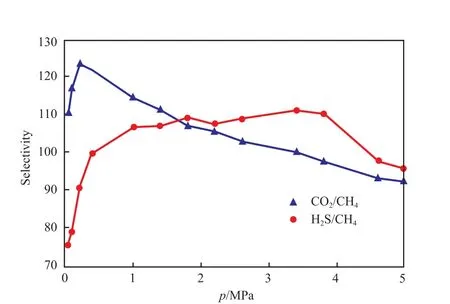
图4 CO2与H2S相对于CH4的选择性随压力的变化关系Fig.4 Selectivity variations of CO2 and H2S relative to CH4 with pressure.
2.2 温度对CO2/H2S/CH4三元混合物分离性能的影响
压力为5 MPa时,三元混合物中各组分吸附量随温度的变化关系曲线见图5。由图5可见,随温度的升高,吸附质分子热运动增强,增大了吸附质分子脱离吸附剂的可能性,尤其是吸附量较大的CO2与H2S气体,因此CO2与H2S的吸附量逐渐降低。而两组分的解吸又使得吸附剂内空点位增多,增加了CH4进入吸附剂内部的可能性,使CH4吸附量呈现上升趋势,这与以前对CO2/CH4以及H2S/CH4二元混合物的研究结果一致[11-12]。

图5 压力为5 MPa时三元混合物中各组分的吸附量随温度的变化关系Fig.5 Variations of adsorption amounts of different components of the ternary mixture under pressure of 5 MPa.
不同温度下CO2与H2S相对于CH4的选择性见图6。由图6可见,随温度的升高,GNHS对CO2和H2S的分离能力均逐渐减弱。温度由300 K升至500 K时,CO2与H2S相对CH4的选择性分别下降了87.0%和86.5%。

图6 CO2与H2S相对于CH4的选择性随温度的变化关系Fig.6 Selectivity variations of CO2 and H2S relative to CH4 with temperature.
2.3 H2S对CO2/CH4组分分离的影响
为了进一步探讨三元混合物中各组分的竞争关系,计算了CO2/CH4和H2S/CH4二元混合物在GNHS内部的吸附分离性能。二元混合物中各组分的摩尔比与它们在三元混合物中所占的比例相等。CO2/CH4二元混合物以及CO2/H2S/CH4三元混合物中CO2和CH4的吸附等温线见图7。由图7可见,由于H2S的存在占据了GNHS内部大量的吸附点位,导致CO2与CH4的吸附量出现不同程度的降低。在所研究的压力范围内,CO2与CH4的吸附量分别降低了47.8%和72.2%。说明H2S的存在可以更有效地抑制CH4吸附。

图7 二元及三元混合物中CO2与CH4的吸附等温线Fig.7 Adsorption isotherms of CO2 and CH4 in binary mixture and ternary mixture.
为了进一步说明H2S的存在对CO2/CH4分离的影响,研究了吸附质-吸附剂以及吸附质间的相互作用能随压力的变化关系,如图8所示。由图8可见,两组分与GNHS间的相互作用能基本不随压力的变化而变化,而吸附质间的相互作用则随着压力的升高而逐渐增强。这是由于随着压力的升高,更多的吸附质分子进入到GNHS内部,吸附质分子间的距离减小所致。另外,气相中H2S的存在导致两组分与GNHS间的相互作用呈现出不同程度的降低。这是由于H2S分子与GNHS间具有更强的相互作用,导致CO2与CH4分子很难靠近GNHS表面。CH4与吸附质间的相互作用能也有所减弱,这是由于大量的H2S分子吸附于GNHS内部形成较大团簇所致。而H2S的存在对CO2与吸附质间的相互作用则影响较小。

图8 吸附质-吸附剂(a)和吸附质-吸附质(b)间的相互作用能随压力的变化Fig.8 Variations of interaction energy between adsorbate and adsorbent(a) and that between adsorbate and adsorbate(b) with pressure.
CO2的选择性随压力的变化关系如图9所示。由图9可见,与三元混合物中CO2的选择性随压力的变化趋势不同,在CO2/CH4二元混合物中CO2的选择性随着压力的升高而逐渐增大至一稳定值。此外,气相中H2S的存在显著提高了GNHS对CO2的分离能力。但随着压力的升高,两者的差距有所降低。

图9 二元及三元混合物中CO2相对CH4的选择性随压力的变化关系Fig.9 Selectivity variations of CO2 relative to CH4 in binary mixture and ternary mixture with pressure.
2.4 CO2对H2S/CH4组分分离的影响
H2S/CH4二元混合物以及CO2/H2S/CH4三元混合物中H2S与CH4的吸附等温线如图10所示。由图10可见,由于气相中CO2组分的存在,导致在所研究的压力范围内H2S与CH4的吸附量分别平均降低了35.5%和39.8%。两值相差较小,说明气相中的CO2对H2S与CH4的吸附存在着相似的影响。

图10 二元及三元混合物中H2S与CH4的吸附等温线Fig.10 Adsorption isotherms of H2S and CH4 in binary mixture and ternary mixture.
H2S的吸附选择性随压力的变化关系如图11所示。由图11可见,在二元和三元混合物中H2S的选择性随压力变化基本一致。GNHS对三元混合物中H2S的分离能力略高于对H2S/CH4二元混合物的分离,但两者差别不大。

图11 二元及三元混合物中H2S相对CH4的选择性随压力的变化关系Fig.11 Selectivity variations of H2S relative to CH4 in binary mixture and ternary mixture with pressure.
3 结论
1)采用GCMC模拟方法研究了GNHS对CO2/H2S/CH4三元混合物的分离能力。GNHS可同时高效地分离天然气混合物中的CO2和H2S组分,两者的吸附选择性均达到100左右。
2)随温度的升高,GNHS对CO2与H2S的分离能力逐渐减弱。
3)与具有相同摩尔比的二元混合物相比,气相中H2S的存在可显著提高GNHS对CO2的分离能力,而CO2的存在对H2S的分离能力没有太大影响。
[1] Zhang J H,Shen B X,Sun H,et al. A study on the desulfurization performance of solvent UDS for purifying high sour natural gas[J].Pet Sci Technol,2011,29(1):48-58.
[2] Shan Meixia,Xue Qingzhong,Jing Nuannuan,et al. Influence of chemical functionalization on the CO2/N2separation performance of porous graphene membranes[J].Nanoscale,2012,4(17):5477-5482.
[3] Huang Liangliang,Zhang Luzheng,Shao Qing,et al. Simulations of binary mixture adsorption of carbon dioxide and methane in carbon nanotubes:Temperature,pressure,and pore size effects[J].J Phys Chem C,2007,111(32):11912-11920.
[4] Cosoli P,Ferrone M,Pricl S,et al. Hydrogen sulphide removal from biogas by zeolite adsorption:Part I. GCMC molecular simulations[J].Chem Eng J,2008,145(1):86-92.
[5] Hamon L,Serre C,Devic T,et al. Comparative study of hydrogen sulfide adsorption in the MIL-53(Al,Cr,Fe),MIL-47(V),MIL-100(Cr),and MIL-101(Cr) metal-organic frameworks at room temperature[J].J Am Chem Soc,2009,131(25):8775-8777.
[6] Feng Wenguo,Kwon S,Borguet E,et al. Adsorption of hydrogen sulfide onto activated carbon fibers:Effect of pore structure and surface chemistry[J].Environ Sci Technol,2005,39(24):9744-9749.
[7] Arab M,Picaud F,Devel M,et al. Molecular selectivity due to adsorption properties in nanotubes[J].Phys Rev B,2004,69(16):165401.
[8] Chen Jiejie,Li Wenwen,Li Xueliang,et al. Improving biogas separation and methane storage with multilayer graphene nanostructure via layer spacing optimization and lithium doping:A molecular simulation investigation[J].Environ Sci Technol,2012,46(18):10341-10348.
[9] Bittolo B S,Valentini L,Kenny J M,et al. Electrodeposition of transparent and conducting graphene/carbon nanotube thin fi lms[J].Phys Status Solidi A,2010,207(11):2461-2466.
[10] Dimitrakakis G K,Tylianakis E,Froudakis G E. Pillared graphene:A new 3-D network nanostructure for enhanced hydrogen storage[J].Nano lett,2008,8(10):3166-3170.
[11] Lei Guangping,Liu Chao,Xie Hui,et al. Removal of hydrogen sulf i de from natural gas by the gra phene-nanotube hybrid structure:A molecular simulation[J].Chem Phys Lett,2014,616-617:232-236.
[12] 雷广平,刘朝,解辉. 石墨烯/纳米管复合结构吸附分离CO2/CH4混合物的分子模拟[J].物理化学学报,2015,31(4):660-666.
[13] Xu Lanqing,Wei Ning,Zheng Yongping,et al. Graphenenanotube 3D networks:Intriguing thermal and mechanical properties[J].J Mater Chem,2012,22(4):1435-1444.
[14] Liu Lang,Nicholson D,Bhati a S K. Adsorption of CH4and CH4/CO2mixtures in carbon nanotubes and disordered carbons:A molecular simulation study[J].Chem Eng Sci,2014,121:268-278.
[15] Nath S K. Mol ecular simulation of vapor-liquid phase equilibria of hydrogen sulf i de and its mixtures with alkanes[J].J Phys Chem B,2003,107(35):9498-9504.
[16] Gupta A,Chempath S,Sa nborn M J,et al. Object-oriented programming paradigms for molecular modeling[J].Mol Simulat,2003,29(1):29-46.
[17] Wang Wenjuan,Peng Xuan,Cao Dapeng. Capture of trace sulfur gases from binary mixtures by single-walled carbon nanotube arr ays:A molecular simulation study[J].Environ Sci Te chnol,2011,45(11):4832-4838.

