有机改性对凹凸棒黏土吸附四环素类抗生素的影响
柴琴琴,呼世斌,刘建伟,李大成,王 嘉,何方健
1.西北农林科技大学资源环境学院,陕西 杨陵 712100 2.陕西有色冶金矿业集团有限公司,陕西 西安 710075 3.西安交通大学能源与动力工程学院环境工程系,陕西 西安 710049
四环素类抗生素(TCs)可以治疗和防御动物疾病并促进动物生长,具有价格低廉、广谱性等特点,长期以来被广泛应用于畜牧业中。TCs难以被动物的消化系统吸收,大多以母体化合物的形式随粪便和尿液排放到环境中。2011年中国畜禽粪便排放量约为21.21亿t,预计到2020年达到28.75亿t[1]。这些粪便多有TCs残留,如猪粪中四环素、土霉素、金霉素平均值分别为5.22、9.09、3.57 mg/kg[2]。TCs水溶性较好,易随畜禽粪便还田并最终进入地表水体。TCs在不同水体中的浓度与其来源有关,猪场废水中TCs残留量较高,可达“mg/L”级别,而地表水多在10 μg/L以下,地下水和饮用水源已检测到土霉素质量浓度为0.008 6 μg/L[1]。TCs在环境中不断积累,对生态系统造成严重威胁,频繁滥用抗生素会产生耐药性细菌,危害人类健康。
凹凸棒黏土(ATP) 存在于自然界中,是一种含水富镁铝硅酸盐,具有来源广泛、比表面积大、价格低廉等优点,已被用来作为吸附剂材料和催化剂的载体,广泛应用于石油化工、医药、污水处理等领域[3-4]。ATP表面带负电荷,且疏水性弱,亲水性强,对有机污染物的吸附能力比较差,经有机改性后,有机阳离子与ATP表面负电荷位点作用,使有机改性ATP的疏水性增强,亲水性降低,从而增强了对有机污染物的吸附能力[2]。抗生素在土壤中的吸附行为已经成为国际上的研究热点[5-7],目前主要集中在此类单一抗生素在土壤上的吸附行为,对于同类中不同种别的抗生素在土壤上吸附研究较少,利用有机改性ATP对水体中TCs的吸附研究国内外鲜见报道。
本研究采用阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)对ATP进行改性,制备了阳离子改性凹凸棒土(CTAB-ATP)。研究pH、吸附剂的投加量、阳离子强度等对吸附效果的影响,并研究其对四环素类物质的吸附性能及吸附机理。以期为有机改性ATP在环境修复方面提供科学依据。
1 实验部分
1.1 试剂与仪器
ATP购于中国;四环素(TC,纯度≥97.5%)、土霉素(OTC,纯度≥97%)、金霉素(CTC,纯度≥99%)均购于中国。高效液相色谱仪(HPLC,Waters 600E-2487,美国)。
四环素、土霉素、金霉素标准溶液配制:分别称取一定量的四环素、土霉素、金霉素标准品,用甲醇溶解定容,配成质量浓度为100 mg/L的标准储备液100 mL,储存于棕色瓶中,置于冰箱4 ℃保存。临用前,取此储备液,用甲醇稀释成所需浓度。
四环素、土霉素、金霉素使用液配制:用0.01 mol/L CaCl2溶液配制。
1.2 有机改性ATP的制备
1.2.1 ATP的纯化
采用2%的 (NaPO3)6对ATP进行纯化处理,将纯化后的ATP与1 mol/L盐酸溶液按水土体积比1∶10在室温下连续搅拌7 h,用蒸馏水洗涤至洗涤液中检测不到氯离子为止,烘干,保存备用。
1.2.2 ATP的有机改性
采用湿法制备CTAB-ATP,CTAB的添加量为1.0倍的ATP的阳离子交换量(ATP的阳离子交换量为293.20 mmol/kg),以1∶10固液体积比搅拌24 h,过滤,用蒸馏水洗涤滤饼4次,105 ℃烘干,过0.125 mm筛,备用。
1.2.3 结构表征
将改性前后的ATP分别用SEM(日本,S-3400N)、XRD(日本,Rigaku Dmax-RA)、FT-IR(德国,Tensor27)和TG-DSC(德国,STA449F3)表征[8]。
1.3 实验方法
1.3.1 影响因素实验
所有影响因素实验在室温避光条件下进行,称取50 mg CTAB-ATP于离心管中,加入质量浓度为40 mg/L抗生素20.00 mL,于190 r/min的恒温摇床内振荡360 min,取上清液,经0.45 μm水系滤膜过滤。为防止四环素在水中降解,在滤液中滴加一滴6 mol/L盐酸使其pH降至2~3[9],再用高效液相色谱仪测定滤液中的3种TCs浓度。
使用NaOH和HCl调节四环素溶液至不同的pH,通过改变投加量(0.50~3.50 g/L),改变CaCl2背景溶液浓度为0.01、0.03、0.05、0.07 mol/L并调节溶液的离子强度,分别考察pH、吸附剂投加量、Ca2+对TCs吸附的影响。
1.3.2 吸附实验方法
吸附实验参照OECD guideline 106批量平衡吸附法进行[10]。分别称取50 mg CTAB-ATP 于离心管中,加入质量浓度为40 mg/L抗生素20.00 mL,溶液pH调至6~7(根据本实验所得),加盖密封,于190 r/min的恒温摇床内振荡,分别于0、15、30、60、90、120、180、240、360、480 min时取样,于5 500 r/min转速下离心10 min,取样测定3种四环素类抗生素,方法同第1.3.1节。
分别称取50 mg CTAB-ATP于离心管中,加入20 mL不同浓度TCs溶液(质量浓度梯度为20、40、60、80、100、150 mg/L)。pH调至7,于190 r/min的恒温摇床内振荡180 min,取样测定3种TCs,同时利用不同等温吸附方程进行拟合。
以上处理均进行3个平行实验,其中未含抗生素的处理作为空白,未含吸附剂的处理作为对照。抗生素在吸附剂上的吸附量和去除率分别由式(1)、式(2)计算,同时利用不同动力学方程进行拟合。
(1)
(2)
式中:Qt为t时刻改性ATP对抗生素的吸附容量,mg/g;C0为溶液中抗生素初始质量浓度值,mg/L;Ct为t时刻溶液中抗生素质量浓度,mg/L;
V为处理溶液体积,L;m为CTAB-ATP质量,g。
1.3.3 测定方法
采用乙酸钠火焰光度法测定ATP的阳离子交换量。测定四环素类物质的高效液相色谱条件[11-13]:进样量为10 μL,柱温25 ℃,流速为1 mL/min,流动相是浓度为0.01 mol/L的草酸与乙腈、甲醇体积比为76∶16∶8,紫外检测器检测波长为355 nm。
1.4 数据处理
数据处理和拟合分析采用Origin 8.0分析软件,相关计算公式和模型见表1。

表1 模型公式Table 1 Model formula
注:qe为平衡吸附容量,mg/g;qt为任意时刻t的吸附容量,mg/g;k1为准一级动力学方程吸附速率常数,L/min;k2为准二级动力学方程吸附速率常数,g/(mg·min);A和B均为常数;Ce为吸附平衡时溶液的质量浓度,mg/L;KL为吸附平衡常数,L/mg;qm为饱和吸附量,mg/g;Kf为当Ce=1时的吸附能力,(mg/g)/(mg/L)n;1/n为吸附强度;Kt1为Temkin常数,mg/g;Kt2为Temkin常数,L/mg。
2 结果与讨论
2.1 影响因素
2.1.1 pH对抗生素吸附的影响
溶液pH是影响CTAB-ATP吸附量的重要参数。TCs具有共同的基本母核,是一种四元弱酸,形态分布见图1,在水溶液中存在4 种形态,当pH<3.3时,四环素分子结构中的二甲氨基被质子化,主要以阳离子形式(TC+)存在;当pH为3.3~7.7时,四环素分子中的酚二酮基团失去质子,以两性离子形式(TC0)存在;当pH>7.7时,以氨基化阴离子(TC-)或者二价阴离子(TC2-)存在[5]。

图1 四环素分子结构在不同pH条件下的形态分布Fig.1 Form distribution of Molecular structure of tetracycline under different pH
pH对CTAB-ATP吸附3种TCs的影响见图2。由图2可知,体系pH为3~7时,CTAB-ATP对3种TCs的吸附量随着溶液pH的增加呈现增长趋势。此后,pH继续增加,吸附量变化不大。
如在强酸条件下(pH=3),CTAB-ATP对四环素、土霉素及金霉素的吸附量分别为1.29、1.09、0.22 mg/g,在pH=7时吸附量分别为11.75、9.92、5.46 mg/g,而在pH=9时分别为12.28、10.21、5.68 mg/g。在酸性条件下,四环素以阳离子形态存在,体系中的H+与四环素会竞争吸附在CTAB-ATP表面上,从而阻碍了四环素在CTAB-ATP上的吸附;pH在3~7范围内升高时,CTAB-ATP逐渐去质子化,使其对四环素的吸附容量逐渐提高;在碱性条件下,ATP表面的电负性进一步增强,另外,接枝在ATP上的CTAB表面正电荷增多,其表面亲水性减弱,疏水性增强[21],通过CTAB-ATP与四环素之间的相互作用力,提高了对四环素的吸附能力,并且在较大的pH范围仍具有优异的吸附性能。土霉素和金霉素的分子结构性质与四环素相似,三者具有相似的吸附机理。

图2 pH对有机改性ATP吸附3种TCs的影响Fig.2 Effects of pH on the absorption of three tetracycline antibiotics in CTAB-ATP
2.1.2 吸附剂投加量对TCs吸附的影响
室温下,四环素质量浓度为40 mg/L,研究CTAB-ATP的投加量对3种四环素的吸附影响如图3所示。从图3可以看出,CTAB-ATP投加量为0.54~2.50 g/L时,CTAB-ATP对3种四环素类抗生素的吸附容量显著减少,主要是因为吸附剂投加量的增加会提高吸附作用的活性吸附位点,投加量为0.54 g/L时,四环素、土霉素及金霉素的吸附量分别高达39.75、27.04、25.49 mg/g。当吸附剂的量超过2.50 g/L时,吸附量的增量呈现缓慢减小趋势,这可能是由于CTAB-ATP用量达到一定数值时四环素类物质与CTAB-ATP之间达到吸附平衡,所以继续增加CTAB-ATP用量,对四环素类物质的吸附容量也无明显提高。吸附剂投加量为2.60 g/L时,四环素、土霉素及金霉素的吸附量分别为14.39、10.79、6.96 mg/g。最终确定CTAB-ATP对3种四环素类抗生素吸附的最佳投加量为2.50 g/L。
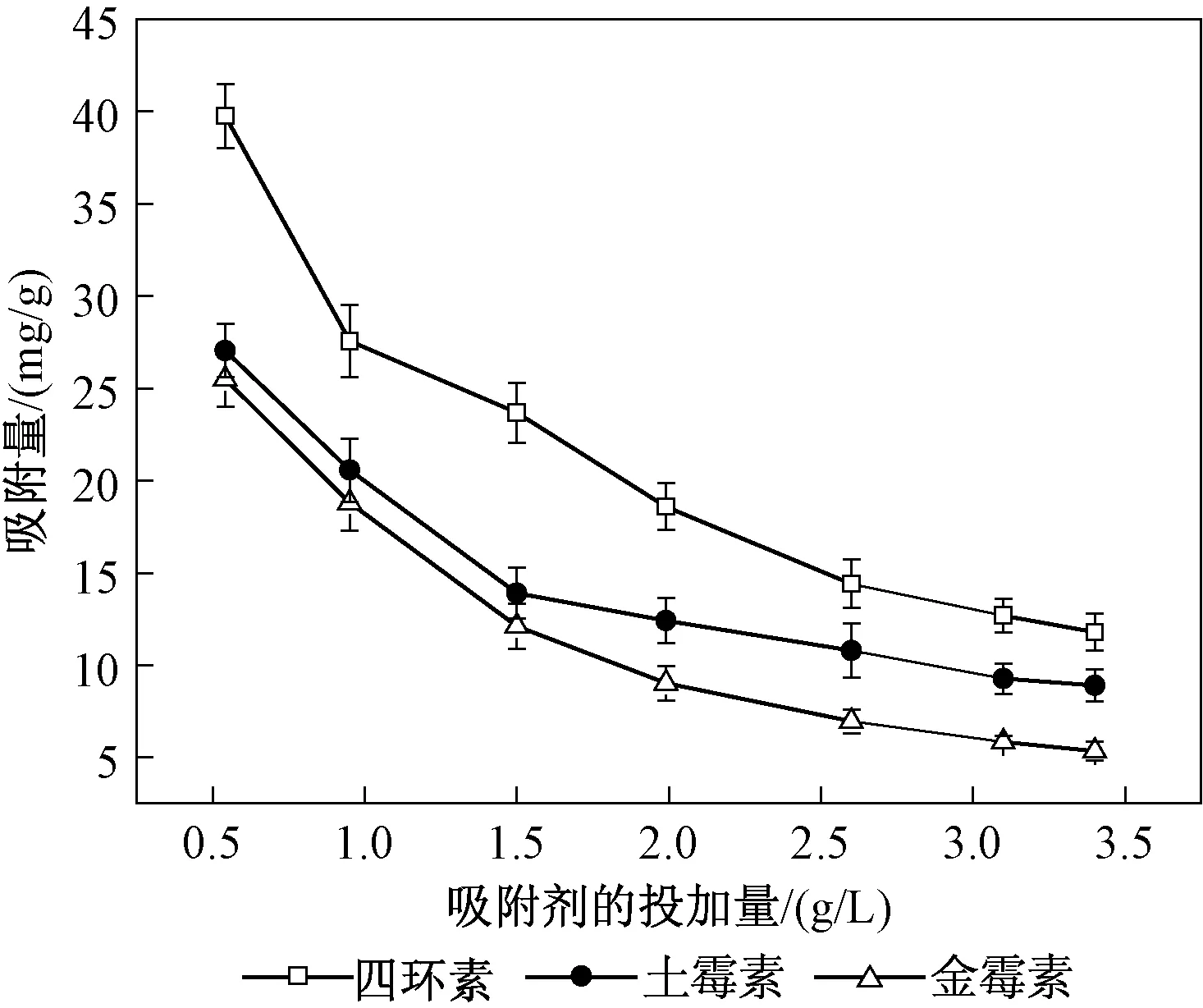
图3 CTAB-ATP的投加量对3种四环素类抗生素吸附的影响Fig.3 Effects of CTAB-ATP dosage on the adsorption of three tetracycline antibiotics
2.1.3 离子强度对CTAB-ATP吸附TCs能力的影响
实验考察了溶液中不同浓度Ca2+对吸附的影响。如图4所示,随着离子强度的增加,3种TCs在CTAB-ATP上的吸附量逐渐减少,Ca2+浓度由0 mol/L增至0.07 mol/L时,四环素、土霉素及金霉素的吸附量分别下降了8.89%、17.24%及20.12%。离子强度的增加降低了CTAB-ATP对3种四环素类抗生素的吸附性能,这可能是由于Ca2+和四环素之间对吸附位点的竞争效应引起的,且随着Ca2+浓度逐渐增大,CTAB-ATP表面的吸附位点越来越少[22-23]。PAROLO等[24]研究发现,在阳离子存在情况下,溶液中的金属阳离子容易与四环素发生螯合反应,可能对吸附产生一定的影响。GAO等[25]研究发现,阳离子会产生静电屏蔽作用,从而影响吸附作用。这均与本文的实验结果一致。
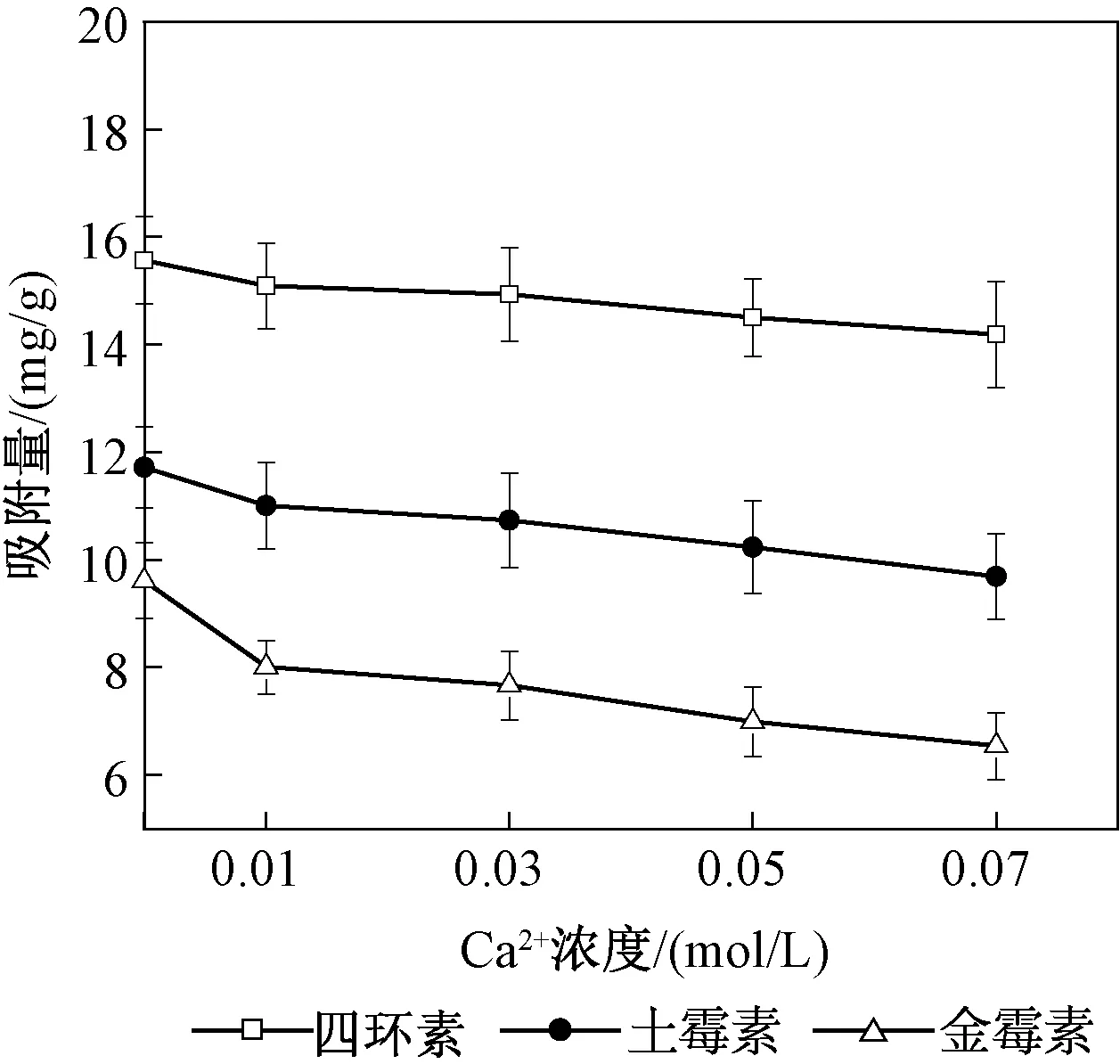
图4 不同阳离子浓度对CTAB-ATP吸附3种TCs的影响Fig.4 Effects of cation concentrations on the adsorptionof three tetracycline antibiotics in CTAB-ATP
2.2 吸附实验
2.2.1 CTAB-ATP对3种TCs的吸附动力学
CTAB-ATP对3种TCs的吸附量随时间变化的趋势见图5。

图5 3种TCs在CTAB-ATP上的吸附动力学曲线Fig.5 Kinetic curves of the adsorption of three tetracycline antibiotics in CTAB-ATP
由图5可知,随着吸附时间的增加,CTAB-ATP对3种TCs吸附大致分为2个阶段:第一阶段为前60 min的快速吸附阶段,其吸附量随着时间的增加而显著增加,四环素和金霉素均达到平衡吸附量的90%左右,而土霉素达到平衡吸附量的80%左右;第二阶段为慢速吸附阶段(60 min后),该阶段吸附量逐渐趋于平稳,CTAB-ATP对3种TCs的吸附均在180 min达到平衡,四环素、土霉素、金霉素的平衡吸附量分别高达13.83、13.01、10.08 mg/g。当CTAB-ATP投入抗生素溶液中时,大量的抗生素被迅速吸附到CTAB-ATP表面,随着时间的延长,CTAB-ATP表面吸附位点逐渐被完全占据,吸附容量将逐渐平稳,最终当吸附达到饱和状态时,吸附量不再增加。比较图5的吸附速率曲线发现,CTAB-ATP对四环素、土霉素、金霉素的吸附变化趋势基本一致,CTAB-ATP对3种TCs的吸附能力从大到小依次为TC>OTC>CTC。
分别采用表1中的准一级动力学模型、准二级动力学模型、颗粒内扩散模型和Elovich 模型对上述吸附过程进行拟合,拟合参数见表2。对比拟合结果的相关系数r可知,CTAB-ATP对四环素、土霉素、金霉素的吸附过程均符合准二级动力学模型[图6(b)],这与NIU等[5]关于有机改性蒙脱土对四环素的吸附结果一致,说明化学吸附是ATP去除抗生素的主要机制[26]。采用准二级动力学模型拟合得到的CTAB-ATP对3种TCs的平衡吸附量(qe)从大到小顺序依次为四环素>土霉素>金霉素。由表2可知,用颗粒内扩散模型拟合得到的常数A≠0,说明CTAB-ATP对TCs的吸附过程复杂,存在一定的离子内扩散过程。
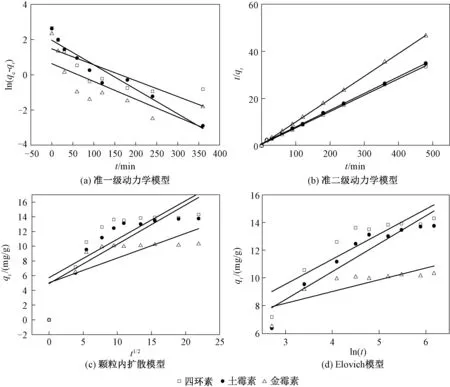
图6 CTAB-ATP吸附3种TCs的动力学模型Fig.6 Adsorption kinetics models of three tetracycline antibiotics on CTAB-ATP

抗生素一级动力学模型二级动力学模型颗粒内扩散模型Elovich模型qek1rqek2rABrABrTC4.3600.0090.61214.4300.0080.99905.7250.5230.5744.1071.8100.764OTC7.1150.0140.93114.0850.0060.99894.9280.5340.6502.3832.0170.8854CTC1.8790.0100.52910.3090.0250.99975.0370.3350.4415.6120.8490.596
2.2.2 吸附等温线
图7为不同初始浓度的抗生素对吸附的影响。
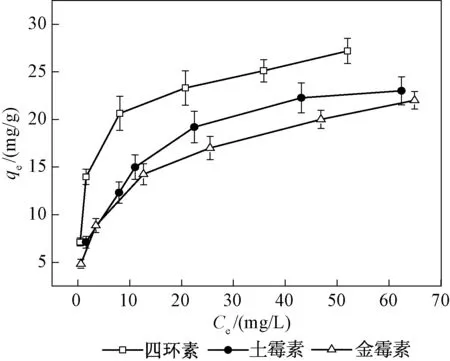
图7 3种TCs在CTAB-ATP上的吸附等温线Fig.7 Adsorption isotherm curves of three tetracycline antibiotics onto CTAB-ATP
由图7看出,CTAB-ATP对3种TCs的平衡吸附量均随着TCs浓度的升高而增加,CTAB-ATP对3种TCs的吸附能力大小依次为四素素>土霉素>金霉素。本研究对3种TCs的吸附等温线分别采用表1中的Langmuir、Freundlich和Temkin进行定量描述。
按上述3种模型进行计算,分别得到了3种抗生素在CTAB-ATP上的相关系数和吸附常数,结果见表3。Freundlich 和Langmuir方程拟合得到的吸附等温线均表现出良好的相关性(图8)。对比相关系数r可知,Langmuir模型对3种抗生素吸附数据的拟合效果最好,r平均值为0.991 9,且每种抗生素在CTAB-ATP上的吸附拟合均能达到显著相关,说明CTAB-ATP对抗生素的吸附过程存在单分子层吸附,属于化学吸附,其次是Freundlich方程,r值均为0.99左右,其中金霉素在CTAB-ATP上吸附数据的拟合达到显著相关,r值为0.995 7。Temkin模型主要表达了吸附剂与吸附质之间发生正负离子强烈的静电作用,3种TCs在CTAB-ATP上的吸附过程也能用Temkin模型拟合,说明吸附过程也存在静电作用。邹星等[27]的研究结果也表明,Langmuir和Freundlich方程均能很好地描述蒙脱石对TCs的吸附。
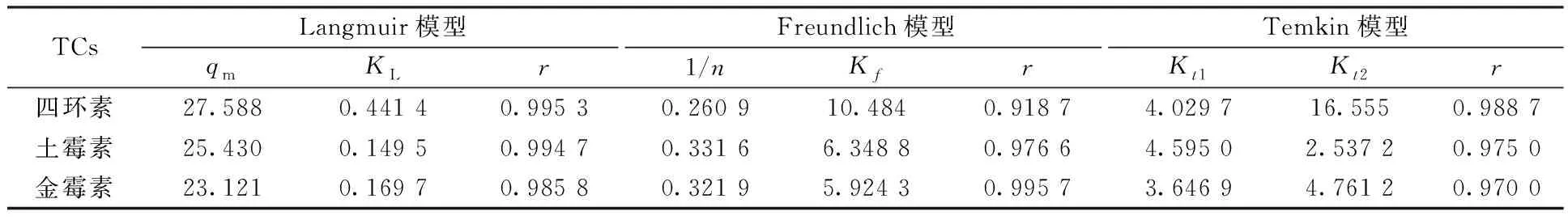
表3 TCs吸附等温线各模型参数Table 3 Model parameters of antibiotics adsorption isotherms
由表3可知,四环素、土霉素和金霉素的1/n很接近,表明吸附机理相似。Kf和1/n分别代表吸附剂对抗生素的吸附能力和吸附强度。其拟合结果表明,CTAB-ATP能强烈地吸附3种TCs抗生素。拟合得到的相关常数Kf从大到小顺序依次为四环素>土霉素>金霉素,说明四环素的吸附容量大于土霉素和金霉素,与图7结果一致,其中四环素、土霉素和金霉素的最大吸附容量分别为27.588、25.430、23.121 mg/g。
Langmuir模型中非常重要的参数是无因次分离常数RL,它可以反映一个吸附系统是有利于还是不利于吸附。通过引入无量纲常数RL来表征Langmuir等温式的基本特征[28],其表达式:
式中:RL用于表示吸附过程的性质,是无量纲常数;KL是Langmuir方程参数,L/mg;Cm是抗生素溶液最大初始质量浓度,mg/L。
计算出CTAB-ATP吸附的RL的值分别为0.0185、0.0528、0.0468,RL均在0~1之间,说明CTAB-ATP对3种抗生素的吸附是有利的,是一种很好的吸附材料。
2.3 有机改性ATP吸附TCs机制的初步探讨
ATP表面带有负电荷,其在水溶液中形成一层薄的水膜,具有亲水性作用,疏水性较弱,对有机污染物的吸附能力较弱。经过CTAB改性的ATP对有机污染物的吸附能力显著增强,这主要是因为CTAB表面的正电荷基团吸附在ATP表面负电荷点位上,ATP表面上CTAB的疏水长碳链相互之间以疏水键形式形成有机相,使有机改性ATP的疏水性增强,亲水性降低,通过有机相的疏水吸附作用将有机物吸附在CTAB-ATP表面上,从而使有机改性ATP对有机污染物的吸附性能力显著增强。以往研究[8,29-30]表明,阳离子表面活性剂改性黏土土样,通过其正电荷与黏土土样表面的负电荷发生静电作用,黏土表面经过疏水键的相互作用从而形成一层有机相,使黏土表面疏水性增强,容易吸附疏水性有机物。由SEM、FT-IR、XRD、和TG-DSC表征结果也可知[8], ATP经过CTAB改性后,ATP的层状硅酸盐架构基本未发生改变,CTAB不是与ATP晶体之间的阳离子进行离子交换,以插层的形式实现改性,而是大部分CTAB+的N+端连接于ATP的表面。ATP经过CTAB改性后,其表面亲水性减弱,疏水性增强。
有机改性的ATP对有机污染物的吸附为有机相疏水吸附-化学吸附相结合的机制。已有研究结果表明[2,8,30],有机改性剂对于黏土表面的改性属于非均匀的改性形式,改性黏土表面同时存在着未被改性剂覆盖的原土表面和被改性剂覆盖的有机相区域。因此,有机改性ATP对有机污染物的吸附同时存在着以下吸附作用:①CTAB有机相中的疏水吸附作用(物理吸附);②ATP未被CTAB覆盖的区域表面会发生化学吸附作用;③在ATP内表面和孔隙的吸附。由于物理吸附作用需要较小的能量,容易发生吸附反应,导致具有较快的吸附反应速率。而化学吸附作用需要较大的能量,较难发生吸附反应,因此吸附反应速率较慢。所以有机污染物在有机改性ATP表面的吸附呈现初始快速吸附阶段和之后的慢速吸附2个阶段。
3 结论
1)CTAB-ATP对3种TCs的吸附量随着溶液pH的增加呈现增长趋势;吸附量的增量随着吸附投加量的增大呈现缓慢减小趋势;随着离子强度的增加呈现逐渐减小趋势。
2)CTAB-ATP对3种TCs的吸附均在180 min基本达到平衡,四环素、土霉素及金霉素的平衡吸附量分别高达13.83、13.01、10.08 mg/g。CTAB-ATP对四环素、土霉素、金霉素的吸附过程均符合准二级动力学模型(r>0.998),吸附等温线较好的符合Langmuir等温式,CTAB-ATP对抗生素的吸附属于单分子层的化学吸附。Temkin模型说明3种TCs在CTAB-ATP上的吸附过程存在静电作用。

