双室微生物燃料电池对电解锰废水中Cr(VI)的去除及其产电性能研究
何则强,张 蕊,龙秋萍,万祖杨,谢 彪,熊利芝
双室微生物燃料电池对电解锰废水中Cr(VI)的去除及其产电性能研究
何则强1, 2,张 蕊2,龙秋萍2,万祖杨2,谢 彪2,熊利芝1, 2
(1. 湖南城市学院 材料与化学工程学院,益阳 413000; 2. 吉首大学 生物资源与环境科学学院,吉首 416000)
构建以F026为阳极产电菌和含Cr(VI)电解锰废水为阴极液的双室微生物燃料电池(MFC)。考察电解锰模拟废水pH、Cr(VI)初始质量浓度、MFC运行温度等因素对废水中Cr(VI)的还原率及MFC产电效果的影响规律,并对最优条件下MFC处理实际电解锰含铬废水的效果和Cr(VI)的还原产物进行研究。结果表明:当废水pH为2、MFC运行温度为303K时,MFC对含Cr(VI)废水具有最佳的处理效果。在此条件下,MFC对Cr(VI)质量浓度为124 mg/L的电解锰废水处理80 h后,92.1%的Cr(VI)可有效还原为-Cr2O3,而155h处理后还原率可达100%,产电功率达到914.7 mW/cm2,表明MFC是一种发展前景良好的含Cr(VI)电解锰废水处理工艺。
电解锰废水;六价铬;微生物燃料电池;产电性能
随着采矿业、冶金业、化工业以及农业的迅速发展,大量重金属以各种形态进入到自然环境中,对水、大气和土壤造成严重的污染[1−2]。六价铬Cr(VI)作为一种典型的工业氧化剂被广泛应用于制药、木材、电镀、皮革鞣制和冶金等领域[3]。由于其高毒性和在生物体内的积累特性,从废水中去除Cr(VI)十分必要。然而,目前用于处理废水中Cr(VI)的物理法和化学工艺[4]或多或少都具有其内在的缺陷如能耗物耗高、处理效率低且产生大量的二次污染物和有毒污泥等[5]。因此,开发一种廉价、高效、可持续的Cr(VI)处理工艺十分必要[6]。
近年来,微生物燃料电池(Microbial fuel cell,MFC)作为一种直接转化有机物所蕴含的化学能为电能的装置,表现出燃料资源丰富、操作条件可控、零能量输入、高效能量利用等特点,受到广大研究者的高度关注[7−8]。MFC是一种绿色、环保的发电装置,它可以通过氧化还原反应将其储存在微生物燃料中的化学能转变为电能并且不通过燃烧,它也不受卡诺循环限制,在实际应用中能量的转换效率便可达到40%~60%,在这个过程中几乎没有氮以及硫氧化物的产生,所以MFC是继水电、火电和核电之后第四种环境友好的绿色、高效发电方式,受到各国政府的高度关注,纷纷出台政策或者公布相关计划以支持和发展MFC技术。当前MFC技术攻关的关键材料主要包括质子交换膜、阴极催化剂、绝缘端板以及双极板等。特别是由于MFC的阴极催化剂存在成本高昂、稳定性差等问题,阻碍了MFC技术的研究与推广。MFC装置由被质子交换膜隔离、并通过外电路中由导线相互连接的阳极室和阴极室组成。有机物被阳极室里的生物催化剂(称为产电微生物或产电菌)氧化,产生H+和电子。H+通过质子交换膜扩散到阴极室,而电子则通过外电路转移到阴极室并被其中的电子受体接受,完成MFC的电荷传递过程[9]。在电子转移过程中,外部电路会有电流形成,即通常所说的“产电”。
目前,在MFC中用作电子受体的常见物质有氧气[10]和铁氰化物[11]两种。25 ℃标准状态下它们在阴极的半反应及其电极电位(酸性条件)如式(1)和(2)所示:
O2+4H++4e→2H2O (Θ=1.23 V) (1)
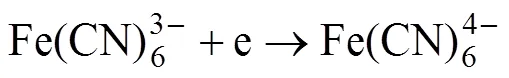
然而,由于这两种电子受体的电极电位有限,使得采用这两种电子受体时通常不但不能有效利用从阳极产生的电子,还可能产生其他有毒污染物。事实上,环境中很多污染物具有很高的还原电极电势,如果将这些污染物作为MFC阴极的电子受体,一方面其高还原电势可以加快电子从MFC阳极产生并向阴极转移的速率,另一方面这些污染物得到电子后将被还原成低价态的无毒或低毒形态。最终MFC阳极产生的电子得到有效利用,而阴极室废水中作为电子受体的高价态重金属离子被逐步还原成低毒或无毒的低价态重金属离子,实现重金属废水解毒的目的。
如25 ℃标准状态下Cr(VI)在酸性条件下的还原电极电势高达1.33 V(见式(3)),比O2的还原电极电势还高,理论上可以取代O2而作为MFC的阴极电子 受体。
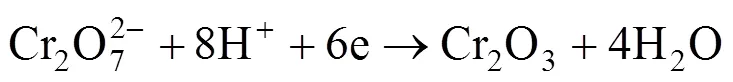
LI等[12]利用含Cr(VI)电镀废水为阴极液,考察了MFC阴极处理含Cr(VI)废水的可行性。WANG等[13]研究发现利用MFC可将Cr(VI)浓度为100 mg/L的废水在150 h内彻底去除。HUANG等[14−15]和LIU等[16]发现通过优化阴极材料和阴极结构可有效改善MFC对Cr(VI)的还原效果。据不完全统计,每年我国产生约40亿吨质量浓度为100~400 mg/L的含铬废水[17],因此理论上每年可从这些含铬废水中回收能量1.3×1012~5.2×1012kJ[13]。
湖南湘西地区是世界著名的“锰三角”地区,具有丰富的锰矿资源。在生产电解锰过程中需要使用K2Cr2O7作为钝化剂,因此电解锰厂通常会产生大量的含Cr(VI)废水。尽管近几年由于无铬钝化剂的开发和使用,含Cr(VI)废水将日益减少。但如何有效处理现有电解锰厂含Cr(VI)废水,仍是一个十分迫切的问题。基于这种情况,本文作者拟采用MFC工艺,将电解锰含Cr(VI)废水作为MFC的阴极液,以Cr(VI)为MFC阴极电子受体,构建双室MFC,在处理含Cr(VI)废水的同时产生电能。考察pH、Cr(VI)初始质量浓度、MFC运行温度等条件对阴极Cr(VI)的还原效果和MFC产电性能的影响规律,为含Cr(VI)电解锰废水的处理提供新的思路。
1 实验
1.1 模拟含Cr(VI)废水的配制
准确称取一定量的K2Cr2O7溶于一定量的去离子水中,配制成质量浓度为20~100 mg/L的Cr(VI)溶液。在此模拟废水中加入一定量的NaCl以增加阴极液的导电性。
1.2 MFC的构建与运行
参照课题组已经报道的方法构建双室MFC[18]。其中,阴阳电极均采用石墨毡制作,电极的有效面积为 25 cm2,而阴阳两极室的有效体积为125 mL,采用质子交换膜隔开。采用从湖南省吉首市某污水处理厂厌氧消化池收集的厌氧污泥在阳极室中进行产电微生物的接种[19]。接种时,以100 mL 200 mg/L的葡糖糖溶液为阳极液、以100 mL 5.0×10−2mol/L的K3Fe(CN)6为阴极液。实验过程中采用KH2PO4为缓冲溶液,1.0 mol/L的NaOH或HCl调节阴阳两极的pH值。根据课题组前期研究结果,阳极产电菌F026最适宜生长的酸碱环境为中性偏碱性[18],因此,本实验过程中阳极液的pH调整至7.5。阳极采用气封方式保证其严格厌氧条件,采用磁力搅拌器中等强度搅拌以保证阳极液的浓度均匀并在阳极上形成稳定的生物膜。而阴极直接暴露于空气即可。当MFC开路电压稳定至0.2V以上时,即认为接种成功。
接种完毕,向阳极室注入100 mL 200 mg/L的乙酸钠溶液为阳极液,阴极室则注入100 mL模拟电解锰含铬废水。阴阳两极采用铜导线连接,并在外电路中接入一个0~10000 Ω之间可调的滑线变阻器。利用电化学工作站(CHI660D,上海辰华)测定不同Cr(VI)初始质量浓度、pH、运行温度等对MFC的输出电压、产电功率密度、库仑效率、Cr(VI)还原率等的影响。
1.3 计算与分析
在电化学工作站上直接连续记录MFC的电压(vs SHE),并按照公式(4)计算产电功率密度(W/m2):
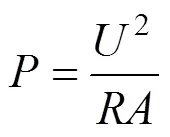
式中:为外阻,Ω;(vs SHE)为MFC的电压,V;为阳极的面积,m2。
利用式(5)计算MFC的库仑效率C:

式中:P为MFC运行过程中产生实际电量,C;T为从消耗掉的乙酸钠计算得到的理论电量。
采用离子色谱法测定MFC运行过程中阳极乙酸钠的消耗量,采用二苯碳酰二肼分光光度法测定阴极室的Cr(VI)的质量浓度(测定540 nm处的吸光度与Cr(VI)浓度之间的关系),采用X射线光电子能谱(XPS)研究反应前后阴极表面产物的成分。
2 结果与讨论
2.1 以Cr(VI)为阴极液的MFC的启动
图1所示为以Cr(VI)为阴极液的MFC的启动过程。MFC阳极充满阳极液并经48 h的活化后开路电压开始上升,直至240 h MFC的开路电压一直维持在0.23~0.25 V左右,表明阳极产电菌F026已经稳定地生长在阳极表面(见图1中插图),MFC活化成功。240 h后,往MFC阴极充满Cr(VI)溶液,发现MFC开路电压迅速上升至0.9~1.1 V之间,而且连续稳定240 h左右,表明采用Cr(VI)为阴极液的MFC可以获得稳定的开路电压。
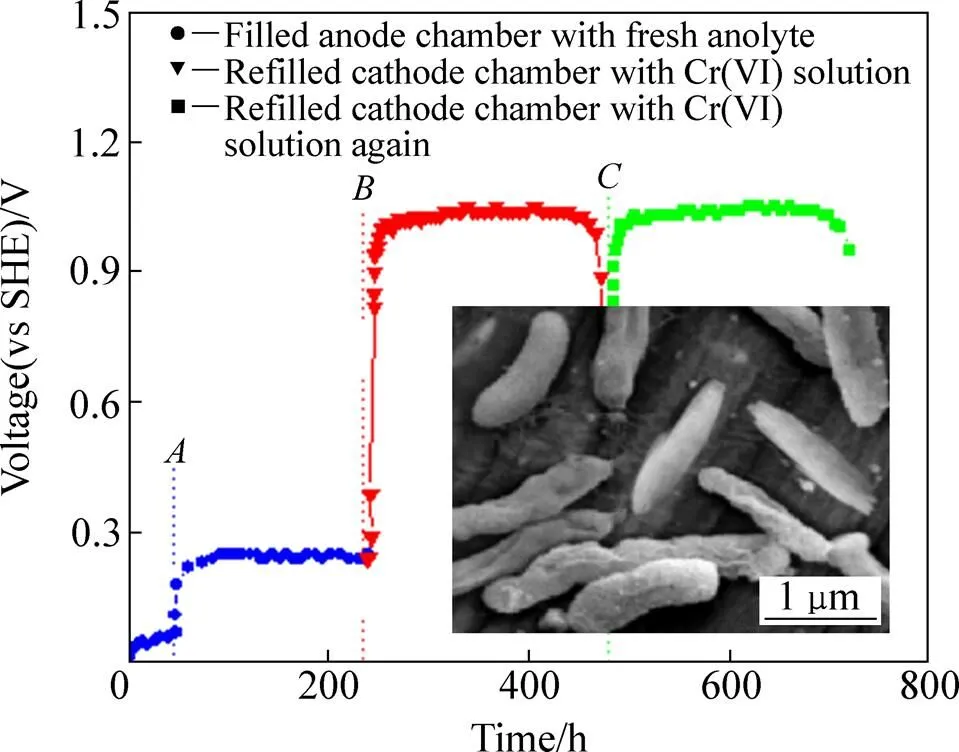
图1 MFC启动过程中的电压变化
2.2 不同反应条件对Cr(VI)还原率的影响
从反应(3)可知,废水中Cr(VI)的质量浓度、溶液的酸碱度以及MFC的运行温度等反应条件都会对Cr(VI)的还原反应具有重要的影响。图2所示为不同反应条件对Cr(VI)还原率的影响。图2(a)所示为电解锰废水pH为2、运行温度为303K的条件下运行时间对MFC处理不同初始Cr(VI)质量浓度含铬废水的Cr(VI)还原效果的影响。
从图2(a)上可见,对于同一初始Cr(VI)质量浓度的废水,随着处理时间的延长,Cr(VI)还原率不断增加。在MFC运行的初期Cr(VI)还原率增速很快,但当MFC运行一定时间后Cr(VI)还原率增速减缓,直至废水中的Cr(VI)被全部还原。而对于不同初始Cr(VI)质量浓度的废水,随着Cr(VI)初始质量浓度的增加,虽然Cr(VI)还原量在增加,但Cr(VI)的还原率有所下降,但下降幅度不大。初始Cr(VI)质量浓度分别为100 mg/L、80 mg/L、60 mg/L、40 mg/L和20 mg/L时,Cr(VI)完全还原所需要的时间分别为140 h、80 h、56 h、37 h和27 h。这个结果与PARK等[20]的研究结果一致。从实验结果来看,当Cr(VI)的初始质量浓度为60 mg/L时,MFC对废水中Cr(VI)具有较好的处理效果:在运行时间为52 h,废水中99.2% Cr(VI)已经被还原,而运行时间为56 h时Cr(VI)已经被完全还原。
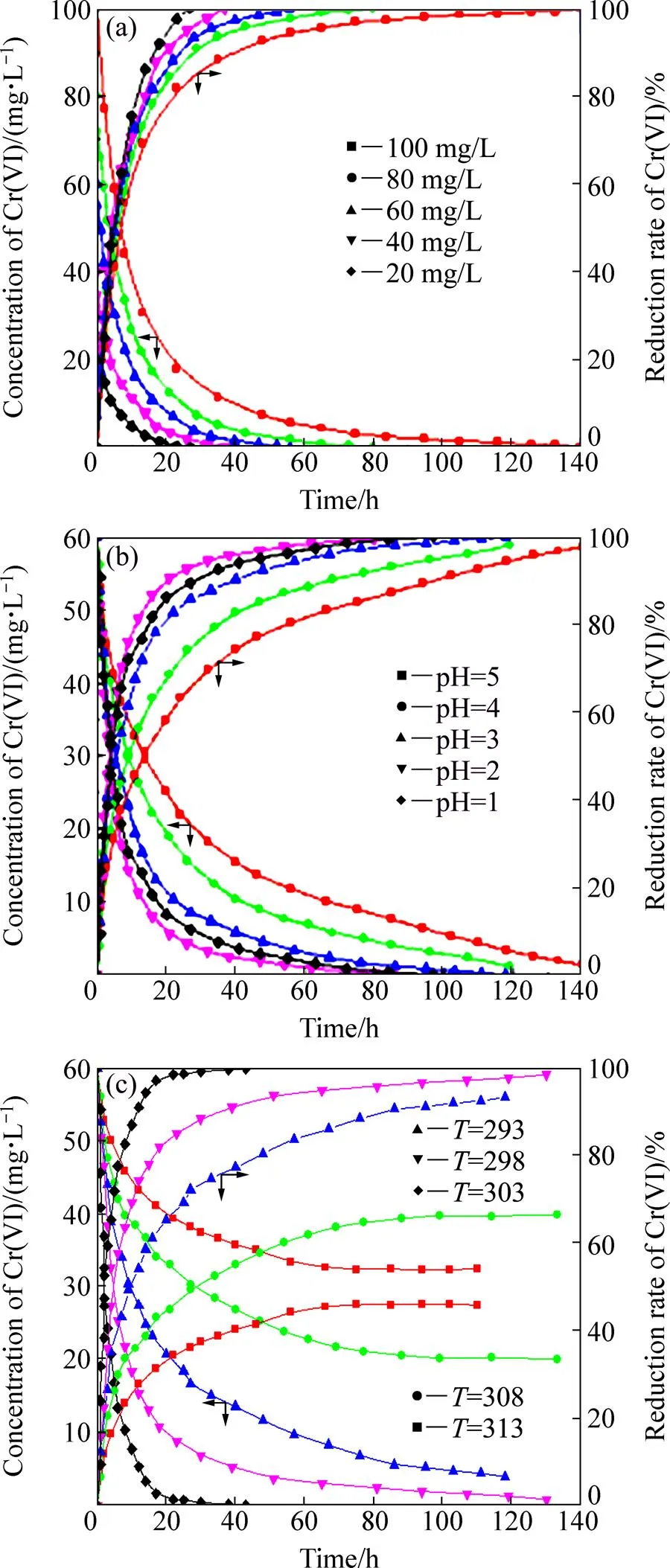
图2 不同反应条件对Cr(VI)还原率的影响
图2(b)所示为电解锰废水初始Cr(VI)质量浓度为60 mg/L、MFC运行温度为303K的条件下不同运行时间MFC对不同pH含铬废水中Cr(VI)的还原效果。 从图2(b)发现,对于pH一定的电解锰含铬废水,随着MFC运行时间的延长,废水中的Cr(VI)逐渐被还原,直到最终Cr(VI)被全部还原。在MFC运行初期,Cr(VI)的还原率随着运行时间的增加迅速增加,但随后还原率增加速度减缓,直至全部Cr(VI)被还原。对于不同pH的电解锰废水,随着pH的降低,MFC对其中Cr(VI)的还原量和还原率都明显增加,表明pH对电解锰含铬废水中Cr(VI)的还原具有重要的影响。这也可从式(3)进行解释:从式(3)可以发现,每还原1 mol Cr(VI)至Cr(III),将消耗8 mol H+,说明H+浓度直接关系到Cr(VI)的还原,而且pH越低,Cr(VI)的还原更有效。但pH为1时MFC对电解锰废水中Cr(VI)的还原量和还原率却明显比pH为2时的更低。这可能是因为,当阴极液的pH很小时,H+浓度很大,在质子交换膜两侧的阴阳两极室的H+浓度差较大,H+将通过质子交换膜向阳极室扩散,导致阳极室的酸度降低,使得阳极产电微生物失活,极化作用增加,最终导致MFC的开路电压和阴极电势降低,MFC产电能力下降。一般而言,含铬废水中Cr(VI)的质量浓度为几十至几百毫克每升,而且通常为pH小于4的酸性废水[21]。研究结果表明,对于初始Cr(VI)质量浓度为60 mg/L的电解锰废水,pH为1、2、3、4和5时,完全还原废水中Cr(VI)所需的时间分别为97 h、85 h、118 h、127 h和148 h。由于含铬废水的质量浓度变化较大,对其进行有效调控并不容易,但对废水的pH可通过简单的酸碱进行简单调节,因此,通过调节废水的pH可有效改善MFC对电解锰废水中Cr(VI)的还原效果。实验结果表明pH为2时MFC对Cr(VI)的还原效果较好。
根据反应(3),提高反应温度应能加速反应,改善Cr(VI)的还原率。但是,在MFC体系中,阳极产电微生物的适合生长温度一般为20~40 ℃之间,温度过高或过低都不利于产电微生物的生长[18]。因此,研究了20~40 ℃的温度区间内温度对电解锰废水中Cr(VI)还原效果的影响。图2(c)所示为电解锰废水初始Cr(VI)质量浓度为60 mg/L、pH为2的条件下MFC运行温度为303K的条件下不同温度在不同运行时间MFC对60 mg/L的电解锰废水中Cr(VI)的还原效果。
很显然,对于同一运行温度,MFC对废水中Cr(VI)的还原与Cr(VI)初始质量浓度和pH对Cr(VI)还原的影响具有类似的规律,均是在运行初期还原率迅速增加,然后还原率增加减缓。所不同的是,在运行温度过高(313K)时,由于微生物在MFC中的活性显著降低,MFC对Cr(VI)的还原率显著降低。当MFC运行66 h后,Cr(VI)的还原率已经基本不变,表明此时微生物基本没有活性。由图2(c)可知,温度过高或过低,对MFC处理含Cr(VI)废水都不利,适宜的运行温度为303K。
2.3 不同反应条件对MFC开路电压和阴极电压的影响
根据反应(3)的能斯特方程可以计算出阴极的电极电势:

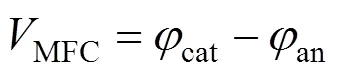
因此,在阳极电极电势固定和温度恒定的情况下,根据式(7)可知MFC的开路电压也将随着[Cr2O72−]和[H+]的升高而提高。
图3所示为MFC运行温度为303K时初始Cr(VI)质量浓度和pH对MFC开路电压和阴极电压的影响规律。从图3(a)可知,随着pH从5降低至2,MFC的开路电压和阴极电压都基本呈线性增加,与从式(6)推断的结论基本一致。从pH为5降低至pH为2时,MFC的开路电压从0.93 V增加至1.04 V,而阴极电压从0.66 V增加至0.76 V,增幅分别为11.8%和15.2%,表明pH对MFC的开路电压和阴极电压具有较显著的影响。但由于电极过程受很多因素的影响,由图3(a)可知,所得MFC开路电压和阴极电压随pH变化曲线的斜率与从式(6)推断的斜率有所差别。特别应该注意的是,当溶液的pH降低至1时,由于H+通过质子交换膜扩散至MFC阳极,导致MFC的开路电压和阴极电压并未按照式(6)所示继续增加,而呈现下降的趋势。同样,从图3(b)可知,随着Cr(VI)初始质量浓度的增加,MFC的开路电压和阴极电压都呈线性增加,与从(6)式推断的结论一致。Cr(VI)初始质量浓度从20 mg/L增加至100 mg/L,MFC的开路电压从0.99 V增加至1.11 V,而阴极电压从0.72 V增加至0.81 V,增幅分别为12.1%和12.5%。上述研究结果表明,虽然溶液的酸碱度与Cr(VI)初始质量浓度对MFC的开路电压具有基本一致的影响,但Cr(VI)初始质量浓度对MFC的阴极电压具有更小的的影响,与WANG等[13]的研究结论一致。YOU等[22]在研究KMnO4作为MFC阴极电子受体时也发现了类似的现象。

图3 不同反应条件对MFC开路电压和阴极电压的影响
2.4 不同反应条件对MFC产电功率和库仑效率的影响
图4所示为不同反应条件对MFC产电功率和库仑效率的影响。从图4(a)可知,随着电解锰废水初始Cr(VI)质量浓度的增加,MFC的产电功率呈增加的趋势,但当Cr(VI)质量浓度超过60 mg/L后,MFC的产电功率增加速度减缓。Cr(VI)质量浓度为20 mg/L、40 mg/L、60 mg/L、80 mg/L和100 mg/L时,MFC的产电功率分别为871.2 mW/m2、901.5mW/m2、914.3mW/m2、918.6mW/m2和927.2mW/m2。尽管MFC的库仑效率随着电解锰废水初始Cr(VI)质量浓度的增加也呈现先增加后降低的趋势,但变化不大,在研究的初始Cr(VI)质量浓度范围内,库仑效率保持在62.9%~71.2%之间,高于文献[13]报道值。这可从如下两方面进行说明:一方面,虽然本研究采用的实验条件有利于MFC充分利用阳极产生的电子,但由于MFC阴极直接暴露于空气中,少量氧气可能通过阴极渗透到阳极室,直接将阳极的有机物降解,降低了阳极微生物的工作效率,导致库仑效率降低[23]。另一方面,虽然前期研究已经证明,在本研究中起主要作用的产电菌为F026,但这并不排除依然有其它微生物(非产电菌)的存在,这些非产电菌的存在同样可参与COD的降解[24−25]。
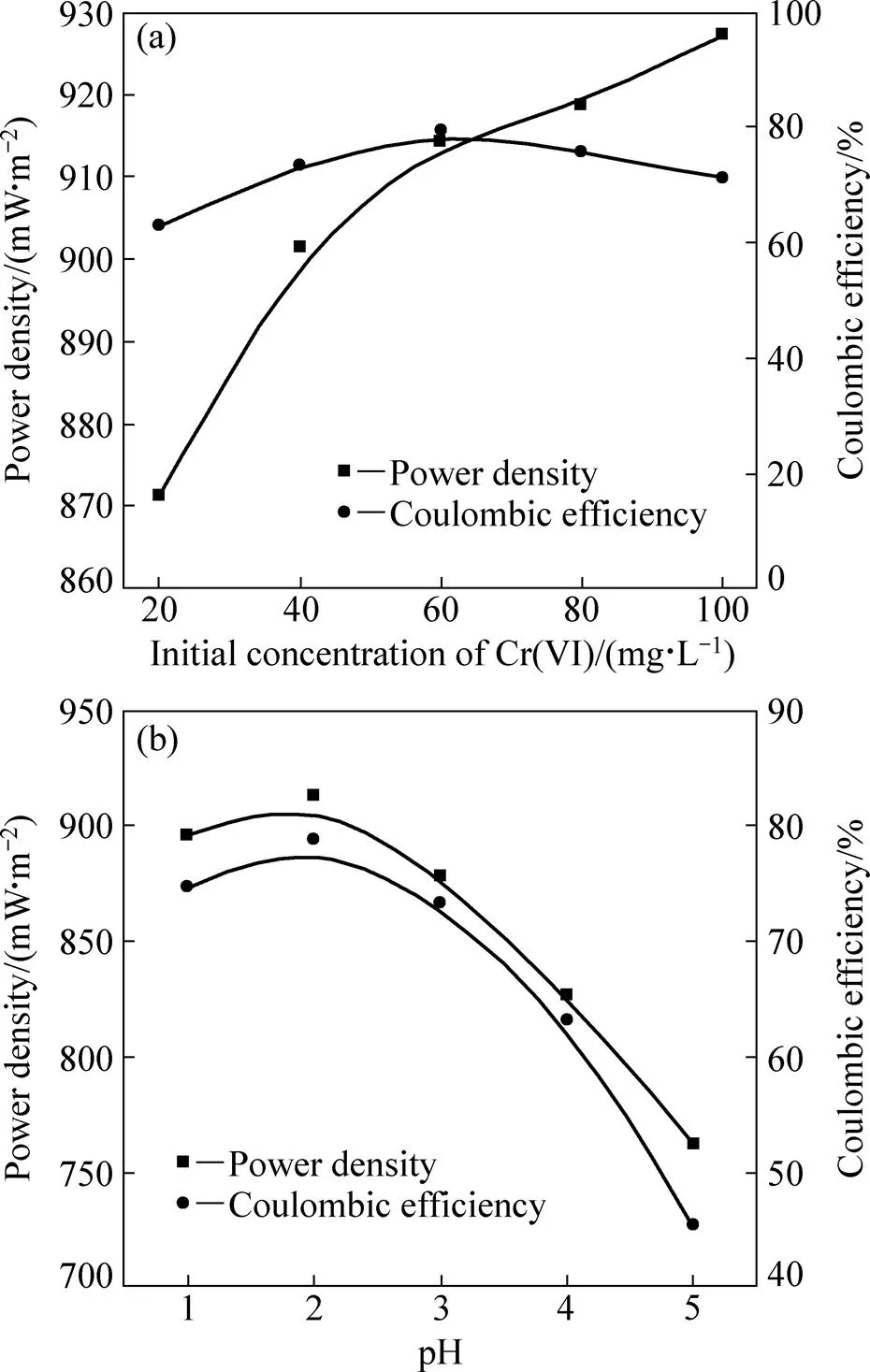
图4 不同反应条件对MFC产电功率和库仑效率的影响
如图4(b)所示,随着酸度的增加,MFC的产电功率呈增加的趋势,当pH为5、4、3和2时,MFC的产电功率分别为762.3 mW/m2、826.8 mW/m2、878.5 mW/m2、913.3 mW/m2,但继续降低pH,MFC产电功率并不增加。在同样的条件下,MFC的库仑效率呈现相似的变化规律,从pH为5时的45.5%增加到pH为2时的78.8%。这是因为在一定程度下增加酸度对反应(3)有利。研究发现,在一定的pH范围内,虽然MFC阴极液的pH对MFC的产电功率和库仑效率影响较大,但其对阳极微生物的生长和产电性能影响甚微[13, 26]。从研究结果来看,在阴极废水的pH从5降低到2的过程中,阳极的pH变化幅度为6%~11%,这可能与阳极缓冲溶液的存在以及阴极Cr(VI)被还原时同时消耗了由阳极产生并通过质子交换膜迁移至阴极的质子有关。但当pH降低至1时,H+通过质子交换膜扩散至阳极后将降低阳极产电菌的生物活性,导致MFC的产电功率反而呈下降趋势,与前面在pH为1时MFC对Cr(VI)的还原效果及MFC的输出电压的研究结果相一致。
从上述研究结果可知,采用MFC处理Cr(VI)电解锰废水的最佳pH为2、MFC最佳运行温度为303K。尽管实验结果得出了最适宜的Cr(VI)初始浓度为60 mg/L,但由于实际应用中对废水进行浓缩或稀释需要消耗更多的能量或水量,通常很少对废水浓度进行调控。因此,本研究在最佳pH和最佳MFC运行温度下对实际Cr(VI)质量浓度为124 mg/L的废水(取自湖南省湘西土家族苗族自治州某电解锰厂)进行了研究。
2.5 MFC对实际电解锰含Cr(VI)废水的处理
图5所示为在pH=2、温度为303K时MFC对实际电解锰废水中Cr(VI)的去除情况和极化曲线与功率密度曲线图。从图5(a)可知,随着MFC运行时间的延长,废水中Cr(VI)不断降低,当运行时间达80 h时,废水中Cr(VI)的还原率达到92.1%,155 h后全部Cr(VI)被全部还原。从图5(b)可以看到,在实际废水处理过程中,MFC的开路电压可达1.03 V,随着电流密度的增大,由于极化作用的存在,电池电压不断下降。在电流密度为0.158 mA/cm2时,MFC可获得的最大产电功率密度为914.7 mW/m2。
表1所列为不同研究小组采用MFC处理含铬废水时的产电情况和Cr(VI)还原情况。从表1可以发现,与已有文献报道相比,本研究中Cr(VI)的还原率以及MFC的产电性能都处于较优的水平,表明利用F026为阳极产电菌的MFC可实现对含铬电解锰废水的有效处理并同时获得较大的产电效能。

图5 MFC对实际废水中Cr(VI)的去除情况与产电性能(实验条件:pH为2、温度为303K、Cr(VI)初始浓度为124 mg/L)
表2所列为本研究中采用的MFC与文献报道的其他Cr(VI)处理工艺对Cr(VI)去除率或还原率的比较。从表2可见,虽然现行吸附[28−31]、化学沉淀[32−33]、化学还原[34−35]、离子交换[36−37]和膜分离[38−39]等工艺对含铬废水中Cr(VI)的去除具有处理时间短、Cr(VI)去除率高等优点,但同时存在处理成本高、只能处理单一废水、产生二次污染等缺点,而MFC工艺不但Cr(VI)还原率高,而且具有无需额外能量输入、可以同时处理有机废水和重金属废水并产生电能等优点,是一种绿色、环保、廉价、高效的处理工艺。
2.6 MFC处理Cr(VI)产物分析
为了弄清Cr(VI)被还原后的存在状态,对MFC阴极表面的扫描电镜进行了分析(见图6)。从图6可以看到,反应前,阴极表面平整平滑(见图6(a))。但当MFC运行一段时间后,电极表面变得很粗糙,出现了很多沉积物(见图6(b))。经EDS分析可知,这些沉积物的成分为Cr2O3,表明MFC阴极室的Cr(VI)已经在反应过程中被还原为Cr(III)并沉积于MFC阴极表面。

表1 不同研究小组采用MFC处理含铬废水的研究结果

表2 不同处理工艺对Cr(VI)去除率或还原率的比较
MFC阴极表面沉淀物的X-射线衍射谱、X-射线光电子能谱和红外光谱的研究结果如图7所示。从图7(a)可知,MFC阴极表面沉淀物在2为24.46°、33.53°、36.12°、39.55°、41.35°、43.95°、49.99°、54.67°、58.10°、63.19°和64.83°处分别出现了Cr2O3标准谱图(JCPDS No.38-1479)中对应于(012)、(104)、(110)、(006)、(113)、(202)、(113)、(202)、(024)、(116)、(122)、(214)和(300)晶面的衍射峰,表明MFC阴极表面沉淀物为具有绿铬矿结构的-Cr2O3晶体[40]。从图7(b)可以看到,在反应前,阴极表面的XPS谱在结合能从570~590 eV范围内基本上为一直线,说明其表面没有任何形式的Cr元素存在。但反应后,阴极表面在577.6 eV和587.4 eV处分别出现了对应于Cr 2p3/2和Cr 2p1/2的能峰,表明Cr(VI)被还原后是以Cr(III)的形式存在[41],与金春姬等[42]的研究结论一致。图7(c)所示为MFC阴极表面沉积物傅里叶红外光谱分析。在1000~400 cm−1范围内,在411.2 cm−1、440.8 cm−1、570.6 cm−1和640.4 cm−1处分别出现了标识-Cr2O3的E1、E2、E3和E4特征振动模式[43],进一步证实Cr(VI)在MFC阴极被有效还原为以-Cr2O3形式存在的Cr(III)。

图6 反应前后MFC阴极的SEM像

图7 阴极表面沉积物的XRD谱、XPS谱和FTIR谱
3 结论
1)采用双室MFC成功处理了含Cr(VI)电解锰废水。研究发现,pH、Cr(VI)和运行温度都对MFC的产电功率密度和Cr(VI)的还原率具有一定的影响,其中pH的影响最为显著。最佳的处理条件为:废水的pH为2,运行温度为303K,Cr(VI)初始浓度为60 mg/L。
2) 对实际Cr(VI)质量浓度为124 mg/L的电解锰废水的研究发现,MFC的最大功率密度可达914.7 mW/m2,采用MFC处理80 h后可将其中92.1%的Cr(VI)还原,而155 h后Cr(VI)可被全部还原。
3) SEM、XRD、XPS和FTIR研究表明,MFC处理含铬废水时,Cr(VI)主要被还原成Cr2O3的形式沉积在阴极表面。
4) 与其他工艺相比,MFC工艺不但可以直接在阴阳两极分别处理含铬废水和有机废水,而且可以产生电能,具有节能、减污双重功效。通过优化工艺条件,MFC工艺可望成为一种应用前景良好的含Cr(VI)电解锰废水处理工艺。
[1] 黄海涛, 魏彩春, 梁延鹏, 温振宇. 重金属污染场地修复技术的研究进展[J]. 宁夏农林科技, 2011, 52(5): 43−46, 68. HUANG Hai-tao, WEI Cai-chun, LIANG Yan-peng, WEN Zhen-yu. Research progress of renovating technology of heavy metal contaminated site[J]. Ningxia Journal of Agriculture And Forestry Science & Technology, 2011, 52(5): 43−46, 68.
[2] 葛俊森, 梁 渠. 水中重金属危害现状及处理方法[J]. 广州化工, 2007, 35(5): 69−70. GE Jun-sen, LIANG Qu. The status and treatment of water heavy metal pollution[J]. Guangzhou Chemical Industry, 2007, 35(5): 69−70.
[3] JADHAV U U, HOCHENG H. A review of recovery of metals from industrial waste[J]. Journal of Achievements in Materials and Manufacturing Engineering, 2012, 54(2): 159−167.
[4] SHARMA S, PETRUSEVSKI B, AMY G. Chromium removal from water: A review[J]. Journal of Water Supply: Research and Technology- AQUA, 2008, 57(8): 541−553.
[5] SAN N O, DONMEZ G. Biosorption of chromium (VI), nickel (II) and Remazol Blue by Rhodotorula muciloginosabiomass[J]. Water Science and Technology, 2012, 65(3): 471−477.
[6] GANGADHARAN P, NAMBI I M. Hexavalent chromium reduction and energy recovery by using dual-chambered microbial fuel cell[J]. Water Science & Technology, 2015, 71(3): 352−358.
[7] ZHANG J, LI J, YE D D, ZHU X, LIAO Q,ZHANG B. Tubular bamboo charcoal for anode in microbial fuel cells[J]. Journal of Power Sources, 2014, 272: 277−282.
[8] LOGAN B E, HAMELERS B, ROZENDAL R, SCHRODER U, KELLER J, FREGUIA S, AELTERMAN P, VERSTRAETE W, RABAEY K. Microbial fuel cells: Methodology and technology[J]. Environmental Science and Technology, 2006, 40(17): 5181−5192.
[9] 赵立新, 孔凡英, 王 宣, 温 青, 孙 茜, 吴 英. 微生物燃料电池处理含铬废水并同步产电[J]. 现代化工, 2009, 29(11): 37−39. ZHAO Li-xin, KONG Fan-ying, WANG Xuan, WEN Qing, SUN Qian, WU Ying. Cr(VI)-containing wastewater treatment coupled with electricity generation using microbial fuel cell[J]. Modern Chemical Industry, 2009, 29(11): 37−39.
[10] ZHAO F, HARNISCH F, SCHRÖDER U, SCHOLZ F, BOGDANOFF P, HERRMANN I. Challenges and constraints of using oxygen cathodes in microbial fuel cells[J]. Environmental Science and Technology, 2006, 40(17): 5193−5199.
[11] WEI L, HAN H, SHEN J. Effects of cathodic electron acceptors and potassium ferricyanide concentrations on the performance of microbial fuel cell[J]. International Journal of Hydrogen Energy, 2012, 37(17): 12980−12986.
[12] LI Z, ZHANG X, LEI L. Electricity production during the treatment of real electroplating wastewater containing Cr6+using microbial fuel cell[J]. Process Biochemistry, 2008, 43(12): 1352−1358.
[13] WANG G, HUANG L P, ZHANG Y F. Cathodic reduction of hexavalent chromium [Cr(Ⅵ)] coupled with electricity generation in microbial fuel cells[J]. Biotechnology Letters, 2008, 30(11): 1959−1966.
[14] HUANG L P, CHAI X L, CHENG S A, CHEN G. Evaluation of carbon-based materials in tubular biocathode microbial fuel cells in terms of hexavalent chromium reduction and electricity generation[J]. Chemical Engineering Journal, 2011, 166(2): 652−661.
[15] HUANG L P, CHAI X L, CHEN G H, LOGAN B E. Effect of set potential on hexavalent chromium reduction and electricity generation from biocathode microbial fuel cells[J]. Environmental Science & Technology, 2011, 45(11): 5025−5031.
[16] LIU L, YANG Y, LI D L. Accelerated hexavalent chromium [Cr(VI)] reduction with electrogenerated hydrogen peroxide in microbial fuel cells[J]. Advanced Materials Research, 2012, 512: 1525−1528.
[17] WANG X S, LI Z Z, TAO S R. Removal of chromium (VI) from aqueous solution using walnut hull[J]. Journal of Environmental Management, 2009, 90(90): 721−729.
[18] 费讲驰, 滕 瑶, 熊利芝, 吴玉先, 陈义光, 何则强. 微生物燃料电池中假单胞菌F026的产电性能研究[J]. 微生物学杂志, 2015, 35(1): 35−39. FEI Jiang-chi, TENG Yao, XIONG Li-zhi, WU Yu-xian, CHEN Yi-guang, HE Ze-qiang. Electricity generation performances ofF026 in microbial fuel cell[J]. Journal of Microbiology, 2015, 35(1): 35−39.
[19] 费讲驰, 滕 瑶, 熊利芝, 吴玉先, 何则强. 微生物燃料电池中产电微生物的系统发育分析及筛选[J]. 微生物学杂志, 2014, 34(1): 33−40. FEI Jiang-chi, TENG Yao, XIONG Li-zhi, WU Yu-xian, HE Ze-qiang. Phylogenetic analyses & screening of electrogenic microorganisms in microbial fuel cell[J]. Journal of Microbiology, 2014, 34(1): 33−40.
[20] PARK D, YUN Y, KIMA J, PARK J M. How to study Cr(VI) biosorption: use of fermentation waste for detoxifying Cr(VI) in aqueous solution[J]. Chemical Engineering Journal, 2008, 136(2): 173−179.
[21] BARAL A, ENGELKEN R D. Chromium-based regulations and greening in metal finishing industries in the USA[J]. Environ Sci Policy, 2002, 5: 121−133.
[22] YOU S, ZHAO Q, ZHANG J, JIANG J, ZHAO S. A microbial fuel cell using permanganate as the cathodic electron acceptor[J]. Journal of Power Sources, 2006, 162(2): 1409−1415.
[23] 朴明月, 滕洪辉, 石淑云, 赵玲子, 高秀红. 空气阴极微生物燃料电池研究进展[J]. 辽宁化工, 2014, 43(10): 1224−1229. PIAO Ming-yue, TENG Hong-hui, SHI Shu-yun, ZHAO Ling-zi, GAO Xiu-hong. Research progress in air-cathode microbial fuel cells[J]. Liaoning Chemical Industry, 2014, 43(10): 1224−1229.
[24] 王慧勇, 呼 唤, 梁 鹏. 不同来源菌群接种微生物燃料电池处理淀粉废水的研究[J]. 工业水处理, 2012, 32(7): 60−63. WANG Hui-yong, HU Huan, LIANG Peng. Study on the treatment of starch processing wastewater using microbial fuel cell inoculated from different bacterial community[J]. Industrial Water Treatment, 2012, 32(7): 60−63.
[25] 王 萍, 徐志兵, 操璟璟. 微生物燃料电池(MFC)技术及其发展前景的研究[J]. 节能技术, 2008, 26(6): 534−538. WANG Ping, XU Zhi-bing, CAO Jing-jing. The research about technique of microbial fuel cells and its progressing foreground[J]. Energy Conservation Technology, 2008, 26(6): 534−538.
[26] CHENG S A, DEMPSEY B A, LOGAN B E. Electricity generation from synthetic acid-mine drainage (AMD) water using fuel cell technologies[J]. Environmental Science & Technology, 2007, 41(23): 8149−8153.
[27] MOHAN B R, SRINIKETHAN G, MEIKAP B C. Materials, energy and environment engineering: Select proceedings of ICACE 2015[M]. Singapore: Springer, 2017: 219−226.
[28] HUANG X, LIU Y, LIU S, TAN X, DING Y, ZENG G, ZHOU Y, ZHANG M, WANG S, ZHENG B. Effective removal of Cr(VI) using b-cyclodextrin-chitosan modified biochars with adsorption/reduction bifuctional roles[J]. RSC Advances, 2016, 6(1): 94−104.
[29] MIN K K, SUNDARAM K S, IYENGAR G A, LEE K P. A novel chitosan functional gel included with multiwall carbon nanotube and substituted polyaniline as adsorbent for efficient removal of chromium ion[J]. Chemical Engineering Journal, 2015, 267: 51−64.
[30] ZHU J, WEI S, GU H, RAPOLE S B, WANG Q, LUO Z, HALDOLAARACHCHIGE N, YOUNG D P, GUO Z. One-pot synthesis of magnetic graphene nanocomposites decorated with core@double-shell nanoparticles for fast chromium removal[J]. Environmental Science & Technology, 2012, 46(2): 977−985.
[31] KRISHNA D, SANTHOSH K G, PRASADA R D R. Removal of chromium (VI) from waste water using mixed adsorbent[J]. International Journal of Current Engineering and Scientific Research (IJCESR), 2017, 4(10): 28−42.
[32] MELLA B. Removal of chromium from tanning wastewater by chemical precipitation and electrocoagulation[J]. Journal Society of Leather Technologists and Chemists, 2016, 100(2): 55−61.
[33] RAMAKRISHNAIAH C R, PRATHIMA B. Hexavalent chromium removal by chemical precipitation method: A comparative study[J]. International Journal of Environmental Research and Development, 2011, 1(1): 41−49.
[34] SÁNCHEZ J, BUTTER B, BASÁEZ L, RIVAS B L, THOTIY M O. Efficient removal of Cr(VI) by polyelectrolyte-assisted ultrafiltration and subsequent electrochemical reduction to Cr(III)[J]. Journal of the Chilean Chemical Society, 2017, 62(3): 3647−3652.
[35] JIN W, ZHANG Z, WU G, TOLBA R, CHEN A. Integrated lignin-mediated adsorption-release process and electrochemical reduction for the removal of trace Cr(VI)[J]. RSC Advances, 2014, 4(53): 27843−27849.
[36] DHARNAIKA S, GHOSH P K. Hexavalent chromium [Cr(VI)] removal by the electrochemical ion-exchange process[J]. Environmental Technology, 2014, 35(18): 2272−2279.
[37] RENGARAJ S, YEON K H, MOON S H. Removal of chromium from water and wastewater by ion exchange resins[J]. Journal of Hazardous Materials, 2001, 87(1/3): 273−287.
[38] JAIN P, VARSHNEY S, SRIVASTAVA S. Application of nitrogen-enriched nanobiopolymer for the effective removal of Cr(VI) from tannery effluent[J]. Separation Science, 2017, 52(9): 1572−1582.
[39] HAN A, ZHANG H, SUN J, CHUAH G K, JAENICKE S. Investigation into bulk liquid membranes for removal of chromium(VI) from simulated wastewater[J]. Journal of Water Process Engineering, 2017, 17: 63−69.
[40] MA H, XU Y, RONG Z, CHENG X, GAO S, ZHANG X, ZHAO H, HUO L. Highly toluene sensing performance based on monodispersed Cr2O3porous microspheres[J]. Sensors and Actuators B, 2012, 174(11): 325−331.
[41] WAGNER C D, RIGGS W M, DAVIS L E. Handbook of X-ray photoelectron spectroscopy[M]. Waltham: Perkin Elmer Corporation, 1979.
[42] 金春姬, 王朋远, 于 辉, 李 方. 基于空气阴极的微生物燃料电池处理含铬(VI)废水[J]. 中国海洋大学学报, 2015, 45(5): 69−74. JIN Chun-ji, WANG Peng-yuan, YU Hui, LI Fang. Treating wastewater contained Cr(VI) based on the microbial fuel cell with an air-cathode[J]. Periodical of Ocean University of China, 2015, 45(5): 69−74.
[43] YAO Z M, LI Z H, ZHANG Y. Studies on thermal dehydration of hydrated chromic oxide[J]. Journal of Colloid and Interface Science, 2003, 266(2): 382−387.
Removal of Cr(VI) from electrolytic manganese wastewater and electricity production by dual-chamber microbial fuel cell
HE Ze-qiang1, 2, ZHANG Rui2, LONG Qiu-ping2, WAN Zu-yang2, XIE Biao2, XIONG Li-zhi1, 2
(1.College of Materials and Chemical Engineering, Hunan City University, Yiyang 413000, China; 2. College of Biology and Environmental Sciences, Jishou University, Jishou 416000, China)
A dual-chamber microbial fuel cell (MFC) was constructed with F026 as electricigen and Cr(VI) containing electrolytic manganese wastewater as catholyte. The influences of pH, initial Cr(VI) concentration of simulated electrolytic manganese wastewater and operating temperature of MFC on the reduction rate of Cr(VI) and electricity generation of MFC were investigated. The results show that when the pH is 2 and operating temperature is 303K, the optimal treatment effect by MFC can be achieved. Under these conditions, 92.1% of Cr(VI) is reduced to Cr2O3in 80 h, and the complete Cr(VI) reduction and more than 914.7 mW/m2powder density are obtained in 155 h for the real electrolytic manganese wastewater with Cr(VI) concentration of 124 mg/L, indicating that MFC may be a promising technology for the treatment of Cr(VI) containing electrolytic manganese wastewater.
electrolytic manganese wastewater; Cr(VI); microbial fuel cell; electricity generation
Projects(51472107, 51672104) supported by the National Natural Science Foundation of China; Project(2017JJ2216) supported by the Natural Science Foundation of Hunan Province, China; Project(JSU0713) supported by the Construct Program of the Key Discipline in Hunan Province, China; Project supported by Aid program for Science and Technology Innovative Research Team in Higher Educational Instituions of Hunan Province, China; Projects(JDZ201503, Jdy16013, Jdx16016, Jdx16017) supported by the Research Foundation of Jishou University, Hunan Province, China; Project(JDSTLY1612) supported by the Research Foundation of Key Laboratory for Ecotourism of Hunan Province; Project(2017[205]-46) supported by program of College students’ inquiry learning and innovative experiment, Hunan Province, China; Project(MCPEGFM2006010) supported by the Research Foundation of Key laboratory of Mineral Cleaner Production and Exploit of Green Functional Materials in Hunan Province, China; Project(NLE201603) supported by the Research Foundation of National & Local United Engineering Laboratory of Integrative Utilization Technology of, China
2017-07-24;
2018-04-10
XIONG Li-zhi; Tel: +86-743-8564416; E-mail: csuhzq@163.com
10.19476/j.ysxb.1004.0609.2018.09.25
1004-0609(2018)-09-1937-11
X703.1
A
国家自然科学基金项目(51472107,51672104);湖南省自然科学基金项目(2017JJ2216);湖南省重点学科建设项目(JSU0713);湖南省高校科技创新团队支持计划项目;吉首大学校级项目(JDZ201503,Jdy16013,Jdx16016,Jdx16017);生态旅游湖南省重点实验室开放项目(JDSTLY1612);湖南省大学生研究性学习与创新性实验计划项目(湘教通2017[205]号-406);矿物清洁生产与绿色功能材料开发湖南省重点实验室开放项目(MCPEGFM2006010);杜仲综合利用技术国家地方联合工程实验室(NLE201603)
2017-07-24;
2018-04-10
熊利芝,教授,博士;电话:0743-8564416;E-mail:csuhzq@163.com
(编辑 王 超)

