超声场中马铃薯淀粉糊的特性粘度变化及其机理
,,,*,, ,
(1.广西大学轻工与食品工程学院,广西南宁 530004;2.广西蔗糖产业协同创新中心,广西南宁 530004)
超声波是一种独特的能源形式,媒质分子在不同的超声时间、超声声强中获取的能量完全不同于传统的热能、光能和离子辐射能。一般小振幅超声波在媒质中传播时,声波与媒质的相互作用可导致声波的相位与振幅等发生变化,而媒质本身并不发生任何明显的改变,或者说声波不会对媒质产生任何明显效应;但当超声波作为功率超声使用时,超声波声强增大,声波传播将会对媒质产生一定的影响和效应,引起媒质的状态、组分、功能或结构等发生变化[1]。
超声技术已经在食品工业中开发并广泛应用于提取、干燥、过滤和分离[2-5]。Kang等[6]观察到在超声处理后,玉米淀粉糊的粘度和流体动力学半径显著降低。Renata等[7]研究了360 kHz超声波对壳聚糖和淀粉分子的影响,用特性粘度表征了高频超声场下淀粉分子的分子量变化规律。Lipatova等[8]研究超声场中浓度为1%~8%的淀粉凝胶物性的变化规律,研究结果表明,超声波的振动效应使淀粉凝胶的粘度、透明度和相组成发生明显变化。Isono等[9]研究40、50、60 ℃超声场中蜡玉米淀粉粘度曲线变化规律,发现40、50 ℃超声场作用后,淀粉的粘度曲线与原淀粉的粘度曲线趋势相似,但超声场作用后淀粉的粘度值降低,60 ℃超声场作用后淀粉的粘度几乎为0 Pa·s。但并未有充分的实验数据证明其变化规律,超声场中粘度变化规律的研究比较零散,其中粘度下降的内在原因和机理尚未弄清楚。因此,要探明超声场中食品体系的粘度变化规律和引起粘度变化的机理,还需要做大量基础性的研究工作。
本文通过研究超声场中马铃薯淀粉糊单体结构和直链淀粉含量的变化,从分子结构水平,探讨超声波与淀粉分子之间的作用机理。通过乌氏粘度计测定淀粉糊特性粘度,研究超声场中马铃薯淀粉糊特性粘度的变化规律,探讨超声场中马铃薯淀粉糊粘度变化的机理。
1 材料与方法
1.1 材料与仪器
马铃薯淀粉 美国国民淀粉(化学)有限公司;二甲基亚砜 广州化学试剂厂;碘化钾 天津市化学试剂一厂;除淀粉纯度为99.5%外,以上试剂均为AR级。
UP400S超声波设备 德国Dr.hielscher公司;UV-2102 PC紫外-可见分光光度计 尤尼科(上海)仪器有限公司;Spectrum 2000傅立叶红外光谱分析仪 美国PE公司;DZF-6050X真空干燥箱 上海博讯实业有限公司;FW80高速万能粉碎机 天津市泰斯特仪器有限公司;1835乌氏粘度计 上海晖创化学仪器有限公司;HH-2数显超级恒温水浴锅 江苏金坛市富华电器有限公司。
1.2 实验方法
1.2.1 马铃薯淀粉糊的制备 称取马铃薯淀粉2.000、4.000、8.000、16.000、24.000、32.000 g,用蒸馏水配成质量浓度为0.5%、1.0%、2.0%、4.0%、6.0%、8.0%的溶液400 mL,搅拌使之充分分散,沸水浴中加热糊化30 min,随后冷却至室温。
1.2.2 超声场中马铃薯淀粉糊的静态实验 实验所用到的超声设备(图1)的超声探头直径为7 mm,将超声探头浸入液面2 cm,超声占空比为0.5,实际超声声强占最大超声声强的百分比可在0~100%之间调节,以此来调节超声声强的大小。在实验过程采用冰水浴的方法,调节反应体系温度(25.0±1.0) ℃。所用到的马铃薯的稀淀粉糊都经过糊化,且每次取样体积为100 mL。

图1 马铃薯淀粉糊超声场处理装置图Fig.1 Apparatus scheme sketch of ultrasonic treatment for potato starch paste注:1:超声波发生器;2:超声波换能器;3:变幅杆;4:隔音箱; 5:铁架台;6:铁夹;7:反应器;8:冷却系统;9:托板。
1.2.2.1 超声场作用时间对马铃薯淀粉糊特性粘度的影响 控制温度、超声声强以及马铃薯淀粉糊浓度不变,研究25.0 ℃下,超声声强为300 W/cm2,马铃薯淀粉糊浓度为0.5%,超声时间分别为:0、0.5、1.0、5.0、10.0、30.0、60.0 min时,马铃薯淀粉糊特性粘度的变化情况。
1.2.2.2 超声场声强对马铃薯淀粉糊特性粘度的影响 控制温度、超声时间和马铃薯淀粉糊浓度不变,研究25.0 ℃下,超声60 min,马铃薯淀粉糊浓度为0.5%,超声声强分别为:75、150、225、300 W/cm2时,马铃薯淀粉糊特性粘度的变化情况。
1.2.2.3 超声场中浓度对马铃薯淀粉糊特性粘度的影响 控制温度、超声时间和超声声强不变,研究25.0 ℃下,超声声强为300 W/cm2,超声时间为60.0 min,马铃薯淀粉糊的浓度分别为0.5%、1.0%、2.0%、4.0%、6.0%、8.0%时,马铃薯淀粉糊特性粘度的变化情况。
1.2.3 马铃薯淀粉糊的干燥和磨碎 将超声场作用前后的马铃薯淀粉液放在平底容器中,随后放入真空干燥箱,50.0 ℃干燥24 h后取出,用高速万能粉碎机将其磨碎,过100目筛,收集筛下物装入塑料瓶,放入真空干燥器中备用。
1.2.4 马铃薯淀粉糊的特性粘度测定 在25.0 ℃下用乌氏粘度计(毛细管内径0.57 mm)测定蒸馏水的流出时间为24.44 s,同时采用恒温水浴一套,选直径100 mm,高约250 mm的玻璃缸,配置电动机搅拌器和恒温装置,将水浴温度控制在±0.05 ℃之间。
称取按1.2.3中方法筛后的马铃薯淀粉,加入0.3 mL 4 mol/L氢氧化钾溶液,使马铃薯淀粉充分溶解,加入4 mL水,用2 mol/L盐酸中和,将pH调至6.5~7.0,用水定容至10 mL,马铃薯淀粉溶液置于离心机中,4000 r/min离心20 min,取上层清液5 mL,用蒸馏水配制成50 mL(浓度定为C1),取该溶液10 mL,移入乌氏粘度计,在恒温水浴中保温10 min,测定溶液流出时间T1。然后量取5 mL蒸馏水,加入到粘度计中,将粘度计中的溶液稀释成C2,混匀后取出部分液体,使粘度计内液体总体积为10 mL,测定溶液流出时间T2。按同样的方法,再依次量取蒸馏水5、10 mL,使粘度计中的溶液浓度分别为C3、C4,并分别测定溶液流出时间T3、T4。稀释后溶液浓度存在以下关系:C1=1.5C2=2C3=3C4,可按下式计算比浓粘度[10]:
式中,ηsp:增比粘度;C:被测溶液浓度;ηsp/C:比浓粘度;T:被测溶液在乌氏粘度计中的流出时间;T0:纯溶剂在乌式粘度计中的流出时间。
式中,ηsp:增比粘度;C:被测溶液浓度;ηsp/C:比浓粘度;[η]:特性粘度。
1.2.5 红外光谱分析 称取约2 mg按1.2.3中方法过筛后样品,在红外灯的照射下,置于玛瑙研钵中研磨4~10 min,再和150 mg干燥的溴化钾粉末充分混合,继续研磨2~5 min。将研磨好的混合物倒在硫酸纸上,灌注于压模中,抽真空2 min。缓慢加压至1×104kg,保持5 min,切断真空,缓慢除去压力,取出样品薄片,放入样品架上,置于红外光谱仪内在500~4000 cm-1波段扫描,绘出红外光谱图。
1.2.6 直链淀粉含量的测定 测定直链淀粉含量最常用的方法是淀粉与碘复合物比色法,实验选用二甲基亚砜作为分散剂,测定淀粉中直链淀粉的含量。称取50 mg按1.2.3中方法过筛后的淀粉,溶于90%二甲基亚砜10 mL中,于60.0 ℃水浴中加热10 min,迅速冷却,用蒸馏水在容量瓶中定容50 mL,取1 mL与0.5 mL碘液作用(每mL碘液含有0.2 mg碘和2 mg碘化钾),于50 mL容量瓶定容,显色10 min,用紫外分光光度计于400~800 nm波长范围进行扫描[11]。
为了进一步验证超声场中马铃薯淀粉分子链变化情况,以蜡玉米淀粉糊中的直链淀粉含量变化为对照,对超声场中马铃薯淀粉糊的直链淀粉含量变化进行了测定,方法与上述步骤相同,在620 nm处测定吸光值。
1.3 数据处理
采用SPSS 20.0软件进行数据的统计与分析。
2 结果与分析
2.1 超声场中马铃薯淀粉糊的静态实验
2.1.1 超声场作用时间对马铃薯淀粉糊特性粘度的影响 超声场作用时间是影响马铃薯淀粉糊特性粘度的重要因素,其对马铃薯淀粉糊特性粘度的影响结果如图2所示。
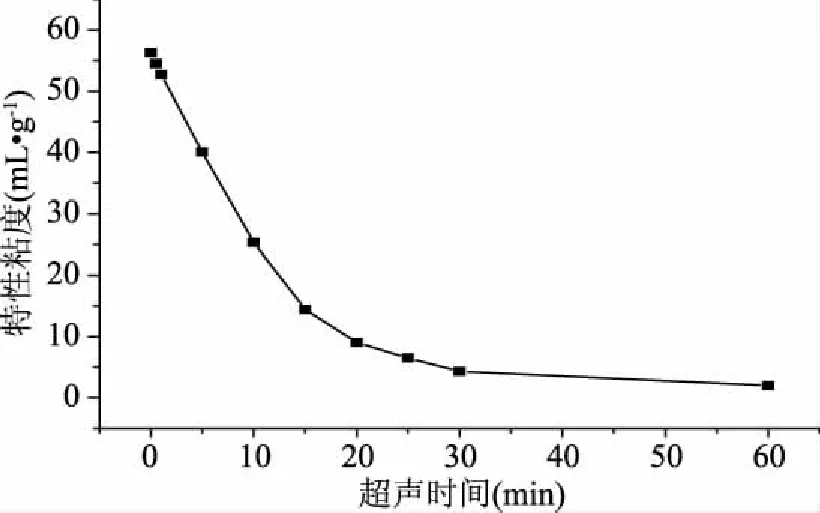
图2 超声时间对马铃薯淀粉糊特性粘度的影响Fig.2 Effect of ultrasonic time on intrinsic viscosity of potato starch paste
由图2可知,马铃薯淀粉糊的特性粘度与作用时间有明显的依赖关系。超声场作用使马铃薯淀粉糊中大分子变成小分子,发生了降解反应,特性粘度变小[10],Azhar等[12]解释可能原因是,超声场所提供的振动动能和空穴作用能致使化学键的断裂。总的来看,马铃薯淀粉糊的特性粘度随超声作用时间的规律是先快速下降后变平缓最后趋于极限值。在超声场作用初期(0~10.0 min),马铃薯淀粉糊的特性粘度大幅度下降,其值从56.302 mL/g迅速降至25.046 mL/g。在超声场作用中期(10.0~30.0 min),马铃薯淀粉糊的特性粘度略有下降,表明在此阶段仍有断链反应发生。在超声场作用后期(30~60.0 min),马铃薯淀粉糊的特性粘度几乎不再发生变化,并趋于一个极限值。流体粘度是液体流动时不同速度层分子间的动量传递及分子间引力作用所产生的内摩擦的表现,与流体内部的微观分子作用有关。超声场作用时间的增长即意味着输入能量的累积,输入能量对淀粉大分子产生高频剪切振动和射流的力场作用[13],使大分子变成小分子;输入能量越大,大分子数目越少,小分子数目越多,对淀粉糊流动产生的粘性阻力减小[14]。所以马铃薯淀粉糊的特性粘度与作用时间有明显的依赖关系。
2.1.2 超声场声强对马铃薯淀粉糊特性粘度的影响 超声场声强的大小对马铃薯淀粉糊特性粘度的影响如图3所示。

图3 超声声强对马铃薯淀粉糊特性粘度的影响Fig.3 Effect of ultrasonic intensity on intrinsic viscosity of potato starch paste
由图3可知,固定超声场作用时间为60.0 min时,特性粘度变化规律为:马铃薯淀粉糊在超声强度分别为75、150、225、300 W/cm2超声场中,超声作用后马铃薯淀粉糊的粘度依次减小。因此,超声场作用使得马铃薯淀粉糊的特性粘度下降,特性粘度下降程度随超声声强的增大而增大。
对声强为I的超声源,超声波传播到距声源X时的声强I为[12]:
I=I0e-2ax(α为声吸收系数)
式(1)
超声声强度越小,所受声压幅值越小,马铃薯淀粉糊发生降解的程度自然就较小;反之,超声场作用的声强越大,发生降解的区域范围也越大,马铃薯淀粉糊发生降解的程度越大。超声声强的增大与时间的增长具有等同效应,都意味着输入能量的累积[15]。因此,特性粘度下降程度随超声场作用声强的增大而增大。
2.1.3 浓度对马铃薯淀粉糊特性粘度的影响 除了超声场作用时间与超声声强对马铃薯特性粘度有影响,马铃薯淀粉糊本身的浓度对其特性粘度的变化也有一定的影响,其影响结果如图4示。

图4 浓度对马铃薯淀粉糊特性粘度的影响Fig.4 Effect of concentration on intrinsic viscosity of potato starch paste
由图4可知,超声场中马铃薯淀粉糊的特性粘度与淀粉糊的浓度有关。马铃薯淀粉糊的浓度越小,超声场作用后淀粉糊的特性粘度越低。0.5%与1.0%的马铃薯淀粉糊在超声场作用10.0 min,特性粘度变化很大,分别为8.778、25.389 mL/g,而2.0%、4.0%、6.0%、8.0%的马铃薯淀粉糊特性粘度变化很小。在流体媒质中,由于内摩擦而引起的吸收系数αη可表示为[16]:
式(2)
式中,ω为声波的角频率,c为声速,η和ρ分别为媒质的切变粘滞系数和密度。
由式(2)可见,超声波在媒质中的衰减程度与媒质的结构及物理状态紧密相关。马铃薯淀粉糊的浓度越小,η和ρ越小,超声波在马铃薯淀粉糊中的衰减程度越小,超声场作用于马铃薯淀粉糊的能量越高,所以马铃薯淀粉糊的浓度越小,特性粘度下降程度越大,超声场作用后马铃薯淀粉糊的特性粘度越小。因此,在超声场中稀溶液或溶胶的降解作用较大。在实验过程中,25.0 ℃下4.0%、6.0%、8.0%马铃薯淀粉糊体系的粘度与密度大,超声波衰减程度大,难以实现空化效应,初始作用的一段时间内没有声音。考虑到超声场作用过程中体系粘度与密度的不断变化、分子的扩散以及输入的能量在链间的重新分配,定量描述超声场作用在马铃薯淀粉糊体系中的强度分布是十分困难的。
2.2 超声场中马铃薯淀粉糊的IR谱图变化
物质的红外光谱是分子结构的反映,组成分子的各种基团由于产生伸缩振动和变形振动,都有特定的红外吸收区域,其它部分对其吸收位置影响较小,因此,红外光谱分析谱图中的特征吸收峰,与分子中基团的振动形式相对应[17]。通过对比超声场作用前后的马铃薯淀粉糊的傅立叶红外光谱(FT-IR)图,分析超声场中马铃薯淀粉糊组成单体结构的变化规律。
由图5知,在红外谱图上,波数在3400 cm-1处有一宽而强的吸收峰,是典型的O-H的伸缩振动[18-20];1642 cm-1处有一中强峰是-CH2中的C-H的弯曲振动[18-20],表明分子中含有吡喃糖苷键构型[21];1414 cm-1处有较强的吸收峰是基团-CH2中C-H的弯曲振动;淀粉的红外光谱中,1300~900 cm-1主要体现了高度耦合的C-O、C-C等键的振动,是淀粉的构型敏感带;常用1047、980 cm-1处来反映淀粉中结晶区的相关信息[22]。对比未经超声处理的马铃薯淀粉糊的FT-IR的特征吸收峰,超声30 min处理后,3400 cm-1处的O-H吸收峰出现变窄的现象,这可能是由于,马铃薯淀粉糊分子间或者分子内的氢键出现了断裂或再生[20]。红外光谱没有产生新的吸收峰,说明超声场中马铃薯淀粉糊的分子降解仅仅限于对分子主链的作用,而对马铃薯淀粉糊的单体α-D-吡喃葡萄糖没有明显影响。

图5 超声前后马铃薯淀粉糊的红外光谱分析谱图 Fig.5 FT-IR spectra of potato starch paste before and after ultrasonic注:1:马铃薯淀粉糊;2:超声30 min的马铃薯淀粉糊。
2.3 超声场中马铃薯淀粉糊与碘络合物的吸收光谱变化
通过测定淀粉和碘络合物的吸收光谱,可判断淀粉中链淀粉的含量大小,测定结果如图6所示。由图6可知,直链淀粉-碘络合物的λmax=622 nm,马铃薯淀粉糊和超声场中的马铃薯淀粉糊与碘络合物的紫外吸收光谱图的形状基本一致,但是最大吸收波长不同。马铃薯淀粉糊的λmax=599 nm,超声场作用30.0 min马铃薯淀粉糊的λmax=608 nm,超声场作用后马铃薯淀粉糊的最大吸收波长向长波方向移动。这是因为,在超声场中,马铃薯淀粉分子发生降解,部分支链淀粉的枝杈点发生断裂,或长链的直链淀粉发生断裂变成短链的直链淀粉,超声场作用后形成了较多的直链淀粉。

图6 马铃薯淀粉糊与碘络合的紫外吸收谱图Fig.6 UV spectra of combination of iodine and potato starch paste注:1:直链淀粉;2:未经超声的马铃薯淀粉糊; 3:超声30 min的马铃薯淀粉糊。
由图7可知,两种淀粉糊的直链淀粉含量随超声场作用时间延长而增加。表明在超声场作用下,马铃薯淀粉的1,6-糖苷键位置发生断裂,或者是直链淀粉分子链中的1,4-糖苷键发生断裂。在淀粉主链中,α-D-吡喃葡萄糖环状结构,由于环内原子之间的相互影响,引起电子云密度平均化,已形成稳定结构[17],环状结构不容易被超声波破坏而断裂,红外光谱谱图分析也证明了这一结论。除吡喃葡萄糖环以外C-O、C-C键是整个分子主链的薄弱环节,其平均键能分别为351.0、347.6 kJ/mol[17]。从键能大小可知,C-O、C-C键的键能比C-H的键能(415.3 kJ/mol)低,分子链易在此处断链。因此,超声场作用导致主链的断裂可能有三种情况,即1,4-糖苷键的断裂、1,6-糖苷键的断裂和1,6-糖苷键相连的C-C键的断裂。即C1、C4、C6位置的C-O键和C5、C6位置的C-C键是超声场作用最可能断裂的化学键。按键能大小推断,理论上C-C键比C-O键容易断裂。但是C-C、C-O键的键能基本相同,因此均有可能断裂。从图5的红外光谱吸收峰的形状变化也证明了超声场作用过程中糖苷键发生了断裂。在糖苷键的特征吸收峰中,1023 cm-1处强峰是-CH2-OH的伸缩振动[13],超声场作用后峰形由圆滑而钝变得尖锐。这说明糖苷键缔合羟基变为游离(无缔合)羟基,峰形因此变尖锐了。由此可以确定,马铃薯淀粉糊在超声场作用过程中,断裂键位置可能发生在糖苷键C-O上。Renata等[7]和Ulanski等[23-25]分别研究了超声场作用降解壳聚糖,研究结果表明1,4-糖苷键是主链断裂的位置。

图7 超声场中作用时间与淀粉糊直链淀粉含量关系图Fig.7 The relationship between ultrasonic time and quantity of amylose of potato starch paste注:右边纵坐标为蜡玉米淀粉糊的吸光度值; 左边纵坐标为马铃薯淀粉糊的吸光度值。
3 结论
马铃薯淀粉糊特性粘度随作用时间的延长而降低,随超声声强的增大而减少;超声场对稀淀粉糊的影响更大,马铃薯淀粉糊的浓度越小,特性粘度下降程度越大,超声场作用后马铃薯淀粉糊的特性粘度越小。傅立叶红外光谱分析表明,组成淀粉分子的单体α-D-吡喃葡萄糖在超声场中下没有明显改变。超声场作用后马铃薯淀粉糊的直链淀粉含量增大,结合键能大小分析,推断出超声场作用马铃薯淀粉糊的断链位置可能发生在糖苷键C-O上。这表明,超声作用使得马铃薯淀粉分子链断裂,马铃薯淀粉分子发生降解,产生较多的直链淀粉分子,链的缠结程度降低,链段的活动性增强,分子间的作用力减弱,马铃薯淀粉糊的特性粘度降低。

