新型SnO-CaO-P2O5系封接玻璃的组成设计及性能研究*
詹文俊 廖红卫 李晓麟 吴港胜
(长沙理工大学材料科学与工程学院 长沙 410114)
封接玻璃作为封接材料的一种,其耐热性和气密性优于有机高分子材料,电绝缘性能优于金属材料,这使得封接玻璃在多个领域能够得到应用。低温封接玻璃指熔点低于普通玻璃(一般低于600 ℃)的一类特种玻璃,具有合成工艺简单、耐温高、线膨胀系数小、机械强度高、抗疲劳性强等特点,适用于包括金属、陶瓷以及玻璃之间的互相封接。低温封接玻璃应用广泛,是半导体器件的气密性封接、集成电路的封装、电子显示器件的粘结[1]等工业生产过程不可或缺的材料。
就目前而言,商用的铅酸盐玻璃和铋酸盐玻璃存在成本较贵的问题,随着社会发展,封接玻璃正朝着无铅化、低熔点化方向快速发展,磷酸盐玻璃的发展潜力巨大,具有特征温度低、膨胀系数可调范围宽(60~250×10-7/℃)、原料价格低、污染少等优点,成为取代含铅低熔点封接玻璃的最佳候选材料[2]。但是磷酸盐玻璃的化学稳定性差,且具有吸湿性,这些缺点严重限制了磷酸盐的应用。
已经研究报道过的磷酸盐玻璃系统有SrO-SB2O3-P2O5[3]、ZnO-B2O3-P2O5[4]、ZnO-Sb2O3-P2O5[2]、SnO-ZnO-P2O5[5]、SnO-MgO-P2O5[6]等,这些磷酸盐系统具有比较低的软化温度,调整范围宽的热膨胀系数的优点,但缺点是化学稳定性差。因此,以氧化亚锡、氧化钙和偏磷酸等作为主要原料,研究了SnO-CaO-P2O5系统玻璃的封接性能,确定该系统玻璃的最佳组成成分,并在此基础上研究添加B2O3对玻璃结构和封接性能的影响。
1 实验
1.1 实验原料
偏磷酸(HPO3,北京精求化工有限责任公司,42%),氧化钙(CaO,天津市恒兴化学试剂制造有限公司,98%),氧化亚锡(SnO,上海麦克林生化科技有限公司,AR),硼酸(H3BO3,天津市恒兴化学试剂制造有限公司,AR)。
1.2 样品制备
采用高温熔融冷淬法制备玻璃样品。以10 g氧化物为基准计算原料用量,每次实验根据配方准确称取原料,于100 mL瓷坩埚中混合均匀,注意应快速称取偏磷酸以防止其吸水。通过预实验得到最佳熔制制度为:从室温以2 ℃/min升至400 ℃以充分排出原料中的挥发物,然后以10 ℃/min的升温速率快速升温至1 300~1 400 ℃,保温30 min,将所得熔体倾倒于预热过的石墨模具上,于400~ 500 ℃马弗炉中退火2 h以消除内应力,随炉冷却至室温后取出样品。将获得的样品分别用玛瑙研钵研磨成粉末和切割成形状规整的块状以用于后续的性能检测。
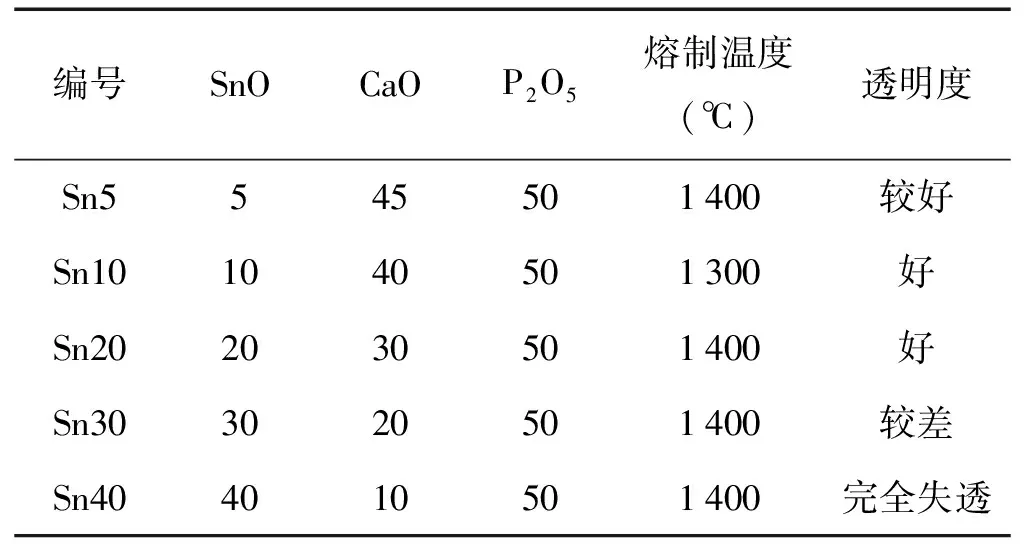
表1 Sn系列玻璃实验组成(mol%)及熔制情况
选择固定n(P2O5)=50mol%,通过用SnO取代部分CaO来探究其组成对SnO-CaO-P2O5系列玻璃结构和性能的影响,即实验组成为xSnO-(50-x)CaO-50P2O5(以下称为Sn系列玻璃)。表1列出了具体实验组成及熔制情况。
选取综合性能最佳的Sn10号玻璃作为基础玻璃组分,研究添加0~10mol%的B2O3对Sn10号玻璃结构和性能的影响,以改善玻璃的封接性能。添加B2O3的SnO-CaO-P2O5系列玻璃以下称为B系列玻璃,其最佳熔制温度为1 350 ℃,B系列玻璃的实验组成及熔制情况见表2。
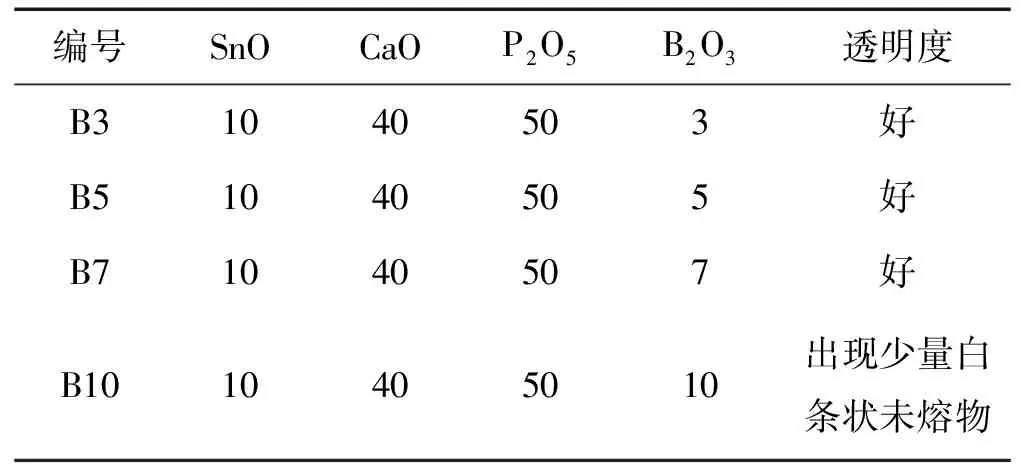
表2 B系列玻璃实验组成(mol%)及熔制情况
1.3 样品结构及性能表征
样品的结构信息由红外光谱(IRTracer-100型傅立叶变换红外光谱仪,日本岛津公司)分析得出,试样为过200目筛玻璃粉末,待测样粉末与KBr以2∶100混合均匀后压制成薄片,测试范围为400~4 000 cm-1;测试了与封接性能相关的热学性质(转变温度(Tg)、软化温度(Tf)、热膨胀系数(α))。采用同步(综合)热分析仪(STA409PC,德国耐驰仪器制造有限公司)获得样品的差热分析(DTA)曲线,确定样品的Tg,测试时升温速率为20 ℃/min,测试氛围为氮气,测试温度为40~1 000 ℃。利用SJY型影像式烧结点试验仪,记录各试样在加热过程中的形变行为,升温过程中试样棱角变圆时对应的温度为Tf。测试时将玻璃试样处理成边长约为5 mm的立方体,将四周打磨平整(升温速率为10 ℃/min);样品的热膨胀系数采用PCY型卧式高温热膨胀仪(湖南湘仪仪器有限公司)进行测量,测试温度为20~25 ℃,升温速率为5 ℃/min。实验试样为5 mm×5 mm×50 mm的长方体。材料热膨胀系数的计算公式为:
αp(T)=(∂L/∂T)/L0
(1)
式(1)中,在温度T时样品的膨胀系数表示为αp(T),长度表示为L,升温前样品初始的长度为L0。
玻璃的化学稳定性由通过测定块状样品为中性,碱性液体中的失重率来表征。测试时,将样品打磨成为15 mm×10 mm×4 mm的长方体,并将断面用砂纸打磨光滑,用蒸馏水清洗表面后置于120 ℃烘箱中烘干,30 min后称重,放入浸泡液中,浸泡48 h后取出,表面用蒸馏水清洗腐蚀层后置于120 ℃烘箱中烘干,30 min后称重,计算两次称重的失重率。浸泡液为蒸馏水及0.5 mol/L的氢氧化钠溶液。
2 结果与讨论
2.1 xSnO-(50-x)CaO-50P2O5系列玻璃的结构和性能
2.1.1 Sn系列玻璃的结构
图1为Sn系列玻璃的红外光谱。表3列出了Sn系列红外光谱主要的振动类型。磷酸盐玻璃网络结构的基本单元[PO4]四面体的4种形式用Qn表示,n的取值为0~3,代表[PO4]的桥氧数。Q3,Q2,Q1,Q0分别被定义为超磷酸盐,偏磷酸盐(P2O62-),焦磷酸盐(P2O74-)和正磷酸盐基团[10]。磷酸盐玻璃网络结构的交联程度取决于Qn的含量和分布。Q3表示不含网络修饰体的纯P2O5结构,此时[PO4]四面体形成一个交联网络;Q2有两个桥氧,在玻璃网络中形成环或者链;Q1则表示该位点为终端阴离子;Q0表示孤立的PO43-阴离子。
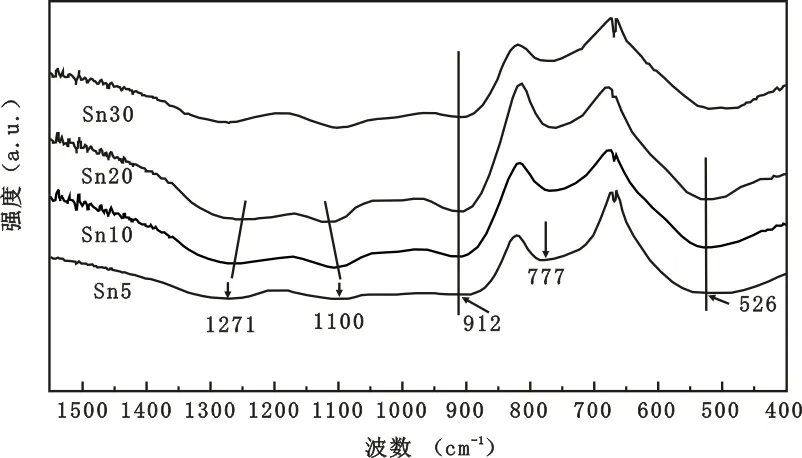
图1 Sn系列玻璃红外吸收光谱

表3 Sn系列玻璃红外光谱主要吸收峰对应振动类型
从图1可以看出,SnO含量上升到10 mol%时,1 100 cm-1处吸收峰明显增强,777 cm-1处吸收峰强度减弱,这表明Q2四面体中O-P-O键的对称伸缩振动加强,P-O-P键的对称伸缩振动有所减弱,这可能是玻璃中层状或架状结构中的P-O-P键断裂,生成更多磷酸盐链的结果。SnO含量为10 mol%~20 mol%时O-P-O键的不对称伸缩振动吸收峰往低波数方向偏移,Q2四面体中O-P-O键的对称伸缩振动吸收峰往高波数方向偏移,这可能是P=O双键打开,生成的P-O-Sn或P-O-Ca键影响了Q2四面体中O-P-O键的对称伸缩振动的结果。当n(SnO)=30mol%时,773 cm-1处P-O-P键的对称伸缩振动吸收峰、1 099 cm-1处Q2四面体中O-P-O键的对称伸缩振动吸收峰以及1 273 cm-1处O-P-O键的不对称伸缩振动吸收峰强度均减弱,同时518 cm-1处O-P-O键的伸缩振动吸收峰向低波数方向偏移,考虑到获得的Sn30号玻璃液较少,这可能是由于P2O5的挥发量较大,玻璃结构中P含量大为减少,导致各种类型的P-O键振动减弱。
2.1.2 Sn系列玻璃的热学性质
表4为Sn系列玻璃的热学性质。由表4可以看出,Sn系列玻璃Tg范围是410~435 ℃,Tf的范围是491~548 ℃,α的范围为(7.65~9.84)×10-6/℃。Tg是玻璃由玻璃态向高弹态转变的温度,Tg的值与玻璃结构的紧密程度有关,一般玻璃结构越趋于紧密Tg越高。Tg和Tf均随SnO含量上升呈先降低后升高的变化趋势,这与红外光谱分析的玻璃网络紧密程度变化一致。整体而言,Sn系列玻璃的软化点偏高,与含铅低熔点玻璃的软化点相比还有一定差距。玻璃的热膨胀系数α与玻璃结构中质点的结合力以及结构的紧密程度有关,结合力越强、结构越松散,则α越小;Sn10号玻璃中网络结构交联程度较低,质点热振动较剧烈,使α较大。Sn30号玻璃的α较Sn20号下降明显,这可能是因为该玻璃中存在少量未熔物的原因,这部分物质的α较小,使整体玻璃的α明显减小。热膨胀系数是封接玻璃使用过程中的一个重要参数,Sn系列玻璃的α可调范围大,有利于封接玻璃的实际使用。
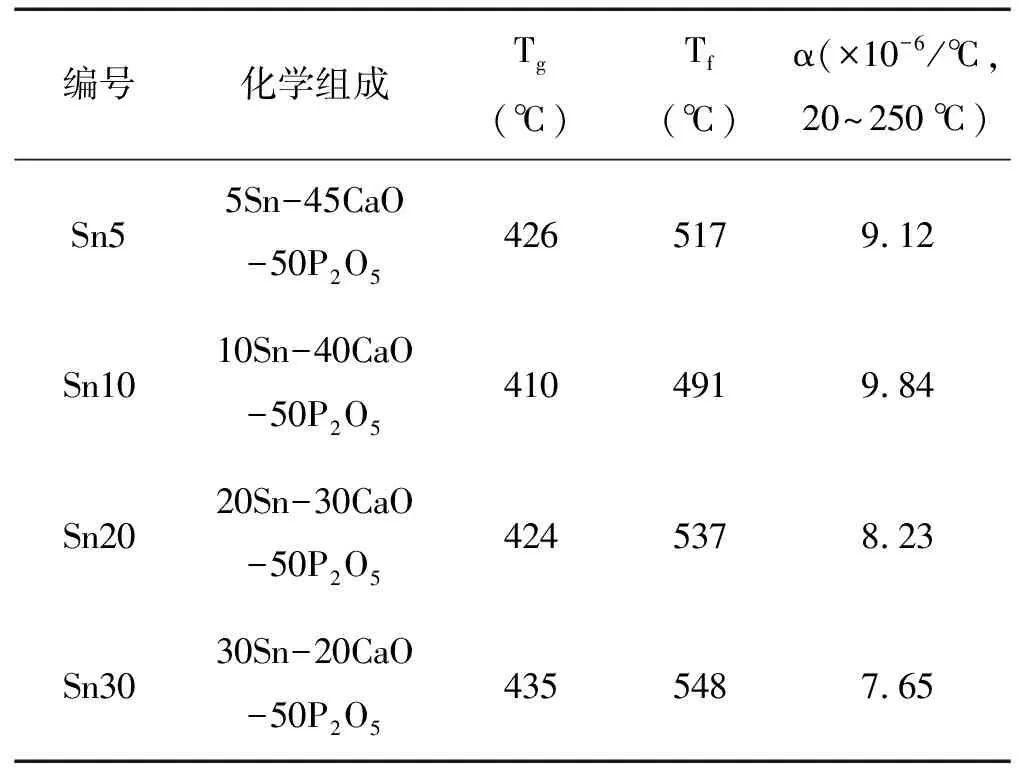
表4 Sn系列玻璃的热学性质
2.1.3 Sn系列玻璃的化学稳定性
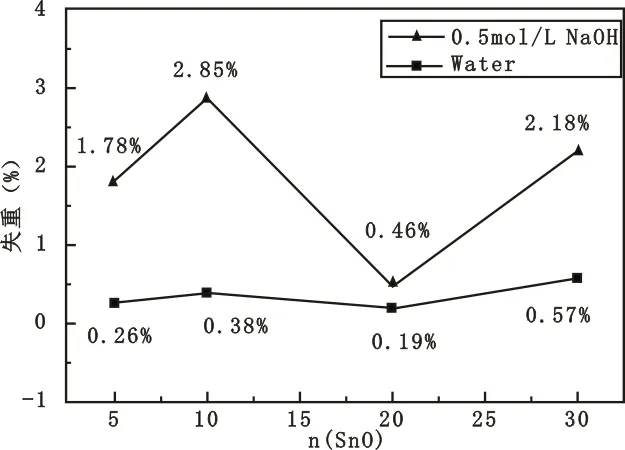
图2 Sn系列玻璃在0.5 mol%/L的NaOH溶液和蒸馏水中的失重率变化趋势
图2是Sn系列玻璃在0.5 mol%/L的NaOH溶液和蒸馏水中的失重率变化趋势。总的来说,Sn系列玻璃在中性环境中化学稳定性较好,碱性环境下较差,并且其失重率均表现为先上升后下降再上升的趋势。这是因为玻璃中磷酸盐网络交联程度发生了变化,首先磷酸盐链的解聚使结构松散,失重率上升,n(SnO)>10 mol%后形成的P-O-Sn键或Sn-O-Ca键能连接磷酸盐链,加固玻璃网络,化学稳定性上升,失重率下降。Sn30号玻璃的失重率较Sn20号玻璃有所上升,这可能是P2O5挥发,磷氧结构减少,使更多阳离子暴露于液体的原因。
2.2 添加B2O3对SnO-CaO-P2O5系列玻璃结构和性能的影响
2.2.1 B系列玻璃的结构
通过对比基础组分Sn10号玻璃和B系列玻璃的红外光谱来分析添加B2O3对SnO-CaO-P2O5系列玻璃结构的影响。图3为Sn10号基础玻璃和B系列玻璃红外吸收光谱图,表5列出了对应的振动类型。
由图3可知,添加B2O3后玻璃的红外光谱中未出现新的吸收峰,原有吸收峰的强度变化不是很大,这可能是因为添加B2O3后玻璃的主体结构未改变。B2O3以硼氧三角体[BO3]和硼氧四面体[BO4]两种结构进入玻璃结构,这两种结构相对含量的不同会对玻璃网络产生不同的影响,[BO3] 为层状结构,[BO4]为三维架状结构,因此[BO3]向[BO4]的转变能加强玻璃网络结构。
随着B2O3的引入,B系列玻璃1 105 cm-1处吸收峰的位置偏移到1 095 cm-1处,由表5可知,这可能是O-P-O键的不对称伸缩振动吸收峰与[BO4]的对称伸缩振动吸收峰叠加的结果,说明B系列玻璃中存在硼氧四面体[BO4],并且1 093 cm-1处的吸收峰不随B2O3的增加而减弱或偏移,说明B系列玻璃中始终存在硼氧四面体[BO4]。
1 260~1 280 cm-1处的吸收峰可能是O-P-O键的不对称伸缩振动吸收峰与[BO3]B-O键的伸缩振动吸收峰叠加的结果,说明了[BO3]结构单元的存在,并且该峰在n(B2O3)<5 mol%时向高波数方向偏移,当n(B2O3)>5 mol%时开始向低波数方向偏移。900~920 cm-1处的吸收峰可能是P-O-P键的不对称伸缩振动吸收峰与[BO4]的对称伸缩振动吸收峰叠加的结果,n(B2O3)<5 mol%时向低波数方向偏移,当n(B2O3)>5 mol%时向高波数方向偏移。1 260~1 280 cm-1和900~920 cm-1这两个位置的吸收峰的偏移可能是因为玻璃中同时存在[BO3]和[BO4]两种结构单元,并且随着B2O3添加量的增多,[BO3]减少而[BO4]逐渐增多。
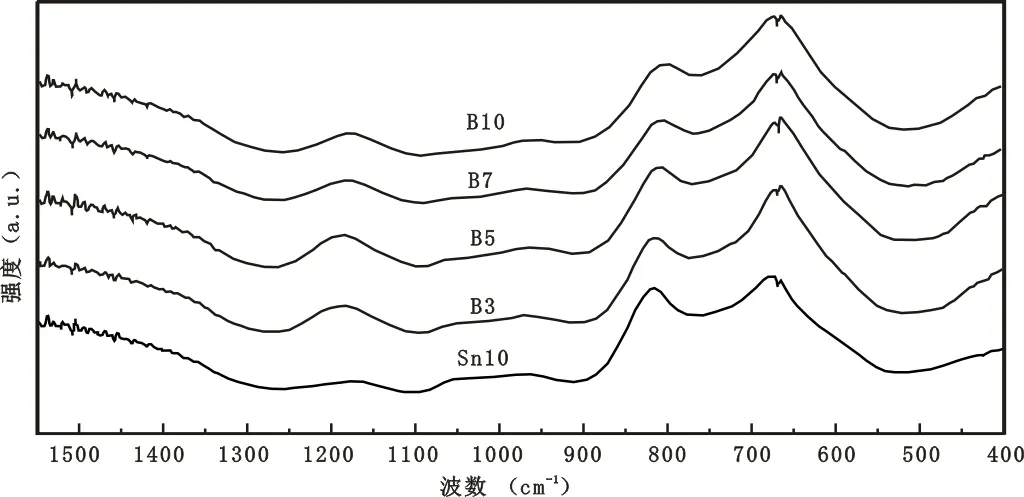
图3 Sn10号基础玻璃和B系列玻璃红外吸收光谱图

表5 B系列玻璃红外光谱吸收峰对应振动类型
2.2.2 B系列玻璃的热学性质

表6 B系列玻璃的热学性质
表6为B系列玻璃的热学性质。从表6可以看出,B系玻璃的Tg和Tf均随B2O3掺入量的增加呈单调增加趋势。Tg和Tf上升的原因是添加的B2O3主要以[BO4]形式存在于玻璃网络结构中,桥氧数增加,玻璃结构趋于紧密,与红外光谱分析结果一致。从表6还可以看出,添加B2O3后Sn10号玻璃的热膨胀系数呈减小趋势。图4为B系列玻璃的DTA曲线,均没有出现明显的析晶峰,表明B系列玻璃在熔融过程中无析晶趋势,保证了封接过程中不会析晶。
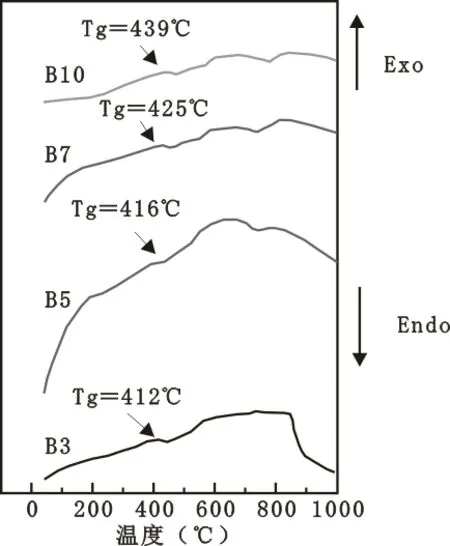
图4 B系列玻璃的DTA曲线
2.2.3 化学稳定性
测得B系列玻璃在中性环境下的失重率小于0.1%,已经具有良好的中性环境下的化学稳定性。图5为B系列玻璃在碱性溶液中失重率变化趋势。由图5可以看出,添加B2O3后,样品的失重率明显减小,化学稳定性大幅提升。根据玻璃的红外分析结果,这是由于硼氧三角体[BO3]和硼氧四面体[BO4]的存在增加了玻璃中桥氧的数目,提高了玻璃的紧密程度。

图5 B系列玻璃在碱性溶液中失重率变化趋势
3 结论
笔者以氧化亚锡、氧化钙、偏磷酸、氧化硼等为主要原料,采用高温熔融冷淬法制备xSnO-(50-x)CaO-50P2O5低熔点玻璃并确定其最佳熔制工艺。运用红外光谱,DTA等分析检测方法,分析组分变化及添加B2O3对玻璃结构和性能的影响,初步得出以下结论:
1)SnO-CaO-P2O5系列玻璃最佳熔制工艺为:以偏磷酸引入P2O5,将原料混合均匀后以2 ℃/min升温至400 ℃预处理,再快速升温至1 300~1 400 ℃后保温30 min,在450~500 ℃下退火2 h,获得的样品均质透明,无气泡。
2)随着SnO含量的增加,xSnO-(50-x)CaO-50P2O5系列玻璃结构由架状或层状结构向链状结构转变,当10 mol% 3)在10SnO-40CaO-50P2O5系列玻璃中添加0~10 mol%B2O3时,B2O3主要以[BO4]四面体结构单元进入玻璃网络。添加B2O3显著改善了玻璃的化学稳定性,同时增加了玻璃的特征温度,小幅减小了热膨胀系数。最佳组成为10SnO-40CaO-50P2O5-5B2O3,Tg=416 ℃,Tf=521 ℃,α=9.72×10-6/℃(20~250 ℃)蒸馏水中失重率小于0.1%,氢氧化钠溶液中失重率为0.18%。

