催化剂Ni-CeO2的制备及其在甲烷二氧化碳重整反应中的催化性能
李 琳,闪 洁,杨 桢,张煜华,李金林
(中南民族大学 催化材料科学国家民委-教育部暨湖北省重点实验室,武汉 430074)
能源的合理利用及能源结构调整在当今社会生活中有着很高的关注度和社会意义,环境问题如全球变暖等变得日趋严重.全球变暖的主要原因是温室效应,改善CO2和CH4等温室气体的利用能在很大程度上减少温室效应[1,2].而甲烷二氧化碳重整反应(简称CRM)为消耗这两种温室气体并将其转化为有用的合成气的一种合理方式,近年颇受关注[3].CRM反应能合成摩尔比接近1∶1的H2和CO[4],对费-托合成反应具有较高的利用价值.目前,CRM的催化剂主要由贵金属催化剂和Fe,Co, Ni基催化剂组成[5].Ni基催化剂由于其高活性、低成本和广泛的适用性而成为CRM的理想催化剂之一.但由于催化剂的烧结和积碳行为的存在,Ni基催化剂在长期稳定性测试期间倾于失活.因此,如何提高Ni基催化剂的抗积碳及抗烧结能力是CRM的关键问题[6,7].
CeO2是一种重要的碱性载体材料,它能通过促进活性组分的分散和增加金属与载体之间的相互作用提高催化性能. CeO2表面的Ce3+和Ce4+之间可进行快速且可逆的交换,产生特殊的储氧囊[8].因此可广泛用作许多催化反应中的活性组分或载体,如CO氧化,水煤气变换反应,NO催化还原,CH4催化部分氧化等[9].Huang等[10]发现Au/CeO2-NR与Au-CeO2纳米颗粒相比具有显著的低温氧化CO的能力,认为CeO2的表面结构和形态是主要的影响因素.Wu等[11]研究表明,CO2吸附在CeO2的{110}和{100}上的结合力更强.还有报道显示,Ni/CeO2催化剂在CRM中也表现出优异的催化性能[12].
本文合成了2种不同形貌的CeO2载体,即CeO2颗粒和CeO2立方体,制备了2种相应的镍基催化剂,即Ni-CeO2(立方体)及Ni-CeO2(颗粒)催化剂.对其催化CRM性能进行了评价,考察了其催化活性及稳定性,分析了不同形貌的CeO2载体对镍基催化剂催化重整反应性能的影响.
1 实验部分
1.1 材料和仪器
硝酸铈Ce(NO3)3·6H2O、氢氧化钾KOH、硝酸镍Ni(NO3)2·6H2O、无水乙醇C2H5OH均为分析纯(上海国药).透射电子显微镜(Tecnai G220,美国FEI);氮气物理吸附-脱附仪(Autosorb-1-TCD-MS,美国Quantachrome),X-射线粉末衍射仪(D8,德国Brucker);化学吸附仪(Altamira AMI-200,美国Zeton);热重分析仪(TG209F3,德国Netzsch);拉曼光谱仪(RM-200,英国Renishaw);气相色谱仪(MicroGC 3000A,美国Agilent).
1.2 催化剂的制备
配置浓度为0.1 mol/L Ce(NO3)3·6H2O溶液,搅拌30 min后,加入浓度为10 mol/L的KOH溶液后持续搅拌2 h.离心洗涤并干燥后,得到CeO2颗粒.将溶液倒入晶化罐,180 ℃保持48 h.将晶化后的沉淀物洗涤至中性,于100 ℃的烘箱中干燥,得CeO2立方体.
配置Ni(NO3)2·6H2O溶液,通过多次浸渍法负载活性金属,活性金属负载量为6%.80 ℃干燥12 h后,于550 ℃下煅烧6 h,制得Ni-CeO2(立方体)和Ni-CeO2(颗粒).
1.3 催化剂的性能测试
CRM在北京拓川反应器上进行.700 ℃下纯H2还原3 h后,切为N2吹扫30 min,流速为60 mL·min-1,最终切换为流量比为1∶1的反应气进行CRM评价,反应空速为36 L·g-1·h-1.活性测试温度区间从400~650 ℃,稳定性测试反应温度为700 ℃,反应时间为10 h.后续尾气的成分测试将在气相色谱上进行即时分析.
2 结果与讨论
2.1 透射电子显微镜(TEM)
立方体和颗粒CeO2载体及其对应的镍基催化剂的TEM结果见图1.

a)CeO2立方体;b) CeO2颗粒;c) CeO2立方体高分辨TEM;d) Ni-CeO2(立方体);e) Ni-CeO2(颗粒)图1 载体及催化剂的TEM图Fig.1 TEM images of supports and catalysts
图1a中合成的CeO2具有规整的立方体形貌,颗粒大小约为20 nm;图1c为立方形貌CeO2的高倍TEM,测得CeO2晶面间距为0.27 nm,表明文中制得立方体CeO2的6个暴露面为(200);图1d和1e为负载镍颗粒并焙烧后的催化剂Ni-CeO2(立方体)及Ni-CeO2(颗粒),可见Ni-CeO2(立方体)形貌有一定程度的破坏,但仍具有较好的立方体形貌.
2.2 X-射线粉末衍射(XRD)
载体负载活性金属Ni前后的XRD图谱结果如图2.由图2可见:2种形貌的CeO2均为面心立方萤石结构,其中28.5°(111),33.1°(200),47.5°(220),56.3°(311),59.1°(222),69.4°(400),76.7°(331),79.1°(420)的衍射峰归属为CeO2.相比CeO2颗粒,CeO2立方体的衍射峰更加尖锐,说明立方体CeO2的晶型较颗粒CeO2更规整.CeO2颗粒较宽的衍射峰证明其晶粒尺寸更小,与TEM结果相符.负载活性金属Ni之后,催化剂的XRD图谱均未出现NiO的特征峰,表明NiO在CeO2立方体及CeO2颗粒上均有较好的分散性,NiO颗粒尺寸较小. 颗粒和立方体Ni-CeO2与未负载CeO2相比,前者XRD峰高均有所降低,说明CeO2载体在负载活性金属之后,其晶型受到了一定程度的影响.
2.3 氮气物理吸附-脱附
Ni-CeO2(颗粒)和Ni-CeO2(立方体)的N2物理吸附-脱附曲线结果见图3.由图3可见:2种催化剂的等温曲线为V型,并在高压区存在H3型回滞环,说明材料中的孔主要是颗粒或立方体大量堆积形成的堆积孔.
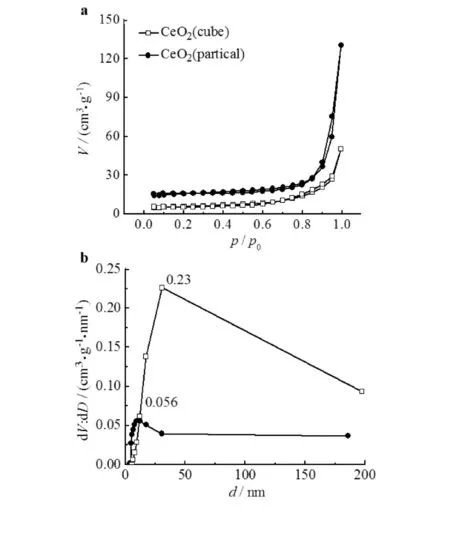
a) N2物理吸附-脱附曲线;b) 孔径分布曲线图3 CeO2立方体和颗粒的N2物理吸附-脱附及孔径分布曲线Fig.3 Nitrogen physical adsorption-desorption and pore size distribution curves of CeO2 cube and particles
CeO2立方体和颗粒的孔结构参数见表1.表1中知,载体CeO2立方体和颗粒具有相似的比表面积.

表1 载体CeO2立方体和CeO2颗粒的孔结构参数Tab.1 Pore structure parameters of CeO2 cube and CeO2 particles
2.4 氢气程序升温脱附(H2-TPD)及氧滴定
2种催化剂的H2-TPD数据和氧滴定数据结果见表2.由表2可见:Ni-CeO2(立方体)具有更高的耗氢量,Ni-CeO2(颗粒)具有较高的耗氧量.由于Ni-CeO2(立方体)表面的Ni颗粒分散度更高,粒径更小,具有更高的耗氢量;Ni 颗粒和载体的结合力更强,不宜被还原,因此在负载量一致时,Ni-CeO2(立方体)具有较少的耗氧量.数据表明Ni-CeO2(立方体)催化剂具有活性金属Ni分散度高,颗粒小,活性相与载体作用力强且不易团聚的良好特性.
表2 催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)的H2-TPD和O2滴定数据
Tab.2 H2-TPD and oxygen titration data of catalyst Ni-CeO2(cube) and Ni-CeO2(particle)

催化剂消耗量/(μmol·g-1) H2O2分散度 / %还原度 / %粒径 / nmNi-CeO2(颗粒)165.5695.032.468.03.1 Ni-CeO2(立方体)197.7688.838.767.42.6
2.5 催化剂的活性评价
图4是不同形貌CeO2负载的镍基催化剂在400~650 ℃下的反应活性数据.从图4a及图4b中可见,随着温度的升高,2种催化剂的活性均有很大程度的提升.在测试温度范围内,催化剂Ni-CeO2(立方体)在每个温度点都表现出了比Ni-CeO2(颗粒)更佳的反应活性.在650 ℃下,Ni-CeO2(立方体)的CH4和CO2转化率分别为28%和38%,Ni-CeO2(颗粒)分别为26%和36%.2种形貌的CeO2载体表面晶面不同,具有不同的表面积,对活性金属颗粒具有不同的作用力[11],故2种催化剂的活性差异归结于Ni颗粒与不同形貌CeO2载体之间的作用力的差别.O原子易穿过CeO2颗粒的(111)面,与4个晶格O原子形成不稳定的五配位结构;而在CeO2立方体的(200)面上,Ni2+占据2个(200)平面之间的空位,与立方体中的临近8个O原子形成稳定八配位结构.因此,在CRM反应中催化剂Ni-CeO2(立方体)在每个温度点的初始活性数据更佳.
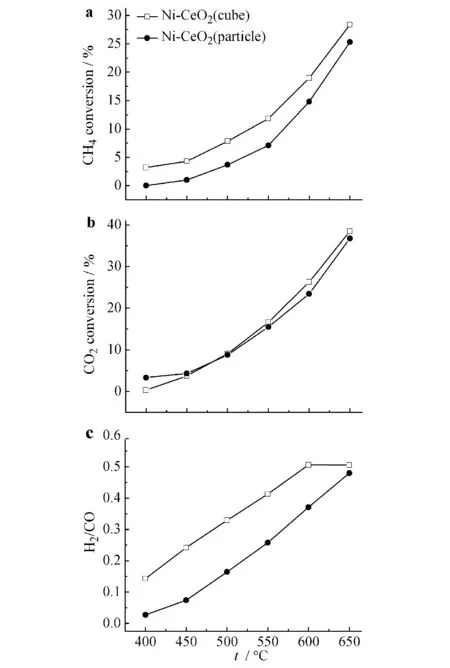
a) CH4转化率;b) CO2转化率;c) 氢碳比图4 催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)的活性数据Fig.4 Activity data of catalyst Ni-CeO2(cube) and Ni-CeO2(particle)
2.6 催化剂的稳定性评价
催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)在700 ℃下反应10 h的稳定性数据结果见图5.图5中稳定性数据随着反应时间的延长逐渐下降,是由于在长时间的高温反应过程中,催化剂烧结并产生部分积碳,导致活性下降.Ni-CeO2(立方体)的CH4转化率和CO2转化率分别下降了约10%和7%,Ni-CeO2(颗粒)分别下降了约15%和10%,在长时间的高温反应条件下,两者的催化活性均存在降低的现象.但在相同的反应时间内,Ni-CeO2(立方体)催化剂的失活程度低于Ni-CeO2(颗粒),展现出了良好的催化稳定性能.归其原因,是源于立方体形貌的CeO2具有特殊的(200)晶面及表面具有强极性.CeO2的(200)面能够使得Ni粒子更佳有效地掺入其晶格中,使得氧空位得到增加,提升对CO2的吸附能力,增强催化剂的活化能力.Ni-CeO2(立方体)氧空位的浓度提升能够有效地消除积碳并提升催化剂的稳定性.同时,Ni粒子被CeO2立方体的强极性面牢牢固定,使Ni纳米颗粒保持在较小的尺寸范围内,有效地抵抗催化剂活性金属颗粒长大烧结.
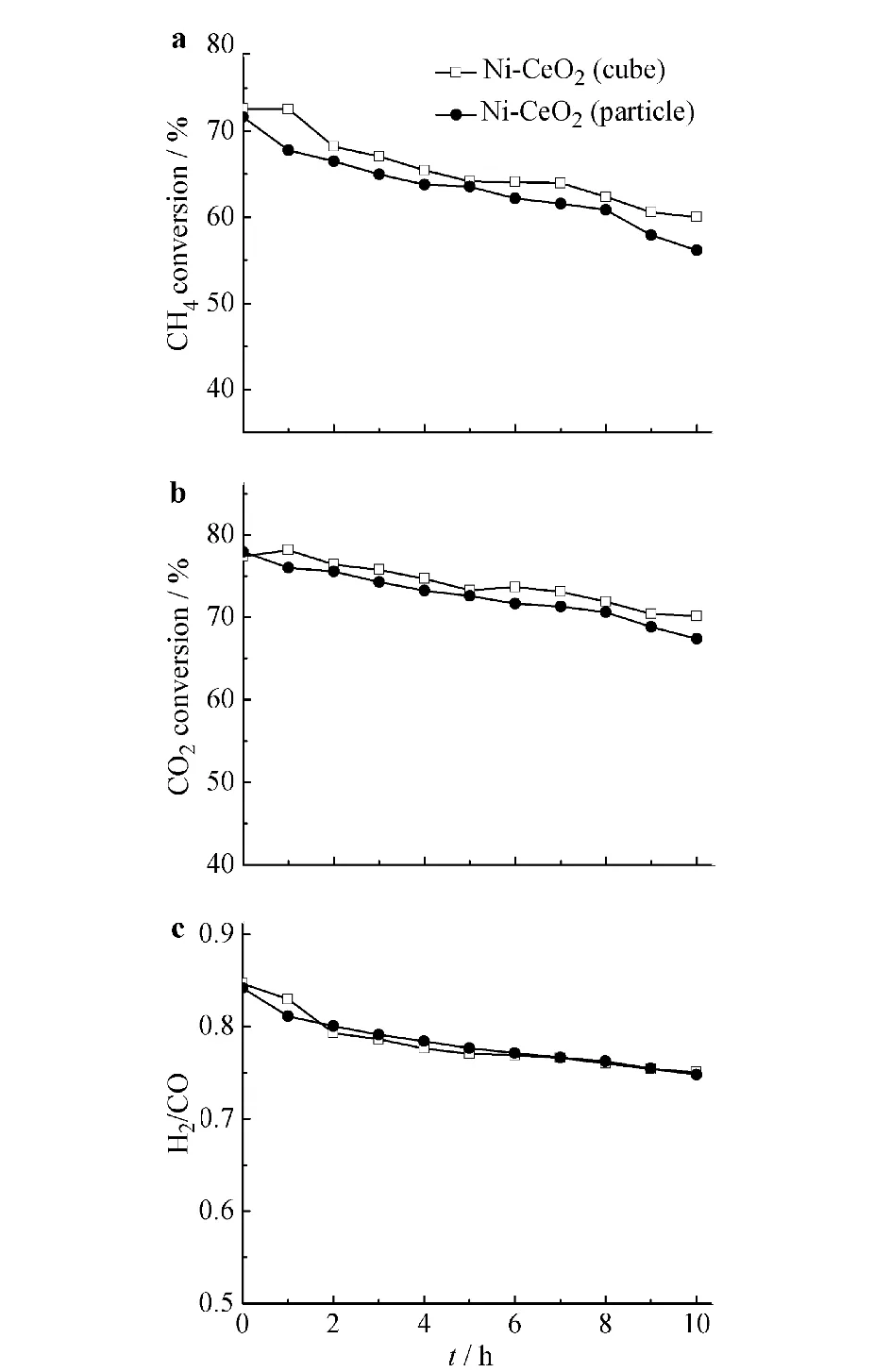
a) CH4转化率;b) CO2转化率;c) 氢碳比图5 催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)在700 ℃反应10 h的稳定性数据Fig.5 Stability data of catalyst Ni-CeO2(cube) and Ni-CeO2(particle) under 700 ℃ for 10 h
2.7 反应后催化剂的TEM表征
反应后催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)的TEM表征结果见图6.对比两种催化剂反应后的电镜图,催化剂Ni-CeO2(颗粒)反应后出现了严重的烧结,同时有更多的积碳存在,这也是Ni-CeO2(颗粒)稳定性测试中活性快速降低并失活的主要原因.催化剂Ni-CeO2(立方体)在催化活性和稳定性方面表现突出,这是由于CeO2立方体对Ni颗粒有很好的固定作用,有效防止Ni颗粒长大烧结,同时消除积碳.CeO2立方体的特殊(200)面还能抑制在反应过程中CH4裂解形成石墨碳所致催化剂失活的现象[13].因此催化剂Ni-CeO2(立方体)在更高的活性条件下产生更少的积碳.

a)Ni-CeO2(立方体);b) Ni-CeO2(颗粒)图6 催化剂在700 ℃反应10 h后的TEM图Fig.6 TEM images of catalysts after reacting at 700℃ for 10 h
2.8 反应后催化剂的TG表征
为了进一步研究反应后催化剂失活原因,对稳定性评价后回收的2种催化剂进行热重分析,表征结果见图7.由图7可见:反应后催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒)的失重量为分别为49.4%和55.1%,与TEM图结果一致,说明反应后Ni-CeO2(立方体)的积碳量更少,抗积碳能力更强.
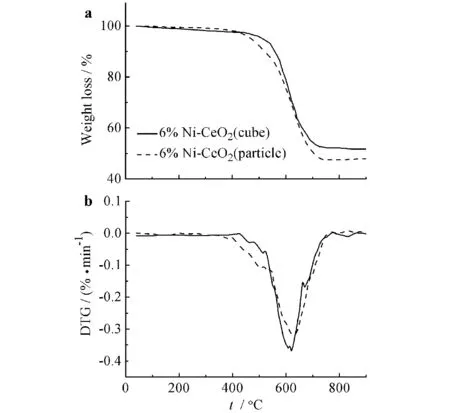
a)TG数据;b )DTG数据图7 反应10 h后催化剂的TG-DTG表征Fig.7 TG-DTG analysis of catalysts after 10 h reaction
2.9 反应后催化剂的Raman表征
反应后催化剂表面积碳的拉曼光谱表征结果见图8.由图8可见:2种催化剂在反应过后均形成无定形碳和石墨碳2种形式的积碳,无定形碳在一定条件下可以消除,而石墨碳则是造成催化剂失活的重要原因.2种催化剂D带及G带比值分别为0.81和0.84.催化剂Ni-CeO2(立方体)积碳中石墨碳含量更低,再次证明Ni-CeO2(立方体)对抑制积碳形成能力更佳.
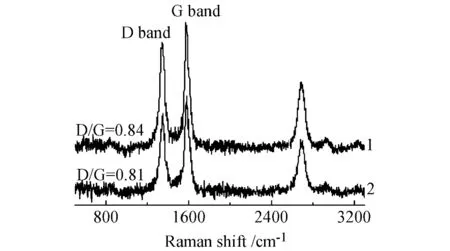
1) Ni-CeO2(立方体);2) Ni-CeO2(颗粒)图8 反应10 h后催化剂拉曼光谱图Fig.8 Raman spectra of catalysts after 10 h reaction
3 结语
本文制备了2种不同形貌的催化剂Ni-CeO2(立方体)和Ni-CeO2(颗粒),测试了催化剂对CRM的催化性能.结果显示:具有特殊晶面的CeO2(200)立方体作为载体的催化剂,具有更高的活性和更好的稳定性.由于CeO2(立方体)的特殊晶面提高了载体对CO2的吸附活化能力,相对强极性的表面提高了金属Ni与载体CeO2之间的相互作用,将Ni纳米颗粒稳定在较小尺寸范围,更有利于提高催化剂的反应活性和稳定性.
——会偷偷侵蚀你的发动机!
- 中南民族大学学报(自然科学版)的其它文章
- 蛋白体外结合实验联合质谱分析鉴定Num1的互作蛋白
- 脊髓灰质炎病毒I型单克隆抗体的制备
- 浅析丛枝菌根共生的生态学意义
- 以碱性聚合酶2(PB2)为靶点的抗流感病毒药物的虚拟筛选
- Discovery of Potential Novel TRPC 4 Inhibitor by Combination of Virtual Screening and 3D-QSAR Modeling
- Optical and Electrical Properties of Organic Semiconductor Thin Films for Optoelectronic Devices

