替比夫定联合恩替卡韦对失代偿期乙肝肝硬化患者血清可溶性红细胞补体受体1的影响
赵继坤

【摘要】 目的:探讨替比夫定联合恩替卡韦对失代偿期乙肝肝硬化患者血清可溶性红细胞补体受体1(sCR1)的影响。方法:选取2015年1月-2018年1月本院收治的62例失代偿期乙肝肝硬化患者,按照随机数字表法分为观察组和对照组,每组31例。对照组给予替比夫定治疗,观察组给予替比夫定联合恩替卡韦治疗。比较两组谷丙转氨酶(ALT)、白蛋白(ALB)、总胆红素(TBIL)、Child-Pugh评分、血清sCR1水平、乙肝病毒的脱氧核糖核酸(HBV-DNA)转阴率、乙肝e抗原(HBeAg)转阴率。结果:治疗后,观察组ALT、TBIL均明显低于对照组,ALB明显高于对照组(P<0.05);观察组Child-Pugh评分明显低于对照组(P<0.05);两组HBV-DNA和HbeAg转阴率比较,差异均无统计学意义(P>0.05);观察组血清sCR1明显低于对照组(P<0.05)。结论:替比夫定联合恩替卡韦治疗可降低失代偿期乙肝肝硬化患者血清sCR1水平,改善肝功能,提高乙肝病毒清除率。
【关键词】 替比夫定 恩替卡韦 失代偿期乙肝肝硬化 可溶性红细胞补体受体1
[Abstract] Objective: To investigate the effect of Telbivudine combined with Entecavir on serum soluble erythrocyte complement receptor 1 (sCR1) in patients with decompensated hepatitis B cirrhosis. Method: A total of 62 patients with decompensated hepatitis B cirrhosis in our hospital from January 2015 to January 2018 were selected and divided into observation group and control group according to random number table method, 31 cases in each group. The control group was treated with Telbivudine, while the observation group was treated with Telbivudine combined with Entecavir. Alanine aminotransferase (ALT), albumin (ALB), total bilirubin (TBIL), Child-Pugh score, serum sCR1 level, HBV DNA negative rate and HBeAg negative rate of two groups were compared. Result: After treatment, ALT and TBIL in the observation group were lower than those in the control group, and ALB was higher than that in the control group (P<0.05). The Child-Pugh score in the observation group was lower than that in the control group (P<0.05). There were no significant differences in HBV-DNA and HBeAg negative conversion rates between two groups (P>0.05). Serum sCR1 in the observation group was lower than that in the control group (P<0.05). Conclusion: Tibivudine combined with Entecavir can reduce the level of sCR1, improve liver function, and increase the clearance rate of hepatitis B virus.
[Key words] Tibivudine Entecavir Decompensated hepatitis B cirrhosis Soluble erythrocyte complement receptor 1
First-authors address: Jiamusi Central Hospital, Jiamusi 154002, China
doi:10.3969/j.issn.1674-4985.2019.34.008
乙型肝炎(乙肝)肝硬化是乙肝病毒(HBV)長期感染、肝炎反复活动导致的结果,进展为失代偿期是乙肝发展的最终结局之一[1]。我国是乙肝大国,HBV携带者达1.2亿左右,约占全球的1/3,且HBV感染人数仍在不断增加[2]。据报道,未治疗的乙肝患者中每年约有3%进展为失代偿期肝硬化[3]。失代偿期乙肝肝硬化病情复杂,容易因静脉破裂出血、感染、肝性脑病等而死亡,威胁患者的生命安全,因而需积极治疗[4]。替比夫定、恩替卡韦均为核苷酸类药物,替比夫定有特异性抑制乙肝病毒增殖的作用,抗病毒能力强,但耐药率较高[5]。恩替卡韦抗病毒能力强,且耐药率较低,可有效改善肝功能,但单用恩替卡韦对抗肝纤维化效果欠佳[6]。既往研究已表明,替比夫定、恩替卡韦均可改善失代偿期乙肝肝硬化患者的肝功能,有效清除血清HBV[7]。红细胞膜补受体1型分子(CR1)糖蛋白是一种免疫清除分子,相关研究显示,CR1在乙型肝炎相关慢加急性肝衰竭患者外周血红细胞中表达异常降低,且其表达水平与患者预后密切相关,其表达增强预示着患者良好预后[8]。可溶性红细胞补体受体1(sCR1)是CR1与黏附病原颗粒及免疫复合物的补体片段结合后形成的物质,进入循环系统后经肝脏代谢,sCR1是判断肝病患者肝功能损害的重要指标之一。本研究联合使用替比夫定与恩替卡韦治疗失代偿期乙肝肝硬化,观察其对患者sCR1的影响,现报告如下。
1 资料与方法
1.1 一般资料 选取2015年1月-2018年1月本院收治的62例失代偿期乙肝肝硬化患者作为观察对象。纳入标准:(1)符合《慢性乙型肝炎防治指南(2010年版)》中诊断标准;乙肝e抗原(HbeAg)阳性;(2)肝硬化;(3)年龄18~80岁;(4)核苷类及核苷酸类药物初治;(5)近3个月未接受干扰素、免疫调节药物治疗者。排除标准:(1)合并获得性免疫缺陷疾病;(2)合并其他全身急慢性感染疾病;(3)合并肝肿瘤、肝吸虫等肝疾病及肝性脑病;(4)药物、酒精等所致的肝炎;(5)合并恶性肿瘤;(6)伴消化系统出血、严重腹水等并发症;(7)严重心、肺、肾功能不全、神经系统疾病及消化性溃疡;(8)妊娠期或哺乳期。按照随机数字表法分为观察组、对照组,每组各31例。本研究经院内医学伦理委员会同意,患者知情同意并签署知情同意书。
1.2 方法 两组入院后均进行保肝、护肝治疗,清淡饮食,保持充足休息。对照组给予替比夫定(生产厂家:北京诺华制药有限公司,批准文号:国药准字H20070028,规格600 mg/片)治疗,600 mg/次,
口服,1次/d。观察组给予替比夫定联合恩替卡韦(生产厂家:福建广生堂药业股份有限公司,批准文号:国药准字H20110172,规格0.5 mg/片)治疗,替比夫定用药与对照组相同,恩替卡韦0.5 mg/次,口服,1次/d。两组均治疗12个月。
1.3 观察指标与评定标准
1.3.1 肝功能指标检测 治疗前后,采集空腹静脉血5 mL,3 000 r/min,离心10 min,取血清,采用速率法检测谷丙转氨酶(ALT),采用甲酚氯终点法检测白蛋白(ALB),采用化学氧化法检测总胆红素(TBIL)含量。
1.3.2 代偿期肝硬化程度评估 治疗前后,采用Child-Pugh评分评价代偿期肝硬化程度,其中5~6分为肝功能良好,7~9分为中等,10分以上为肝功能差。
1.3.3 sCR1水平检测 治疗前,治疗3、6、12个月后,采集空腹静脉血5 mL, 3 000 r/min,离心10 min,取血清,采用酶联免疫吸附实验法检测sCR1水平。本组所用试剂盒均购自北京科美生物技術有限公司。
1.3.4 阴转情况测定 治疗3、6、12个月后,测定乙肝病毒的脱氧核糖核酸(HBV-DNA)和乙肝e抗原(HBeAg)转阴率。
1.4 统计学处理 采用SPSS 19.0软件对所得数据进行统计分析,计量资料用(x±s)表示,组间比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 两组性别、年龄、病程等比较,差异均无统计学意义(P>0.05),具有可比性,见表1。
2.2 两组治疗前后肝功能指标比较 治疗后,两组ALT、TBIL均较治疗前明显下降,ALB均较治疗前明显升高,且观察组均明显优于对照组(P<0.05),见表2。
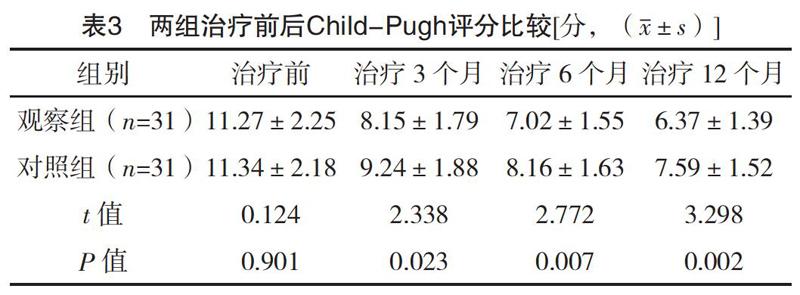
2.3 两组治疗前后Child-Pugh评分比较 随着治疗时间延长,两组Child-Pugh评分均明显降低,且观察组均明显低于对照组(P<0.05),见表3。
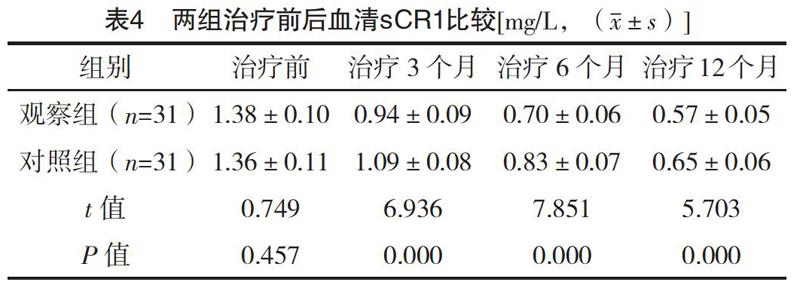
2.4 两组治疗前后血清sCR1比较 随着治疗时间延长,两组血清sCR1均明显降低,且观察组均明显低于对照组(P<0.05),见表4。
2.5 两组治疗后HBV-DNA、HbeAg转阴率比较 随着治疗时间延长,两组HBV-DNA、HBeAg转阴率均明显升高,但两组比较差异均无统计学意义(P>0.05),见表5。
3 讨论
我国乙肝感染人数庞大,乙肝疾病防治形势严峻。HBV感染所致的炎症刺激及免疫病理损伤导致肝炎进展为肝纤维化、肝硬化。肝纤维化贯穿整个乙肝的各个发展阶段,进而导致肝硬化,失代偿期乙肝肝硬化是乙肝肝硬化的终末阶段[9]。抗病毒治疗是延缓患者病情进展、控制肝硬化进一步发展的关键[10]。最新的美国肝病研究协会指南建议:失代偿期肝硬化患者应立即使用核苷和核苷酸类药物进行治疗。我国《慢性乙型肝炎防治指南(2010年版)》亦指出,乙肝病毒的脱氧核糖核酸(HBV-DNA)阳性的失代偿期乙肝肝硬化患者应积极采取核苷和核苷酸类药物进行抗病毒治疗。由于失代偿期乙肝肝硬化患者病情重,加上抗病毒治疗时间长、HBV病毒有一定的耐药性、变异性,临床抗病毒药物的选择需谨慎。
替比夫定为选择性抑制HBV-DNA聚合酶活性的核苷酸类药物,能够显著抑制HBV病毒复制,起到抗病毒的作用,并能够改善肝脏的储备功能,但容易出现耐药毒株[11]。恩替卡韦是2005年开始应用于抗HBV治疗,当前已成为一线抗病毒药物,抗病毒能力强,5年耐药率低于1.20%,耐药率极低,具有较好的抗肝纤维化的作用[12]。替比夫定联合恩替卡韦能够发挥协同作用,抑制HBV病毒复制增殖,延缓肝纤维化进程。研究显示,替比夫定联合恩替卡韦治疗可降低失代偿期乙肝肝硬化患者的血清TBIL、ALT及凝血酶原活动度水平,改善患者肝功能[13]。本研究结果显示,治疗后,观察组ALT、TBIL均明显下降,ALB明显升高,Child-Pugh评分显著降低,且效果优于对照组,差异均有统计学意义(P<0.05)。表明,替比夫定联合恩替卡韦能够显著改善失代偿期乙肝肝硬化患者的肝功能,效果优于单用替比夫定。
红细胞是人机体循环系统中数量最多的细胞,红细胞表面含有多种免疫功能相关物质,其具有免疫黏附功能、识别抗原、消除病原菌、促进抗原物质等作用[14]。其中,红细胞的黏附功能主要通过CR1进行,CR1属于一种补体活化抑制因子,同时也是补体C3b、C4b片段的受体[15]。CR1参与了黏附补体、结合免疫复合物、结合免疫抗原等过程,其形成的物质主要通过肝脏代谢[16]。红细胞表面的CR1在水解后形成sCR1,并进入血液循环,可通过血清检测。人感染HBV后,可激活补体C3,产生补体C3b、C4b片段,被红细胞表面的CR1黏附产生免疫复合体,其可结合、活化吞噬细胞,产生蛋白水解酶。在蛋白水解酶的作用下,免疫复合体水解产生sCR1,释放入血液循环;同时,携带抗原或病原体的sCR1抗原复合体被运输至肝脏、脾脏代谢[17]。因此,血清中的sCR1与肝脏sCR1呈正比,血清sCR1反映肝脏的代谢能力及损伤程度[18]。本研究结果显示,随着治疗时间延长,失代偿期乙肝肝硬化患者的血清sCR1明显降低,其中观察组明显低于对照组(P<0.05)。表明,替比夫定联合恩替卡韦能够降低乙肝肝硬化患者的血清sCR1水平,分析原因可能与清除HBV后肝炎活动度下降、肝功能改善有关,但具体机制尚需进一步论证。本研究结果显示,随着治疗时间延长,观察组HBV-DNA、HbeAg转阴率稍高于对照组,但两组比较差异均无统计学意义(P>0.05),表明联合用药对清除HBV有一定的优势,同时当前越来越多研究证实无交叉耐药的联合用药治疗优于单药治疗[19-21]。因此,失代偿期乙肝肝硬化治疗中,相对单用替比夫定,替比夫定与恩替卡韦联合用药仍是优先考虑方案。
综上所述,替比夫定联合恩替卡韦治疗可降低失代偿期乙肝肝硬化患者sCR1水平,改善肝功能,抑制HBV-DNA复制。
参考文献
[1]张国民,缪宁,郑徽,等.中国2005-2016年乙型病毒性肝炎报告发病的年龄和地区特征[J].中国疫苗和免疫,2018,24(2):121-126.
[2]张晖敏,吕加令,李丽萍.失代偿期肝硬化患者临床特点及预后分析[J].临床消化病杂志,2017,29(1):39-42.
[3]肖玉柱.阿德福韦酯联合恩替卡韦治疗老年失代偿期乙型肝炎相关肝硬化患者疗效及血清细胞因子水平变化[J].实用肝脏病杂志,2017,20(5):546-549.
[4]李忠东.恩替卡韦联合复方鳖甲软肝片治疗乙肝肝硬化失代偿期临床分析[J].重庆医学,2017,46(46):307-309.
[5]刘少杰,王桂芬,郭伟,等.恩替卡韦在失代偿期乙型肝炎肝硬化患者长期治疗的安全性和有效性[J].肝脏,2017,22(4):41-43.
[6]王艳红,魏军,张雨.乙肝肝硬化失代偿期腹水患者血钠水平与其并发症及临床预后的关系[J].临床与病理杂志,2017,37(6):37-40.
[7]胡大山.恩替卡韦分散片与阿德福韦治疗乙型肝炎肝硬化疗效比较[J].肝脏,2018,23(2):56-59.
[8]廖金瑶,肖艺,黄晶,等.替比夫定与恩替卡韦对乙型肝炎病毒感染患者的治疗疗效研究[J].中华医院感染学杂志,2018,28(7):983-986.
[9]李珂,李明传.恩替卡韦联合水飞蓟素对乙型病毒性肝炎失代偿期肝硬化患者炎症指标及氧化应激水平的影响[J].中国药房,2018,29(1):98-101.
[10]葛建祥,孙晔子,赵云.恩替卡韦治疗乙型肝炎肝硬化伴肝源性糖尿病患者疗效及其对糖代谢指标的影响[J].实用肝脏病杂志,2018,21(5):677-680.
[11]陈逊,刘海滨.前列地尔联合替比夫定对乙肝肝硬化患者疗效和血清炎性因子的影响[J].河北医学,2017,23(12):1963-1966.
[12]罗先平,经继生,陈红波,等.恩替卡韦治疗失代偿期乙型肝炎肝硬化3年疗效观察[J].实用肝脏病杂志,2017,20(5):614-615.
[13]张伟,许荣放,田锐锋,等.阿德福韦酯与替比夫定联合恩替卡韦对失代偿期乙肝肝硬化患者肝功能及血清病毒学指标的影响[J].解放军医学杂志,2016,41(12):1041-1044.
[14]陶强,郭建荣,金孝岠.红细胞微粒及其在机体生理病理过程中作用的研究进展[J].山东医药,2017,57(40):110-113.
[15]白志超,张宏方,于鹏龙,等.调衡方多糖对Lewis肺癌荷瘤体红细胞免疫功能的影响[J].西北药学杂志,2018,33(5):616-621.
[16]于歌,谢风.补体C1q(complement C1q)在临床研究中的最新进展[J].中国实验诊断学,2018,22(5):164-166.
[17]赵茜,吴立玲,李丽.补体C1q/肿瘤坏死因子相关蛋白15的研究进展[J].生理科学进展,2017,48(3):193-196.
[18]郭飞波.慢性乙肝患者血清补体C3、C4与肝炎分级程度以及肝纤维化程度的关系研究[J].中国免疫学杂志,2017,33(3):426-428.
[19]徐静,陶琳琳,叶娇娇,等.替比夫定联合阿德福韦酯治疗失代偿期乙型肝炎肝硬化患者疗效及其对肾功能的影响[J].实用肝脏病杂志,2019,22(1):94-97.
[20]张国顺,孟冬梅,方正亚,等.HBeAg阳性与阴性乙型肝炎肝硬化患者乙肝病毒载量及肝功能指标的研究[J].中国现代医学杂志,2018,28(16):54-57.
[21]沈华江,丁丰,王志炜,等.替比夫定和恩替卡韦治疗代偿期乙型肝炎肝硬化患者對肾小球滤过率估计值的影响[J].中华传染病杂志,2017,35(5):261-267.
(收稿日期:2019-06-11) (本文编辑:程旭然)

