磺胺间甲氧嘧啶钠注射液A、B 在猪体内的药代动力学比较试验
肖裕章 ,毕海林 ,张 超 ,袁启峰 ,胡 军 ,陈汇鑫 ,唐建华,
(1.重庆方通动物药业有限公司,重庆荣昌402460 ;2.西南大学荣昌校区,重庆荣昌 402460)
磺胺间甲氧嘧啶(Sulfamonomethoxine,SMM)在动物体内外都具有很强的抗菌活性,是磺胺类中抗菌作用最强的一种,且对大多数革兰阳性菌和阴性菌都有较强的抑制作用,细菌对此药产生耐药性较慢[1],是一种广谱抗菌药,其作用机制主要是与对氨基苯甲酸(PABA)竞争性作用于细菌体内的二氢叶酸合成酶,阻止叶酸的合成,减少具有代谢活性的四氢叶酸的量,从而抑制细菌的生长繁殖。SMM 口服后经胃肠道吸收良好,血液中浓度较高,乙酰化率低,乙酰化物在尿中溶解度大,不易引起结晶尿和血尿,能用于由敏感菌引起的各种疾病,对猪弓形虫病,禽、兔球虫病的疗效也是非常明显的[1]。
目前国内兽医临床上所使用的磺胺药剂型比较少,大都是中、短效类制剂,长效类制剂在市面上较少且经常出现刺激性大等不良反应,所以磺胺类长效制剂是目前兽药研发针对短板解决问题迫在眉睫的有效途径之一。为了延长SMM 注射液的持效时间,减少临床治疗周期,重庆方通动物药业有限公司对此研制出了一种具有长效性的磺胺间甲氧嘧啶注射液,它不仅能快速释放药物,还能较长时间的维持有效浓度,且刺激小,用药周期短,能更好地起到疗效,减少细菌对药物的耐药性。为了更能突出新研制SMM 注射液的优势,与常规SMM 注射液在猪体内的药代动力学过程参数进行比较,为临床应用以及产品开发提供试验与理论依据。
1 材料与方法
1.1 药品和试剂 SMM-Na 注射液A、B,两种产品均由重庆方通动物药业有限公司提供;SMM 对照品(批号C0031610,含量为99.5%)购自中国兽医药品监察所;甲醇:色谱级,赛默飞世尔科技(中国)有限公司;乙腈:色谱级,赛默飞世尔科技(中国)有限公司;磷酸:分析纯,重庆川东化工(集团)有限公司;N-N-二甲基甲酰胺:分析纯,重庆川东化工(集团)有限公司;乙腈:分析纯,重庆川东化工(集团)有限公司;水:屈臣氏蒸馏水,广州屈臣氏食品饮料有限公司。
1.2 仪器设备 安捷伦1260 高效液相色谱仪:四元泵VL:G7129A;DAD 检测器:G7115A;自动进样器:G7111A;LC1260 色谱工作站。TGL-16G 台式离心机:上海菲恰尔分析仪器有限公司;XW-80A 漩涡混合器:上海青浦沪仪器厂;80-2 台式低速离心机:上海手术器械厂;移液枪:上海求精生化试剂仪器有限公司;BP211D 电子天平:赛多利斯科学仪器(北京)有限公司。
1.3 试验动物 荣昌杂交健康猪10 头,公母各半,近期无用药史,体重(20.67 ±3.07)kg,由重庆市畜牧科学院实验猪场提供,试验期间单独分笼饲喂不含抗生素的全价饲料,自由饮水及采食,试验前2 周打耳号、分组、采血。检测结果所有试验猪不含磺胺间甲氧嘧啶。
1.4 给药和血样采集 荣昌杂交健康猪10 头,公母各半,平均体重为(20.67 ±3.07)kg,随机分成2 组,每组5 头,按50 mg/kg·bw 剂量分别在耳后方颈部肌肉注射磺胺间甲氧嘧啶钠注射液A、B。给药前采一次空白血样,给药后分别于0.25、0.5、1、2、3、5、7、9、12、24、36、48、72 h 自前腔静脉采集血样,采血量为2~3 mL 置于含肝素钠的离心管中,轻轻旋转混匀,防止凝固,在4 000 r/min 的离心机中离心10 min,分离血浆,-20 ℃保存待测。
1.5 血浆样品的处理 准确取新鲜或解冻血浆样品800 μL 于2.5 mL 带盖聚丙烯的离心管中,加入乙腈800 μL,旋涡混匀1 min,以16 000 r/min 离心15 min,取全部上清液经0.2 μm 微孔滤膜后,进行HPLC 测定分析。
1.6 HPLC 测定色谱条件及溶液的配制 色谱条件:色谱柱Welch Uitimate®XB-C18(5 μm,4.6 mm×250 mm),流动相:0.1%磷酸溶液-乙腈(80∶20);柱温:40 ℃;检测波长:271 nm;流速:1.0 mL/min。对照品储备溶液的制备:取SMM 对照品适量,精密称定,加入少量的N-N-二甲基甲酰胺溶解后,加乙腈制成每1 mL 含SMM 1.0 mg 溶液,即得。0.1%的磷酸溶液:精密移取磷酸1 mL 于1 000 mL 容量瓶中,加蒸馏水混匀后并定容即得。流动相:取0.1%的磷酸溶液800 mL 和200 mL 乙腈,混匀,过ϕ 0.2 μm微孔滤膜,超声脱气,待用。标准曲线溶液的制备:精密取对照品储备溶液0.5 μL、20 μL、50 μL、100 μL、200 μL、500 μL、1 000 μL 分别置于10 mL 容量瓶中,加乙腈定容制成0.05、2.00、5.00、10.00、20.00、50.00、100.00 μg/mL 的标准溶液。过ϕ 0.2 μm 微孔滤膜,即可进样。血样加样回收率溶液的制备:设置高、中、低3 个不同的浓度进行加样回收率测定,取12 份400 μL 空白血样分成高、中、低3 组,每组4 份,分别精密移取200 μL 标准溶液浓度为50.00 μg/mL、10.00 μg/mL、5.00 μg/mL 于各组血样中,再在每组血样中加入乙腈使之制成高浓度组浓度为12.50 μg/mL,中浓度组浓度为2.50 μg/ mL,低浓度组浓度为1.25 μg/mL 的溶液,过ϕ 0.2 μm 微孔滤膜,即可进样。
1.7 数据分析 药代动力学参数使用3P97 药代动力学计算程序处理。
2 结果
2.1 线性关系与回收率
2.1.1 线性关系 对SMM 对照品、空白血样、添加样品及给药后血浆样品进行液相色谱分析,得到图谱(见中插彩版图1)。SMM 与杂质分离度好,无干扰峰,峰形较好,保留时间在13 min 左右。在试验前,对含量测定方法进行了方法验证,在0.05~100.00 μg/mL 范围内,以0.05、2.00、5.00、10.00、20.00、50.00、100.00 μg/mL 7 个浓度进行标准曲线的制备,并以样品浓度和吸收峰面积作线性回归(见图2),得出回归方程为Y=71.64X -46.43,相关系数为R2=0.999 8。
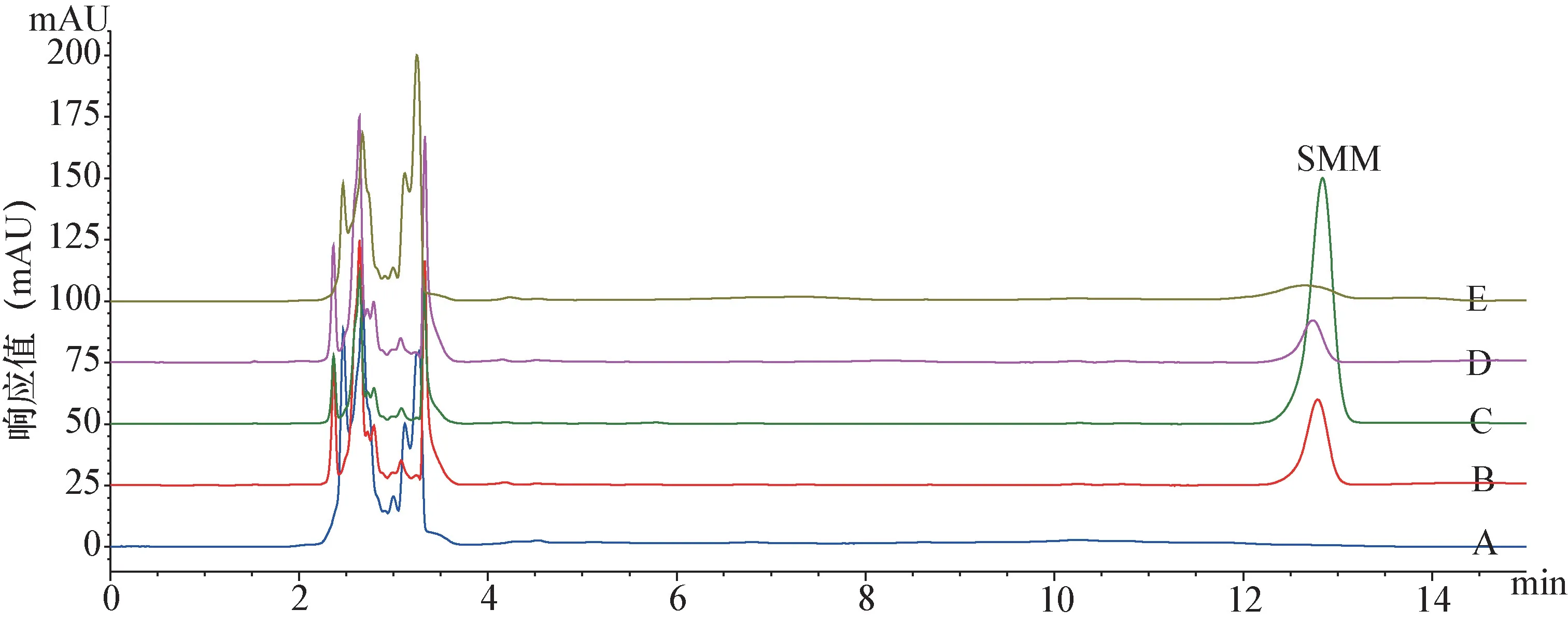
图1 猪血浆中SMM 的HPLC-DAD(271 nm)色谱分析
2.1.2 回收率 以浓度1.25、2.50、12.50 μg/mL的SMM 血样添加样品测定回收率,结果见表1。检测限(S/N=3)为0.025 μg/mL,定量限(S/N=10)为0.05 μg/mL。日内变异系数小于5.26%,日间变异系数小于4.85%。
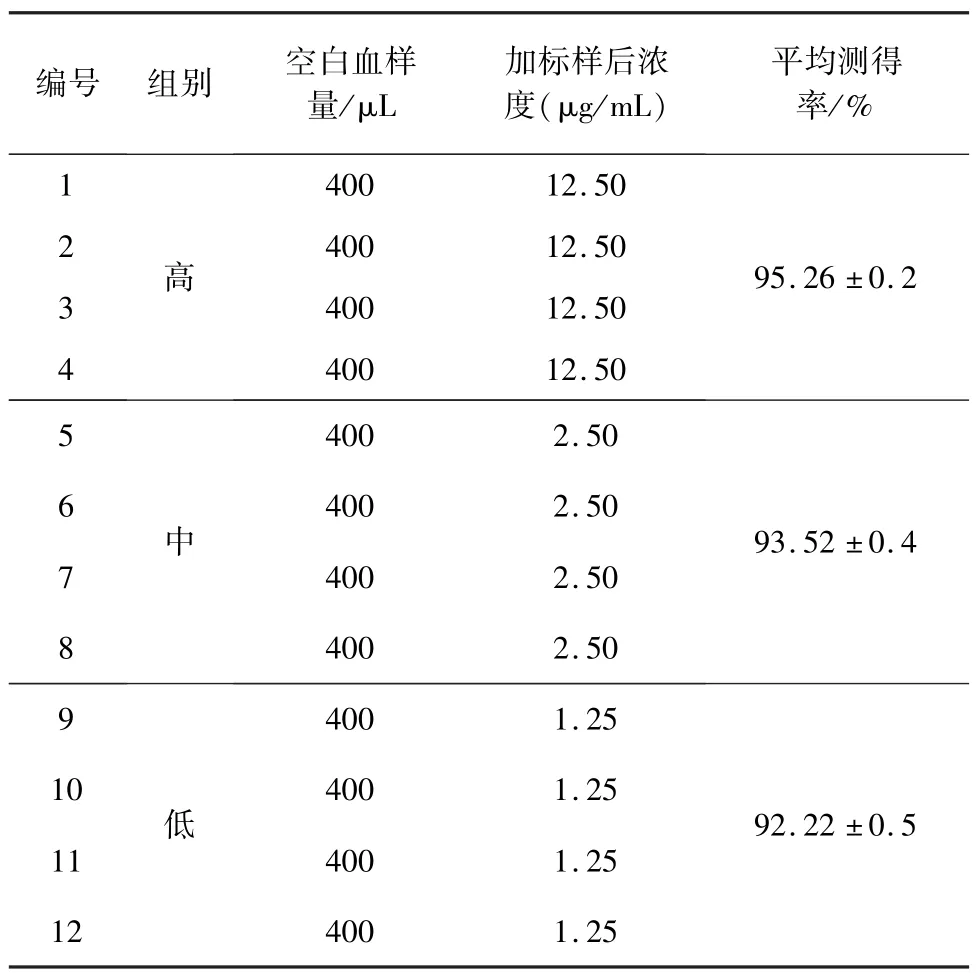
表1 加样回收率测定结果 (n=12)
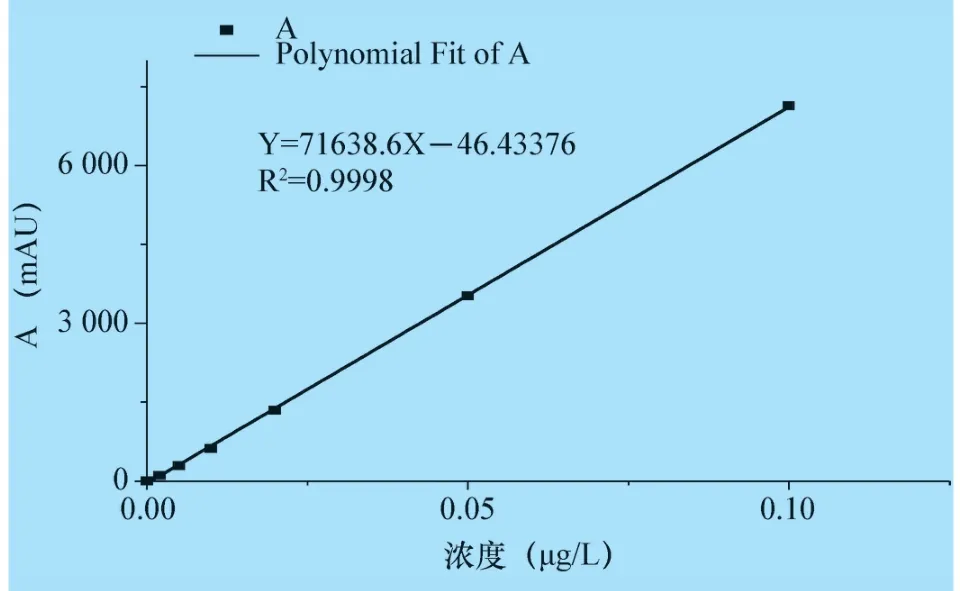
图2 线性回归图
2.2 血药浓度及药代动力学参数
2.2.1 SMM 在猪体内的药代动力学参数 以50 mg/kg·bw 的剂量给2 组猪肌肉注射后,制剂A、B 在猪体内的血药浓度随时间变化情况见表2,药代动力学参数见表3,药时曲线见图3,由表可知:A、B制剂的半衰期t1/2β分别为(20.75 ±1.29)h、(6.73±1)h,达峰时间分别为T(peak)=(2.15 ±0.12)h、T(peak)=(0.42 ±0.05)h,C(max)分别为(146.98 ±7.61)μg/mL、(270.83 ±16.71)μg/mL,48 h 时,A 制剂在猪体内的血药浓度降到(8.61 ±0.66)μg/mL,B制剂在猪体内的血药浓度未检测到。
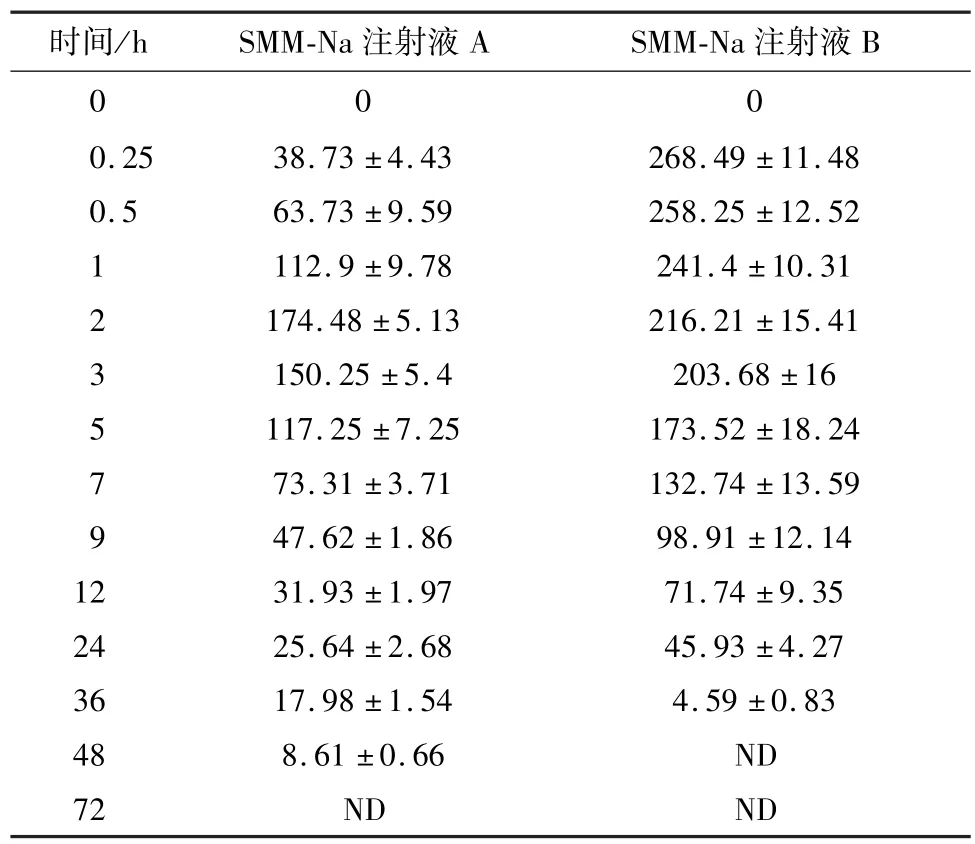
表2 2 种制剂给猪肌注50 mg/kg·bw 后SMM 在猪体内随时间变化的血药浓度 (μg/mL)
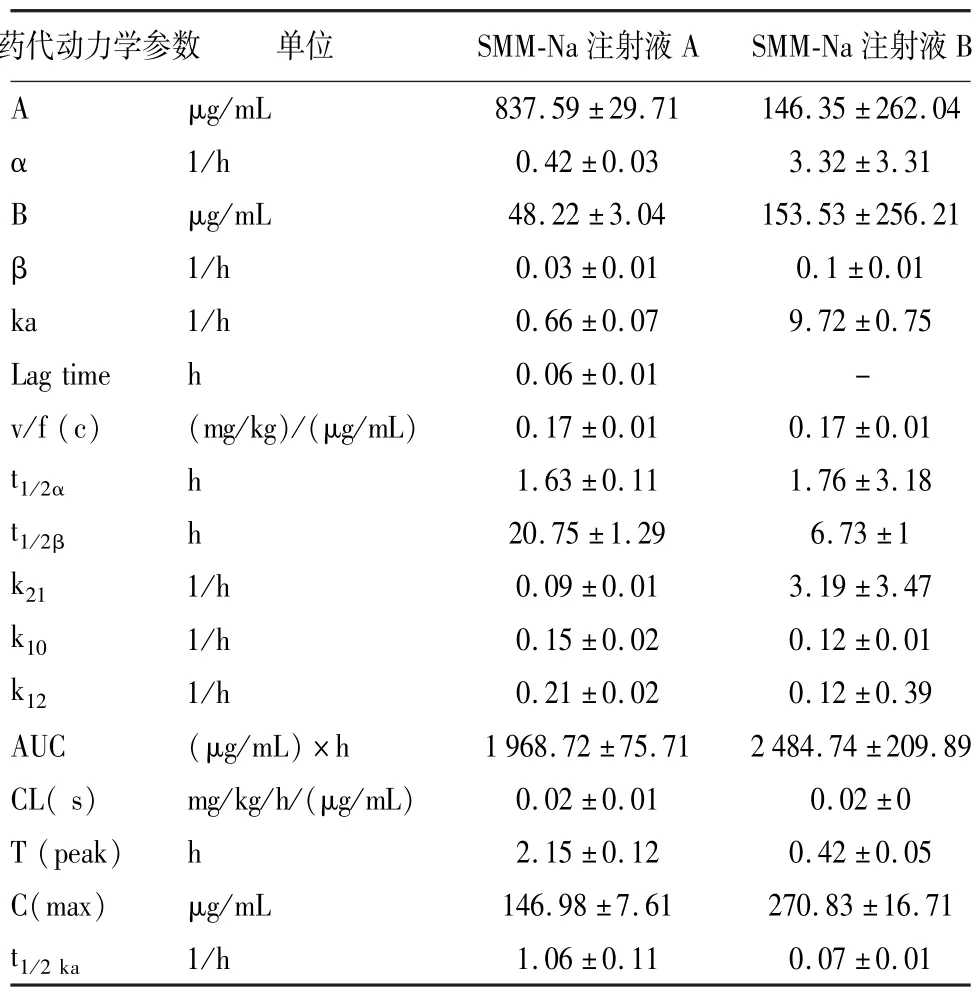
表3 2 种制剂给猪肌肉注射50 mg/kg·bw 后的药代动力学参数(n=5)
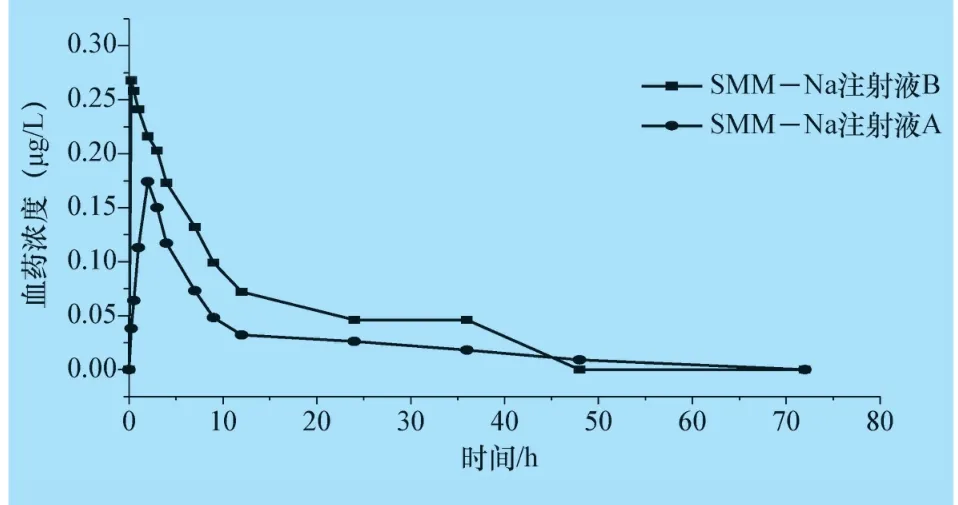
图3 肌肉注射后血药浓度-时间曲线
3 讨论
3.1 SMM 药代动力学 SMM 的抗菌作用相比其他相同类型的药物强,SMM 吸收后分布于全身组织以及体液,在肾、肝、尿液中含量最高,且在尿和血中的乙酰化率都比较低,但不同剂型、不同给药方式、不同剂量以及不同种属,甚至同种剂型不同制剂辅料和技术,其抗菌作用、药代动力学特征也存在差异。如在人体口服用药1 g,其半衰期为36 -48 h,在4 h 血药浓度才达到最高[2],属于一种长效类药物。而对于动物,大量文献资料显示,家禽类对SMM 吸收率最高,肉杂食动物要比草食动物吸收率高,单胃动物吸收率高于复胃动物吸收率且犬>猪>马>羊>牛。给兔以SMM 50 mg/kg·bw 单剂量快速静脉注射其半衰期为2.08 h[3];口服200 mg/kg·bw SMM 后血浆半衰期为2.87 h[4]。奶山羊的半衰期为1.45 h[5];水牛24 h,绵羊2 h,山羊7 h,猪5.8 h[1]。以化脓链球菌、金黄色葡萄球菌、肺膜炎双球菌、大肠杆菌为例,SMM 血中有效浓度分别为0.5μg/mL、8μg/mL、0.25 μg/mL、8 μg/mL。以SMM 50 mg/kg·bw 肌肉注射剂量制剂A 有效血液浓度可维持时间48 h 以上,制剂B 有效血液浓度可维持时间36 h 以上,在兽医临床上给猪一般采用肌肉注射的方式进行给药,其平均半衰期为16.9 h,远大于静脉注射给药。由此可见,在大部分家畜体内的半衰期都比较短,为短效类。本试验结果表明,制剂A 的消除半衰期为(20.75 ±1.29)h,制剂B 的消除半衰期为(6.73 ±1)h,有效血液浓度持续时间长,能够起到更好的治疗效果且制剂A 肌肉注射给药具有延缓吸收的作用,可达到缓释的效果;而制剂B 作用效果快,但有效血液浓度维持短,在临床治疗上需要多次注射才能达到治疗要求,增加了复杂性。
3.2 关于血样未测到检测限的问题 检测限为0.025 μg/mL,在48 h、36 h 分别所测的血样浓度要远高于检测限,而在72 h 和48 h 却未检测到血药浓度,可能是在24 h 和12 h 之内已被代谢完全,在第72 h 和48 h 无法检测到血药浓度,这与相关文献报道[6]的结果有一致性。另外检测限表示的是方法和仪器灵敏度的一个指标,表示在这个范围之内的可靠程度,并非所测样品要在这个值上测定。从药时曲线可以看出,制剂A、制剂B 分别在48 h 和36 h之后的时间血药浓度是缓缓降低,并非在这时间点就终止,再往后测定就没有实际意义。
3.3 2 种制剂药代动力学参数结果的讨论 根据结果表2,应用3P97 药代动力学计算软件进行计算,拟合血药浓度-时间的曲线,经F 检验表明,制剂A、B 在猪体内的药代动力学参数都符合二室模型,这与其他研究者在猪[7]、兔[8]、虾[9]体内的药代动力学模型是一致的,均为二室模型,而其他动物,像肌肉注射水牛[10]、肌肉注射黑山羊[11]、静脉注射猪[12]以及奶山羊[5]体内的药代动力学模型为一室模型,由此可见,SMM-Na 注射液在不同种属动物以及使用不同的给药方式会产生不同差异的[13-14]。
根据结果表3,比较制剂A、B 药代动力学参数发现,两者之间的AUC、消除半衰期差别比较大,原因可能是两者制剂的溶媒不一样,对主药的包合程度不一样,制剂A 以聚乙烯比咯烷酮30 和2-吡咯烷酮作为溶媒,可以与磺胺药结合成大分子复合物,从而在体内会起到一种缓慢释放的效果[15]。而制剂B 使用的比例较小的同种溶媒,两者之间在注入动物体内吸收程度不一样,制剂B 吸收程度要比制剂A 吸收程度大。结果表明,2 种注射液的AUC以及消除半衰期具有极显著差异(P<0.01)。消除半衰期与给药方式、剂型、剂量、种属以及同种制剂中不同工艺也有所差异。
由参数可知,A 制剂明显比B 制剂更长效,作用时间更持久,更能到达治疗的效果。制剂A 按50 mg/kg·bw 的给药剂量在猪体内的有效血液浓度可以维持48 h 以上,由此建议,在临床治疗上按50 mg/kg·bw 的给药剂量给猪肌肉注射可2 d 注射1 次即可。

