NGR与isoDGR对抗菌肽在乳腺癌中抗瘤活性影响
侯 磊,赵永丽,安改丽,何 莉,陈 鑫
(1 陕西省人民医院肿瘤内科,西安 710068;2 陕西省康复医院手术室;3 陕西省人民医院肿瘤放疗科;*通讯作者,E-mail:s.ob@qq.com)
多肽具有分子量小、免疫原性低、易于修饰及不易耐药等特点,因此,被越来越多地应用于肿瘤诊断与治疗中,其中大部分多肽衍生于某些特异性抗体片段或配体分子,主要作为靶向载体携带抗肿瘤药物定位于肿瘤组织发挥作用。如经典的RGD模序,能够特异性识别在肿瘤血管内皮细胞与肿瘤细胞表面高表达的整合素αvβ3,将抗肿瘤药物或显影剂特异性转运至肿瘤组织发挥靶向性抗肿瘤作用或肿瘤特异性成像[1-4]。近年来还有一种被称为NGR(Asn-Gly-Arg,NGR)模序的小分子多肽被发现[5-7],它能够特异识别在肿瘤新生血管表达的氨基肽酶N(CD13),并能在脱酰胺作用后生成isoDGR,一种相较于RGD模序对αvβ3具有更高亲和力的小分子多肽[8,9]。此外,研究还表明,环状结构可以增加小分子多肽对靶点的亲和力,提高载体肿瘤靶向转运的效率。目前除了具有载体作用的多肽外,还有另一类小分子多肽,并不具备靶向载体功能,而是拥有杀伤肿瘤细胞的能力,通常通过自身二级结构和靶细胞膜的理化性质来杀死目标细胞。如抗菌肽(AMP),能够通过破坏带负电的肿瘤细胞膜诱导细胞凋亡与坏死。
1 材料与方法
1.1 细胞与主要试剂
1.2 细胞培养
采用L-15不完全培养液(含10%血清)在5%CO2、饱和湿度、37 ℃培养箱内培养MDA-MB-231细胞。每2-3 d传代1次,待细胞处于对数生长期后行后续实验。
1.3 细胞存活试验
取对数生长期细胞,接种于96孔板,待细胞生长至对数增长期时,分别换用含不同浓度CDAK(20,40,100,200,400 μg/ml)、CNAK(20,40,100,200,400 μg/ml)及CRLK(200 μg/ml)无血清培养液100 μl,孵育20 h,设4个复孔,各孔中加入5 mg/ml MTT 20 μl,继续培养4 h,弃掉培养液,加入100 μl DMSO,37 ℃振荡15 min,酶标仪检测各孔A490值,取均值。使用软件Graphpad Prism 5.0计算细胞半抑制浓度(IC50)。
1.4 荧光显微镜观察多肽识别
取对数生长期细胞,加入不同多肽(CDAK,CNAK,CRLK;10 mg/ml;氨基酸C端K残基用于连接标记荧光罗丹明B)孵育12 h,PBS缓冲液冲洗3次,于荧光显微镜下观察,550 nm激发波长,620 nm发射波长,曝光400 ms。细胞核染色采用DAPI染色,用PBS稀释,最终浓度100 ng/ml。加入150 μl至每个细胞培养皿中,孵育15 min,荧光显微镜下观察。
1.5 流式细胞仪检测多肽结合
将细胞接种于6孔板中,培养24 h用CDAK,CNAK和CRLK处理细胞(10 mg/ml;氨基酸C端K残基用于连接标记荧光罗丹明B)12 h。孵育结束,通过胰蛋白酶消化细胞,PBS缓冲液洗涤3次,流式细胞仪分析荧光强度。
1.6 流式细胞仪检测凋亡
用CDAK、CNAK和CRLK处理细胞(200 mg/ml)24 h,胰酶消化细胞,加入400 μl 1×Binding Buffer和5 μl AnnexinⅤ-FITC室温避光15 min,10 μl PI冰浴避光5 min,流式细胞仪检测凋亡率。
1.7 Western-blot检测Caspase-3蛋白表达
细胞处理同凋亡检测,蛋白裂解液提取蛋白,BCA法测定蛋白浓度。相同剂量蛋白样品使用SDS-PAGE凝胶分离,目的条带用PVDF膜转膜,含5%脱脂牛奶的TBST封闭2 h,加一抗4 ℃孵育过夜,TBST洗膜15 min 3次,加入相应二抗,室温孵育1 h,TBST洗膜15 min 3次,ECL发光法检测蛋白表达状况。使用Image-ProPlus软件分析灰度值。以Caspase-3条带与内参β-actin灰度值比值代表Caspase-3蛋白相对表达量。
1.8 统计学分析
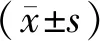
2 结果
2.1 多肽对细胞生长抑制
使用MTT检测CDAK、CNAK对MDA-MB-231细胞毒性,并计算IC50值。CDAK、CNAK对MDA-MB-231细胞存在生长抑制作用,且呈现剂量依赖性(见图1)。24 h的IC50分别为227 μg/ml(CDAK)、210 μg/ml(CNAK)。结果表明,两种多肽均能抑制MDA-MB-231细胞生长,相对CDAK,CNAK细胞毒性更大,但其差异无统计学意义(P>0.05)。

图1 不同浓度CDAK与CNAK作用24 h对MDA-MB-231细胞生长抑制Figure 1 Effect of CDAK and CNAK on the proliferation of MDA-MB-231 cells after treatment for 24 h
2.2 多肽对细胞识别与结合能力
为了观察多肽靶向识别能力与在细胞内分布情况,我们合成了一部分携带罗丹明B的多肽。首先通过荧光显微镜观察,结果显示,CDAK与CNAK均能进入MDA-MB-231细胞内,但HFF细胞内没有观察到荧光(见图2A)。接着通过DAPI核染色观察多肽在细胞内分布,发现多肽能够进入细胞核内,在胞浆及核内均有分布(见图2B)。最后我们在MDA-MB-231细胞上使用流式细胞仪检测两种多肽细胞结合能力。CRLK、CDAK、CNAK荧光强度分别为4.3 ±0.61 ,22 ±2.16,28 ±2.98,CDAK与CNAK荧光强度较CRLK明显增多(P<0.05),CNAK较CDAK荧光强度明显增多(P<0.05)。结果表明CNAK相较于CDAK对MDA-MB-231细胞具有更高结合能力(见图2C),其差异具有统计学意义(P<0.05)。
2.3 多肽对细胞凋亡影响
流式细胞仪检测结果显示,CDAK、CNAK、CRLK作用细胞24 h,MDA-MB-231凋亡率分别为(23.56 ±2.16)%,(25.33 ±2.77)%,(4.3 ±0.5)%(见图3)。结果表明,相对于空白对照,CDAK与CNAK均能诱导MDA-MB-231细胞凋亡(P<0.05),而CRLK对细胞凋亡并无显著影响(P>0.05)。CNAK相较于CDAK,诱导细胞凋亡能力增加,但差异无统计学意义(P>0.05)。提示CNAK与CDAK诱导MDA-MB-231细胞凋亡能力无明显差异。
2.4 Western-blot检测多肽对MDA-MB-231细胞Caspase-3蛋白影响
空白对照、CRLK、CDAK、CNAK中Caspase-3相对蛋白表达量分别为0.96 ±0.09,0.87 ±0.09,1.6 ±0.14,1.87 ±0.21(见图4)。相较于空白对照组与CRLK组,CNAK和CDAK组Caspase-3蛋白相对表达量增加,差异具有统计学意义(P<0.05)。但CNAK组与CDAK组相比,差异无统计学意义(P>0.05)。CRLK组与空白对照组相比,差异无统计学意义(P>0.05)。表明CDAK与CNAK均能诱导Caspase-3蛋白表达,但诱导Caspase-3蛋白表达能力无显著差异。

图2 CDAK与CNAK对MDA-MB-231细胞识别与结合能力Figure 2 Affinity of CDAK and CNAK against MDA-MB-231 cells

与空白对照组比较,* P<0.05;与CRLK组比较,#P<0.05图3 CDAK与CNAK作用24 h对MDA-MB-231细胞凋亡影响Figure 3 Effect of CDAK and CNAK on the apoptosis of MDA-MB-231 cells for 24 h

与空白对照组比较,* P<0.05;与CRLK组比较,#P<0.05图4 Western blot检测CDAK与CNAK作用24 h对MDA-MB-231细胞中Caspase-3表达影响Figure 4 Effect of CDAK and CNAK on the expression of Caspase-3 in MDA-MB-231 cells for 24 h by Western blot
3 讨论



