甘蔗最终糖蜜制备原色食用糖浆及抗氧化性分析
李美玲,王卓琳,黎庆涛,李明星,戴宇超
(广西大学 轻工与食品工程学院,南宁 530004)
甘蔗最终糖蜜,亦称废蜜、桔水,是甘蔗制糖工业的三大副产物之一,除含有大量的蔗糖(30%~40%)和还原糖(15%~20%)外,还含有许多活性成分,如:酚类、游离氨基酸、蛋白质、维生素和矿物质[1-5]。现代研究表明其具有抗氧化、防衰老和美容养颜等功能[6,7]。最终糖蜜中含有大量的胶体和盐分等杂质,工业上通常作为原料发酵生产酒精,不仅产品结构单一,市场适应力差,还造成了营养活性成分的浪费。因此,采用有效的清净工艺去除糖蜜中的杂质,并开发出高值化产品是糖厂目前急需解决的问题。
膜分离有分离效率高、无化学添加、无相变等特点[8],在甘蔗制糖工业中的应用研究已经有很多[9,10],但是膜法处理最终糖蜜的报道还很少[11,12]。离子交换作为一种脱色除灰技术,已在许多行业得到广泛应用。国内外有关膜法和离子交换联用在食品、医药、化工等行业的报道有很多[13-15],显示了很好的应用价值。本研究采用膜分离和离子交换联用处理最终糖蜜制备原色食用糖浆,从而实现对糖分和功能性成分的有效利用,并进一步分析了产品的抗氧化性,以期为甘蔗最终糖蜜的高附加值利用提供一定的参考。
1 材料与方法
1.1 材料与仪器
1.1.1 材料
原料:甘蔗最终糖蜜,取自广西某糖厂,锤度为85 °Bx,蔗糖含量为34.25%,还原糖含量为18.15%,pH为4.9。树脂:通用型大孔强碱阴离子树脂(简记为GBA)、通用型凝胶强酸阳离子树脂(简记为GAC)、HZ016、D201、D202,上海华震科技有限公司;试剂: Folin酚试剂,合肥博美生物科技有限责任公司;没食子酸标准品(纯度≥98%),上海金穗生物科技有限公司;1,1-二苯代苦基苯肼(DPPH),Sigma公司;其他试剂,均为分析纯。
1.1.2 仪器与设备
SHB-ⅢT循环水式多用真空泵 郑州长城科工贸有限公司;Labscale System小型切向流超滤系统、Pelicon XL超滤膜包(5,8,10 kDa) 密理博(中国)有限公司;WYA-2S数字阿贝折光仪 上海申光仪器仪表有限公司;普通玻璃层析柱(1.6 cm×40 cm) 上海楚定分析仪器有限公司;RE-52AA旋转蒸发器 上海亚荣生化仪器厂;UV-1100型紫外可见分光光度计 上海美谱达仪器有限公司;酸度计、电导率仪 梅特勒-托利多仪器(上海)有限公司;哈纳HI98713浊度计 上海数信仪器仪表有限公司;WZZ-2S自动旋光仪 上海仪电物理光学仪器有限公司。
1.2 实验方法
1.2.1 原色食用糖浆的制备工艺流程
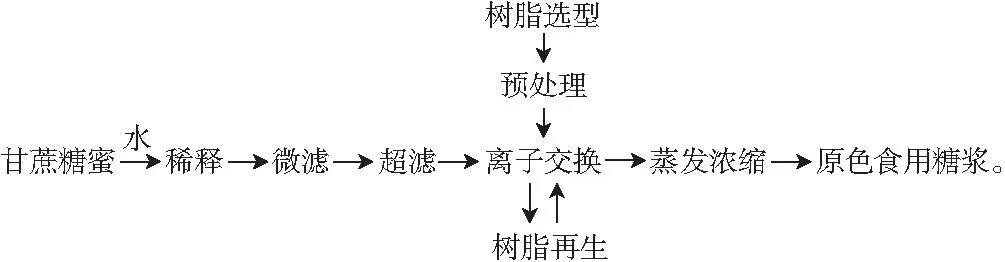
1.2.2 微滤
取一定质量的甘蔗最终糖蜜,分别按糖蜜与水质量比(1∶3、1∶4、1∶5、1∶6、1∶7、1∶8)稀释后,在0.055 MPa的跨膜压力下采用0.45 μm的滤膜进行微滤,收集滤液,并测定浊度。按公式(1)计算除浊率。

(1)
式中:Tp和Tf分别是透过液的浊度和进料液的浊度。
1.2.3 超滤
取一定体积的微滤透过液,在0.16 MPa的跨膜压力下,分别采用5,8,10 kDa的超滤膜包进行超滤,并测定膜通量、脱色率和除浊率,选择出超滤效果最佳的超滤膜包。然后采用该超滤膜包,在不同的跨膜压力(0.10~0.25 MPa)下超滤,并测定脱色率和除浊率,选择出最佳的跨膜压力。在最佳跨膜压力下,以膜通量为评价指标,选出最佳的操作时间。除浊率、膜通量和脱色率的计算分别按公式(1)、(2)和(3)进行。
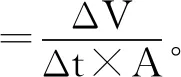
(2)
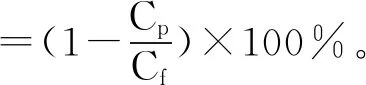
(3)
式中:ΔV为一定时间间隔内透过液的体积,Δt为时间,A为膜面积,Cp和Cf分别为透过液和进料液的色值。
1.2.4 离子交换
在阳离子与阴离子树脂的总体积为40 mL、流速为3 BV/h的前提下,选用5种串联树脂组对超滤透过液进行脱盐处理,分别固定树脂类型、树脂比例和处理量3个变量中的2个,进行单因素实验,以总酚损失率、脱盐率、总糖损失率、pH为评价指标,选择出最优的处理工艺。总酚含量的测定参照文献[16]中的方法,蔗糖和还原糖含量的测定分别参照《糖品分析实验技术》中的二次旋光法和兰艾农-恒容法进行[17],总酚损失率、脱盐率和总糖损失率分别按公式(4)、(5)和(6)进行。
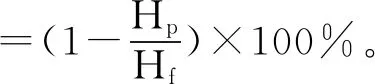
(4)
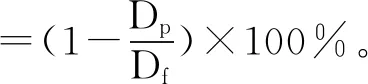
(5)
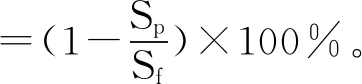
(6)
式中:Hp和Hf分别为透过液和进料液的总酚含量;Dp和Df分别为透过液和进料液的电导率,μs/cm。Sp和Sf分别为透过液和进料液的总糖分。
1.2.5 总酚含量及抗氧化能力的测定
1.2.5.1 原色食用糖浆的制备
取上述清净处理后的糖液100 mL,用旋转蒸发器在温度55 ℃、真空度0.055 MPa条件下浓缩至(70±0.5) °Bx,即为原色食用糖浆。准确称取1.3 g糖浆,溶解并定容至50 mL,即为样品溶液。
1.2.5.2 总酚含量的测定
参照文献[16]的方法,并稍作修改,取100 μL样品溶液于5 mL棕色容量瓶中,加入0.5 mL Folin酚,摇匀后静置10 min,再加入1.5 mL 7.5%的Na2CO3溶液,定容至刻度,于40 ℃下暗水浴60 min,在760 nm处测定吸光度值,以100 μL蒸馏水代替样品溶液作空白对照。总酚含量以mg GAE/g(每克样品中没食子酸的毫克数)表示[18]。
1.2.5.3 抗氧化性的测定
a.对DPPH·清除能力的测定[19]
取500 μL样品溶液于10 mL比色管中,加入4 mL 0.10 mmol/L的DPPH·的醇溶液,摇匀后定容至刻度,室温下避光反应30 min,在517 nm处测定吸光度值,以乙醇做空白对照。按式(7)计算DPPH·的清除率,清除能力以mg VCE/g(每克样品中维生素C的毫克数)表示[20]。
(7)
式中:Ax为加入样品溶液时DPPH·的吸光度值,A0为不加样品溶液时DPPH·的吸光度值。
b.对NO2-清除能力的测定[21]
取8 mL样品溶液于25 mL比色管中,加入5 μg/mL的NaNO2溶液2 mL,于37 ℃下恒温水浴10 min,取出后立即加入1 mL 0.4%的对氨基苯磺酸溶液,混匀后静置5 min,再加入0.5 mL 0.2%的盐酸萘乙二胺溶液,定容至刻度。室温避光反应15 min,在538 nm处测定吸光度值,以蒸馏水做空白对照。按式(8)计算NO2-的清除率,清除能力以mg VCE/g(每克样品中维生素C的毫克数)表示。
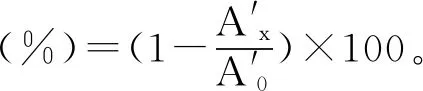
(8)
式中:A′x为加入样品溶液时NO2-的吸光度值,A′0是不加样品溶液时NO2-的吸光度值。
c.还原能力的测定[22]
取1.5 mL样品溶液于25 mL比色管中,加入2.5 mL 0.2 mol/L pH 6.6的磷酸缓冲溶液,再加入2.5 mL 1%的铁氰化钾溶液,摇匀后于50 ℃下保温20 min,加入2.5 mL 10%的三氯乙酸终止反应,定容至刻度,于3000 r/min离心10 min。静置后取上清液2.5 mL于比色管中,加入2.5 mL蒸馏水和0.5 mL 0.1%的FeCl3,混匀。在室温下反应30 min,于700 nm处测吸光度值。以5 mL蒸馏水和0.5 mL 0.1%的FeCl3混合液为空白对照。吸光度值越大,表明还原能力越强,还原能力以mg VCE/g(每克样品中维生素C的毫克数)表示。
2 结果与分析
2.1 稀释度对微滤效果的影响

图1 稀释度对微滤效果的影响Fig.1 Effect of dilution degree on the effect of microfiltration
由图1可知,随着糖蜜稀释度的增大,除浊率先增大后减小,当稀释度为1∶5时,除浊率达到最大值,即稀释度太低或者太高都不利于对样品中杂质的去除。这可能是溶液的渗透压、杂质的溶解度和滤饼厚度综合作用引起的。因此,选择适宜的稀释度为1∶5。
2.2 超滤对澄清效果的影响
2.2.1 超滤膜的选型
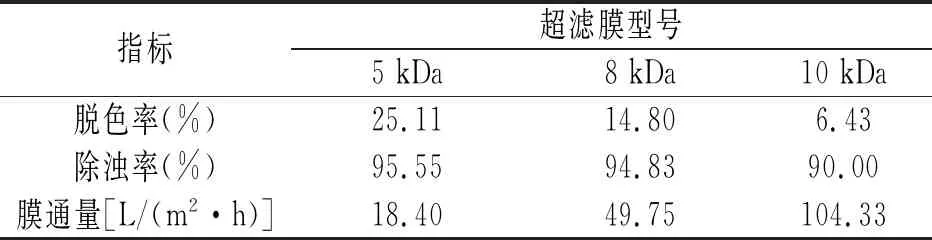
表1 不同类型超滤膜的澄清效果和膜通量Table 1 Clarification effect and flux of different types of ultrafiltration membranes
由表1可知,5 kDa 超滤膜的脱色率和除浊率优于其他2种,而10 kDa超滤膜的膜通量最大,表明截留分子量小的膜分离效果更佳。3种膜的除浊率都超过90%,而脱色率较低,表明超滤对去除大分子量杂质如悬浮物和胶体的效果明显,但对小分子量色素的去除效果有限,Gupta等人的研究也有类似的结果[23]。综合考虑,选择8 kDa超滤膜。
2.2.2 跨膜压力对超滤效果的影响

图2 跨膜压力对脱色率和除浊率的影响 Fig.2 Effect of transmembrane pressure on decolorization rate and turbidity removal rate
由图2可知,当跨膜压力在0.16 MPa之前,随着跨膜压力的增加,脱色率和除浊率没有显著变化,当跨膜压力大于0.16 MPa时,跨膜压力的进一步增加会导致脱色率和除浊率的迅速降低。

图3 跨膜压力对膜通量的影响Fig.3 Effect of transmembrane pressure on membrane flux
由图3可知,随着跨膜压力的增加,膜通量近似呈线性增加,高跨膜压力虽能使膜通量增加,但很快会产生浓差极化现象,造成膜快速污染[24]。综合考虑,应选择0.16 MPa的跨膜压力。
2.2.3 操作时间对膜通量的影响
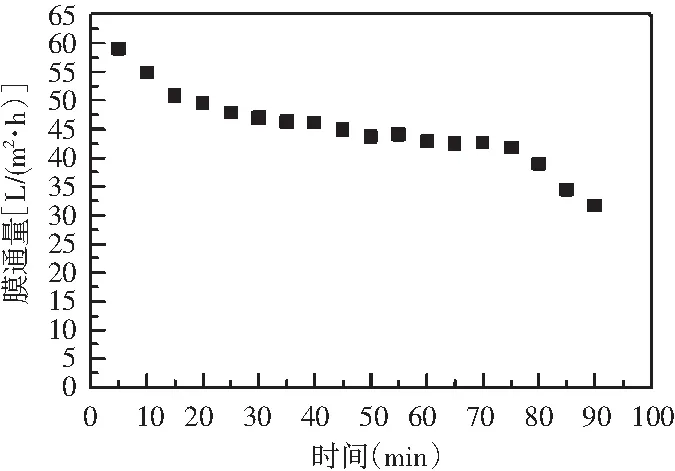
图4 操作时间对膜通量的影响Fig.4 Effect of operating time on membrane flux
由图4可知,随着时间的增长,在前15 min内,膜通量有较大幅度的下降,操作进行15 min后,膜通量的减小速率变缓,操作时间在60~75 min时,膜通量基本稳定,当操作进行到75 min后,膜通量又迅速下降。分析认为:超滤过程随着操作时间的增加,由于孔隙堵塞、吸附、浓差极化、凝胶层的形成等原因,膜通量随之下降[25],考虑到最经济的超滤效果,操作时间应选择75 min。
2.3 离子交换
2.3.1 树脂的选型
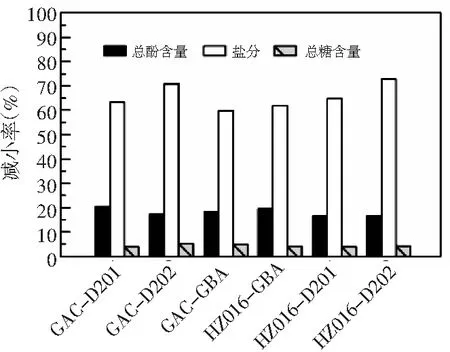
图5 不同树脂组对离子交换效果的影响Fig.5 Effect of different resin groups on the effect of ion exchange
注:处理体积为50 mL。
由图5可知,不同树脂组的脱盐率差异显著,其中GAC-D202和HZ016-D202树脂组表现最佳。所有树脂组对总糖和总酚含量影响的差异不显著,总糖损失率都不高(<5%),而总酚损失率为15%~20%,可能是因为糖类物质不带电荷,受离子交换的影响较小,而酚类物质中有一部分带有电荷,受离子交换的影响较大。考虑到HZ016树脂的成本较GAC树脂低,选择HZ016-D202树脂组。
2.3.2 树脂比例对离子交换效果的影响
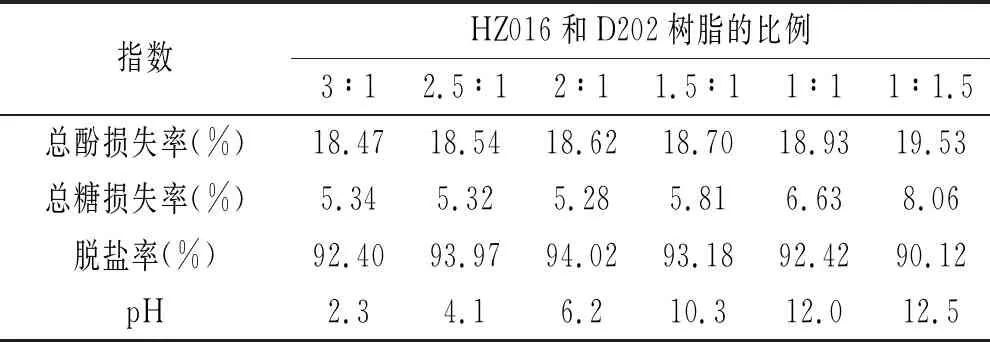
表2 HZ016和D202树脂比例对离子交换效果的影响Table 2 Effect of ratios of HZ016 and D202 resins on ion exchange effect
由表2可知,随着树脂比例(V阳∶V阴)的减小,总酚损失率和pH不断增大,这是D202大孔树脂的离子交换和物理吸附作用增强导致的。总糖损失率先保持稳定后逐渐增大,这可能是碱性条件下葡萄糖和果糖分解成的副产物增多造成的[26]。脱盐率先小幅度增大后减小,分析可能是溶液中氢离子和金属离子浓度变化相互作用的结果。考虑到一般液体糖的pH在5.0~6.5,因此,为了保证在高脱盐率的前提下,兼顾总糖分和总酚含量,HZ016和D202树脂的比例应为2∶1。
2.3.3 处理量对离子交换效果的影响
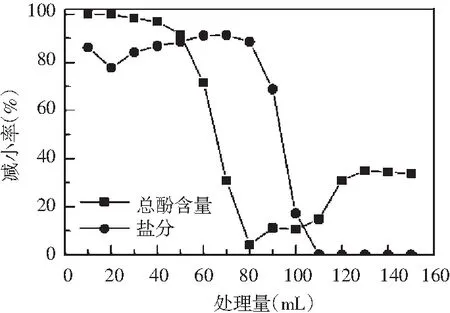
图6 处理量对离子交换效果的影响 Fig.6 Effect of treatment volume on ion exchange effect
由图6可知,随着处理量的增加,总酚损失率的变化经历了4个阶段:缓慢下降期(0~50 mL),快速下降期(50~80 mL),增长期(80~120 mL)和稳定期(120~150 mL)。脱盐率经历了3个阶段:稳定期(0~80 mL),快速下降期(80~110 mL)和稳定期(110~150 mL)。分析可能是HZ016和D202树脂的吸附容量与pH之间相互作用的结果,因此选择处理量为80 mL。
2.4 原色食用糖浆品质分析
2.4.1 理化指标

表3 原色食用糖浆理化指标Table 3 Physical and chemical indicators of primary-color edible syrup
由表3可知,经真空浓缩后的原色食用糖浆的锤度为(70±0.5) °Bx,达到了QB/T 4093─2010对液体糖锤度的要求。总糖分(占干物质)为(92.9±1.8)%,达到了GB/T 20882─2007中对F42果葡糖浆总糖分的要求。样品色值为(1200±13) IU,呈金黄色。电导率为(40±1.5) μs/cm,说明盐分去除得比较完全。
2.4.2 总酚含量和自由基清除能力

表4 原色食用糖浆的总酚含量和抗氧化能力Table 4 Total phenolic content and antioxidation activity of primary-color edible syrup
由表4可知,原色食用糖浆的总酚含量为(4.21±0.05) mg GAE/g,这个结果较Munawar等对糖蜜的研究结果(3.75 mg GAE/g)高[27],而对DPPH·、NO2-的清除能力、还原能力分别为(0.42±0.02),(0.58±0.04) mg VCE/g和(0.90±0.02) mg VCE/g,说明制备的原色食用糖浆保留了糖蜜中较多的抗氧化性成分。
3 结论
采用膜法和离子交换联用对甘蔗最终糖蜜进行清净处理。微滤优化实验确定了最佳稀释倍数为1∶5(m糖蜜∶m水),超滤实验表明8 kDa超滤膜的处理效果最好,在0.16 MPa的跨膜压力下操作75 min可以获得最佳超滤效果。进一步的离子交换实验表明选用HZ016-D202树脂组,树脂比例1∶1,处理量为80 mL时可以获得最佳的处理效果。
在最佳处理条件下得到的原色食用糖浆,经真空浓缩至(70±0.5) °Bx制得成品原色食用糖浆并进行理化指标分析,结果显示蔗糖分为(40.3±1.1)%,还原糖分为(25.4±0.7)%,且灰分基本去除(电导率≤41.5 μs/cm)。进一步的分析可知,原色食用糖浆含有的酚类物质达(4.21±0.05) mg GAE/g,对DPPH·、NO2-的清除能力和还原能力分别为(0.42±0.02),(0.58±0.04) mg VCE/g和(0.90±0.02) mg VCE/g。说明膜法和离子交换结合的工艺不仅可以有效地对甘蔗最终糖蜜进行清净处理,还能较好地保留其中的抗氧化性成分,这将为甘蔗最终糖蜜的高值化利用提供一定的借鉴。

