溶胶-凝胶法制备NiFe2O4载氧体及其化学链制氢反应性能
魏国强, 周 欢, 吴宪爽, 冯 杰, 李海滨
(1.太原理工大学 煤科学与技术教育部和山西省重点实验室,山西 太原 030024;2.中国科学院 广州能源研究所,广东 广州 510640)
氢气是一种高效、清洁能源和重要工业原料,当前主要来源于化石燃料重整、甲醇制氢及电解水制氢等途径[1]。化石燃料重整制氢技术已经较为成熟,是目前工业制氢的主要路线,但该路线能耗较高,且制得的氢气中含有CO2等杂质,需要进一步分离提纯。在此背景下,工艺简单且氢气产物纯度较高的化学链制氢(Chemical looping hydrogen,CLH)技术进入研究人员的视野[2]。
化学链制氢系统由3个反应器构成[3],分别为燃料反应器(FR)、制氢反应器(SR)与空气反应器(AR)。首先在FR中,载氧体与燃料反应,生成合成气或终端产物CO2与H2O,其自身被还原为金属单质或低价态金属氧化物;然后载氧体进入SR中,金属单质或低价态金属氧化物与水蒸气发生部分氧化,生成高纯H2;被部分氧化的载氧体进入AR再生,完成一个化学链制氢过程。化学链制氢产物H2纯度较高、无需额外催化剂、工艺简单,环境友好,具有较好的应用前景。
高活性载氧体是化学链制氢的关键。当前,国内外研究较多的载氧体主要集中在Ni、Cu、Fe、Mn等单一或复合金属氧化物[4-10]。其中,铁基复合载氧体因载氧能力强、机械强度高及热稳定性好、价格低廉、环境友好而受到研究者广泛关注[11-16],而基于Fe/Ni金属间协同作用构筑的尖晶石型NiFe2O4载氧体则具有晶格氧传递能力强、产物选择性高、机械稳定性好等优点[17-18]。日本东京工业大学Tamaura等[19]报道了MFe3+δO4型复合氧化物传递晶格氧(O2-)及分解H2O的反应机理,奠定了该载氧体应用于化学链转化过程的基础。美国科罗拉多大学Aston等[20]对比NiFe2O4与Fe2O3的化学链制氢反应性能发现,在相似条件下NiFe2O4产氢量是Fe2O3的4倍。作者所在课题组前期研究[21]也表明NiFe2O4载氧体可以实现化学链制氢,且在20次循环反应中性能稳定;另外发现,采用溶胶-凝胶法制备的载氧体具有更好的反应活性。
在此基础上,笔者采用溶胶-凝胶法制备了NiFe2O4载氧体,并用于化学链制氢过程,采用正交实验方法考察柠檬酸与总金属离子摩尔比(RCAMI)、溶液pH值、凝胶温度等制备条件对NiFe2O4载氧体化学链制氢反应性能的影响,优化制备条件,改善载氧体的比表面积、粒径、晶格氧释放等物化特性,进一步提高其化学链制氢性能。
1 实验部分
1.1 试剂
六水合硝酸镍 Ni(NO3)2·6H2O(质量分数98%),九水合硝酸铁 Fe(NO3)3·9H2O(质量分数98.5%),无水柠檬酸C6H8O7(质量分数99.5%),氨水 NH3·H2O(质量分数25%~28%),均为AR,购于麦克林公司。高纯氩气Ar(φ≥99.999%),生物质热解模型气,体积组成(根据文献[22]确定)为:15%H2+5%CO2+12.5%CH4+30%CO+37.5%N2,由广州盛盈公司提供。去离子水,采用四川优普超纯科技公司UPR-I-ST仪器制备。
1.2 正交实验设计
为简化溶胶-凝胶制备NiFe2O4载氧体工艺条件,采用正交实验设计法,考察制备过程中反应RCAMI(因素A)、溶液pH值(因素B)、凝胶温度(因素C)等3个因素对制备载氧体的物化特性和反应性能的影响。每个因素设3个水平,如表1所示。
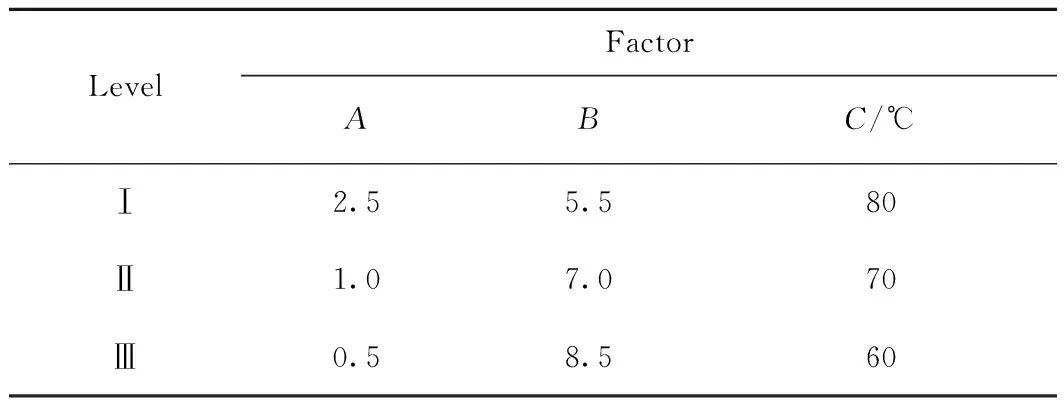
表1 正交实验考察因素及水平Table 1 Orthogonal experimental design
正交实验设计结果及多指标综合平衡分析方法如表2所示。其中,K1行的3个数字分别为因素A、B、C的第Ⅰ水平所在的实验中对应的实验结果之和。k1、k2、k3分别为各水平所对应的平均值。极差值为k1、k2、k3中最大值减去最小值。极差值越大,表示该因素水平改变时对实验结果影响越大,极差最大值所对应的因素就是影响反应的最主要因素。
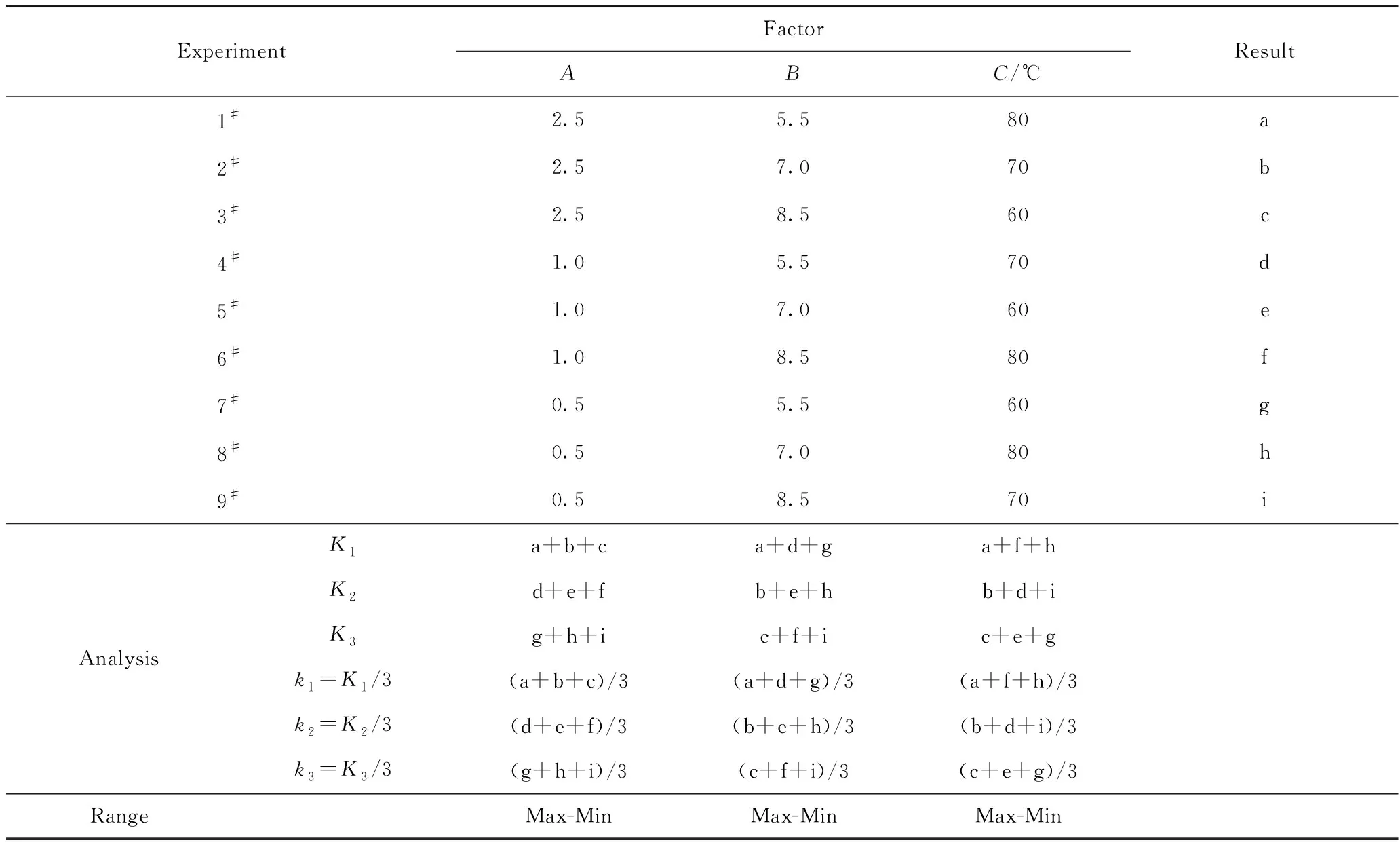
表2 正交实验设计结果与多指标综合平衡分析法Table 2 Multi-index comprehensive balance analysis and orthogonal experiment design result
1.3 载氧体制备
以Ni(NO3)2·6H2O、Fe(NO3)3·9H2O为原料,无水柠檬酸作为螯合剂,采用溶胶-凝胶法制备载氧体。首先,用去离子水分别溶解Ni(NO3)2·6H2O与Fe(NO3)3·9H2O配制成溶液,按表2中1#~9#实验条件分别取溶液各50 mL置于烧杯中,加入相应摩尔比的柠檬酸,溶解并混合均匀;加入氨水,调pH值至设计值;在设计凝胶温度下蒸去3/4的水,生成溶胶;溶胶在105 ℃下真空干燥12 h,形成凝胶;在马弗炉内以10 ℃/min升温至1000 ℃,煅烧2 h后获得NiFe2O4载氧体,依次命名为1#~9#载氧体。
1.4 载氧体表征
采用荷兰PANalytical X’Pert PRO MPD型X射线衍射仪分析载氧体晶型结构,Cu靶Kα射线,波长λ=0.15046 nm,电流40 mA,电压40 kV,扫描速率为0.0167°/s,2θ扫描范围为5°~90°。采用日立S-4800型冷场发射扫描电子显微镜表征载氧体微观形貌,工作加速电压2 kV,工作距离5 mm。通过美国康塔DI-MP-10/PoreMaster 33型全自动比表面积分析仪研究载氧体比表面积,样品在250 ℃下脱附12 h去除杂质,再转移至工作站进行N2吸附-脱附测试。采用德国Linseis PT1600同步热分析仪研究载氧体晶格氧释放特性,载氧体质量约40 mg,温度范围307~950 ℃,升温速率15 ℃/min,H2(体积组成5%H2+95%N2)流量5 mL/min,保护气N2流量100 mL/min。
1.5 固定床装置及实验流程
采用图1所示固定床反应器开展化学链制氢实验,反应器内径15 mm,总长800 mm。实验中载氧体质量为2 g,温度为850 ℃。实验开始前,将石英棉平铺于反应器筛板上,放入载氧体,开始升温,同时通入Ar。当温度达到设定值后稳定10 min,通入生物质热解模型气与载氧体反应,气体流量为100 mL/min,反应30 min。热解模型气反应完毕,通入Ar吹扫20 min,引入水蒸气开始制氢反应,Ar流量为120 mL/min,水蒸气流量为0.15 mL/min,制氢反应时间为35 min。
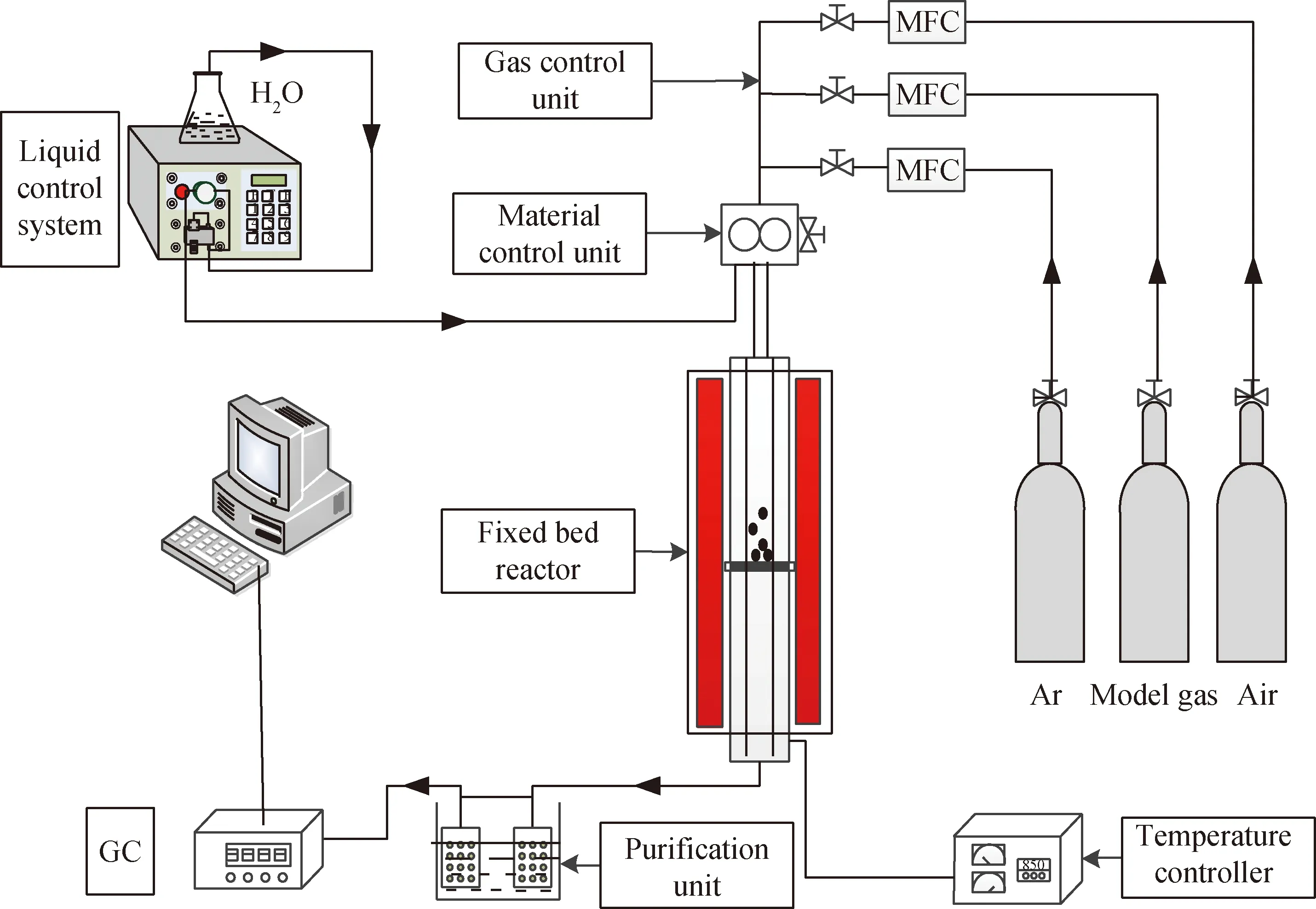
图1 固定床反应器化学链制氢实验装置示意图Fig.1 Scheme of the fixed-bed reactor for Chemical Looping Hydrogen (CLH)
1.6 数据评价和分析
在热解气与载氧体反应阶段,气体产物体积通过N2平衡计算,气体消耗率按公式(1)计算。
(1)
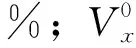
在制氢阶段,产物H2体积通过Ar平衡计算,因Ar流量为120 mL/min,制氢反应时间为35 min,因此计算式(2)为:
(2)
式中:QH2—每克载氧体生成H2的体积,mL/g;cH2、cCO、cCO2为制氢阶段实测的产物中H2、CO、CO2体积分数,%;mCO—载氧体质量,g。
制氢产物中扣除载气Ar后,H2体积分数(φH2,%)按公式(3)计算。
(3)
2 结果与讨论
2.1 制备条件对载氧体晶型构成的影响
不同条件制备载氧体样品的XRD表征如图2所示(样品编号为对应的实验编号)。从图2可以发现,基于溶胶-凝胶法制备的4#~9#载氧体在(111)、(220)、(311)、(222)、(400)、(422)、(511)、(440)、(533)、(620)和(622)晶面显示了尖晶石结构NiFe2O4的特征衍射峰,与标准NiFe2O4特征峰一致,表明该条件下可以制备单一晶型的NiFe2O4载氧体。而1#~3#载氧体样品中除了检测到NiFe2O4晶型之外,还出现Fe2O3衍射特征峰。

图2 制备载氧体的XRD分析Fig.2 XRD patterns of synthesized oxygen carriers
通过综合分析制备载氧体的晶型构成,发现柠檬酸与金属离子摩尔比(RCAMI)是影响载氧体晶型构成的主要因素。当RCAMI低于1时,可以生成NiFe2O4单一晶型的载氧体。这是由柠檬酸分子结构决定的,柠檬酸拥有3个羧基与1个羟基,理论上羧基与羟基均可与金属离子结合形成载氧体前驱体。当RCAMI为0.5时(9#),理论上1个柠檬酸分子平均与2个金属离子结合,在水解、缩合、缩聚形成凝胶的过程中,以金属离子为结合点,可以形成相对密集的颗粒空间网络;而RCAMI为1时(6#),理论上1个柠檬酸分子平均与1个金属离子结合,形成凝胶过程中,以金属离子为结合点横向生长,颗粒网络相对疏松;而RCAMI为2.5时(3#),金属离子相互间隔,不能通过金属离子构建有序的空间结构,导致反应中Fe、Ni元素无法全部有序组合生成NiFe2O4,而出现部分Fe2O3。
图3为不同RCAMI下制备载氧体的SEM扫描形貌。由图3可以看出,不同RCAMI下制备载氧体微观形貌呈不规则块状结构,颗粒粒径在0.1~0.8 μm,不同颗粒之间存在孔道结构。随着制备溶液中RCAMI从2.5(3#)降低到0.5(9#),载氧体颗粒粒径逐渐变小,颗粒空间排列也变得紧密有序,颗粒间孔道减少。这主要是因为不同RCAMI下柠檬酸分子与金属离子结合数量不同,形成前驱体空间结构也不同,经煅烧消除有机物框架后,生成NiFe2O4空间排列存在差异;RCAMI越小,柠檬酸分子与金属离子结合越多,后续生成载氧体的颗粒空间排列越紧密。

图3 溶胶-凝胶法制备载氧体SEM形貌图Fig.3 SEM images of oxygen carriers synthesized by sol-gel method3#—RCAMI=2.5; 6#—RCAMI=1; 9#—RCAMI=0.5
2.2 制备条件对载氧体比表面积的影响
不同条件下制备载氧体BET比表面积如表3所示。对表3结果进行极差分析可知,影响因素中A、B、C的极差分别为1.475、0.481、0.041,因素A的极差最大,其次为因素B,因素C的极差最小,表明RCAMI是对载氧体比表面积影响最大的因素,其次为溶液pH值,而凝胶温度对表面积的影响最小。RCAMI对载氧体比表面积的影响主要在于柠檬酸与金属离子配比不同造成成胶过程中载氧体结构上的差异。RCAMI越小,在溶胶阶段柠檬酸分子与金属离子结合越多,后期凝胶及煅烧过程中结构越致密,制得载氧体比表面积越小;而RCAMI越大,金属离子在成胶过程相互间隔,无法构建有序的空间结构,导致后期载氧体比表面积较大。
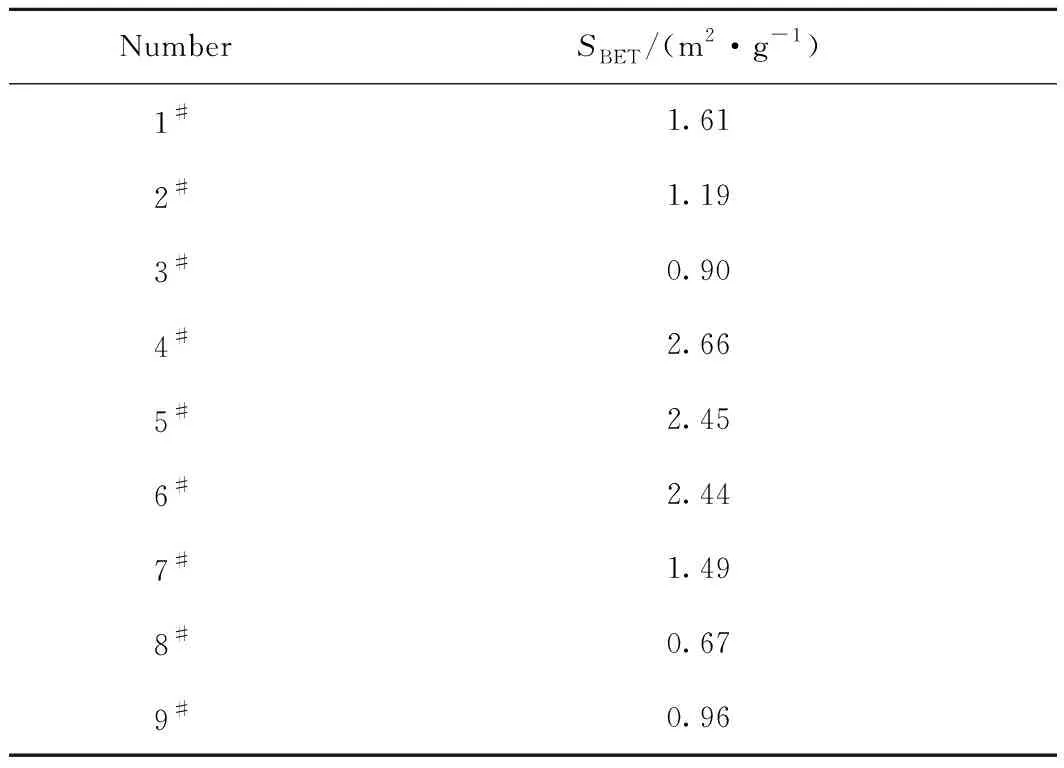
表3 载氧体BET比表面积Table 3 BET specific surface area of oxygen carriers
溶液pH值影响柠檬酸络合物水解缩聚速率,pH值较小时,缩聚反应速率大于水解反应,水解反应符合H+的亲电机理,缩聚物交联度低,生成载氧体比表面积相对较大;pH值较大时,水解反应由[OH-]的亲核取代引起,水解速率大于缩聚速率,易形成大分子聚合物,交联度较高,制备载氧体比表面积相对较小。因此,在RCAMI为1、pH值较低时可获得较大比表面积载氧体,如4#和5#载氧体制备溶液的pH值为5.5和7.0,其BET比表面积较大,分别为2.66和2.45 m2/g。
2.3 制备条件对载氧体晶格氧反应特性的影响
为了考察制备载氧体的晶格氧释放特性,在热重(TG)反应器上开展载氧体在H2气氛下的还原实验,结果如表4所示。由表4可以看出,载氧体样品在升温过程中释放晶格氧被氢气还原,其质量损失为26.34%~27.72%。3#载氧体样品质量损失最大,为27.72%,超过NiFe2O4载氧体理论质量损失(27.35%)。结合XRD分析可以看出,3#载氧体中除含有NiFe2O4晶型之外,还有少量Fe2O3,导致3#样品表现出最大的晶格氧质量损失。1#、6#、8#载氧体显示了较小的质量损失,其中8#的质量损失最小,为26.34%。针对单一晶型NiFe2O4载氧体,60 ℃凝胶温度制备的5#、7#载氧体显示了较大的质量损失和较低的最大质量损失峰温度。其中,5#载氧体对应最低质量损失峰温度为574 ℃,显示了更好的晶格氧反应活性。

表4 载氧体H2热重实验结果Table 4 H2 TG results of oxygen carriers
基于多指标综合平衡法分析,发现因素A、B、C对载氧体最大质量损失影响的极差分别为0.56、0.17、0.87,而对最大质量损失峰温度影响极差分别为52、2、4。很明显RCAMI是影响载氧体晶格氧释放,即反应活性的主要因素。其次为凝胶温度,提高凝胶温度可提高载氧体前驱体离子成核速率。原因在于温度升高,溶液离子动能增加,碰撞几率也增大,聚合速率提高,从而导致溶胶时间缩短;另一方面,温度升高溶剂挥发加快,反应物浓度相应提高,也加快了凝胶速率。但是,温度升高会导致生成的溶胶稳定性下降,影响后续制备载氧体的晶型及比表面积,从而影响载氧体晶格氧释放比例,因此较低凝胶温度更有利于载氧体晶格氧释放。
2.4 载氧体化学链制氢反应性能分析
2.4.1 载氧体与生物质热解气还原反应性能
在分析载氧体物化特性基础上,进一步考察所制备载氧体化学链制氢反应性能。采用生物质热解模型气还原1#~9#载氧体。由于1#~3#载氧体晶型构成为NiFe2O4和Fe2O3,而6#~9#载氧体则为单一晶型NiFe2O4载氧体(图2),因而其与热解气的反应较为复杂,主要涉及载氧体还原反应(式(4)~(6))、CH4裂解反应(式(7))、CH4干重整反应(式(8))、CH4蒸汽重整反应(式(9))、水汽变换反应(式(10))和歧化反应(式(11))等诸多反应。反应过程中,载氧体的NiFe2O4/Fe2O3被还原为Fe/Ni单质或低价态复合氧化物,而热解气组成也发生改变。
NiFe2O4+4H2=2Fe+Ni+4H2O
(4)
NiFe2O4+CH4=2Fe+Ni+2H2O+CO2
(5)
NiFe2O4+4CO=2Fe+Ni+4CO2
(6)
CH4=C+2H2
(7)
CH4+CO2=2CO+2H2
(8)
CH4+H2O=CO+3H2
(9)
CO+H2O=CO2+H2
(10)
CO2+C=2CO
(11)
H2O+C=CO+H2
(12)
该阶段反应过程中,反应器输入H2、CO2、CH4、CO的体积分别为450、150、375、900 mL,反应器出口输出气体体积及其消耗率如表5所示。对表5进行极差分析可知:在3个因素中,RCAMI对H2、CH4、CO的消耗结果极差值最大,分别为19.1、19.3、35.9,表明RCAMI是影响载氧体与H2、CH4和CO反应的主要因素。当RCAMI为1时,H2与CO消耗率最大,分别为57.8%和54.7%,而CH4的消耗率最小,为15.1%。这是因为RCAMI为1时载氧体为尖晶石结构NiFe2O4晶型,具有较高的晶格氧释放反应活性,可以提供晶格氧促进CO、H2转化,且还原后的Ni和Fe单质可以为CH4催化裂解及重整提供活性位点,促进反应进行。相比之下,由极差分析可知,溶液pH值和凝胶温度对载氧体热解气还原反应影响较小。其中,随着溶液pH值升高,产物中H2与CO的消耗率也随之升高,而CH4的消耗率则随之减小,表明较低pH值下制备的载氧体有利于促进CH4的裂解。
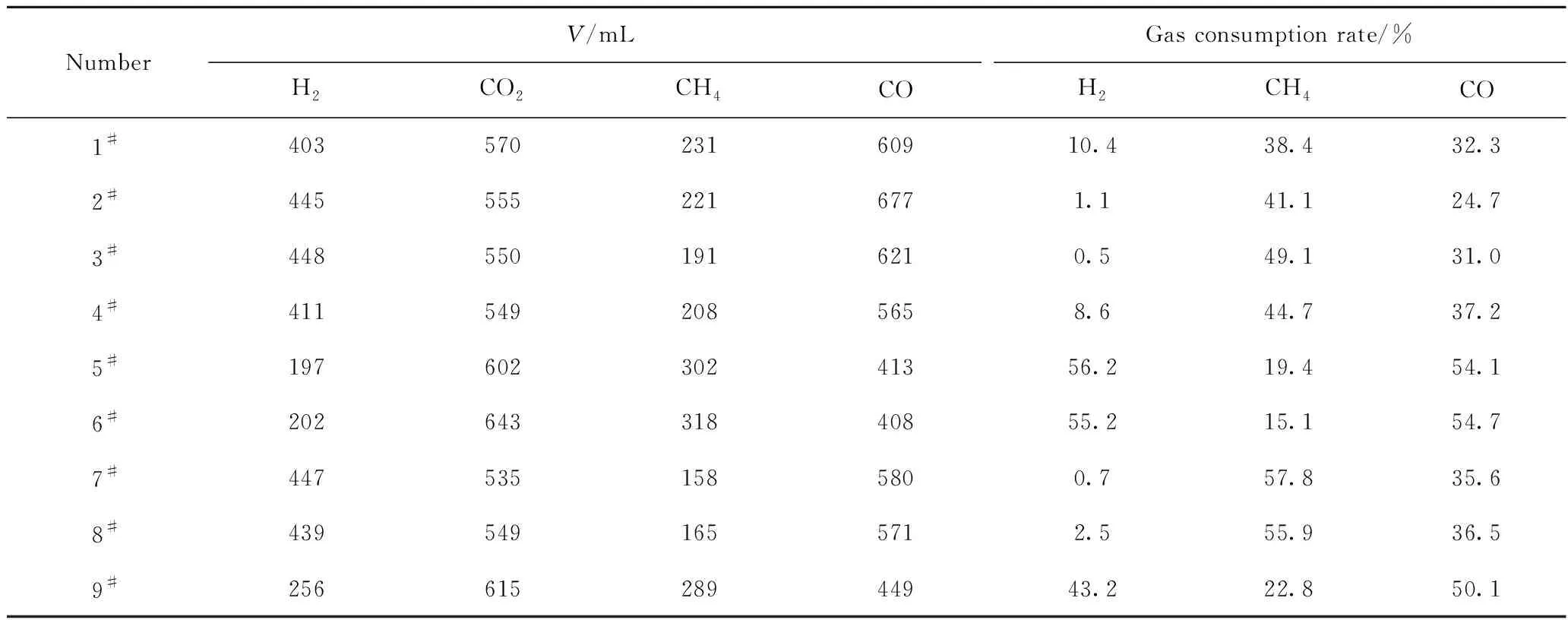
表5 热解气与载氧体反应阶段的输出气体消耗率Table 5 Gas consumption rate in reaction process of biomass pyrolysis gas and oxygen carriers
2.4.2 载氧体在制氢阶段的反应性能
载氧体与热解气还原反应完毕,采用Ar吹扫之后通入水蒸气进入化学链制氢阶段。其涉及的主要反应如下:
3Fe+Ni+4H2O=Ni+Fe3O4+4H2
(13)
在制氢反应过程中,H2O在载氧体表面与Fe发生反应生成H2与Fe3O4。受热力学限制,H2O无法完全氧化Fe生成Fe2O3,也无法直接与Ni发生反应。要完全恢复载氧体的元素价态及晶型构成,需要通过进一步空气氧化来实现。化学链制氢阶段,通过不同载氧体制备得到的氢气体积产量及组成如表6所示。由表6可以看出,不同载氧体在化学链制氢阶段获得纯H2产量为263.7~283.5 mL/g,5#和7#载氧体获得纯H2产量较高。

表6 不同载氧体化学链制氢(CLH)实验结果Table 6 Experimental results of oxygen carriers in CLH
根据综合平衡分析,A、B、C因素对载氧体制H2产量影响的极差分别为20.3、14.9、7.1,而对氢纯度影响的极差则分别为3.4、2.2、1.2。很明显,RCAMI是影响载氧体制氢反应的主要因素。这是由于合适的RCAMI使制备得到的载氧体形成单一NiFe2O4晶型,Fe/Ni金属间协同作用使载氧体晶格氧传递能力大大增强;同时载氧体具有更大的比表面积,有利于水蒸气向载氧体的扩散,促进反应转化,从而使其氢产量比含有Fe2O3、比表面积小的载氧体大幅提高[20]。不同载氧体在反应中获得氢气纯度(体积分数)在93.4%~100%,1#、5#和6#载氧体制氢气纯度接近100%。这主要因为在热解气反应阶段,甲烷裂解生成的积炭沉积在载氧体表面;在制氢阶段,其与H2O反应生成杂质气体(CO和CO2),影响H2纯度。从极差分析来看,溶液pH值对氢纯度影响仅次于RCAMI,其主要通过强化或抑制热解气反应过程中CH4裂解积炭的生成来影响产H2纯度。
2.5 正交实验分析汇总
基于上述正交实验分析,载氧体制备因素对载氧体物化特性和化学链制氢性能的影响程度及相应的优化结果如表7所示。由表7可以看出,3个因素对载氧体物化特性及其制氢反应性能影响由大到小的次序为RCAMI、溶液pH值、凝胶温度。其中,RCAMI对制备载氧体比表面积、H2还原最大质量损失温度、产H2量、产H2纯度影响最大,原因在于不同RCAMI时制备得到的载氧体的晶型、比表面积、结构不同,进而影响其还原反应性能和制氢性能;溶液pH值对载氧体比表面积、产H2量、产H2纯度的影响其次,但对载氧体的最大质量损失和最大质量损失温度影响较小;凝胶温度对载氧体的最大质量损失影响最显著,对最大质量损失温度的影响其次,而对比表面积、产H2量、产H2纯度的影响很小。
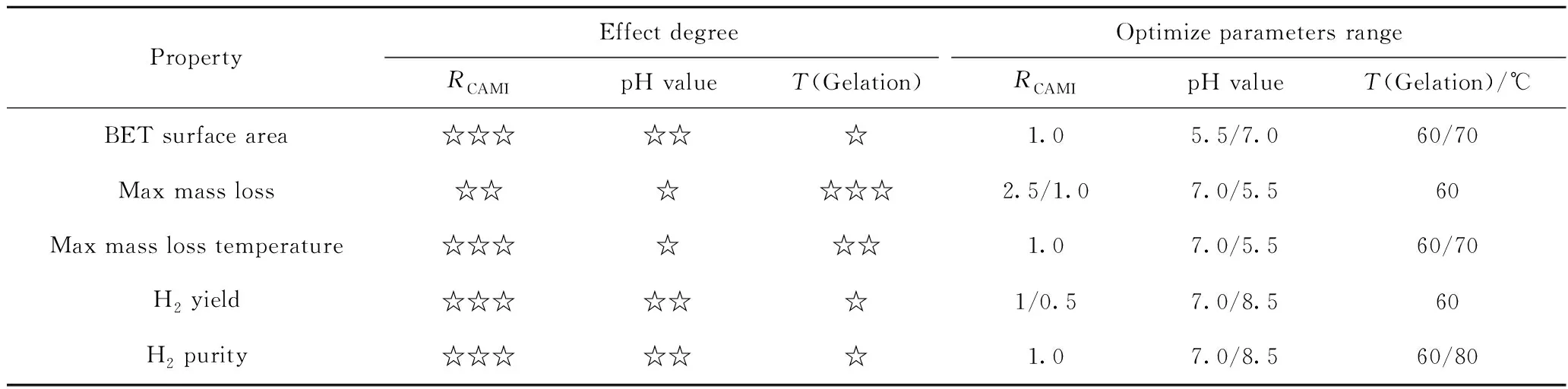
表7 正交分析汇总Table 7 The orthogonal analysis results
在RCAMI为1、pH值在5.5~7、凝胶温度在60~70 ℃时,获得的载氧体具有较大质量损失(27.32%和27.34%)和较低最大质量损失峰温度(574 ℃);而在RCAMI为0.5~1、pH值为7~8.5、凝胶温度为60 ℃时,可获得较高纯H2产量和产H2纯度。综合考虑载氧体比表面积、质量损失峰温度、H2产量及纯度,适用于化学链制氢过程的载氧体制备条件为RCAMI为1、pH值为7、凝胶温度为60 ℃。该条件下制备载氧体显示了较好的晶格氧反应活性,且在化学链制氢阶段可获得纯H2产量283.5 mL/g,产H2纯度接近100%。
3 结 论
溶胶-凝胶法制备NiFe2O4载氧体过程中,对载氧体物化特性及其制氢反应性能影响由大到小的次序为柠檬酸与金属离子摩尔比(RCAMI)、溶液pH值、凝胶温度。其中,RCAMI是最主要的影响因素,调控载氧体的晶型构成、晶格氧传递及产氢量关键在于控制柠檬酸与金属离子摩尔比;溶液pH值影响柠檬酸络合物水解缩聚速率,并通过强化或抑制热解气还原过程中CH4裂解积炭来影响产H2纯度;凝胶温度对载氧体前驱体离子成核速率具有积极作用,但温度升高会导致生成的溶胶相对不稳定,影响后续制备载氧体晶型构成及比表面积,较低凝胶温度有利于载氧体晶格氧释放。
适用于化学链制氢过程的NiFe2O4载氧体制备优化条件为RCAMI为1、pH值为7.0、凝胶温度60 ℃。

