应用多模影像技术分析多发性一过性白点综合征
雍红芳 韩宁 吴瑛洁 吴倩倩 左玲
(吉林大学第二医院眼科 长春 130041)
多发性一过性白点综合征(multiple evanescent white dot syndrome,MEWDS)在1984年由Jampol等[1]首先报道。近30年来,对于其临床表现及影像学检查已有许多文献报道,但其发病机制尚未明确。随着多模影像技术在眼科中的应用,人们对许多眼底病的认识逐渐深入。本文应用多模影像技术深入分析MEWDS临床特点,并据此进一步探讨其发病机制。现将结果报道如下。
1 资料与方法
回顾性系列病例研究。2018年1月~2019年1月在我科确诊为MEWDS的7例患者(7眼)纳入本研究。其中男性2例(2眼)、女性5例(5眼)。年龄为20~49岁,平均33.8岁。7例患者均为首诊,以闪光感、眼前点状黑影及视力下降为主诉,出现症状至就诊时间2~15 d,出现症状至就诊的平均时间为8.3 d。所有患者既往体健,无眼部疾病史,均否认感冒及发热史。
所有患者均行最佳矫正视力(best corrected visual acuity, BCVA)、裂隙灯显微镜、间接检眼镜、眼压、眼底彩色照相以及眼底自发荧光(fundus autofluorescence,FAF)、吲哚菁绿血管造影(indocyanine green angiography,ICGA)、频域光学相干层析成像(spectral domain optical coherence, SD-OCT)、OCT血管成像(OCT angiography, OCTA)、多焦视网膜电图(multifocal electroretinogram, mf-ERG)检查。采用Snellen视力表行BCVA检查;采用日本Kowa Nonmyd免扩瞳眼底照相机行眼底彩色照相;采用德国Heidelberg公司共焦激光扫描眼底血管造影仪同步行FAF、FFA、 ICGA检查;采用德国Heidelberg公司Spectralis OCT仪行双眼黄斑区放射状和线性扫描;OCTA检查采用美国Optovue公司RTVue-XR Avanti OCT仪进行;采用德国罗兰RETIscan视觉电生理系统,记录mf-ERG并结果分析。
患眼BCVA为0.25~0.8,平均0.47;屈光不正7例,屈光度为-1.5~-5.5 DS;眼前节检查正常;玻璃体内见灰色颗粒状细胞1眼。所有患眼对侧眼行BCVA、裂隙灯显微镜、眼底彩色照相、FAF、FFA、ICGA、SD-OCT 检查均未见异常。根据MEWDS临床诊断标准[2],结合患眼彩色眼底像、间接检眼镜、FAF、FFA、ICGA、SD-OCT、OCTA、mf-ERG检查结果,对比分析后作出诊断。
所有患者定期随访,随访观察2~6个月,平均3个月。随访期间所有患者均进行了BCVA、 裂隙灯显微镜、扩瞳后间接检眼镜检查及彩色眼底照相、FAF、FFA、ICGA、SD-OCT、mf-ERG检查。
2 结果
眼底彩色照相检查发现所有患眼黄斑区均呈橘红色颗粒样改变,伴中心凹反光消失,未见明显视盘水肿;2例患者后极部可见散在黄白色或灰白色点状病灶,病灶边界不清,数量不等;视网膜血管未见明显改变,未见视网膜静脉血管鞘(图1A)。
FAF可见视盘附近及后极部大小不一的点片状强荧光及不均匀弥漫性相互融合的强荧光病灶,周边部病灶相对离散且更显多灶性(图1B)。
FFA早期隐约可见散在点状强荧光(图1C),中晚期可见与自发荧光所在部位相一致的强荧光,边界模糊,呈花环状排列(图1D)。7眼中,晚期可见视盘着染3眼;后极部视网膜血管壁荧光素着染2眼;所有患眼未见荧光素渗漏。
ICGA早期脉络膜背景荧光正常,大、中血管形态未见异常(图1E)。中晚期可见视盘周围、黄斑区及中周部脉络膜多发散在点状弱荧光病灶,病灶大小不等,部分病灶融合成小片状。病灶与FAF及FFA检查中的强荧光病灶对应(图1F)。
SD-OCT检查所有患眼黄斑区外层视网膜结构紊乱或中断(图2)。黄斑区椭圆体带结构紊乱7眼;中断2眼。嵌合体带结构紊乱4眼。4眼外核层可见形态大小不等的强反射物质存积,其中2眼强反射的物质位于黄斑中心凹周围区(图2B、D);另2眼位于黄斑中心凹下(图2E、F),其形态呈锥形或圆屋顶形,基底部位于视网膜色素上皮(retinal pigment epithelium, RPE)层,尖端指向内层视网膜,可延伸至外核层及外丛状层。mf-ERG可见患眼的黄斑峰值低于对侧眼(图3)。
OCTA检查可见浅层视网膜、深层视网膜、外层视网膜及脉络膜的血管未见异常(图4A)。En-face OCT在脉络膜血管层水平没有显示任何异常或扩张的脉管系统;在椭圆体带水平,可见散在大小不一的类圆形片状弱反射病灶,这些病灶与FAF的强荧光、FFA的晚期强荧光及ICGA的晚期弱荧光相对应(图4B);在外核层水平可见散在小颗粒状强反射病灶(图4C)。
发病后6~8周患者自述视力恢复至发病前水平。末次随访时,患眼BCVA为0.6~1.0,平均0.8。后极部灰白色或黄白色点状病灶全部消失,SD-OCT检查见强反射物质消失,黄斑中心凹各层结构清晰,形态正常。眼底彩色照相、FAF、FFA、ICGA检查结果均显示眼底病变完全消退。mf-ERG黄斑峰值也恢复正常。En-face OCT图像可见类圆形片状弱反射病灶逐渐变淡至完全消失,小颗粒状强反射病灶逐渐消退。

图1 眼底特征 A.右眼彩色眼底像:黄斑区呈橘红色颗粒样改变。B.FAF:视盘附近及后极部可见大小不一的点片状强荧光及不均匀弥漫性相互融合的强荧光病灶。C.右眼FFA早期:隐约可见散在点状强荧光。D.右眼ICGA早期:脉络膜背景荧光正常,大、中血管形态未见异常。E.右眼FFA晚期:可见与自发荧光所在部位相一致的强荧光,呈“花环状”排列,后极部血管管壁着染,视盘着染。F.右眼ICGA晚期:视盘周围、黄斑区及中周部脉络膜多发散在点状弱荧光病灶,病灶大小不等,部分病灶融合成小片状。病灶与FAF及FFA检查中的强荧光病灶对应。
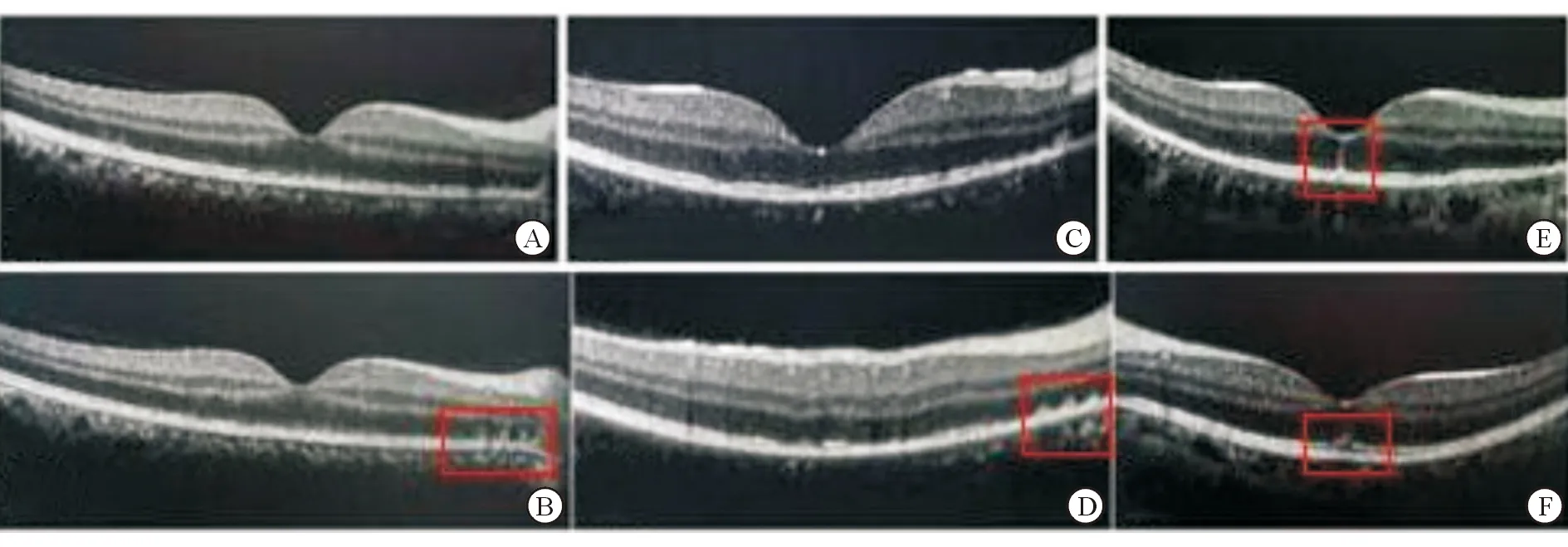
图2 SD-OCT检查 黄斑区外层网膜结构中断、紊乱 A.椭圆体带结构紊乱;B.黄斑中心凹周围区有形态大小不等的强反射物质存积(红色方框所示),其形态呈锥形或圆屋顶形,基底部位于RPE层,尖端指向内层视网膜,可延伸至外核层及外丛状层;C.椭圆体带连续性破坏,嵌合体带结构紊乱;D.椭圆体带中断,黄斑中心凹周围区可见强反射物质堆积(红色方框所示);E.椭圆体带及嵌合体带结构紊乱,黄斑中心凹下可见强反射物质堆积(红色方框所示);F.椭圆体带结构紊乱,黄斑中心凹下可见强发射物质存积(红色方框所示)。

图3 mf-ERG黄斑峰值 A.患眼mf-ERG黄斑峰值为49.5μV;B. 对侧眼mf-ERG黄斑峰值为87.8μV。

图4 OCTA检查及En-face OCT检查情况 A.OCTA检查可见浅层视网膜、深层视网膜、外层视网膜及脉络膜的血管未见异常。En-face OCT图像:B.在椭圆体带水平,可见散在大小不一的类圆形片状弱反射病灶;C.在外核层水平可见散在小颗粒状强反射病灶。
3 讨论
MEWDS在1984年由Jampol等[1]首先报道,其特点是好发于青年女性,单眼发病,起病急,具有自限性,多在1~2个月恢复。该病患者多有轻、中度的视力下降,眼前出现暗点或生理盲点扩大,闪光感等。通过临床表现以及FAF、FFA、ICGA、SD-OCT、视野、电生理等相关检查,可以确诊本病。但是本病的发病机制尚未阐明,一部分研究者[3-4]认为MEWDS是视网膜外层及RPE层的疾病;还有一些研究者[5-6]认为是脉络膜的疾病,因为部分MEWDS患者在急性期有非特异性脉络膜增厚。这在许多脉络膜视网膜炎性疾病中很常见。
本次研究中, SD-OCT检查所有患眼病灶主要位于外层视网膜,可以看到嵌合体带及椭圆体带的结构紊乱、中断,还有形态呈锥形或圆屋顶形、大小不等的强反射物质堆积,其基底部位于RPE层,尖端指向内层视网膜,可延伸至外核层及外丛状层。有研究[7]指出,这些强反射堆积物可能是由于脂褐素从受损的RPE细胞迁移到外层视网膜中,或者代表感光细胞碎片脱落并累积到外层视网膜。通过SD-OCT检查可以将MEWDS的病变定位到外层视网膜,主要是椭圆体带结构的破坏。这与一些文献[8-10]的报道相一致。
FAF在急性期表现为点片状强荧光,恢复后复查FAF,自发强荧光消失。由于脂褐素是RPE不断吞噬光感受器末端脱落盘膜形成不能完全消化的终产物,是反映视网膜感光细胞外节更新速度、RPE细胞代谢功能的重要指标,所以有研究[8-9,11]认为这种自发荧光主要是由于脂褐素的增加或者光感受器过度脱落引起的。如果RPE细胞功能减退,细胞内脂褐素不能及时代谢,也会造成细胞内脂褐素的堆积,从而引起较强的自发荧光[8-9]。因此,FAF点片状的强自发荧光,可能是由于光感受器过度脱落、RPE功能障碍或者二者共同导致的。近年来,近红外自发荧光(near-infrared autofluorescence,NIR-AF)也涉入MEWDS发病机制的探讨中。有研究[12]发现在NIR-AF图像中可见与FFA及ICGA部位相一致的弱荧光病灶,而这些弱荧光的病灶随着病情的恢复,部分也不会消失,考虑与RPE细胞内黑色素重新分布相关。
对于FFA强荧光,有研究[13]认为,早期阶段的点状强荧光,其主要病灶在中间视网膜上,而晚期融合成片的斑片状强荧光,认为其病变在深层视网膜上。这种现象认为与RPE的功能损害以及黄斑区色素紊乱有关。这种强荧光还可能是由于RPE色素的脱失,形成窗样缺损而产生的透见荧光[9]。结合SD-OCT及FAF,我们发现FFA上强荧光病灶与SD-OCT椭圆体带的病灶息息相关,并且与FAF的点片状强荧光大小、形态、部位相一致。所以FFA上强荧光病灶可能是由于RPE的功能障碍所致。
在ICGA中,RPE荧光的作用很少被发现。有研究认为,RPE在临床血管造影中不仅仅是一个透明层, RPE通过主动转运的方式对ICG进行摄取,摄取的ICG聚集在RPE细胞,有助于背景荧光的形成。随着更多ICG在RPE中累积,这种荧光应该在血管造影的后期阶段更加突出[14-15]。当RPE细胞的功能障碍时,对ICG的摄取减少,在造影照片上会观察到晚期低荧光。当RPE细胞受到更严重的损伤时,ICG可能会进入受损的细胞膜,更容易产生在ICGA上观察到的强荧光[14,16]。因此MEWDS患者,ICGA晚期的弱荧光可能是由于RPE的功能障碍造成的,由于MEWDS患者在复查时,这种弱荧光已经完全消失,说明MEWDS患者只是RPE细胞的功能障碍,并没有严重的细胞损伤。
所有患者黄斑峰值的降低,在随访过程中,患者的黄斑峰值逐渐恢复正常,所以这种峰值的降低是可逆的,这与Jampol等[1]的观点相符合。mf-ERG反映视网膜中央的视锥细胞功能,有研究[17]指出MEWDS患者mf-ERG振幅的降低与光感受器的炎症有关。而光感受器破坏最初认为是由于原发性RPE异常所致,后来又提出光感受器的炎症可以继发性造成RPE的损害,而易消逝的特征表明,感光细胞体保持完好,在大多数情况下确保完整的恢复感光器的内外节段,与所有患者恢复过程相适应[13]。
患者OCTA检查显示浅层和深层视网膜毛细血管和脉络膜血管系统都没有明显异常。有研究[12,18]指出,在疾病的急性期脉络膜毛细血管循环的正常外观表明MEWDS的病理过程可能与RPE和光感受器中的原发性损伤有关。通过En-face OCT平面扫描的观察,我们发现MEWDS的病变主要集中在外层视网膜上。有研究[9,19]发现,椭圆体带水平的类圆片状弱反射病灶可能是光感受器的炎症导致光感受器内、外节段的损伤,而外核层颗粒状强反射病灶可能是光感受器损伤后的碎片或炎性物质的堆积。
本次研究通过对SD-OCT、FAF、FFA、ICGA、电生理、OCTA及En-face OCT的检查结果的阐述,认为MEWDS发病机制更倾向于可能是由于RPE功能的障碍造成的,是视网膜外层的疾病。虽然部分学者[20-21]提出MEWDS是脉络膜的炎性疾病,其依据是部分MEWDS 患者的急性期会有脉络膜厚度增加,而恢复后脉络膜的厚度减少,但是脉络膜炎症常常伴有OCTA的血管扩张,FFA及ICGA会有荧光素渗漏。本研究中OCTA、FFA及ICGA均未见上述改变。脉络膜作为动态血管床,它的厚度可由于许多全身或眼部因素而变化。因此,单独的脉络膜厚度可能不足以分析健康或疾病中的眼灌注[19]。
综上所述,MEWDS是一种自限性疾病,多在1~2个月后恢复正常。通过多模影像技术深入分析MEWDS的发病机制,考虑这种独特的疾病是外层视网膜的疾病,可能与RPE的功能障碍相关,但不能排除是光感受器炎症造成的继发性RPE功能障碍。因此,多模影像技术对MEWDS诊断及发病机制的探讨具有重要临床意义。
但本研究存在样本量小且随访时间有限等不足, 因此MEWDS在上述多种影像学检查中的改变是否具有普遍意义,需要进一步扩大样本量以及延长随访时间加以证实。

