齐墩果酸硫脲类衍生物的合成及以VEGFR-2为靶点的分子对接研究
李 杰,宋艳玲
(沈阳化工大学 制药与生物工程学院, 辽宁 沈阳 110142)
齐墩果酸(oleanolic acid,OA.结构式如图1所示)是一种重要的五环三萜类化合物,可以通过女贞子、苹果皮、橄榄叶和丁香花等植物中提取得到[1-2].齐墩果酸及其衍生物具有广泛的药理活性,如抗肿瘤、降血糖、抗炎、抗菌、抗氧化等[3-8].但齐墩果酸水溶性差,生物利用度低[9],限制了其临床应用.硫脲类化合物是目前最具前景的抗癌制剂,研究表明其对肺癌、乳腺癌、肉瘤等多种肿瘤具有抑制作用[10-12].齐墩果酸C-3或C-28链的延长能够增加其抗肿瘤活性[3].根据活性叠加原理,将硫脲片段引入齐墩果酸C-3位,以期提高化合物抗肿瘤活性.

图1 齐墩果酸结构式Fig.1 Chemical structures of OA
计算机辅助药物设计(computer-aided drug design,CADD)因其准确的信息成为新药研究和药物设计方面的重要工具[13].分子对接(molecular docking)是通过研究小分子配体与受体生物大分子相互作用,将配体分子置于受体分子的活性位点,利用化合物与受体蛋白的三维结构进行对接,预测化合物的生物活性.VEGFR是一类酪氨酸激酶跨膜糖蛋白,属于受体型蛋白酪氨酸激酶,VEGFR-2在与肿瘤相关的血管生成中发挥重要作用,是诱导血管生成和增加血管渗透性的主要受体[14].以VEGFR-2为靶点的小分子酪氨酸激酶抑制剂已成为目前研究热点,如已上市药物舒尼替尼和索拉菲尼等[15-16].本文通过计算机辅助设计方法研究齐墩果酸衍生物与VEGFR-2靶蛋白分子对接,预测目标化合物抑制VEGFR-2 的活性.
1 实验部分
1.1 仪器与试剂
Bruker ARX-600型核磁共振仪,美国Bruker公司; Agilent 1100 SL离子阱质谱仪,美国安捷伦公司;Büchi B-540熔点测定仪,瑞士Büchi公司;薄层色谱(GF-254)、柱色谱硅胶(200-300目),青岛海洋化工有限公司.
齐墩果酸(质量分数98 %),陕西慈缘生物技术有限公司;芳香胺类药品,国药集团化学试剂有限公司;其他溶剂和药品均为市售分析纯.
1.2 合成实验
齐墩果酸衍生物的合成路线如下所示.


1.2.1 齐墩果酸甲酯(化合物1)的制备
将齐墩果酸OA(5.00 g,10.94 mmol)和无水K2CO3(3.78 g,27.35 mmol)溶于50 mL干燥的N,N-二甲基甲酰胺中,搅拌下缓慢滴加碘甲烷(1.37 mL,21.89 mmol),室温下继续搅拌反应6 h,TLC监测反应.反应结束后加水稀释,乙酸乙酯萃取,饱和NaCl溶液洗涤,水洗,合并有机相,无水硫酸钠干燥,抽滤,减压蒸干溶剂,得白色固体,干燥过夜.甲醇重结晶得白色针状晶体化合物齐墩果酸甲酯4.40 g,产率85 %,mp:196~198.8 ℃(文献mp:197~198.2 ℃)[17].
1.2.2 3-羰基-齐墩果酸甲酯(化合物2)的制备
将齐墩果酸甲酯(4.40 g,9.35 mmol)溶于100 mL丙酮中,冰浴下缓慢滴加琼斯试剂(11.5 mL),直至反应液橘红色不再消失,滴毕,室温下反应1~2 h,TLC监测反应.反应完毕,加入130 mL异丙醇淬灭.反应结束后,减压蒸除部分溶剂,乙酸乙酯萃取,饱和NaCl溶液洗涤,水洗,合并有机相,无水硫酸钠干燥,抽滤,减压蒸干,得淡黄绿色固体,干燥,甲醇重结晶得白色晶体化合物3-羟肟基-齐墩果酸甲酯4.15 g,产率95 %,mp:186~187 ℃(文献mp:185~186 ℃)[18].
1.2.3 3-羟肟基-齐墩果酸甲酯(化合物3)的制备
将3-羰基-齐墩果酸甲酯(4.15 g,8.87 mmol)溶于50 mL吡啶中,加入盐酸羟胺(2.76 g,39.74 mmol),50 ℃下反应2 h,TLC监测反应.反应结束后加入适量二氯甲烷稀释,质量分数10 %盐酸洗涤3次,饱和NaCl溶液洗涤,水洗,合并有机相,无水硫酸钠干燥,抽滤,减压蒸干,得白色固体化合物3-羟肟基-齐墩果酸甲酯3.24 g,产率75.5 %,mp:244~246 ℃(文献mp:247~249 ℃)[18].
1.2.4 3-氨基-齐墩果酸甲酯(化合物4)的制备
将3-羟肟基-齐墩果酸甲酯(4.88 g,10.10 mmol)溶于100 mL甲醇中,加入乙酸铵(9.04 g,117.30 mmol),再加入NaBH3CN(7.08 g,112.70 mmol),充分搅拌溶解,冰浴下缓慢滴加质量分数15 %的三氯化钛溶液(29.33 mL,34.22 mmol),室温下反应12 h,TLC监测反应.反应结束后,蒸除部分溶剂,用体积分数为2 %的NaOH溶液调节pH至10,二氯甲烷萃取,蒸馏水洗涤,合并有机相,无水硫酸钠干燥,抽滤,减压蒸干,硅胶柱层析分离(200~300目),洗脱剂:甲醇/二氯甲烷(体积比1∶20),得白色固体化合物3-氨基-齐墩果酸甲酯3.78 g,产率80 %,mp:221.3~223.7 ℃.ESI-MS,m/z:470.8[M+H]+.1H NMR(600 MHz,CDCl3),δ:5.29(1H,s,H-12),3.64(3H,s,H-31,—COOCH3),3.21(s,2H,H-3,—NH2),2.87(1H,d,J=13.6 Hz,H-3),1.85(s,2H,H-2),1.14(3H,s,Me),1.02(3H,s,Me),0.94(3H,s,Me),0.91(6H,s,Me),0.81(3H,s,Me),0.74(3H,s,Me).13C NMR(600 MHz,CDCl3),δ:178.32(C-28),143.77(C-13),122.37(C-12),60.05(C-3),55.77(C-31),51.54,47.66,46.74,45.87,41.66,41.30,39.22,38.84,37.67,37.13,33.86,33.12,32.68,32.39,30.70,29.71,28.47,27.69,25.93,23.65,23.35,23.08,18.59,16.85,15.97,15.20.
1.2.5 化合物Ⅰ1~Ⅰ6的制备
1.2.5.1 化合物Ⅰ1的制备
将3,4-二氯苯胺(0.155 3 g,0.958 7 mmol)加入盛有5 mL甲苯溶液的25 mL反应瓶中,60 ℃,油浴条件下搅拌,再逐滴滴加硫光气(0.073 4 g,0.639 1 mmol).滴加过程中看到反应液变浑浊,有橙黄色絮状物产生,并产生白烟.3 h后,将反应液抽滤,滤去絮状物,再将溶液进行减压旋蒸.将化合物4(0.300 2 g,0.639 1 mmol)用5 mL甲苯溶液完全溶解后加入上述浓缩的反应瓶中,反应液颜色为淡黄色,溶液澄清,常温反应0.5 h,TLC监测反应全过程,展开剂:V(石油醚)/V(乙酸乙酯)=5∶1,显色剂:H2SO4-EtOH溶液.反应完成后,用配置好的饱和NaOH溶液将反应液洗3次取上层溶液,乙酸乙酯萃取(100 mL)3次,饱和食盐水冲洗3次,合并有机相,无水Na2SO4干燥过夜,静置,抽滤,洗涤,旋蒸除去溶剂,50 ℃真空干燥过夜,最终得淡黄色固体物质,用硅胶柱色谱分离,V(PE)/V(EA)=8/1洗脱,得化合物Ⅰ1白色粉末0.146 g,产率73 %,mp 199.0~201.0 ℃.1H NMR(600 MHz,DMSO),δ:9.72(s,1H,—NH),8.11(s,1H,—NH),7.57(d,J=9.0 Hz,1H,Ar—H5),7.52(d,J=8.7 Hz,1H,Ar—H6),7.39(d,J=7.4 Hz,1H,Ar—H2),5.19(s,1H,H-12),3.54(s,3H,H-31,—COOCH3),2.78(d,J=13.6 Hz,1H,H-3),1.83(s,2H,H-2,—CH2),1.12(s,3H,Me),0.88(d,J=5.7 Hz,12H,Me),0.82(s,3H,Me),0.67(s,3H,Me).
1.2.5.2 化合物Ⅰ2的制备
按照化合物Ⅰ1的合成方法,2-氟-4-甲基苯胺(0.139 5 g,0.958 7 mmol)与化合物4(0.301 2 g,0.639 1 mmol)反应,得化合物Ⅰ2淡黄色粉末0.128 g,产率64 %,mp:208.7~210.6 ℃.1H NMR(600 MHz,DMSO),δ:9.15(s,1H,—NH),7.70(t,J=8.2 Hz,1H,Ar—H5),7.44(d,J=9.0 Hz,1H,Ar—H3),7.05(d,J=11.4 Hz,1H,—NH),6.94(d,J=7.9 Hz,1H,Ar—H6),5.19(s,1H,H-12),3.54(s,3H,H-31,—COOCH3),2.78(d,J=10.1 Hz,1H,H-3),1.83(s,2H,H-2,—CH2),1.12(s,3H,Me),0.88(d,J=3.0 Hz,12H,Me),0.78(s,3H,Me),0.66(s,3H,Me).
1.2.5.3 化合物Ⅰ3的制备
按照化合物Ⅰ1的合成方法,邻氨基三氟甲苯(0.154 4 g,0.958 7 mmol)与化合物4(0.300 7 g,0.639 1 mmol)反应,得化合物Ⅰ3微黄色粉末0.156 g,产率78 %,mp:179.7~180.9 ℃.1H NMR(600 MHz,DMSO),δ:9.01(s,1H,—NH),7.73~7.66(m,2H,Ar—H3、6),7.61(d,J=7.8 Hz,2H,Ar—H4、5),7.41(d,J=6.7 Hz,1H,—NH),5.20(s,1H,H-12) 3.54(s,3H,H-31,—COOCH3),2.78(d,J=12.2 Hz,1H,H-3),1.83(s,2H,H-2,—CH2),0.89(d,J=12.5 Hz,15H,Me),0.81(s,3H Me,),0.67(s,3H,Me).
1.2.5.4 化合物Ⅰ4的制备
按照化合物Ⅰ1的合成方法,2-氟苯胺(0.106 5 g,0.958 7 mmol)与化合物4(0.301 5 g,0.639 1 mmol)反应,得化合物Ⅰ4白色粉末0.162 g,产率81 %,mp:204.8~206.7 ℃.1H NMR(600 MHz,DMSO),δ:9.26(s,1H,—NH),7.97(t,J=7.4 Hz,1H,Ar—H3),7.60(d,J=9.1 Hz,1H,Ar—H6),7.25~7.19(m,1H,—NH),7.13(dd,J=13.8、6.0 Hz,2H,Ar—H4,5),5.20(s,1H,H-12),3.54(s,3H,H-31,—COOCH3),2.78(dd,J=13.7、3.8 Hz,1H,H-3),1.83(s,2H,H-2,—CH2),1.13(s,3H,Me),0.88(d,J=3.9 Hz,12H,Me),0.80(s,3H,Me),0.67(s,3H,Me).
1.2.5.5 化合物Ⅰ5的制备
按照化合物Ⅰ1的合成方法,3-氟苯胺(0.110 5 g,0.958 7 mmol)与化合物4(0.301 2 g,0.639 1 mmol)反应,得化合物Ⅰ5白色粉末0.124 g,产率62 %,mp:187.9~190.0 ℃.1H NMR(600 MHz,DMSO),δ:9.69(s,1H,—NH),7.78(d,J=11.5 Hz,1H,—NH),7.48(d,J=9.1 Hz,1H,Ar—H4),7.34~7.27(m,1H,Ar—H2),7.18(d,J=7.8 Hz,1H,Ar—H6),6.86(s,1H,Ar—H5),5.20(s,1H,H-12),3.54(s,3H,H-31,—COOCH3),2.78(d,J=10.4 Hz,1H,H-3),1.83(s,2H,H-2,—CH2),0.88(d,J=4.9 Hz,15H,Me),0.82(s,3H,Me),0.67(s,3H,Me).
1.2.5.6 化合物Ⅰ6的制备
按照化合物Ⅰ1的合成方法,4-氟苯胺(0.118 9 g,0.958 7 mmol)与化合物4(0.301 2 g,0.639 1 mmol)反应,得化合物Ⅰ6白色粉末0.166 g,产率83 %,mp:201.2~203.7 ℃.1H NMR(600 MHz,DMSO)δ:9.49(s,1H,—NH),7.49(d,J=5.0 Hz,2H,Ar—H2、6),7.28(d,J=9.0 Hz,1H,—NH),7.13(t,J=8.8 Hz,2H,Ar—H3、5),5.20(s,1H,H-12),3.54(s,3H,H-31,—COOCH3),3.32(s,3H),2.81~2.73(m,1H,H-3),1.83(s,2H,H-2,—CH2),1.12(s,3H,Me),0.88(d,J=4.0 Hz,12H,Me),0.80(s,3H,Me),0.67(s,3H,Me).
2 结果与讨论
MVD软件能够通过函数打分形式,预测并计算蛋白质与小分子配体的相互作用,评分数值的绝对值越大表明化合物与受体亲和力越好[19],齐墩果酸及其衍生物与VEGFR-2靶蛋白分子对接结果见表1.结果表明化合物与VEGFR-2靶蛋白(PDB编号:5EW3)的结合能均高于先导化合物齐墩果酸,其中化合物Ⅰ5和Ⅰ6的结合能较高,分别为-554.73 kJ/mol和548.73 kJ/mol,同索拉菲尼与靶蛋白的对接结合能相当.索拉菲尼是一种小分子VEGFR-2抑制剂,通过分子虚拟对接方法研究与VEGFR-2靶蛋白(PDB编号:5EW3)的相互作用(图2),分子对接结果表明索拉菲尼与VEGFR-2靶蛋白氨基酸残基之间形成多个牢固的氢键,与靶蛋白产生较大结合力.化合物Ⅰ5与靶蛋白的分子虚拟对接结果(图3)表明Ⅰ5能较好地插入靶蛋白的活性口袋中,其中酯基、硫脲基和苯环取代基苯环上的氟取代基与氨基酸残基(VAL A:899,HIS A:895,ARG A:1027)紧密结合,形成牢固的氢键;同时,化合物Ⅰ5还可通过π—σ键、π—烷基键和碳氢键等与VEGFR-2靶蛋白的多个氨基酸残基(GLY A:893、ASN A:900、IEL A:892、HIS A:1082、ALA A:881、HIS A:894)结合.

表1 不同化合物与靶蛋白VEGFR-2的 结合能(PDB:5EW3)Table 1 Molecular docking scores between compounds and VEGFR-2 kinase
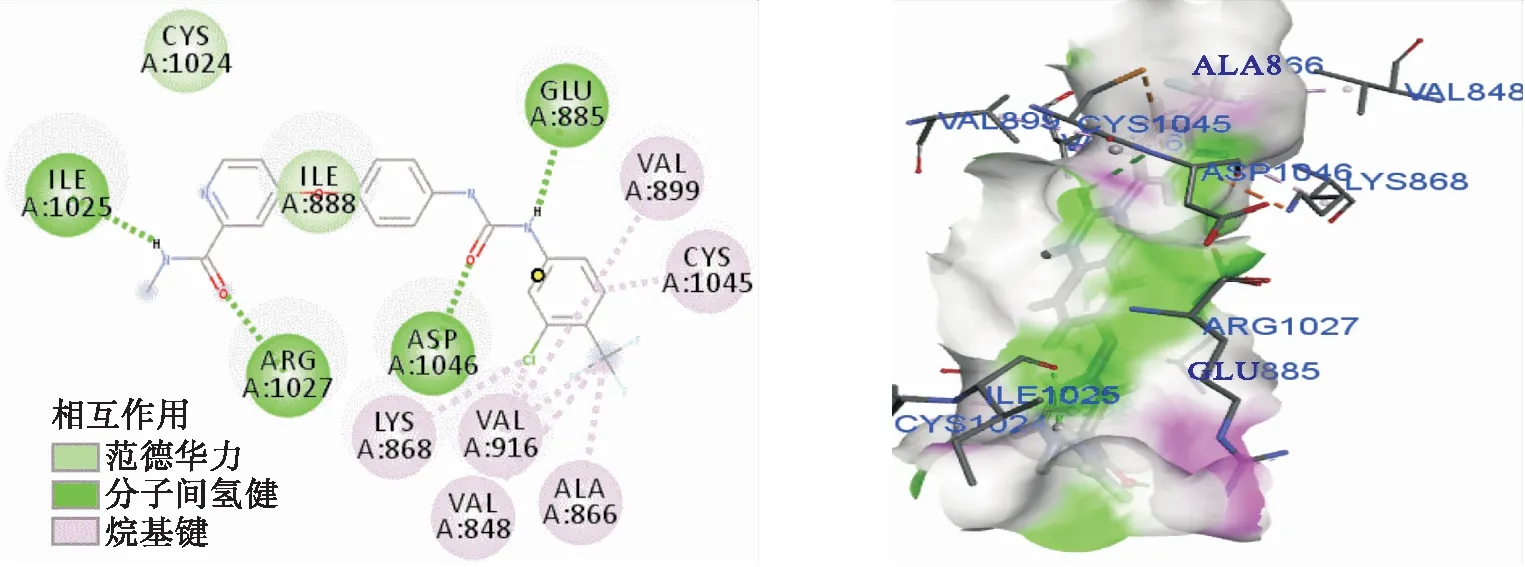
图2 索拉菲尼与VEGFR-2靶蛋白的分子对接模式Fig.2 Molecular docking mode between sorafenib and VEGFR-2 kinase
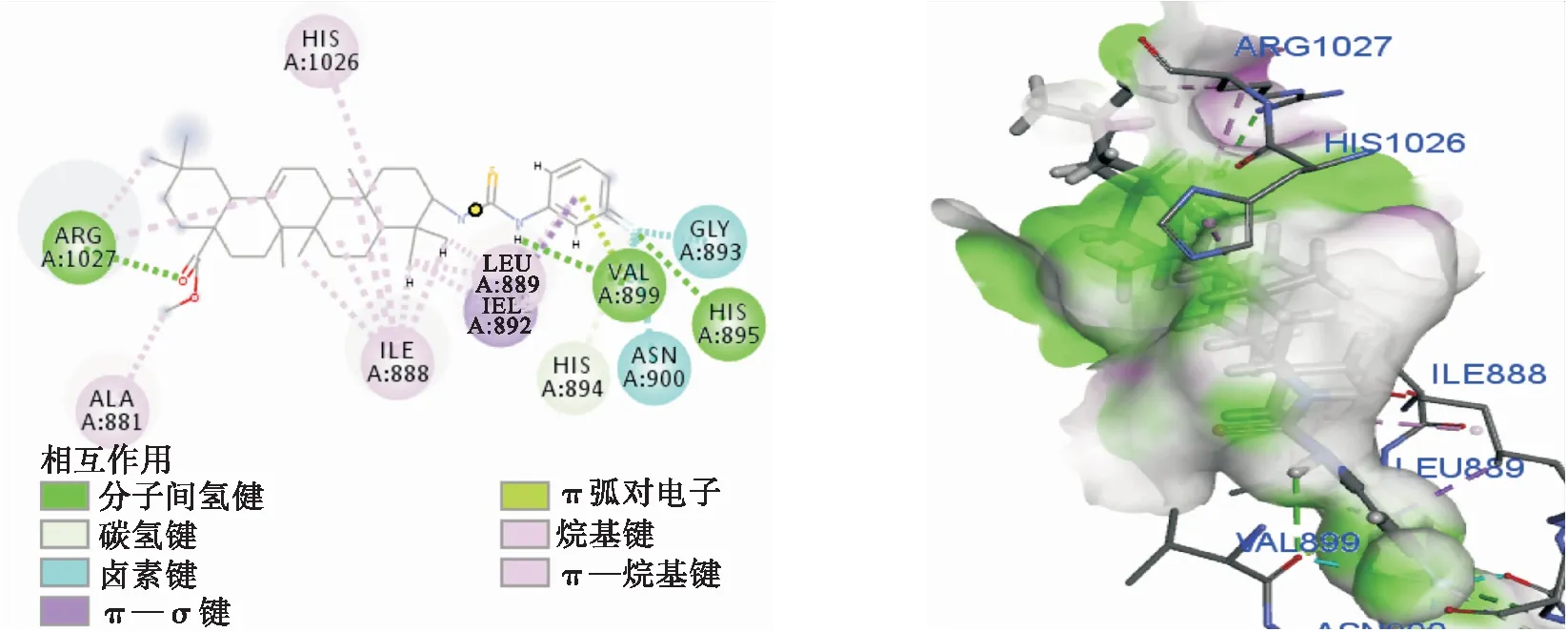
图3 化合物Ⅰ5与VEGFR-2靶蛋白的分子对接模式Fig.3 Molecular docking mode between Ⅰ5 and VEGFR-2 kinase
3 结 论
以齐墩果酸为先导化合物,设计并合成了6个未见文献报道的齐墩果酸硫脲类衍生物,目标产物结构经1H NMR确认.利用计算机辅助设计分子模拟对接法研究目标化合物和VEGFR-2激酶的结合情况,结果表明目标化合物与靶蛋白的结合能均明显高于齐墩果酸,其中化合物Ⅰ5和Ⅰ6与靶蛋白的结合能同索拉菲尼相当,具有进一步研究的价值.利用分子模拟对接方法对药物作用机制的研究具有重要意义,本研究对进一步优化设计齐墩果酸衍生物作为VEGFR-2抑制剂具有一定的参考价值.

