短时程脊髓电刺激与背根神经节双极脉冲射频治疗带状疱疹后神经痛的疗效比较
王成龙,宋涛
(中国医科大学附属第一医院疼痛科,沈阳 110001)
带状疱疹后神经痛(postherpetic neuralgia,PHN)是水痘-带状疱疹病毒感染后累及周围神经所产生的严重并发症之一,属于典型神经病理性疼痛,具体表现为针刺样、烧灼样或电击样痛,还可出现痛觉过敏、痛觉超敏、自发痛及异常性疼痛等[1-2]。带状疱疹患者PHN发病率约为15%,多见于50岁以上、免疫力低下且并发慢性疾病、急性期皮损及疼痛程度严重的患者[3]。PHN的产生机制复杂,寻求确切有效的PHN治疗方式始终是临床关注的热点。
临床上PHN治疗方法很多,目前较为公认的治疗方法为背根神经节双极脉冲射频(pulsed radiofrequency,PRF)及短时程脊髓电刺激(short-term spinal cord stimulation,stSCS),已有研究[4-5]表明2种治疗方案对PHN均有较好的疗效。本研究比较stSCS与背根神经节PRF治疗PHN的疗效及安全性,旨在为患者选择更优的治疗方案提供参考。
1 材料与方法
1.1 临床资料及分组
收集中国医科大学附属第一医院疼痛科2015年6月至2017年6月收治的175例PHN患者的临床资料。纳入标准:(1)明确诊断为带状疱疹,并且有典型的带状疱疹后神经痛;(2)带状疱疹起疹部位为胸、腰段(T1~L5);(3)起疹时间<4个月;(4)连续口服加巴喷丁(0.3 g/次,3次/d)1周后疼痛仍存在,且日平均视觉模拟评分(visual analogue score,VAS;早、中、晚、睡前测定VAS评分)≥4分。排除标准:(1)患有严重心脏、脑、肝脏、肾脏疾病等无法耐受微创手术;(2)凝血功能异常;(3)患有严重精神类或其他疾病无法正确进行疼痛评分或不能客观描述症状;(4)无法按期随访。165例患者纳入研究。根据患者意愿,90例采用了背根神经节PRF治疗(A组);75例采用stSCS治疗(B组),所有患者均在术前签署知情同意书。2组患者年龄、性别、病程无统计学差异(均P>0.05),见表1。
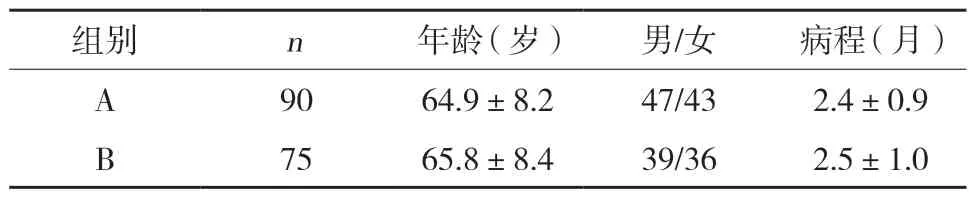
表1 患者一般情况比较
1.2 治疗方法
治疗操作均由有多年手术经验的副主任医师及以上职称医师完成。
1.2.1 背根神经节PRF治疗:患者取俯卧位,持续心电监护,根据患者疼痛的位置确定受损神经节段,CT扫描后确定相应椎间孔水平,做好标记,根据CT影像确定穿刺点(2个)及穿刺路径。碘伏消毒,铺无菌巾,穿刺点局部浸润(0.5%利多卡因)麻醉,18 G Baylis射频穿刺套针在CT引导下穿刺,当针尖抵达靶点位置处(图1)连接Baylis射频治疗仪,调至感觉测试模式(100 Hz,1.0 ms),微调针尖位置,刺激电压 <0.3 V时引出相应神经根异感后固定针尖位置。调至手动脉冲射频模式。参数设定为治疗温度42 ℃,频率3 Hz,脉宽30 ms,场强由40 V开始逐渐增加,根据患者耐受程度最多可加至90 V,时间450 s。交换正负电极再次设定以上参数脉冲450 s,治疗结束后缓慢拔除穿刺针,碘伏消毒,无菌敷料覆盖,待患者生命体征平稳转送至病房。
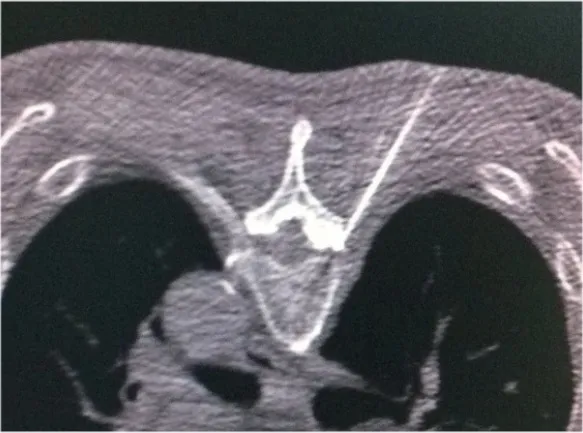
图1 PRF靶点位置
1.2.2 stSCS治疗:患者取俯卧位,充分暴露腰部及背部,常规消毒、铺巾、局麻,X线下定位L2~3或L1~2棘突间隙为穿刺进针点,穿刺针到达硬膜外腔后开始置入电极(均使用单根8触点电极),注意患者反应。最终电极上端置入位置为皮损节段的上1~2个椎体,腰段带状疱疹患者电极上缘置入于T9~10椎体水平。尽量靠近中线偏患侧(图2),到达目标点位后行术中电生理测试,确保电流能完整覆盖疼痛区域,且无其他区域的不适感(双腿或对侧躯体)。若电流分布不理想,则反复调整电极位置,最终达到理想的覆盖区域。然后用锚在皮肤上固定电极导线,辅料包扎。术毕连接体外神经刺激器,调整参数至最佳(电流能完整覆盖疼痛区域,且无其他区域不适感),连续刺激7 d后拔除测试电极,观察疗效。

图2 X线下电极放置位置(正、侧位)
1.3 观察指标
采用VAS评分来评价患者疼痛的改善情况。VAS评分标准:0分,完全无痛;1~3分,轻度疼痛,不影响日常活动;4~7分,中度疼痛,影响睡眠时为5分以上;8~10分,剧烈疼痛。采用匹兹堡睡眠质量指数(Pittsburgh sleep quality index,PSQI)来评价患者的睡眠质量改善情况。PSQI评分标准:评分范围0~21分,评分≥8分表示患者存在睡眠障碍。PSQI评分越高,说明患者的睡眠质量越差。记录2组治疗前(T0)及术后1 d(T1)、7 d(T7)、30 d(T30)、90 d(T90)、180 d(T180)的VAS评分、PSQI评分及不良反应与并发症发生情况。
1.4 统计学分析
2 结果
2.1 2组患者VAS评分、PSQI评分比较
结果显示,2组治疗前VAS评分、PSQI评分无统计学差异(均P> 0.05)。与治疗前比较,2组治疗后各个时间点的VAS评分、PSQI评分均降低(均P<0.05)。与A组比较,B组术后各个时间点VAS评分均降低(均P< 0.05);除术后1 d,B组其他时间 PSQI评分均低于A组(均P< 0.05)。见表2。
2.2 2组不良反应及并发症发生情况
2组患者术后均未发生明显不良反应,所有患者治疗过程中均无出血、感染等严重并发症产生。

表2 2组患者各时间VAS评分、PSQI评分比较
3 讨论
PHN是一种非常棘手的神经病理性疼痛,带状疱疹患者水疱消退后皮损区疼痛超过4个月时,这类神经病理性疼痛会形成中枢敏化,发展至后遗症期治疗十分困难。因此在急性期(1个月)或亚急性期(1~4个月)进行治疗干预十分重要。PHN产生机制复杂,带状疱疹病毒侵犯背根神经节和感觉末梢,破坏了脊髓上行抑制性传导,导致过量兴奋性信号传入中枢,引起交感传出纤维激活外周感受器,使初级感受器的兴奋性增高[6]。
目前,临床上针对PHN的治疗方法很多,包括口服药物(加巴喷丁、普瑞巴林等联合抗病毒及营养神经药物)、局部外用药及椎旁注射、神经阻滞等,但是效果却不理想[7-10]。PRF作为疼痛科常用的介入治疗技术,已被广泛应用于各类神经病理性疼痛[11]。2016年,万成福等[4]采用了高电压、长时程、PRF技术应用于PHN患者,根据个体化原则使患者受到最大程度的场效应,达到了更好的治疗效果。
脊髓电刺激(spinal cord stimulation,SCS)是将刺激电极置入硬膜外腔,通过电流刺激脊髓后柱传导束,阻断疼痛信号以达到治疗疼痛的目的。SCS镇痛机制复杂,目前认为主要基于Melzack和Wall提出经典的疼痛“闸门控制理论(gate control theory,GCT)”,即SCS通过刺激脊髓后柱中的厚髓鞘、粗神经纤维逆行干扰薄髓鞘、细神经纤维传递的痛觉信号,从而抑制脊髓背角的疼痛上传[12]。近年来,SCS已广泛应用于各类慢性顽固性疼痛,包括腰椎术后失败综合征、复杂区域性疼痛综合征、下肢缺血性疾病、顽固性心绞痛、阴部神经痛[13]等。本研究采用的stSCS是将电极置入患者硬膜外腔7~14 d,治疗后将电极拔除,这样做的好处是在保证SCS治疗效果的前提下,同时也可以节省发生器植入的费用。
本研究结果显示,2种治疗方法均可明显缓解PHN患者的疼痛。但与背根神经节PRF治疗比较,stSCS从术后第1天开始就能显著地降低患者疼痛。这可能与脉冲射频的机制及注入的药物起效时间有关。研究显示,stSCS治疗时间更长,术后1~7 d在电流刺激下可更好缓解患者的疼痛。而从远期效果(超过3个月)来看,stSCS较背根神经节PRF缓解患者的疼痛效果更好。在改善患者睡眠质量方面,术后第1天stSCS治疗患者由于在电流刺激下有些患者可能过于紧张造成睡眠质量较背根神经节PRF治疗患者差;但术后7 d拔除电极后,stSCS治疗的患者睡眠质量明显改善,并且好于背根神经节PRF治疗的患者。因此,从远期疗效上看,stSCS可更好改善患者睡眠质量,与以往研究[5]结果一致。研究结果也显示患者均无严重不良反应及并发症发生,stSCS和背根神经节PRF治疗均安全有效。
综上所述,stSCS和背根神经节PRF治疗均可缓解PHN患者的疼痛,改善患者的睡眠质量。与背根神经节PRF比较,stSCS治疗效果持续时间更长。但本研究为单中心、样本量较小,且随访时间较短,未来仍需要多中心、大样本进一步研究论证。

