Au/TiO2复合物的制备、表征及其增强光催化灭菌活性
王玉梅,冀海伟,常通,毕玉水
(山东第一医科大学(山东省医学科学院)化学与制药工程学院,山东泰安271016)
半导体光催化是20 世纪70 年代发展起来的新兴催化技术,具有高效、安全、环境友好等优点,在能源开发、环境保护、生物医药等领域具有良好应用前景[1]。随着光催化技术的发展,ZnO、TiO2、CdTe、CdS 等多种光催化材料得到广泛关注[2]。自1972 年Fujishima 和Honda 发现TiO2单晶能够光催化分解水产氢以来[3],n 型半导体氧化物TiO2凭借其活性高、化学稳定性好、价廉、无毒等优点成为光催化研究热点。
TiO2的能带是由低能价带、高能导带和两者之间的禁带组成。当TiO2被能量大于或等于其带隙能的光子照射时,价带上的电子被激发,越过禁带进入导带,形成带负电的电子(e-),同时在价带上形成带正电的空穴(h+),即电子-空穴对。这些高活性载流子能与水、氧气等分子反应,生成具有强氧化作用的活性氧(ROS),如羟基自由基(·OH)。ROS 不仅能将有机污染物降解为H2O 和CO2等小分子无害物质,还能氧化损伤肿瘤细胞的细胞膜并诱其凋亡,分解细菌细胞壁和细胞膜上的生物分子从而杀死细菌[4]。但是,TiO2的禁带宽度较大,光响应范围窄,只能吸收紫外光(占太阳光的3%~5%),难吸收可见光,限制了其对太阳光的利用;此外,即使光子被TiO2吸收,由于电荷复合,光生电子和空穴会迅速淬灭[5],导致光催化效率降低。因此,有必要通过扩展其光响应范围和减少电子-空穴对复合来提升其光催化作用。
为提高TiO2在可见光下的吸收并增强其催化效能,研究人员提出了金属掺杂、非金属掺杂、复合半导体、染料敏化等方法[6-8]。其中,表面贵金属沉积法在拓宽TiO2光响应范围、抑制电子-空穴对复合,提高光催化效率方面具有明显优势。理论上,Au 纳米粒子表面等离子体共振效应能显著改善TiO2的可见光响应性能,并且贵金属和TiO2之间形成的肖特恩势垒可实现光生电子在TiO2和贵金属之间的高效转移,促进光生电子与空穴有效分离,从而提高TiO2光催化能力[9],在抗菌领域具有潜在的应用价值。
大肠杆菌(E.coli)是广泛分布于自然界的典型的革兰阴性菌代表菌。生产和生活中,未经处理的工业废水、生活废水、医疗废水等水体中大量存在的E.coli不仅对环境造成污染更严重威胁人类健康。目前常用的E.coli抗菌剂包括天然、有机和无机三类。天然抗菌剂一般从植物中提取,但由于来源有限、提取成本高、提取物稳定性差等短板受到一定限制。有机抗菌剂的耐受性和稳定性较弱,易产生耐药性,自身分解产物和挥发物或对人体有害。无机抗菌剂包括金属型和光催化型两大类,具有持久抑菌、耐高温、无耐药性等优势。自1985年Matsunaga 等[10]首次发现无机TiO2在紫外光照射下具有催化杀菌作用以来,TiO2作为一种便捷的催化氧化材料在光催化抗菌领域的应用愈来愈受关注。Huang 等[11]用TiO2结合紫外光作用于E. coli,使其细胞壁、细胞质膜及细胞内成分相继发生变化最终导致死亡;Sunada等[12]成功地应用TiO2光催化氧化法去除饮用水中E.coli;Tom 等[13]采用有机溶剂热还原法制备了核壳结构的Au@TiO2纳米颗粒,但该法操作较为复杂且易产生二次有机污染;此外,该工作仅考察了Au@TiO2的光谱学特征,并未进行灭菌性能的相关研究。
本文采用较为简便的沉积-沉淀法制备了可见光响应性较好的负载型Au/TiO2系列复合物,利用XRD、FTIR、XPS、UV-vis DRS、荧光发射光谱、自由基捕获等对样品进行表征;以氙灯为光源模拟太阳光,将Au/TiO2运用于光催化杀灭E. coli实验并与纯TiO2作比较,详细考察了Au 含量、光照时间、光照强度、光催化剂用量等因素对Au/TiO2光催化灭菌性能的影响,探讨了光催化剂结构、表面性质、光学性质与催化活性之间的关系。
1 实验材料和方法
1.1 试剂与仪器
无水乙醇(AR),购自天津市永大化学试剂有限公司;氢氧化钠(AR)、浓盐酸(AR),购自国药集团化学试剂有限公司;钛酸四丁酯(CP)、氯化金(Ⅲ)三水合物(CP),购自上海阿拉丁生化科技股份有限公司;E.coli,实验室自留;琼脂粉、蛋白胨、氯化钠、酵母提取物均为分析纯;蒸馏水自制。
DF-101S型集热式磁力加热搅拌器,上海予名仪器设备有限公司;KQ-600DB 型超声波振荡器,昆山市超声仪器有限公司;DT5-2B 型离心机,北京时代北利离心机有限公司;HPX-9052MBE 型电热恒温干燥箱,上海博讯实业有限公司;SX-4-10型马弗炉,天津市泰斯特仪器有限公司;YXQSG46-280SA 型高压蒸汽灭菌器,上海博迅医疗生物仪器有限公司;SW-CJ-2F型超净工作台,苏州安泰空气技术有限公司;DHZ-300L型台式冷冻恒温振荡器,宁波新芝生物科技有限公司;GNP-9050 型隔水式恒温培养箱,上海精宏实验设备有限公司;HSX-F300型氙灯平行光源,北京纽比特科技有限公司。
1.2 材料的制备
溶胶-凝胶法制备TiO2步骤如下:向锥形瓶中加入20mL 无水乙醇、7mL 钛酸四丁酯,超声分散6min,于40℃水浴中磁力搅拌30min,缓慢滴加20mL 无水乙醇、2mL 蒸馏水和0.14mL 浓盐酸组成的混合液,搅拌反应20min,形成凝胶,常温陈化60min,之后在70℃烘箱中干燥,研细后于450℃马弗炉中焙烧4h。
沉积-沉淀法制备Au/TiO2系列复合物步骤为:用1mol/L 氢氧化钠将计算量氯化金(Ⅲ)三水合物水溶液(1g/100mL)调节pH 至7,搅拌条件下将1.64g TiO2分散于其中,在60℃水浴中反应1.5h;将悬浮液离心,水洗滤饼数次,常温干燥24h后在60℃烘箱中烘干,研磨后置于马弗炉中450℃焙烧4h。所得系列Au/TiO2复合物中Au含量为质量分数。
1.3 Au/TiO2复合物的表征
1.3.1 表征仪器
利用X射线衍射仪(XRD,TD-3500型,通达科技公司)分析样品的晶相结构,Cu Kα激发源,管压35kV,管流25mA,连续扫描速度0.2°/s。利用傅里叶红外光谱(FTIR,AVATAR370 型,美国Thermo Nicolet 公司)分析样品的官能团,以KBr压片法进行测试。利用X 射线光电子能谱(XPS,ESCALAB 250Xi 型,美国Thermo Fisher 公司)分析样品的表面化学组成和结合状态,以污染碳C1s(284.8eV)校准结合能。固体紫外可见漫反射测试(UV-vis DRS) 使 用 日 本Shimadzu 公 司 的UV-2450PC型紫外可见分光光度计进行,以高纯硫酸钡固体粉末为标准试剂,波长测量范围220~800nm。荧光发射光谱由日本Shimadzu 公司RF-5301PC 型荧光光谱仪在激发波长325nm,发射波长扫描范围350~600nm条件下测量。
1.3.2 羟基自由基测定
利用对苯二甲酸荧光探针技术[14]对样品表面在光激发下产生的·OH 进行检测。测定过程:分别配置浓度为1×10-3mol/L 对苯二甲酸水溶液和浓度为4×10-3mol/L 氢氧化钠水溶液;分别称取100mg Au/TiO2复合物和纯TiO2,加入装有100mL 对苯二甲酸和氢氧化钠等体积混合液的烧杯中;将其置于氙灯光源下(液面光强3.7mW/cm2)磁力搅拌,每15min 取5mL 混悬液,经12000r/min 离心机离心8min 取上清液。对照实验为黑暗条件下处理的混悬液。上述离心所得上清液采用荧光分光光度计检测荧光强度,检测条件:激发波长为315nm,发射波长扫描范围315~650nm。
1.4 Au/TiO2复合物对大肠杆菌的光催化抗菌活性测定
将液体培养基和加入琼脂的固体培养基分装于锥形瓶中,在120℃高压灭菌锅内灭菌30min;培养皿置于170℃高温灭菌箱内灭菌2h。将200μLE.coli菌液(浓度1010cfu/mL)接种到装有30mL 液体培养基的锥形瓶中,置于37℃、转速170r/min恒温摇床中培养12h。取出后将菌液稀释100 倍。称取0.01g Au/TiO2分散到1mL水中,制成10mg/mL 水分散液。在24 孔板相应的孔中加入10μL Au/TiO2水分散液和990μL 菌液,得到浓度100μg/mL 悬液。进行分组实验,实验分为空白组、光照对照组、光催化剂对照组和实验组。空白组为常规培养的细菌;光照对照组为光照条件下培养细菌;光催化剂对照组为黑暗条件下只加光催化剂培养细菌;实验组为光照+光催化剂条件下培养细菌。光化学实验用氙灯为光源进行照射(光强7mW/cm2)。实验完毕,将24 孔板相应孔中的菌悬液利用液体培养基进行二次梯度稀释,稀释104倍,取出150μL 菌悬液均匀涂布于固体培养基表面,涂布完成后将平板置于超净台中放置20min,再将平板倒置放入培养箱中在37℃恒温条件下培养36h。取出后用相机单独拍照观察,并采用菌落计数法计算细菌存活率,重复实验3次。存活率计算如式(1)。

式中,N0为初始(空白)菌落数;Nt为不同处理时间点的菌落数。
2 结果与讨论
2.1 物相结构分析
为了确定样品的物相结构,采用X射线衍射仪对样品进行了XRD 表征。图1 是纯TiO2和Au/TiO2系列复合物的XRD 图,由图1 可知,纯TiO2和Au/TiO2复 合物在25.57°、37.99°、48.16°、54.15°、55.28°、62.77°处均出现了特征衍射峰,分别对应于锐钛矿TiO2标准XRD 卡片(JCPDS 65-5714)的(101)、(004)、(200)、(105)、(211)、(204)衍射晶面,并且与Xiao[15]和Ismail 等[16]的研究结果相一致。上述结果表明,所制样品中TiO2均为锐钛矿相,且Au的负载没有改变TiO2晶相结构。

图1 不同Au含量的Au/TiO2复合物的XRD
从图1 可以看出,当Au 负载量小于0.5%时,未出现Au的衍射峰,这是由于Au负载量太少或处于高分散状态所致。当Au负载量大于0.5%时,在38.09°、44.17°、64.79°、77.39°处的衍射峰分别对应 于Au 标 准XRD 卡 片(JCPDS 65-2870) 的(111)、(200)、(220)、(311)晶面,表明零价金(Au0)成功负载至TiO2;Au 负载量越高,其衍射峰越强。根据谢尔乐方程[17]计算得,TiO2的平均粒径为12.7nm;Au/TiO2系列复合物中Au的平均粒径为8.7~10.6nm;Au/TiO2中,随着Au 含量的增加,Au粒径略有增加(见表1)。TiO2和Au/TiO2水分散液的动态光散射(DLS)实验测试结果显示,由于粒子在水相中二次团聚其水合粒径均高于XRD 计算值,此结果与文献结果一致[18];随着Au 含量的增加,Au/TiO2水合粒径逐渐变大(见表1)。
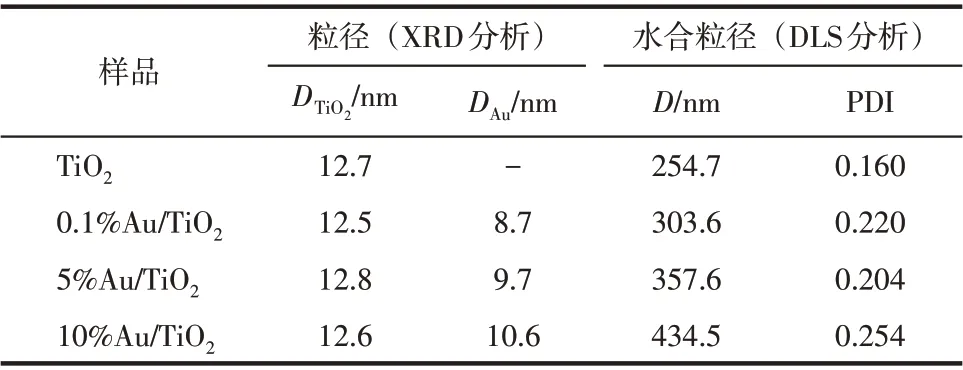
表1 Au/TiO2的XRD和DLS分析结果
2.2 FTIR分析
为了研究样品的结构和化学键,采用红外光谱仪对纯TiO2和Au/TiO2系列复合物进行FTIR 表征。由图2 可知,400~650cm-1的吸收峰为TiO2晶体中Ti O Ti 键的伸缩振动产生的特征吸收峰[19];1350cm-1附近的弱吸收峰归属于Ti OH 的吸收峰[20];1641cm-1附近的吸收峰源自TiO2表面吸附水分子的 OH 弯曲振动;3434cm-1附近的宽峰是由表面吸附水分子的 OH 基团伸缩振动产生的特征吸收[21]。不同Au 含量的Au/TiO2的红外光谱与纯TiO2比较,其吸收峰的峰形和峰位未见明显变化,表明Au负载量的变化对TiO2的结构没有显著影响。
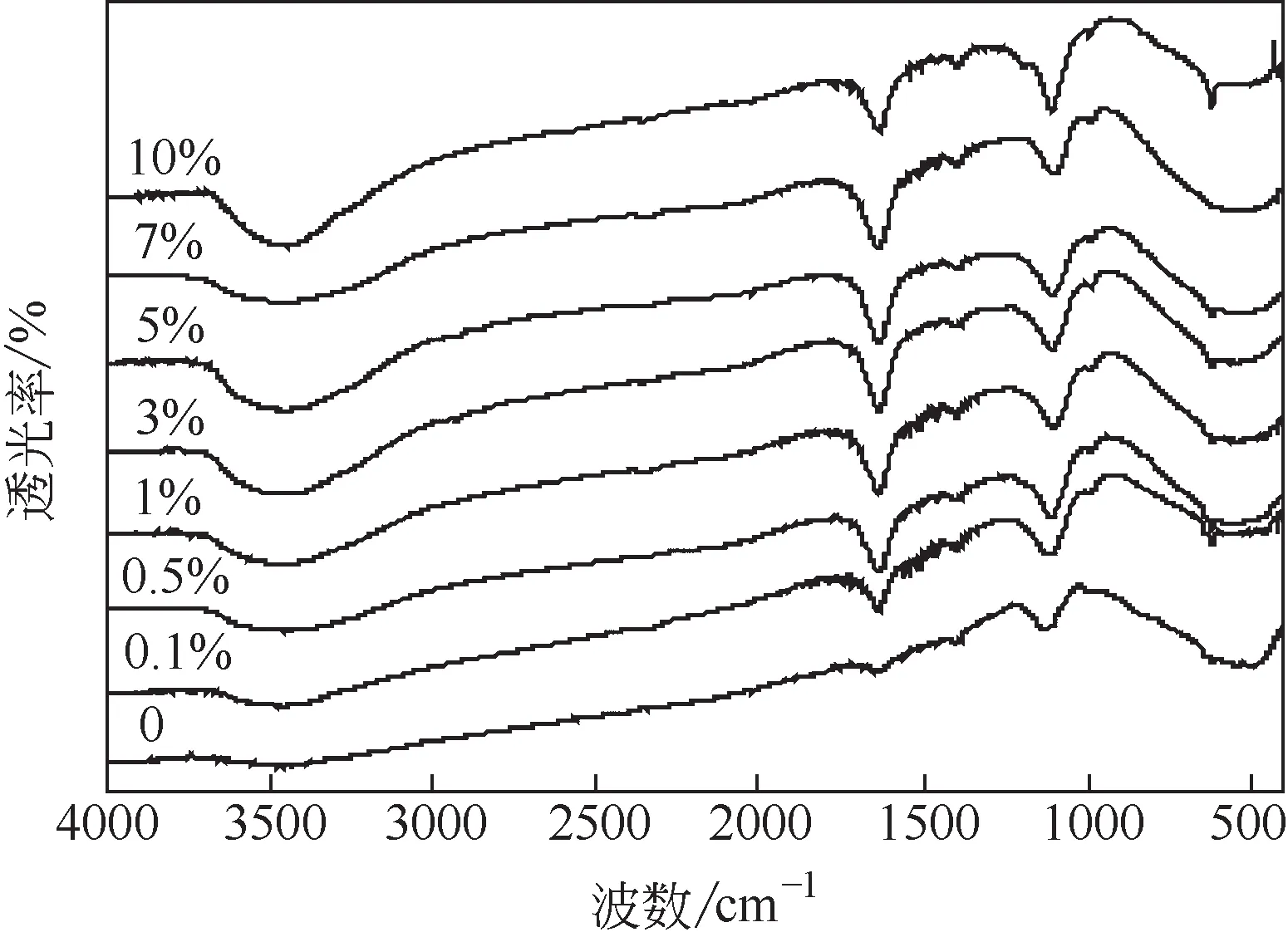
图2 不同Au含量的Au/TiO2复合物的FTIR
2.3 Au含量对Au/TiO2复合物光催化灭菌活性评价
以氙灯为光源,考察了Au含量对Au/TiO2复合物灭菌活性的影响,在光照时间60min、光照强度7mW/cm2、光催化剂浓度100μg/mL 条件下,其灭菌效果如图3 所示,计算结果见图4。空白组、光照对照组、3%Au/TiO2复合物无光照组,灭菌效果如图3(a)、(b)、(h)所示;与空白组相比,单独光照、单独Au/TiO2复合物对E. coli存活率虽有一定影响,但不明显;60min 时E.coli存活率均在90%以上,分别为92.1%、91.6%。Au/TiO2光催化处理组均具有较好的灭菌活性,且掺杂Au 的TiO2比纯TiO2具有更高的光催化灭菌活性[图3(c)~(k),图4]。对于纯TiO2,光催化处理60min 时,E. coli存活率仍高达63.6%。对于Au/TiO2,当Au 掺杂量较少时,随着掺杂量的增加,Au/TiO2对E.coli的光催化灭菌率逐渐增大;当Au掺杂量增至3%时,E.coli的存活率仅为8.7%;当Au 掺杂量大于3%时,若继续加大Au含量,E.coli的灭活率反而逐渐下降。

图3 不同Au含量的Au/TiO2复合物对大肠杆菌光催化杀灭效果
2.4 XPS分析

图4 Au/TiO2复合物和纯TiO2光催化作用对大肠杆菌存活率的影响
为探究Au/TiO2的表面化学组成和结合态,选取3%Au/TiO2进行了XPS 测试,结果如图5 所示,样品的结合能以C1s(284.8eV)为标准进行了荷电校正。图5(a)是Au/TiO2的XPS 全谱分析,由图可知,Au/TiO2中含有C、Ti、Au和O元素,C为用于校正XPS 谱峰而引入的污染碳。图5(b)是Au/TiO2中Ti2p 的XPS 谱,电子结合能位于458.5eV 和464.2eV 处的峰,分别对应Ti4+的Ti2p3/2和Ti2p1/2,与文献[22]报道一致。图5(c)是Au/TiO2中Au4f的XPS谱,由图可知,Au4f7/2在83.1eV 的结合能和Au4f5/2在86.7eV 的结合能与Au+4f7/2(84.6eV)和Au3+4f5/2(87eV) 的结合能存在显著差异,但与Au04f7/2(84.0eV)标准结合能相似,说明Au主要以零价态存在[23]。但Au4f7/2峰位与Au0(84.0eV)相比发生了0.9eV 的负位移,这是因为金粒子与TiO2载体产生了一定的相互作用,金表现出俘获电子的特征,而这种相互作用通常在催化活性中具有重要的促进作用[24]。图5(d)是Au/TiO2中O1s 的XPS 谱,O1s 峰形不对称,说明至少存在两种形式的氧,分峰处理后可见,O1s 的核心谱峰位于529.7eV,这归因于TiO2的表面晶格氧;另一个小峰出现在531.6eV,表明样品表面还存在另一种类型的氧,这种吸附氧可归结于样品表面羟基氧[25]。
2.5 UV-vis DRS分析
为分析Au/TiO2的光催化活性,对其紫外-可见吸收性能进行了UV-vis DRS 分析,同时与纯TiO2进行比较。由图6可知,纯TiO2在395nm波长附近显现出陡峭的吸收边,表明对光能的吸收集中在紫外区,而对400nm以上的可见光难以响应。相比纯TiO2,Au/TiO2不仅能吸收紫外光,对可见光也表现出很强的吸收,负载少量Au 的TiO2即可出现明显的红移现象;这是由于Au 纳米粒被入射光激发时因内部自由电子的协同振荡而产生局域表面等离子体共振,Au 表面的局域电磁场被增强,表现出很强的表面等离子体共振吸收[23],使Au/TiO2对可见光的吸收波长范围增加,加速了光生电子对在Au 与TiO2之间的转移。Au 的吸收和TiO2的本征吸收相叠加即Au与TiO2之间形成肖特基势垒特征[26],有效地促进光生载流子的分离。这种增强的可见光吸收效应和载流子分离作用对提高Au/TiO2的光催化活性尤为关键。由图6 还可发现,随着Au 含量的增加,Au/TiO2对可见光的吸收能力逐渐加强;但当Au含量大于3%后,其对可见光的吸收能力逐渐下降;究其原因,一方面可能是由于Au 颗粒的大量聚集减小了TiO2对可见光的曝光面积,使光响应范围变窄,从而降低了催化能力;另一方面,随着Au 的含量增加,其粒径变大(如图1 和表1),Au的有效利用率降低;这与活性评价结果一致。

图5 Au/TiO2复合物的XPS图

图6 不同Au含量的Au/TiO2复合物的UV-vis DRS
2.6 荧光发射光谱分析
对于半导体材料,光致荧光光谱与光生电子、光生空穴的转移性能密切相关,通过荧光强度能直接反映半导体光催化材料中光诱导载流子的分离性能和复合率。较低的荧光强度说明光催化剂具有更高的光生电子-空穴对分离效率。为进一步探究Au掺杂对TiO2中光致电子-空穴对复合的影响,进行了荧光光谱测试。由图7可知,纯TiO2在395nm和468nm 处呈现出强荧光峰,而Au/TiO2的荧光强度明显低于TiO2,表明Au掺杂促进了电子-空穴对分离,降低了二者的复合,有利于提高光催化效率[27]。分析图7 并结合前面的光催化活性结果还发现,随着Au 掺入量的增加,Au/TiO2中电子-空穴对的复合率逐渐降低,从而使其光催化效率逐渐提升;3%Au/TiO2中电子-空穴对重组受到最明显的抑制,光催化效率达到峰值;当Au掺杂量大于3%时,电子-空穴对复合率反而有所上升,致使光催化效率有所下降。

图7 不同Au含量的Au/TiO2复合物的PL
2.7 羟基自由基测定
对苯二甲酸是一种羟基自由基捕获剂,其本身是无荧光的物质,但对苯二甲酸极易与·OH 反应生成高荧光产物2-羟基对苯二甲酸,2-羟基对苯二甲酸的荧光峰强度正比于·OH自由基形成数量[28-29];因此,可利用对苯二甲酸作为荧光探针对样品表面在光激发下产生的·OH 进行定性检测。图8 是3%Au/TiO2在经氙灯照射处理不同时间段、特定激发波长(315nm)下·OH 的产生效果图。由图可知,Au/TiO2复合物随着光照时间的增加,2-羟基对苯二甲酸(峰位427nm)的荧光强度逐渐增大,此结果表明形成·OH 的数量与光照时间成正相关。荧光强度的增加意味着Au/TiO2产生了更多的·OH,这些·OH 活性氧物质在光催化氧化灭菌过程中扮演了重要角色。
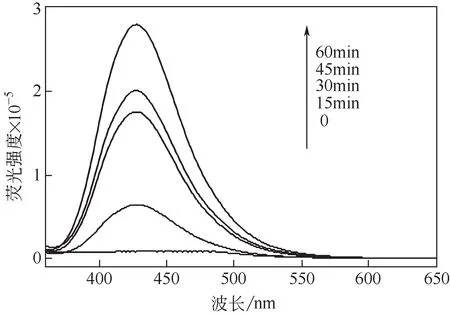
图8 Au/TiO2复合物光致发光荧光强度随时间的变化
2.8 光照时间对Au/TiO2复合物光催化灭菌活性的影响
为进一步考察光照反应时间对Au/TiO2光催化灭菌活性的影响,以高活性的3%Au/TiO2为例,研究了其在特定光照强度(7mW/cm2)、特定催化剂浓度(100μg/mL)条件下,光照时间对E.coli灭菌效果的影响。从图9 可以看出,3%Au/TiO2与纯TiO2二者对E.coli的光催化杀灭活性均随着时间的推移而递增,且3%Au/TiO2比纯TiO2具有更优异的光催化活性。光照60min 时,3%Au/TiO2和纯TiO2对E.coli的灭菌率分别为91.3%和36.4%。这主要是因为大量的光子从TiO2的价带跃迁至导带形成许多光生-电子空穴对,电子-空穴对不断地将OH-和O2氧化成·OH,活性·OH氧物质持续攻击细菌并最终使之氧化损伤死亡[30]。Au 修饰后的TiO2由于拓宽了光响应范围并显著抑制了载流子复合,因而其催化活性得以更好持续发挥。
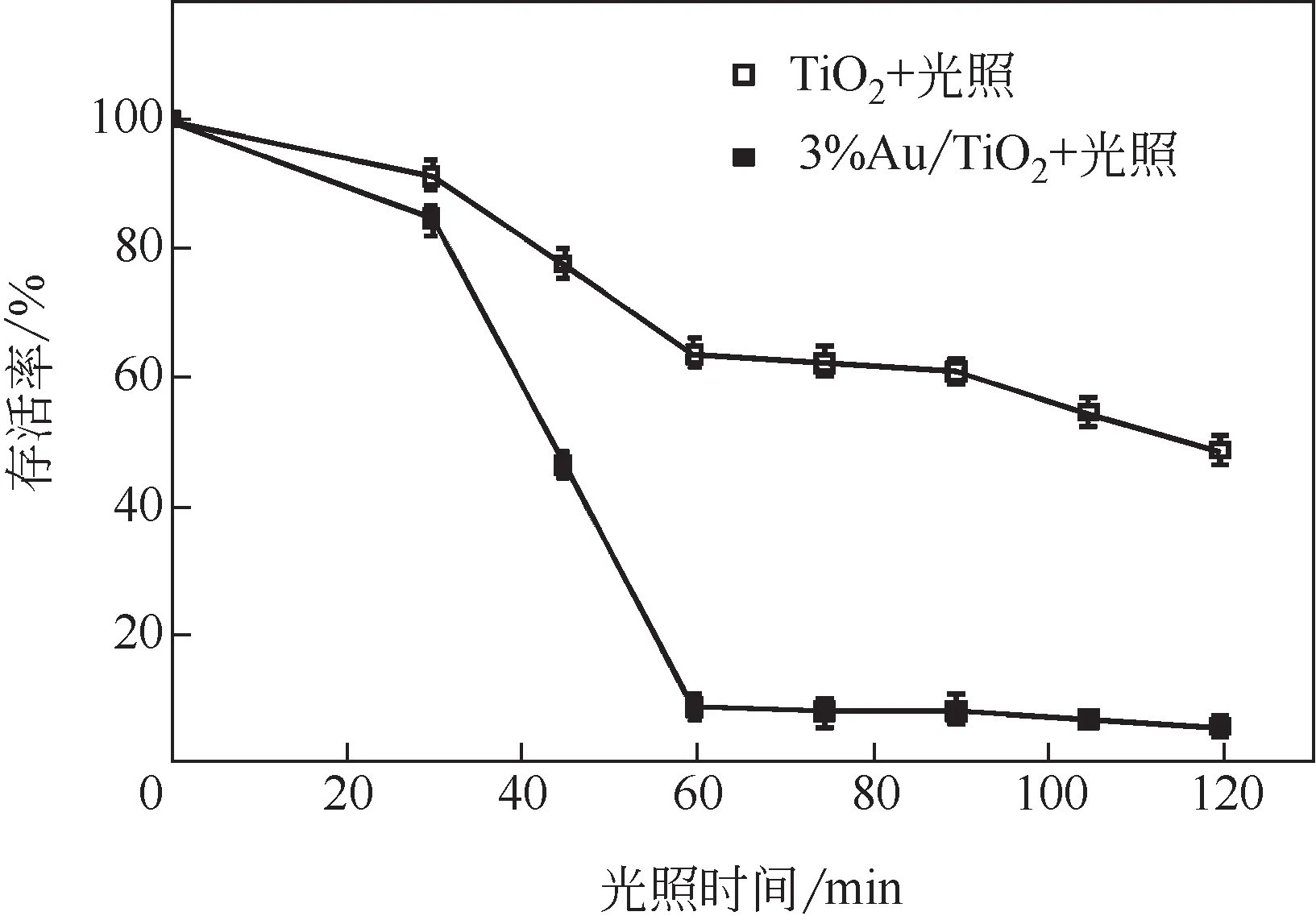
图9 3%Au/TiO2和纯TiO2光催化杀灭大肠杆菌的存活率随光照时间的变化
2.9 光照强度对Au/TiO2复合物光催化灭菌活性的影响
为进一步研究光照强度对Au/TiO2光催化灭菌性能的影响,以活性较佳的3%Au/TiO2为例,测试其在特定光照时间(60min)、特定催化剂浓度(100μg/mL)条件下,光照强度对E.coli灭菌效果的影响。从图10可以看出,无论是3%Au/TiO2还是纯TiO2,随着光照强度的增加,E.coli存活率逐渐降低。这种变化趋势是由于随着光照强度的增加,可被吸收的光子增多,产生更多的羟基自由基等氧化剂的缘故[31]。

图10 3%Au/TiO2和纯TiO2光催化杀灭大肠杆菌的存活率随光照强度的变化
2.10 催化剂浓度对Au/TiO2复合物光催化灭菌活性的影响
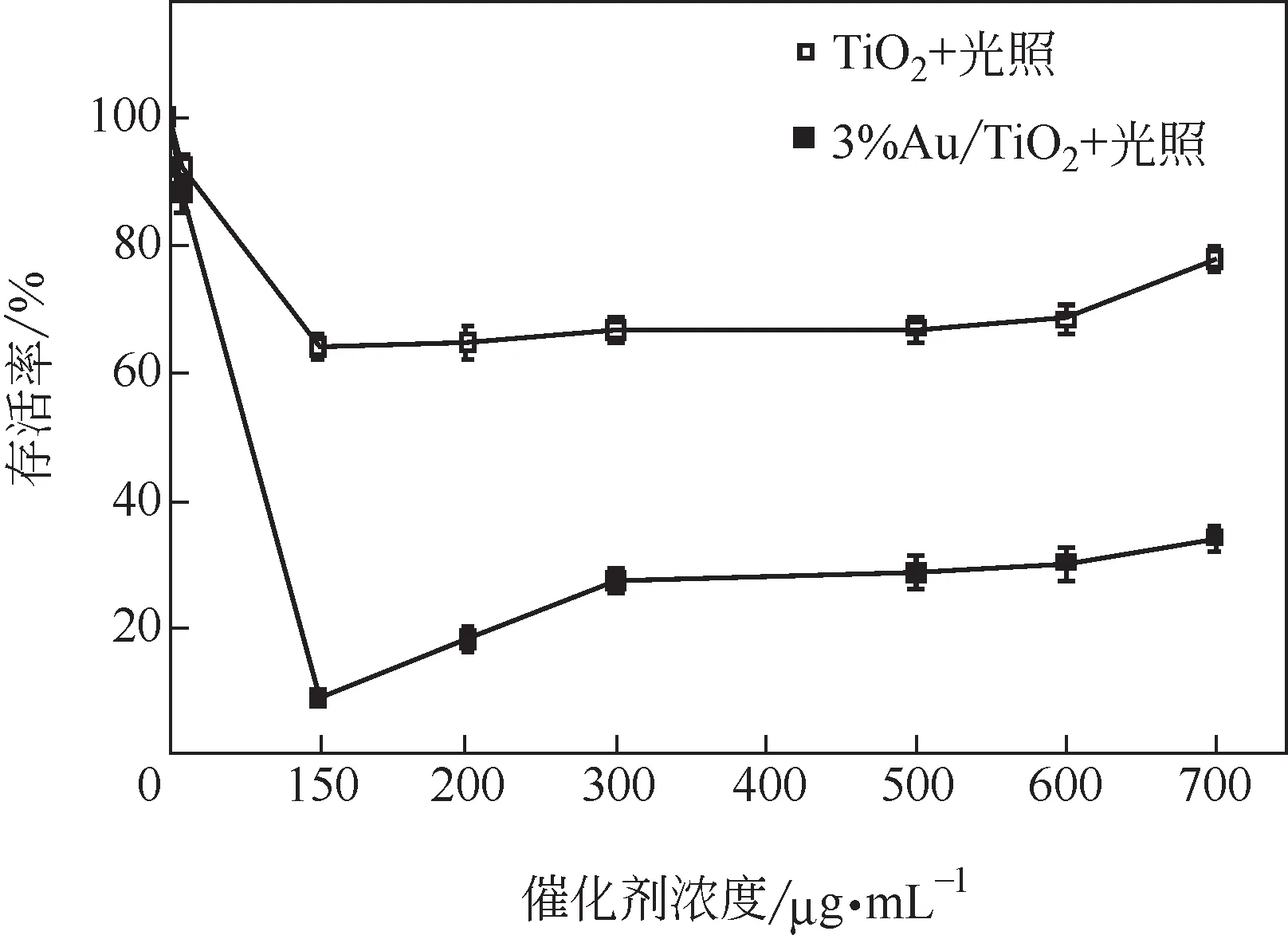
图11 3%Au/TiO2和纯TiO2光催化杀灭大肠杆菌的存活率随催化剂浓度的变化
本文还考察了催化剂浓度对E.coli杀菌性能的影响,同样选取3%Au/TiO2为代表,在特定光照时间(60min)、特定光照强度(7mW/cm2)的条件下进行测试,结果如图11所示。E.coli的存活率随着Au/TiO2浓度的增加呈现出先减小后增加的趋势。当Au/TiO2浓度为10μg/mL时,E.coli的存活率仍较高,为87.9%;这可能是由于Au/TiO2浓度太低,光照射激发产生的电子-空穴对及·OH等活性位点较少所致。随着Au/TiO2浓度提高到100μg/mL,E.coli的存活率低至8.7%,灭菌效率最高;原因是一定范围内,催化剂浓度的增加,使得吸收光子几率增大,被光激发产生的光生电子与空穴增加,衍生的·OH 等活性位点数量增多,灭菌效率得到提升。然而,当Au/TiO2浓度进一步增大后,在200~700μg/mL 范围内E. coli存活率渐渐升高,这可能是由于Au/TiO2颗粒含量的增加使溶液变得浑浊,散射和反射加剧,影响了光的透射,可利用的光相对减少,使得催化剂对光子的吸收减少,从而光催化效率降低;另一方面,过多Au/TiO2的加入可能会导致其自身发生团聚,不仅会减少反应的活性位点,还有可能成为载流子的重组中心,降低量子效率[32-33],从而使光催化效率降低。
3 结论
本文采用沉积-沉淀法制备了系列Au/TiO2复合物光催化剂。XRD 和XPS 等结果证实Au/TiO2中TiO2为锐钛矿相且Au 以零价态存在。UV-vis DRS和荧光发射光谱结果证明,利用Au 进行表面修饰不仅拓宽了TiO2的光响应范围,还显著抑制了光生载流子的复合,有助于提高其光催化效能。以氙灯为光源,将Au/TiO2运用于光催化杀灭E. coli,同时与纯TiO2进行了对比研究。结果表明:Au/TiO2与TiO2的光催化灭菌活性与光照时间和光强度均成正比,Au 改性TiO2的光催化灭菌活性高于单纯TiO2,掺杂Au的最佳质量含量为3%,Au/TiO2的浓度宜控制在100μg/mL 左右。与纯TiO2相比,Au/TiO2复合物具有显著增强的光催化灭菌活性,是一种有应用前景的灭菌光敏剂。

