女黄颗粒对小鼠的急性毒性和大鼠的亚慢性毒性试验
闫志强,陈春林,付文贵,郑华,翟少钦
(重庆市畜牧科学院,重庆 402460)
随着养殖业向集约化迅速发展,养殖密度不断增加,化学药物大量使用或滥用及某些病毒性疾病(鸡传染性法氏囊病、鸡马立克氏病)感染等造成畜禽机体免疫功能下降,对疫苗免疫应答减弱及各类疾病频频发生,最终导致畜禽生产性能降低[1-3]。基于此,本课题组通过临床试验,筛选出由女贞子(LIGUSTRI LUCIDI FRUCTUS)、黄芪(ASTRAGALI RADIX)、枸杞子(LYCII FRUCTUS)和菟丝子(CUSCUTAE SEMEN)组成的中药复方,该复方可有效增强雏鸡免疫功能,提高新城疫疫苗、法氏囊病疫苗抗体水平,促进生长[4]。为临床用药方便,课题组通过优化工艺,将其制备成颗粒剂。前期研究[5-6]表明,女黄颗粒对免疫抑制小鼠具有一定的调节作用,但其毒理学研究尚未知。为了更系统评价女黄颗粒的急性毒性及长期用药的安全性,本研究中,依据《兽药研究技术指导原则汇编》中“兽药急性毒性试验指导原则”和“兽药30 天和90 天喂养试验指导原则”,进行女黄颗粒对小鼠的急性毒性试验和大鼠的亚慢性毒性试验,对女黄颗粒的安全性进行评价,旨在为其临床用药方案的制定提供依据。
1 材料与方法
1.1 材料
1.1.1 试验药物
女黄颗粒由质量比为4∶4∶1∶1 的女贞子、黄芪、枸杞子和菟丝子(均购自重庆荣昌区桐君阁大药房)经提取后湿法制粒而成,其规格为1.0 g 颗粒中含原生药1.0 g,特女贞苷含量为1.46 mg/g。
1.1.2 试验动物
SPF 级昆明小鼠80 只,体质量18~20 g,雌、雄各半;SPF 级SD 大鼠80 只,体质量70~90 g,雌、雄各半。供试动物均由中国人民解放军第三军医大学实验动物中心提供。试验环境为屏障级,温度22~24 ℃,相对湿度50%~60%。试验前进行适应性饲养3 d,自由采食和饮水,灌胃前停食8 h,不限饮水。
1.1.3 主要仪器
PYX-DHS-60C×25-BS 型隔水式电热恒温恒湿培养箱(上海跃进医疗器械厂);Centrifuge 5340R型高速冷冻离心机(Eppendorf);BC-6900 型血细胞分析仪(深圳迈瑞生物医疗电子股份有限公司);AU680 型生化分析仪(Beckman Coulter);SUBAqua-12plus 型水浴锅(Grant);RM2235 轮转切片机(德国徕卡);CX31 型显微镜(OLYMPUS);MP12001 型普通天平(上海舜宇恒平科学仪器有限公司)。
1.2 急性毒性试验
1.2.1 预试验
40 只小鼠随机分为16、4、1、0.5 g/kg 的剂量组及空白组,每组8 只,雌、雄各4 只。分笼饲养。小鼠禁食10 h 后,药物组分别以16、4、1、0.5 g/kg的剂量灌胃给药,空白组灌胃等体积的蒸馏水,各组小鼠的灌胃体积为每10 g 体质量0.2 mL,给药后禁食2 h,然后观察7 d,记录小鼠的表现及死亡情况。当给药剂量按体质量计大于5 000 mg/kg 时小鼠没有出现死亡,表明半数致死量(LD50)大于5 000 mg/kg,需进行最大给药量试验[7]。
1.2.2 最大给药量试验
将女黄颗粒置研钵中研细,过孔径180 μm 的网筛,加水溶解,以刚好通过16 号灌胃针的混悬液浓度为最大质量浓度[8],其值为1.125 g/mL。
40 只小鼠随机分为女黄颗粒组和空白组2 组,每组20 只,雌雄各半。小鼠的最大灌胃体积为每次每10 g 体质量0.4 mL,2 次/d,灌胃间隔6 h,女黄颗粒组用最大质量浓度(1.125 g/mL)的女黄颗粒混悬液灌胃,空白组用蒸馏水灌胃,可计算出女黄颗粒组的灌胃剂量为90 g/kg。给药后禁食2 h,然后观察14 d,记录小鼠的反应及死亡情况。试验结束时处死小鼠并解剖,观察组织器官有无肉眼可见的病理变化。
1.3 亚慢性毒性试验
1.3.1 试验药物制备
将女黄颗粒置研钵中研细,过孔径180 μm 的网筛,用蒸馏水将药粉调制成质量浓度分别为0.9、0.3、0.1 g/mL 的药液备用。
1.3.2 分组及处理
将80 只大鼠随机分为女黄颗粒高、中、低剂量组(18、6、2 g/kg)及空白组,共4 组,每组20 只,雌、雄各10 只。药物组分别以18、6、2 g/kg 的剂量灌胃给药,空白组灌胃等体积的蒸馏水,每天定时灌胃,1 次/d,各组大鼠灌胃体积为每100 g 体质量2.0 mL,连续灌胃30 d,给药后禁食2 h[9]。
1.3.3 血液学和血液生化指标的测定
末次给药后禁食不禁水12 h,麻醉,眼眶采血,每只大鼠血样分成抗凝血和促凝血,抗凝血用于血液学检测,促凝血用于血液生化指标检测。血液学检测内容包括血红蛋白(Hg)含量、红细胞数(Ec)、白细胞数(Lc)和白细胞分类占比(嗜中性粒细胞(NL)、嗜酸性粒细胞(AL)、嗜碱性粒细胞(BL)、淋巴细胞(LM)和单核细胞(ML)在白细胞中占比)。血液生化指标检测内容包括谷丙转氨酶(ALT)、谷草转氨酶(AST)活性和尿素(BUN)、肌酐(Cr)、葡萄糖(Glu)、总蛋白(TP)、白蛋白(ALB)、总胆固醇(TCH)、甘油三酯(TG)、球蛋白(GLO)含量。
1.3.4 大体解剖
试验结束,采血后处死大鼠并解剖,肉眼观察肾、肺、心、脾、肝、卵巢、睾丸等脏器的色泽、硬度、形态等有无异常。
1.3.5 脏器指数的测定
剖检大鼠前称体质量,剖检后对大鼠的主要脏器进行分离,称质量,计算各个脏器的相对质量,即脏器指数[10]。
1.3.6 组织病理学检查
对高剂量组和空白组大鼠的主要脏器进行组织病理学检查,其具体方法为:用4%多聚甲醛固定组织样本后进行组织修块,放入病理包脱水,包埋组织块于石蜡中;将包埋好的组织切成5 µm 厚的薄片,脱蜡,HE 染色、封片;最后于显微镜下观察组织病理学变化,采用显微成像系统拍照,记录组织学损伤情况[11-12]。
1.4 数据分析
试验数据运用SPSS 20.0 进行单因素方差分析。
2 结果与分析
2.1 急性毒性试验结果
预试验期间,各组小鼠灌胃给药后精神正常,被毛整齐,食欲旺盛,粪便、尿液无异常;试验结束时剖检,发现试验小鼠的肝脏、心脏、脾脏、胃、肠道、肺脏、肾脏、膀胱等均无肿大、出血、粘连等异常变化,未见任何肉眼可见的病理变化。试验期间小鼠无死亡,无法测出其半数致死量。
最大给药量试验期间,试验组小鼠精神状态良好,被毛整齐,采食、饮水正常,粪便成形,无稀便、血便,尿液正常;试验结束时剖检,发现试验小鼠的肝脏、心脏、脾脏、胃、肠道、肺脏、肾脏、膀胱等均无肿大、出血、黏连等异常变化,未见任何肉眼可见的病理变化;因此,女黄颗粒的最大给药剂量为90 g/kg。
2.2 亚慢性毒性试验结果
2.2.1 女黄颗粒对大鼠临床表现的影响
在亚慢性毒性试验期间,药物组大鼠精神状态正常,被毛整齐,食欲旺盛,未见异常行为,无死亡,表明女黄颗粒对大鼠临床表现无不良影响。
2.2.2 女黄颗粒对大鼠体质量的影响
由表1 可知,与空白组相比,女黄颗粒各剂量组雌性、雄性大鼠在给药前和给药7、14、21、30 d时的体质量均无显著变化(P>0.05),表明女黄颗粒对大鼠生长无不良影响。

表1 各组大鼠的体质量 Table 1 Body weight of the studied rats
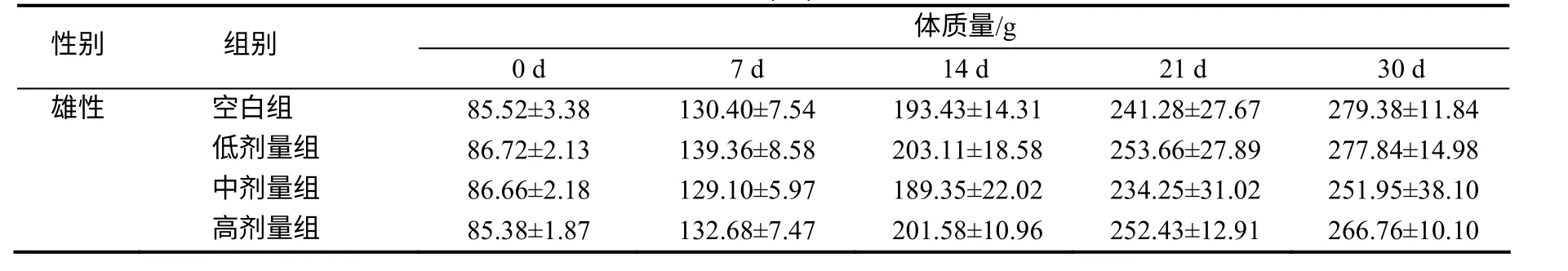
表1(续)
2.2.3 女黄颗粒对大鼠血液学指标的影响
由表2 可知,与空白组相比,给药结束后,女黄颗粒组大鼠血液红细胞数、白细胞数、血红蛋白含量及白细胞分类占比均无显著性变化(P>0.05),且无量效关系;女黄颗粒中剂量组白细胞数和淋巴细胞在白细胞中占比有增长趋势,但组间差异无统计学意义,表明女黄颗粒对大鼠血液学指标无不良影响。
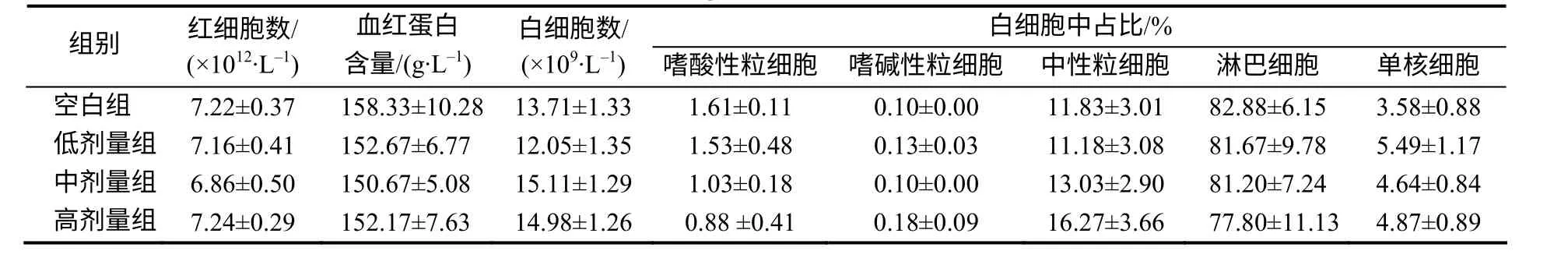
表2 各组大鼠的血液学指标 Table 2 Hematological indexes of the studied rats
2.2.4 女黄颗粒对大鼠血液生化指标的影响
由表3 可知,与空白组相比,女黄颗粒组大鼠血液谷丙转氨酶、谷草转氨酶活性和总蛋白、白蛋白、球蛋白、尿素、肌酐、葡萄糖、总胆固醇、甘油三酯含量均无显著性变化(P>0.05),表明女黄颗粒对大鼠血液生化指标无不良影响。
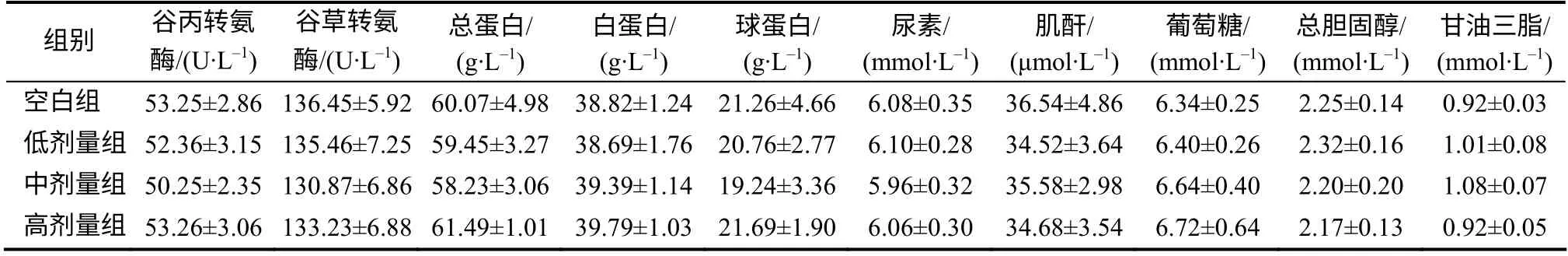
表3 各组大鼠的血液生化指标 Table 3 Blood biochemical indexes of the studied rats
2.2.5 女黄颗粒对大鼠大体解剖的影响
剖检观察发现,各试验组大鼠的心脏、肝脏、脾脏、肺脏、肾脏、胃、肠的形态、颜色、质地均正常,无明显肉眼可见病变。
2.2.6 女黄颗粒对大鼠主要脏器指数的影响
由表4 可知,与空白组相比,给药后,大鼠的主要脏器(心脏、肝脏、脾脏、肺脏及肾脏)指数均无显著性变化(P>0.05),说明女黄颗粒不会导致大鼠实质脏器损伤或异常变化。
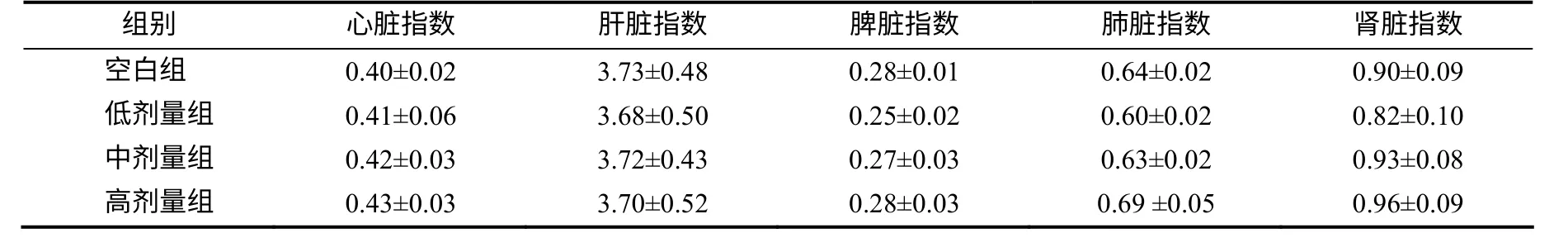
表4 各组大鼠的脏器指数 Table 4 Organ indexes of the studied rats %
2.2.7 女黄颗粒对大鼠组织切片的影响
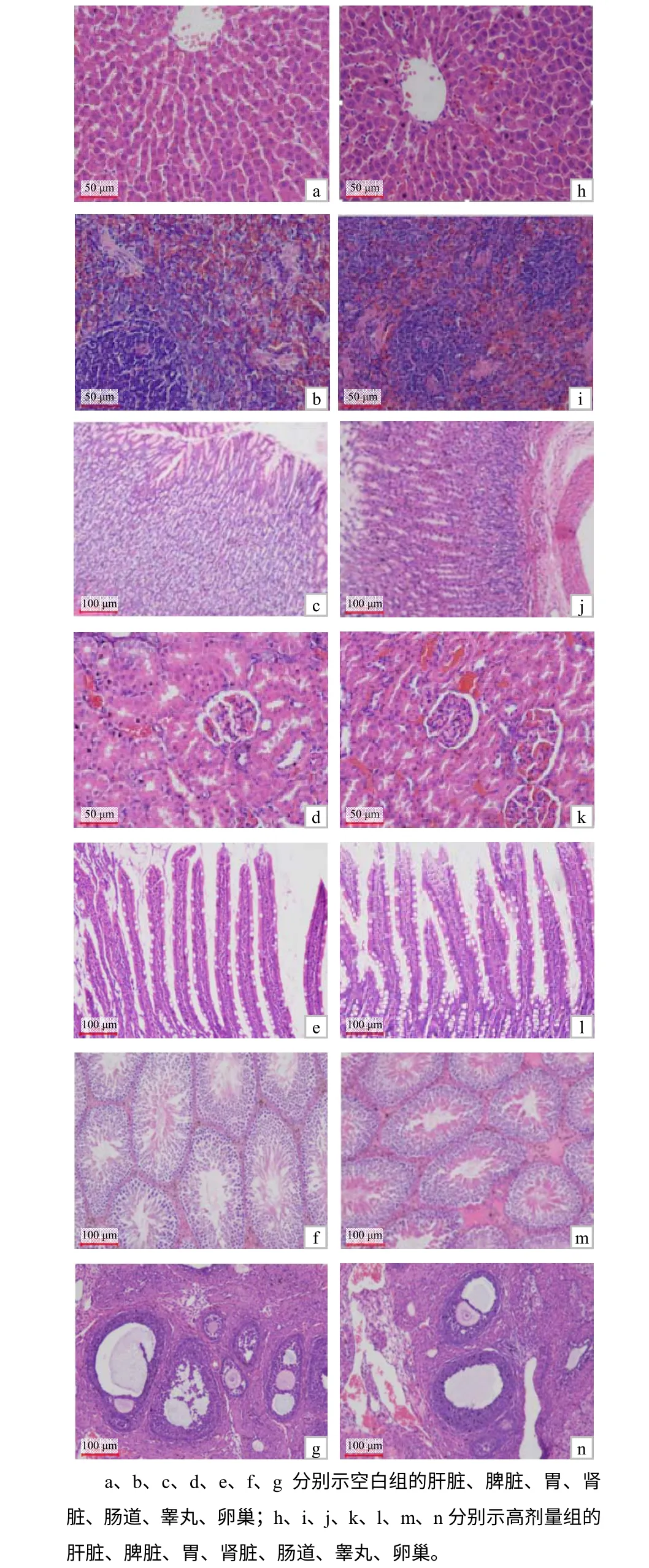
图1 各组大鼠的主要脏器组织形态 Fig.1 Main organ morphology of the studied rats
如图1 所示,肝细胞呈辐射状排列于中央静脉周围,肝细胞形态清晰,肝脏组织结构正常,未见 明显组织病理损伤;脾静脉窦、红髓、白髓及淋巴小结组织结构清晰,脾实质无异常变化,未见明显组织病理学损伤;胃黏膜层、黏膜下层和黏膜肌层 组织结构清晰,未见异常变化;肾小球及各级肾小管组织结构完整,细胞排列紧密,肾单位结构清晰未见明显组织病理学变化;肠黏膜层、固有层黏膜下层等组织结构正常,细胞排列整齐,未见明显病理损伤;睾丸支持细胞及各级精母细胞与精子细胞形态完整,未见明显病理损伤;卵巢镜下见各级卵泡,卵泡组织结构清晰完整,卵母细胞的细胞核、细胞质等清晰可见,未见明显病理损伤。
3 结论与讨论
本研究中,在急性毒性试验期间,试验小鼠精神状态良好,采食、饮水、二便均正常,无异常临床表现,试验小鼠无死亡;试验结束时,剖检,发现小鼠主要的脏器均无肉眼可见的病理变化;因此,未能测出女黄颗粒的LD50。依据毒理学评价标准及药物毒性分级标准,认为女黄颗粒无毒性。根据中国新兽药研发规范与申报指南,对无法测出LD50的药物需分析其最大给药量[13]。本试验以90 g/kg 的剂量灌胃给药女黄颗粒,发现小鼠临床表现正常,剖检后发现其主要脏器无肉眼可见的病理变化,试验期间小鼠无死亡,表明临床合理使用女黄颗粒,对动物机体无急性毒性作用。
当评价某受试药物的毒性作用特点时,在了解受试药物的理化性质后,可进行亚慢性毒性试验,以提出较长期饲喂不同剂量的受试药物对动物引起有害效应的剂量、毒作用性质和靶器官,估计亚慢性摄入的危险性,是新兽药临床前安全性评价的重要环节[14]。本研究中,主要从试验动物的临床表现,血液生理生化指标及病理检查3 个方面对女黄颗粒进行亚慢性毒性评价。亚慢性毒性试验期间,各组试验大鼠精神状态良好,被毛整齐,二便、采食、饮水与空白组相比均无异常;女黄颗粒组血液学各项指标与空白组间的差异均无统计学意义,但女黄颗粒中剂量组白细胞数和淋巴细胞在白细胞中占比有增长趋势,这可能与女黄颗粒可增强机体免疫功能有关,与文献[5]报道一致;女黄颗粒组血液生化各项指标与空白组间的差异无统计学意义;病理切片观察无异常病理变化。
本试验结果表明,女黄颗粒按照临床推荐剂量使用,对受试动物无亚慢性毒性作用,有较高的安全性。

