水合稀土硫酸盐的制备及热分解试验研究
乔 军,侯睿恩,王 哲,崔建国,陈禹夫
(1.包头稀土研究院 白云鄂博稀土资源研究与综合利用国家重点实验室,内蒙古 包头 014030;2.稀土冶金及功能材料国家工程研究中心,内蒙古 包头 014030)
近年来,高纯稀土盐类尤其是稀土硫酸盐在农业、医学、催化、电解领域都有广泛应用。硫酸铈溶液对金盏菊的生理指标和形态指标有积极促进作用,喷洒后可以使叶片叶绿素含量增加,提高植株活性;硫酸钆与氨基酸组成的稀土配合物具有很强的抗癌活性;硫酸铈铵能够提高藻类植物中岩藻黄素含量,而岩藻黄素对于抑制癌细胞的生长有积极作用;硫酸铈铵对玉米根细胞有遗传毒性,对医学试验有重要意义[1-4]。稀土硫酸盐还可作为催化剂合成高品质酯类,催化酯化效率很高,催化剂可回收[5];对于重稀土硫酸盐体系,采用电解还原法可以先得到纯度较高的硫酸镱,从而简化其他元素分离流程[6]。稀土硫酸盐的应用越来越受到重视,但有关稀土硫酸盐制备的研究报道却很少。因此,从实验室及工业生产角度研究稀土硫酸盐的制备都有重要意义[7-8]。
试验研究了用硫酸溶液溶解稀土氧化物并以蒸发结晶法[9-13]制备系列水合稀土硫酸盐,为稀土生产企业提供切实可行的生产水合稀土硫酸盐的技术方案。
1 试验部分
1.1 试剂、原料及设备
硫酸、H2O2,分析纯,天津化工试剂厂;水,由Heal Force型超纯水仪制备,二次水,电导率>18.0 MΩ·cm;Y2O3、La2O3、Pr6O11、Nd2O3,江阴加华新材料资源有限公司;Sm2O3、Eu2O3、Gd2O3、Tb4O7、Dy2O3、Ho2O3,广东从化市建丰稀土有限公司;Er2O3、Tm2O3、Yb2O3、Lu2O3、Sc2O3,深圳鸿博稀土新材料有限公司;Ce2(CO3)3,包头市新源稀土高新材料有限公司。稀土氧化物及碳酸铈原料的化学组成见表1。
电动搅拌器,JB90-S型,上海梅颖普公司;循环水真空泵,SHB-Ⅲ型,西安太康生物科技有限公司;电子天平,HZF-B 型,2 000 g/0.1 g,福州华志科学仪器有限公司;双孔水浴锅,DZKW-D-2型,500 W,北京永光明医疗仪器有限公司;万用电炉,DL型,12 kW,北京永光明医疗仪器有限公司;调压变压器,3 000 VA,电压250 V,德力西集团有限公司;封口机,SF-300型,温州市兴业机械设备有限公司。

表1 稀土氧化物及碳酸铈原料的化学组成
1.2 分析方法
H+浓度以酸碱中和滴定法测定,RE3+浓度以乙二胺四乙酸二钠络合滴定法测定,Ca2+、Fe3+、Pb2+杂质离子以原子吸收及质谱法测定,Si4+离子以分光光度法测定,稀土总量采用容量法测定,稀土纯度采用质谱法测定。
晶体形貌用S-3400N型扫描电子显微镜(日本Hitachi公司制造)观察,热分解过程用STA449F3型热分析仪(德国耐驰公司制造)分析。
1.3 试验方法
根据前期制备稀土盐类化合物的试验结果[9-13],水合稀土硫酸盐的制备包括稀土氧化物的硫酸溶解及稀土硫酸盐溶液的蒸发结晶两部分。溶解相关反应如下:

(1)

(2)

(3)

(4)
式中,Ln=La,Nd,Sm,Eu,Cd,Dy,Ho,Er,Tm,Yb,Lu,Y,Sc。
从稀土矿石浸出液中萃取分离稀土时,传统工艺的第一步是钕-钐分组萃取。钕-钐分离系数较高,前后元素性质差别较大。氧化钐是轻稀土与中、重稀土的分界氧化物,其与硫酸溶液的反应条件,所有稀土氧化物都可参考,所以,试验以氧化钐为例研究稀土氧化物的硫酸溶解条件。
2 试验结果与讨论
2.1 硫酸溶解稀土氧化物
2.1.1 硫酸浓度对氧化钐溶解的影响
氧化钐与硫酸溶液质量体积比为1 g∶0.6 mL,溶解温度85 ℃,溶解时间15 min,硫酸浓度对氧化钐溶解率的影响试验结果如图1所示。

图1 硫酸浓度对氧化钐溶解率的影响
由图1看出,在热硫酸溶液中,氧化钐逐渐溶解。氧化钐溶解和硫酸钐逐渐结晶析出的2个 过程中间是透明硫酸钐溶液的浓缩蒸发,其稀土浓度随反应时间延长不断提高,达到饱和时析出晶体;硫酸浓度小于0.30 mol/L时,氧化钐的溶解反应极易进行,可得到透明清澈的黄色硫酸钐溶液,浓缩2 min即开始析出黄色硫酸钐晶体,此时溶液中稀土质量浓度(折算氧化钐)为28 g/L;而硫酸浓度为0.35 mol/L时,溶解未完全就开始有晶体析出,溶液中硫酸钐和氧化钐共存。可见,0.30 mol/L是氧化钐溶解和硫酸钐晶体析出的临界硫酸浓度,综合考虑,硫酸浓度取0.25 mol/L为宜。
2.1.2 氧化钐与硫酸溶液质量体积比对氧化钐溶解的影响
硫酸浓度0.25 mol/L,溶解温度85 ℃,溶解时间15 min,氧化钐与硫酸溶液质量体积比对氧化钐溶解率的影响试验结果如图2所示。

图2 氧化钐与硫酸溶液质量体积比对氧化钐溶解率的影响
由图2看出:氧化钐与硫酸溶液质量体积比为1 g∶0.5 mL,即浓硫酸用量为理论量时,氧化钐溶解率只有93%,有一小部分没有溶解;而当氧化钐与硫酸溶液质量体积比为1 g∶0.6 mL,即浓硫酸用量为理论量的1.2倍时,氧化钐100%溶解。可见,硫酸稍微过量可以极大提高化学反应速度,节省反应时间。浓缩结晶后剩余的少量酸液可以返回使用。
2.1.3 溶解时间对氧化钐溶解的影响
硫酸浓度0.25 mol/L,氧化钐与硫酸溶液质量体积比为1 g∶0.6 mL,溶解温度85 ℃,溶解时间对氧化钐溶解率的影响试验结果如图3所示。

图3 溶解时间对氧化钐溶解率的影响
由图3看出:热硫酸溶液溶解氧化钐的速度很快,2~6 min即可溶解大部分氧化钐,15 min溶解完全。因此,溶解时间以15 min为宜。
2.1.4 溶解温度对氧化钐溶解的影响
硫酸浓度0.25 mol/L,氧化钐与硫酸质量体积比为1 g∶0.6 mL,溶解时间15 min,溶解温度对氧化钐溶解率的影响试验结果如图4所示。

图4 溶解温度对氧化钐溶解率的影响
由图4看出:溶解温度较低时,氧化钐溶解率较低;随温度升高,氧化钐溶解率升高,温度为85 ℃ 时,溶解率达100%;继续升温会有刺激性硫化物气体逸出。综合考虑,确定溶解温度以85 ℃为宜。
2.1.5 溶解温度对溶清时间及硫酸钐饱和溶液中氧化钐质量浓度的影响
溶解是指氧化钐在硫酸溶液中逐渐浸出的过程,溶解率小于100%;溶清是指氧化钐在硫酸溶液中100%溶解时溶液呈现的清亮透彻的状态。溶解温度对溶清时间的影响试验结果如图5所示。溶解温度对饱和硫酸钐溶液中氧化钐质量浓度的影响试验结果如图6所示。

图5 溶解温度对溶清时间的影响
由图5看出:在50 ℃较低温度下,氧化钐在硫酸溶液中经过60 min溶解才能溶清,得到硫酸钐淡黄色清亮溶液,溶液中氧化钐质量浓度23 g/L,此时没有硫酸钐晶体析出;继续在50 ℃下蒸发近2 h,待溶液中氧化钐质量浓度达67 g/L时开始有硫酸钐晶体析出,表明在50 ℃时硫酸钐饱和溶液中氧化钐质量浓度为67 g/L(见图6)。
由图5还看出:随溶解温度升高,氧化钐溶解速度加快,溶清时间缩短;在85 ℃较高温度下,氧化钐经过15 min即溶清,得到硫酸钐淡黄色清亮溶液,溶液中氧化钐质量浓度为23 g/L。此时只需持续在85℃下蒸发10 min,当氧化钐质量浓度达30 g/L时就开始有硫酸钐晶体析出,表明85 ℃时硫酸钐饱和溶液中氧化钐质量浓度为30 g/L(见图6)。

图6 溶解温度对硫酸钐饱和溶液中氧化钐质量浓度的影响
由图6看出,随溶解温度升高,硫酸钐饱和溶液中氧化钐质量浓度逐渐降低。这与稀土硫酸盐在水中溶解时低温下溶解度大、高温下溶解度小的论述[14]吻合。低温下溶解氧化钐,溶清时间较长,但操作环境好,没有刺激性气体产生,得到的饱和溶液中氧化钐浓度较高;而高温下溶清时间短,但有刺激性气体产生,得到的饱和溶液中氧化钐浓度相对较低。
为加快试验进度,试验统一在85 ℃高温条件下溶解氧化钐。实际生产中,结合通风及节能环保等具体情况,可采用先低温长时间溶解得到浓度较高的硫酸稀土饱和溶液,再升高溶液温度、快速析出稀土硫酸盐的工艺制度。
2.1.6 水合稀土硫酸钐的蒸发结晶
取5份硫酸钐饱和溶液,每份2.1 L,其中氧化钐质量浓度均为23 g/L,将溶液加热至85 ℃并保持恒温搅拌,当溶液中析出硫酸钐晶体时开始计时。析晶一段时间后过滤,得硫酸钐晶体和母液。晶体风干后称重,母液集中存放备用。硫酸钐晶体析出时间与析出质量之间的关系如图7所示。可以看出,硫酸钐晶体的析出速度较快:蒸发15 min,晶体析出质量50 g,析出率为50%;随析出时间延长,晶体析出质量增加,蒸发75 min,析出晶体100 g,析出率达100%。
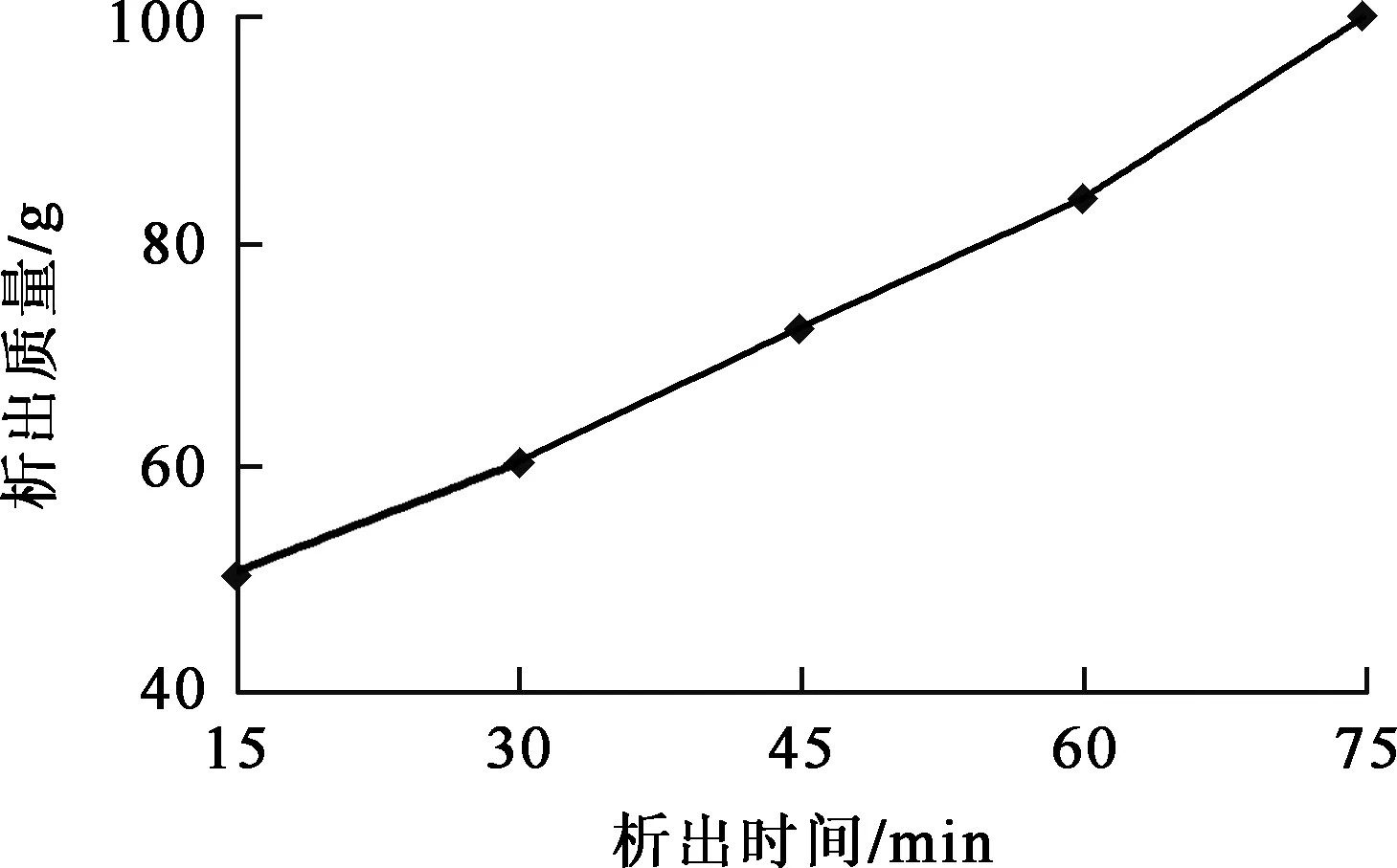
图7 硫酸钐晶体析出时间与析出质量之间的关系
2.2 系列稀土氧化物的溶解
根据硫酸溶解氧化钐的试验结果,对系列稀土氧化物进行溶解。系列稀土氧化物溶解所需硫酸浓度和溶解时间对比试验结果如图8、9所示。其中,重稀土1包括镝、钬、铒,重稀土2包括铥、镱、镥。

图8 系列稀土氧化物溶解所需硫酸浓度对比

图9 系列稀土氧化物溶解时间对比
由图8看出:随稀土元素原子序数增大,溶解稀土氧化物所需硫酸浓度逐渐提高;轻稀土氧化物用0.15 mol/L硫酸溶液即可溶解完全,而中、重稀土氧化物则需要用0.25、0.35 mol/L甚至更高浓度硫酸才能溶解。据此可实现轻、中、重稀土氧化物溶解临界点的准确控制。溶解氧化钇、氧化钪所需硫酸浓度为0.35 mol/L,与溶解重稀土氧化物所用硫酸浓度接近。
由图9看出:溶解时间随稀土元素原子序数增大而延长;轻稀土氧化物在3 min内就能溶解完全,而中、重稀土氧化物则需要15、25 min甚至35 min才能够溶解完全。氧化镨和氧化铽为过氧化物,需加入还原剂双氧水助溶,溶解过程较为缓慢,因此,其溶解时间与同组氧化物相比要长很多,氧化镨溶解需10 min、氧化铽溶解需60 min。氧化钇、氧化钪溶解时间均为25 min,与重稀土1氧化物的溶解时间接近。
溶解同组稀土氧化物所需硫酸浓度、溶解时间接近,这符合稀土元素分组规律。随稀土元素原子序数增大,硫酸浓度增大,溶解时间延长,这是镧系收缩使稀土元素离子半径减小,硫酸根离子与稀土离子结合更困难所致。溶解氧化钇、氧化钪所需硫酸浓度和溶解时间都和重稀土1组氧化物相近,表明其元素性质与氧化镝、氧化钬、氧化铒比较接近,同属于重稀土。
2.3 稀土硫酸盐饱和溶液的测定
在稀土氧化物与硫酸溶液质量体积比1 g∶0.6 mL、温度85 ℃下,梯度提高硫酸浓度,分别用硫酸溶解轻稀土(镧、铈、镨、钕)氧化物、中稀土(钐、铕、钆、铽)氧化物、重稀土1(镝、钬、铒)氧化物、重稀土2(铥、镱、镥)氧化物、钇氧化物、钪氧化物试验结果见表2。可以看出,饱和溶液中稀土质量浓度随原子序数增大而增大,与理论最大质量浓度相吻合。

表2 饱和溶液中稀土元素质量浓度
2.4 水合稀土硫酸盐的组成
对蒸发所得水合稀土硫酸盐进行热重(TG)分析。根据TG曲线,硫酸镧、轻稀土(铈、镨、钕)硫酸盐、中稀土(钐、铕、钆、铽)硫酸盐、重稀土1(镝、钬、铒)硫酸盐、重稀土2(铥、镱、镥)硫酸盐、硫酸钇、硫酸钪的各阶段失重分析结果见表3。

表3 水合硫酸稀土的热失重分析结果 %
由表3看出,大部分水合稀土硫酸盐的热分解都经历4个阶段:1.1阶段,脱去部分结晶水;1.2阶段,脱去全部结晶水;2.1阶段,无水稀土硫酸盐脱去2个SO3;2.2阶段,硫氧化稀土继续脱去1个SO3,最终生成稀土氧化物,其中铈、镨、铽的稀土氧化物和少量氧发生过氧化反应,最后生成稳定的过氧化稀土。
水合硫酸镧的热分解反应如下:




水合轻稀土(铈、镨、钕)硫酸盐的热分解反应如下:




水合中稀土(钐、铕、钆、铽)硫酸盐的热分解如下:



水合重稀土(镝、钬、铒、钇)硫酸盐的热分解反应如下:




水合重稀土(铥、镱、镥)硫酸盐的热分解反应如下:




水合硫酸钪的热分解反应如下:

由表3看出:水合硫酸镧在1.1和1.2阶段的热失重累计21.93%,热失重最大,所含结晶水最多,为9个;水合轻稀土(铈、镨、钕)硫酸盐在1.1、1.2阶段的热失重累计为12%,热失重较小,所含结晶水也少,为5个;而水合中稀土(钐、铕、钆、铽)硫酸盐、水合重稀土1(镝、钬、铒)硫酸盐、水合重稀土2(铥、镱、镥)硫酸盐在1.1和1.2阶段的热失重累计分别为19.42%,18.90%和18.53%,都为19%左右,表明这些稀土硫酸盐所含结晶水数量一样,都为8个;水合硫酸钇在这2个阶段的热失重累计为23%,含8个结晶水;水合硫酸钪在这2个阶段的热失重累计为19.64%,所含结晶水为5个。水合硫酸钪的脱硫反应一步完成。
水合稀土硫酸盐中的REO质量分数和结晶水数量的化学检测和热重检测结果见表4。水合稀土硫酸盐中非稀土杂质质量分数分析结果见表5。

表4 水合稀土硫酸盐中REO质量分数及结晶水数量检测结果

表5 水合稀土硫酸盐中非稀土杂质质量分数
2.5 水合稀土硫酸盐的形貌
水合稀土硫酸盐的晶体形貌如图10所示,照片均放大500倍。可以看出:九水合硫酸镧晶体呈柱状,长度300~400 μm,六棱柱状,结构致密;五水合硫酸铈、镨、钕晶体呈棒状,长度100~200 μm,由10~20 μm小片组成,棒状结构疏松,容易断裂成片;八水合硫酸钐、铕、钆、铽晶体为片状多面体,粒径30~50 μm;八水合硫酸镝、钬、铒晶体为大粒状多面体,粒径20~30 μm;八水合硫酸铥、镱、镥晶体为小粒状多面体,粒径10~20 μm;八水合硫酸钇晶体为粒状多面体,粒径20~30 μm,与八水合硫酸镝、钬、铒晶体相似;五水合硫酸钪晶体呈均匀小棒状,长度40~60 μm。从九水合硫酸镧到八水合硫酸镥,随原子序数增加,晶体分别为致密长柱、紧密棒状、疏松棒状、片状多面体、粒状多面体、大粒多面体、小粒多面体, 5个结晶水的晶体都呈棒状结构,8个结晶水的晶体都呈粒状结构,同时原子序数越大,水合硫酸稀土晶体颗粒越小,从宏观角度看,这与镧系收缩的规律相符。

a—La2(SO4)3·9H2O; b—Ce2(SO4)3·5H2O;c—Pr2(SO4)3·5H2O; d—Nd2(SO4)3·5H2O;e—Sm2(SO4)3·8H2O; f—Eu2(SO4)3·8H2O;g—Gd2(SO4)3·8H2O; h—Tb2(SO4)3·8H2O;i—Dy2(SO4)3·8H2O; j—Ho2(SO4)3·8H2O;k—Er2(SO4)3·8H2O; l—Tm2(SO4)3·8H2O;m—Yb2(SO4)3·8H2O; n—Lu2(SO4)3·8H2O;o—Y2(SO4)3·8H2O;p—Sc2(SO4)3·5H2O。
3 结论
以稀土氧化物为原料,以硫酸溶解-蒸发结晶法可制备系列(16种)水合硫酸稀土,适宜条件下所得稀土硫酸盐中杂质含量很低,产品纯度较高。

